Los agentes utilizados en quimioterapia se clasifican en varios grupos farmacológicos de acuerdo con su estructura, mecanismo de acción, y metabolismo.
La clasificación de Goodman y Gilman es ampliamente reconocida y ha servido de referencia a generaciones de médicos y oncólogos durante varias décadas (20). Esta clasificación agrupa los diferentes agentes en cinco grandes categorias:
- Agentes Alquilantes.
- Antimetabolitos.
- Productos Naturales
- Hormonas y Agonistas.
- Agentes Misceláneos.
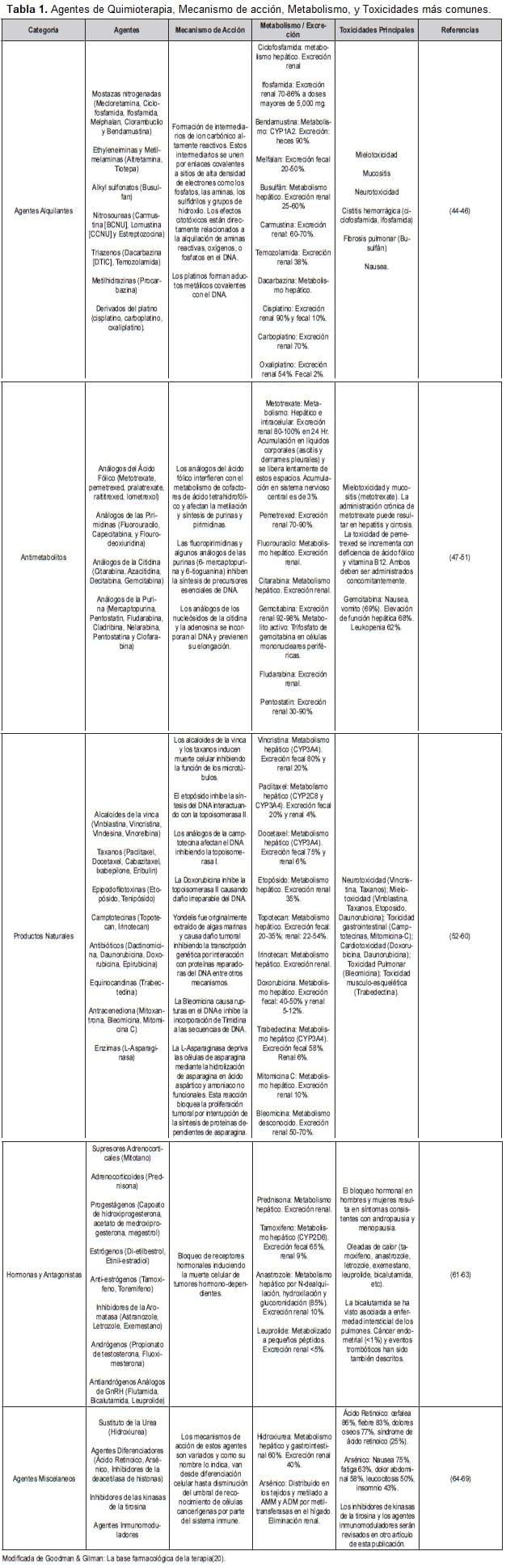
Los diferentes grupos, agentes más representativos, mecanismo de acción, metabolismo y principales toxicidades están resumidos en la tabla 1.
Esta tabla no incluye inhibidores de tirosín kinasas (terapias diana) ni inmunoterapia, por cuanto estos agentes no son normalmente considerados agentes citotóxicos.
Aunque en realidad desde un principio todos los agentes de uno u otro modo han sido “terapias diana” debido a la capacidad de inhibir o afectar alguna estructura crítica para el funcionamiento de células malignas, dicho término se acuñó a partir de 2001, con la aprobación del Imatinib Mesylate (Gleevec, Glivec).
Este nuevo grupo de agentes, conocidos también como inhibidores de las tirosín kinasas o terapias dirigidas, fue desarrollado para bloquear, inhibir, o modificar estructuras celulares críticas idealmente únicas a células con comportamiento biológico maligno.
El Imatinib fue diseñado para inhibir la proteína de la kinasa de tirosina de bcr-abl creada por la translocación cromosómica conocida como el cromosoma Filadelfia y responsable de la transformación oncológica en la leucemia mieloide crónica. Gleevec también inhibe c-Kit, el cual se encuentra mutado en pacientes con el tumor estromal gastrointestinal (GIST), y controla esta enfermedad en un número considerable de pacientes (21).
Respuesta tumoral a la quimioterapia
Siempre ha sido conocido que el cáncer era el resultado de división celular descontrolada.
De manera lógica, se infería que los agentes para tratar la enfermedad debían tener la capacidad de destruir los mecanismos de mitosis celular.
Fue así como, desde un principio, la quimioterapia fue desarrollada a partir de observaciones que confirmaban su toxicidad en tejidos humanos o se sintetizaban a partir de compuestos con la capacidad para destruir células en diferentes fases de proliferación (22, 23).
Los tratamientos generalmente están diseñados para destruir masas tumorales y erradicar todas las células tumorales.
A veces, este plan es exitoso y se alcanza la cura; pero frecuentemente, los tumores disminuyen de tamaño y crecen de nuevo tornándose resistentes al tratamiento original.
Resistencia tumoral
La resistencia tumoral es un proceso biológico complejo responsable de las respuestas tumorales que observamos después de la exposición a agentes citotóxicos (Figura 1).
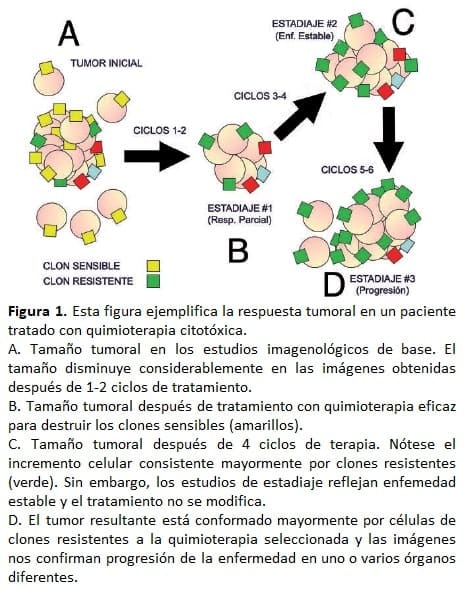
El ejemplo representado en la figura 1 demuestra un tumor expuesto a seis ciclos de quimioterapia. Las letras A-D corresponden a diferentes tiempos del tratamiento y la transición de clones de color amarillo a verde en el tumor, y el crecimiento celular asociado, reflejan respuestas comúnmente observadas en la consulta oncológica.
En este caso en particular, cabe preguntarnos si el tratamiento administrado destruyó clones tumorales sensibles dejando intactos aquellos clones resistentes a la quimioterapia, y que esos clones resistentes continuaron creciendo de manera exponencial durante el tratamiento (Hipótesis de Goldie-Coldman) (24), o si por el contrario, la progresión en el tamaño y número de esos implantes tumorales es el resultado de resistencia adquirida asociada a mutaciones tumorales que surgieron como respuesta a los agentes tóxicos administrados durante el tratamiento (resistencia inducida) (25).
Esta última, relacionada con flujo celular de drogas, persistencia de células madre cancerígenas (CSCs), transición epitelial- mesenquimal (EMT), y disminución de apoptosis. La adquisición de resistencia a drogas también está mediada por mutaciones, cambios en la expresión de genes, ajustes alternativos en el RNA, etc.
Estas observaciones iniciales llevaron al desarrollo del modelo de Skipper-Schabel-Wilcox
Mediante el cual se postulaba que “una dosis determinada de un agente determinado debía destruir aproximadamente la misma fracción, más no el mismo número de tumores de tamaño diferente, siempre y cuando se utilizara la misma exposición a la droga, y la fracción de crecimiento y la proporción de poblaciones celulares con fenotipo resistente fueran iguales” (26).
A su vez, este modelo dió nacimiento a la hipótesis de muerte celular exponencial (Log-Kill) mediante la cual se postulaba que si la duplicación celular es constante, el tiempo (x) que toma un tumor en crecer de 1.000 células a 10.000 células es igual al tiempo que toma para crecer de 10 millones a 100 millones de células (22).
Basándose en el modelo de crecimiento celular Gompertziano en el cual, a medida que la masa celular crece, aumenta por una disminución constante de la proporción de su tamaño por una unidad de tiempo determinada (27), Larry Norton y Richard Simon desarrollaron la hipótesis de Norton y Simon, la cual postula que las células tumorales son destruidas por quimioterapia a una tasa directamente proporcional a la tasa de crecimiento celular al principio del tratamiento (28).
Estos conceptos fundamentales de crecimiento celular han dado origen a través de los años a conceptos de gran importancia clínica como el uso secuencial de agentes de quimioterapia, y los esquemas de dosis densas en linfoma y seno (29, 30). Una excelente fuente de consulta para este tema se encuentra en esta dirección electrónica de la Librería Nacional de Medicina: https://www.ncbi.nlm.nih.gov/books/NBK20771/
La predicción y caracterización de estas respuestas y procesos biológicos se hace más compleja por fenómenos como la heterogeneidad tumoral que a su vez dificulta el desarrollo e interpretación de modelos matemáticos de crecimiento y migración celular.
Desde el punto de vista clínico, estas observaciones han sido aplicadas estadísticamente bajo diferentes figuras como “tiempo para progresión (TTP)”, “duración de la respuesta (DOR)” o “sobrevida libre de progresión (PFS)” para evaluar la eficacia de agentes quimioterapéuticos (31).
Es también común observar tumores del mismo tipo histológico sustancialmente más sensibles que otros expuestos al mismo agente durante el mismo periodo de tiempo. Estos diferentes fenómenos de respuesta tumoral tienen una variable común: sensibilidad tumoral. En este aspecto, es también pertinente e importante anotar que la primera línea de tratamiento es generalmente aceptada como la más eficaz y que las líneas subsecuentes son en general consideradas paliativas y asociadas a menor eficacia. Esta observación y dogma de manejo clínico nos reitera la presencia de resistencia tumoral, ya sea adquirida o existente y nos debe invitar a reflexionar y planear el siguiente agente para tratar la enfermedad.
Otro aspecto importante para tener en cuenta durante el uso de combinaciones de quimioterapia es la proyección de la respuesta tumoral basada en la toxicidad acumulada y la muerte celular medida por medio de estudios radiográficos (CT, MRI), metabólicos (PET/ CT), o bioquímicos (marcadores tumorales) (Figura 2). En este sentido, la respuesta tumoral radiográfica y metabólica temprana ya ha sido reconocida como un factor predictivo importante de sobrevida en pacientes con linfoma Hodgkin y no Hodgkin (32). Es probable que este principio también aplique a otros subtipos histológicos.
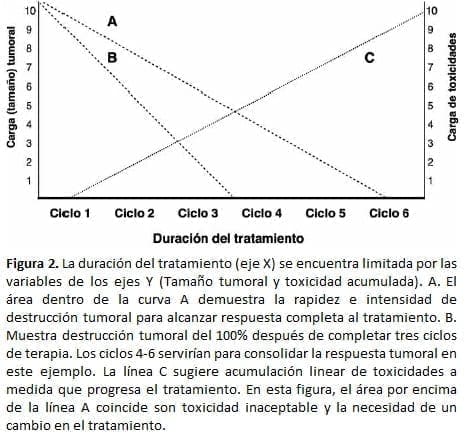
Sabemos también que el tratamiento con agentes individuales es generalmente utilizado para el cuidado paliativo de pacientes con estado funcional pobre y a quienes un perfil de toxicidad bajo conlleva a una mejor calidad de vida, pero pocas probabilidades de grandes respuestas tumorales.
Alternativamente, las combinaciones de compuestos generalmente resultan en mayores respuestas antitumorales y mayor índice de curabilidad, pero desde luego, también están asociadas a mayor toxicidad. De esta manera, en el arte de la administración de quimioterapia, a veces se utilizan terapias combinadas para inducir una mayor respuesta y recuperar la función de algún órgano en particular, pero de manera similar, frecuentemente utilizamos regímenes con agentes únicos dirigidos a prestar una función paliativa y menos tóxica para el huésped.
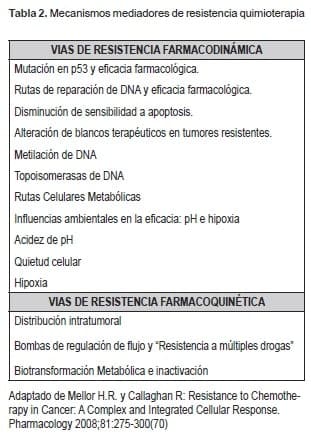
En términos generales, la resistencia a agentes de quimioterapia está mediada por dos procesos generales: farmacoquinético (alteración de la exposición celular intracelular), o farmacodinámico (p.e. inhabilidad para inducir citotoxicidad). Infortunadamente, muchas veces la resistencia a agentes específicos es mixta y resulta de diferentes mecanismos de resistencia (Tabla 2). Diferentes grupos de investigación exploran estos diversos mecanismos y buscan terapias para reducir el desarrollo de resistencia a la quimioterapia.
(Lea También: Historia Oral de la Oncología Clínica en Colombia)
Futuro de la quimioterapia
La aplicación de modernos avances tecnológicos a los agentes existentes ha resultado en el desarrollo de nuevos agentes quimioterapéuticos. Quizás uno de los ejemplos más exitosos es el nab-paclitaxel (nanoparticle albumin-bound paclitaxel). Este compuesto es una formulación de paclitaxel libre de solventes. El paclitaxel requiere del uso de solventes como Cremphor- EL en su preparación, el cual está asociado a algunas de sus toxicidades. La nueva formulación es preparada formando una suspensión coloidal de nanopartículas por homogenización del paclitaxel a alta presión en presencia de albúmina sérica. El Nab-paclitaxel tiene varias ventajas prácticas sobre el Cremphor-EL-paclitaxel incluyendo una infusión más corta (30 minutos) y la no necesidad de premedicación. El Nab-paclitaxel utiliza los mecanismos de transporte de la albúmina endógena para concentrar el agente dentro del tumor (33). Su eficacia y perfil de toxicidades le valió la aprobación por la FDA para pacientes con cáncer de seno, pulmón y páncreas.
La capacidad de las terapias citotóxicas para inducir respuestas significativas cuando se administran en combinación con otras formas de tratamiento como la radioterapia, los agentes inmuno-moduladores (34), y las terapias diana (35) ha sido demostrada en diferentes estudios y ha llevado a posicionar estos regímenes como tratamiento estándar en cáncer de pulmón (36- 39), linfoma (40-42), seno (43), y muchos otros en las últimas décadas.
Las mutaciones genómicas críticas y responsables del comportamiento maligno de la mayoría de los clones celulares de un tumor se limitan a menos de un 15% en el común de las neoplasias sólidas. Por ello, aunque las terapias dirigidas y la inmunoterapia son eficaces en un alto número de pacientes, su combinación con quimioterapia es todavía necesaria en la mayoría de pacientes.
Es muy probable que la heterogeneidad tumoral presente en la gran mayoría de tumores obligue a seguir utilizando terapias combinadas encaminadas a desactivar y destruir diferentes mecanismos de crecimiento e invasión celular tumoral.
Finalmente, la combinación de diferentes formas de tratamiento (neo-adyuvante, adyuvante, y diferentes líneas de terapia para enfermedad sistémica) va a continuar mejorando la sobrevida de pacientes con cáncer en el siglo XXI y convertir el cáncer en una dolencia crónica similar a otras tantas que enfrentamos a diario.
Referencias
-
1. Long PH. Paul Ehrlich and modern chemotherapy. Bull N Y Acad Med. 1952;28(5):344-6.
-
2. Lectures N. Paul Ehrlich – Biographical. NobelMedia AB 20201967; 2020 [consultado 09 septiembre 2020]. Disponible en: https://www.nobelprize.org/prizes/medicine/1908/ehrlich/biographical/.
-
3. Thorburn AL. Paul Ehrlich: pioneer of chemotherapy and cure by arsenic (1854-1915). Br J Vener Dis. 1983;59(6):404-5.
-
4. Pechura CM. From the Institute of Medicine. JAMA. 1993;269(4):453.
-
5. Wilke C. From Chemical Weapon to Chemotherapy, 1917–1946 The Scientist. 2019 [consultado 22 septiembre 2020]. Disponible en: https://www.the-scientist.com/foundations/from-chemical-weapon-to-chemotherapy–19171946-65655.
-
6. Goodman LS, Wintrobe MM, Dameshek W, Goodman MJ, Gilman A, McLennan MT. Nitrogen mustard therapy. Use of methyl-bis(beta-chloroethyl)amine hydrochloride and tris(beta-chloroethyl)amine hydrochloride for Hodgkin’s disease, lymphosarcoma, leukemia and certain allied and miscellaneous disorders. JAMA. 1984;251(17):2255-61.
-
7. DeVita VT, Jr., Chu E. A history of cancer chemotherapy. Cancer Res. 2008;68(21):8643-53.
-
8. Gellhorn A, Jones LO. Chemotherapy of malignant disease. Am J Med. 1949;6(2):188-231.
-
9. Schepartz SA. Historical overview of the National Cancer Institute Fermentation Program. Recent Results Cancer Res. 1978;63:30-2.
-
10. Li MC. Current status of cancer chemotherapy. J Natl Med Assoc. 1960;52(5):315-20.
-
11. Li MC, Whitmore WF, Jr., Golbey R, Grabstald H. Effects of combined drug therapy on metastatic cancer of the testis. JAMA. 1960;174:1291-9.
-
12. Devita VT, Jr., Serpick AA, Carbone PP. Combination chemotherapy in the treatment of advanced Hodgkin’s disease. Ann Intern Med. 1970;73(6):881-95.
-
13. FDA. Approval for Imatinib Mesylate for the treatment of patients with chronic myelogenous leukemia after therapy with interferon. FDA.gov. 2001 [consultado 19 octubre 2020]. Disponible en: https://www.accessdata.fda.gov/drugsatfda_docs/nda/2001/21335_Gleevec.cfm.
-
14. Benitez JC, Remon J, Besse B. Current Panorama and Challenges for Neoadjuvant Cancer Immunotherapy. Clin Cancer Res. 2020;26(19):5068-77. 15. Higby DJ, Wallace HJ, Jr., Holland JF. Cis-diamminedichloroplatinum (NSC-119875): a phase I study. Cancer Chemother Rep. 1973;57(4):459-63.
-
16. FDA. Approval package for gemcitabine hydrochloride – Center for Drug Evaluation and Research accessdata. fda.gov.1996 [consultado 4 octubre 2020 ]. Disponible en: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=020509.
-
17. FDA. Azacitidine approval – Center for Drug Evaluation and Research access.fda.gov. 2004 [consultado 04 octubre 2020]. Disponible en: https://www.accessdata.fda.gov/drugsatfda_docs/nda/2004/50-794_Vidaza_Prntlbl.pdf.
-
18. Fili C, Malagola M, Follo MY, Finelli C, Lacobucci I, Martinelli G et al. Prospective phase II Study on 5-days azacitidine for treatment of symptomatic and/or erythropoietin unresponsive patients with low/INT-1-risk myelodysplastic syndromes. Clin Cancer Res. 2013;19(12):3297-308.
-
19. Takimoto CH. Maximum tolerated dose: clinical endpoint for a bygone era? Target Oncol. 2009;4(2):143-7.
-
20. Goodman AL, Gilman A. Goodman & Gilman’s The Pharmacological Basis of Therapeutics. 12a ed. Brunton L, Chabner B, Knollman B, editors; 2011.
-
21. Heinrich MC, Blanke CD, Druker BJ, Corless CL. Inhibition of KIT tyrosine kinase activity: a novel molecular approach to the treatment of KIT-positive malignancies. J Clin Oncol. 2002;20(6):1692-703.
-
22. Norton L. Cancer log-kill revisited. Am Soc Clin Oncol Educ Book. 2014:3-7.
-
23. Hansen E, Read AF. Cancer therapy: Attempt cure or manage drug resistance? Evol Appl. 2020;13(7):1660- 72.
-
24. Chen JH, Kuo YH, Luh HP. Optimal policies of noncross- resistant chemotherapy on Goldie and Coldman’s cancer model. Math Biosci. 2013;245(2):282-98.
-
25. Aleksakhina SN, Kashyap A, Imyanitov . Mechanisms of acquired tumor drug resistance. Biochim Biophys Acta Rev Cancer. 2019;1872(2):188310.
-
26. Surbone A, Norton L. Kinetics of breast neoplasms. Minerva Med. 1994;85(1-2):7-16.
-
27. Norton L, Simon R, Brereton HD, Bogden AE. Predicting the course of Gompertzian growth. Nature. 1976;264(5586):542-5.
-
28. Norton L, Simon R. The Norton-Simon hypothesis revisited. Cancer Treat Rep. 1986;70(1):163-9.
-
29. Untch M, Bergh J, Citron M, Hudis CA, Huober J, Mobus V et al. Dose-Dense Therapy. Breast Care (Basel). 2008;3(2):134-8.
-
30. Hudis CA, Schmitz N. Dose-dense chemotherapy in breast cancer and lymphoma. Semin Oncol. 2004;31(3 Suppl 8):19-26.
-
31. Saad ED, Katz A. Progression-free survival and time to progression as primary end points in advanced breast cancer: often used, sometimes loosely defined. Ann Oncol. 2009;20(3):460-4.
-
32. Querellou S, Valette F, Bodet-Milin C, Oudoux A, Carlier T, Harousseau JL et al. FDG-PET/CT predicts outcome in patients with aggressive non-Hodgkin’s lymphoma and Hodgkin’s disease. Ann Hematol. 2006;85(11):759- 67.
-
33. Miele E, Spinelli GP, Miele E, Tomao F, Tomao S. Albumin- bound formulation of paclitaxel (Abraxane ABI-007) in the treatment of breast cancer. Int J Nanomedicine. 2009;4:99-105.
-
34. Garon EB, Rizvi NA, Hui R, Leighl N, Balmanoukian AS, Eder JP et al. Pembrolizumab for the treatment of nonsmall- cell lung cancer. N Engl J Med. 2015;372(21):2018- 28.
-
35. Hurwitz H, Fehrenbacher L, Novotny W, Cartwright T, Hainsworth J, Heim W et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer. N Engl J Med. 2004;350(23):2335-42.
-
36. West H, McCleod M, Hussein M, Morabito A, Rittmeyer A, Conter HJ et al. Atezolizumab in combination with carboplatin plus nab-paclitaxel chemotherapy compared with chemotherapy alone as first-line treatment for metastatic non-squamous non-small-cell lung cancer (IMpower130): a multicentre, randomised, open-label, phase 3 trial. Lancet Oncol. 2019;20(7):924-37.
-
37. Paz-Ares L, Luft A, Vicente D, Tafreshi A, Gumus M, Mazieres J et al. Pembrolizumab plus Chemotherapy for Squamous Non-Small-Cell Lung Cancer. N Engl J Med. 2018;379(21):2040-51.
-
38. Gandhi L, Rodriguez-Abreu D, Gadgeel S, Esteban E, Felip E, De Angelis F et al. Pembrolizumab plus Chemotherapy in Metastatic Non-Small-Cell Lung Cancer. N Engl J Med. 2018;378(22):2078-92.
-
39. Garon EB, Ciuleanu TE, Arrieta O, Prabhash K, Syrigos KN, Goksel T et al. Ramucirumab plus docetaxel versus placebo plus docetaxel for second-line treatment of stage IV non-small-cell lung cancer after disease progression on platinum-based therapy (REVEL): a multicentre, double-blind, randomised phase 3 trial. Lancet. 2014;384(9944):665-73.
-
40. Ogura M, Ando K, Taniwaki M, Watanabe T, Uchida T, Ohmachi K et al. Feasibility and pharmacokinetic study of bendamustine hydrochloride in combination with rituximab in relapsed or refractory aggressive B cell non- Hodgkin’s lymphoma. Cancer Sci. 2011;102(9):1687-92.
-
41. Martino R, Perea G, Caballero MD, Mateos MV, Ribera JM, de Oteyza JP et al. Cyclophosphamide, pegylated liposomal doxorubicin (Caelyx), vincristine and prednisone (CCOP) in elderly patients with diffuse large B-cell lymphoma: results from a prospective phase II study. Haematologica. 2002;87(8):822-7.
-
42. Zinzani PL, Santoro A, Gritti G, Brice P, Barr PM, Kuruvilla J et al. Nivolumab Combined With Brentuximab Vedotin for Relapsed/Refractory Primary Mediastinal Large B-Cell Lymphoma: Efficacy and Safety From the Phase II CheckMate 436 Study. J Clin Oncol. 2019;37(33):3081- 9.
-
43. Slamon D, Eiermann W, Robert N, Pienkowski T, Martin M, Press M et al. Adjuvant trastuzumab in HER2-positive breast cancer. N Engl J Med. 2011;365(14):1273-83.
-
44. Wheeler GP. Studies related to the mechanisms of action of cytotoxic alkylating agents: a review. Cancer Res. 1962;22:651-88.
-
45. Emadi A, Jones RJ, Brodsky RA. Cyclophosphamide and cancer: golden anniversary. Nat Rev Clin Oncol. 2009;6(11):638-47.
-
46. Reedijk J, Lohman PH. Cisplatin: synthesis, antitumour activity and mechanism of action. Pharm Weekbl Sci. 1985;7(5):173-80.
-
47. White JC. Recent concepts on the mechanism of action of methotrexate. Cancer Treat Rep. 1981;65 Suppl 1:3- 12.
-
48. Parker WB, Cheng YC. Metabolism and mechanism of action of 5-fluorouracil. Pharmacol Ther. 1990;48(3):381- 95.
-
49. Maslak P, Chanel S, Camacho LH, Soignet S, Pandolfi PP, Guernah I et al. Pilot study of combination transcriptional modulation therapy with sodium phenylbutyrate and 5-azacytidine in patients with acute myeloid leukemia or myelodysplastic syndrome. Leukemia. 2006; 20(2):212-7.
-
50. Robak T, Lech-Maranda E, Korycka A, Robak E. Purine nucleoside analogs as immunosuppressive and antineoplastic agents: mechanism of action and clinical activity. Curr Med Chem. 2006;13(26):3165-89.
-
51. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oxaliplatin: mechanism of action and antineoplastic activity. Semin Oncol. 1998;25(2 Suppl 5):4-12.
-
52. Liu LF, Desai SD, Li TK, Mao Y, Sun M, Sim SP. Mechanism of action of camptothecin. Ann N Y Acad Sci. 2000;922:1-10.
-
53. Sartiano GP, Lynch WE, Bullington WD. Mechanism of action of the anthracycline anti-tumor antibiotics, doxorubicin, daunomycin and rubidazone: preferential inhibition of DNA polymerase alpha. J Antibiot (Tokyo). 1979;32(10):1038-45.
-
54. Martinez-Serra J, Maffiotte E, Martin J, Bex T, Navarro- Palou M, Ros T et al. Yondelis(R) (ET-743, Trabectedin) sensitizes cancer cell lines to CD95-mediated cell death: new molecular insight into the mechanism of action. Eur J Pharmacol. 2011;658(2-3):57-64.
-
55. van Maanen JM, Retel J, de Vries J, Pinedo HM. Mechanism of action of antitumor drug etoposide: a review. J Natl Cancer Inst. 1988;80(19):1526-33.
-
56. Dorr RT. Bleomycin pharmacology: mechanism of action and resistance, and clinical pharmacokinetics. Semin Oncol. 1992;19(2 Suppl 5):3-8.
-
57. Larsen AK, Galmarini CM, D’Incalci M. Unique features of trabectedin mechanism of action. Cancer Chemother Pharmacol. 2016;77(4):663-71.
-
58. Muller WE, Zahn RK. Bleomycin, an antibiotic that removes thymine from double-stranded DNA. Prog Nucleic Acid Res Mol Biol. 1977;20:21-57.
-
59. Kumar K, Kaur J, Walia S, Pathak T, Aggarwal D. Lasparaginase: an effective agent in the treatment of acute lymphoblastic leukemia. Leuk Lymphoma. 2014;55(2):256-62.
-
60. Pagliardi GL, Gabutti V, Gavosto F. Mechanism of action of L-asparaginase on the cell cycle and growth in acute lymphoblastic leukemia. Acta Haematol. 1973;50(5):257-68.
-
61. Lipov EG, Joshi JR, Sanders S. A new mechanism of action for tamoxifen. Lancet Oncol. 2009;10(6):542.
-
62. Miller WR. Aromatase inhibitors: mechanism of action and role in the treatment of breast cancer. Semin Oncol. 2003;30(4 Suppl 14):3-11.
-
63. Furr BJ, Tucker H. The preclinical development of bicalutamide: pharmacodynamics and mechanism of action. Urology. 1996;47(1A Suppl):13-25; discussion 9-32.
-
64. Camacho LH, Soignet SL, Chanel S, Ho R, Heller G, Scheinberg DA et al. Leukocytosis and the retinoic acid syndrome in patients with acute promyelocytic leukemia treated with arsenic trioxide. J Clin Oncol. 2000;18(13):2620-5.
-
65. Camacho LH. Clinical applications of retinoids in cancer medicine. J Biol Regul Homeost Agents. 2003;17(1):98- 114.
-
66. Camacho LH. CTLA-4 blockade with ipilimumab: biology, safety, efficacy, and future considerations. Cancer Med. 2015;4(5):661-72.
-
67. Camacho LH. Novel therapies targeting the immune system: CTLA4 blockade with tremelimumab (CP-675,206), a fully human monoclonal antibody. Expert Opin Investig Drugs. 2008;17(3):371-85.
-
68. Brahmer JR, Tykodi SS, Chow LQ, Hwu WJ, Topalian SL, Hwu P, et al. Safety and activity of anti-PD-L1 antibody in patients with advanced cancer. N Engl J Med. 2012;366(26):2455-65.
-
69. Yarbro JW. Mechanism of action of hydroxyurea. Semin Oncol. 1992;19(3 Suppl 9):1-10.
-
70. Mellor HR, Callaghan R. Resistance to chemotherapy in cancer: a complex and integrated cellular response. Pharmacology. 2008;81(4):275-300.
Recibido: Diciembre 16, 2020
Aceptado: Diciembre 17, 2020
Correspondencia:
Luis H. Camacho
lhcamacho@cobd.us