La naturaleza estocástica del cáncer refuerza la noción de que el desarrollo y progresión del cáncer no sigue un curso lineal fijo, sino más bien, una desestabilización integrada de múltiples procesos celulares clave.
Incluso después de la transformación maligna, el cáncer permanece dinámico y continúa evolucionando para generar un ecosistema heterogéneo con elementos formes que albergan formas moleculares distintas, con niveles diferenciales de sensibilidad a las terapias.
Esta heterogeneidad puede resultar de cambios genéticos, transcriptómicos, epigenéticos y/o fenotípicos. A nivel poblacional, la heterogeneidad tumoral puede dividirse en intertumoral e intratumoral; la heterogeneidad intertumoral se refiere a los cambios entre pacientes que tienen tumores del mismo linaje histológico y se relacionan con variaciones germinales, en el perfil de mutaciones somáticas, y factores ambientales.
Por otra parte, la heterogeneidad intratumoral puede manifestarse como cambios a nivel espacial, que describen la distribución desigual de subpoblaciones tumorales genéticamente diversas en diferentes sitios de la enfermedad o dentro de una sola enfermedad, sitio o tumor, y como heterogeneidad temporal, un término aplicado a la diversidad genética de un tumor individual a lo largo del tiempo (procesos endógenos (como la replicación del ADN y/o errores de reparación, estrés oxidativo) (40). La Figura 5 describe gráficamente los diferentes tipos de heterogeneidad tumoral.
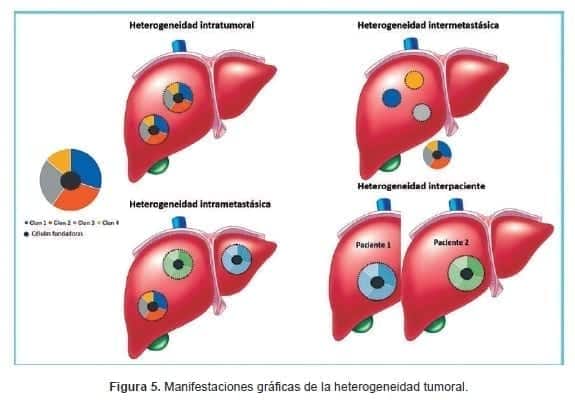
En conjunto, las principales causas de heterogeneidad tumoral son:
la inestabilidad genómica y la evolución y selección clonal. La primera, puede variar en magnitud, desde las sustituciones de una sola base hasta duplicaciones completas del genoma. Tal inestabilidad puede resultar de la exposición a mutágenos exógenos (como radiación UV o humo por combustión de tabaco) y aberraciones en los procesos endógenos (como la replicación del ADN y/o errores de reparación, estrés oxidativo) (40).
Por ejemplo, la inestabilidad microsatelital, relacionada a deficiencias en la reparación del ADN (MMR), impulsa la transformación neoplásica y aumenta sustancialmente la carga de mutaciones somáticas de un subconjunto de cáncer colo rectal (CCR) y otros cánceres con este fenotipo distintivo.
Estudios que involucran el análisis del genoma completo han permitido la identificación de firmas genéticas características asociadas con algunos de estos procesos mutagénicos que favorecen la heterogeneidad.
Por ejemplo, las neoplasias de pulmón ligadas a la exposición al humo por combustión del tabaco están enriquecidos con transversiones C>A y, de manera similar, los CCR deficientes en MMR son más propenso a las transiciones C>T.
Además, aunque no contribuye a la inestabilidad genómica basal:
La exposición a la quimioterapia también puede aumentar el espectro mutacional un tumor generando deregulación genómica. Según ciertas teorías, la tumorigénesis es dependiente de una elevada tasa de mutaciones espontáneas (41).
Esta hipótesis no ha sido probada definitivamente y puede que no sea aplicable a todos los cánceres, aunque los datos de múltiples estudios han demostrado que los cánceres a menudo tienen procesos homeostáticos endógenos con el fin de aumentar la carga mutacional global.
Por ejemplo, la deaminación de citosinas del ADN, resultante de la regulación al alza del mismo a través de la dC → dU-enzima de edición (APOBEC3B) contribuye con la mutagénesis.
La firma mutacional de APOBEC, que se caracteriza por la presencia de mutaciones C>T y C>G en los sitios TpC, está particularmente enriquecida en las etapas avanzadas del desarrollo del tumor, y se hace más prevalente después de la exposición a la quimioterapia.
Los altos niveles de expresión de APOBEC3B presagian un peor resultado entre pacientes con ciertas neoplasias sólidas; por ejemplo, un estudio sobre el análisis de 1.500 muestras de cáncer de seno reveló una asociación entre los altos niveles de expresión de APOBEC3B y una menor supervivencia libre de enfermedad y global.
La inhibición de estas enzimas podría reducir la inestabilidad genética y mejorar así los resultados de los pacientes, en particular, en tumores cerebrales. La inestabilidad genómica también puede conducir a inestabilidad cromosómica por errores de segregación que ocurren durante la división celular, alterando el equilibrio entre la activación de los oncogenes y los genes supresores de tumor (42).
La evolución clonal también puede darse por desequilibrio en el número de copias y por la pérdida uniforme de segmentos cromosómicos que albergan segmentos génicos específicos. Estos hallazgos permiten documentar variaciones intratumorales de orden subclonal que capacitan a las células en derivados más competitivos.
Se han propuesto varios modelos para explicar cómo la diversidad clonal se genera y mantiene, aunque la mayoría continúan utilizando el marco de selección propuesto por Peter Nowell en 1976, basado en la hipótesis de que la iniciación del cáncer ocurre gracias a la ventaja de crecimiento selectivo que conduce a la rápida proliferación.
Posteriormente, la inestabilidad genómica de la población de tumores en expansión crea más diversidad genética que está sujeta a presiones de selección evolutiva, lo que resulta en la emergencia secuencial de células cada vez más anormales genéticamente. La evolución lineal de la enfermedad permite la adquisición sucesiva de mutaciones que proporcionan superioridad sobre el ancestro común.
Alternativamente, la evolución ramificada denota la aparición y propagación divergente de múltiples poblaciones de células tumorales subclonales que comparten un ancestro común. La evolución ramificada permite un mayor nivel de oportunidad para crear un tumor heterogéneo. La mayoría de las neoplasias sólidas optan por un patrón ramificado de evolución, mientras las hematológicas invocan la secuencia lineal. Curiosamente, estos supuestos han sido desafiados por la necesidad de cooperación celular entre distintos subclones para la propagación tumoral (43).
Vías de señalización
A pesar de la inmensa complejidad de los genomas tumorales, progresivamente hemos adquirido la capacidad de controlar algunos de los genes conductores, como lo demuestran las respuestas en pacientes con alteraciones particulares en EGFR (receptor para el factor de crecimiento epidérmico), ALK (quinasa del linfoma anaplásico) y BRAF (homólogo B del oncogén viral del sarcoma murino v-Raf), entre otros (44).
Aunque transitorias, significan que la interferencia con un solo producto génico mutado es suficiente para detener temporalmente la evolución de la enfermedad. Hay dos conceptos esenciales al momento de considerar esta información para sustentar el uso de la oncología de precisión.
Primero, el 99% de las alteraciones genéticas del cáncer (incluidas las mutaciones puntuales, alteraciones en el número de copias, translocaciones y cambios epigenéticos distribuidos a lo largo del genoma, no solo en las regiones codificantes), como se expuso previamente, son irrelevantes para la neoplasia. Son simplemente cambios pasajeros que marcan el tiempo que ha transcurrido entre las sucesivas expansiones clonales.
Sin embargo, las células normales están programadas para ejecutar la muerte celular en respuesta a tales alteraciones, quizás como mecanismo protector contra el cáncer. Por el contrario, las células tumorales han evolucionado para tolerar la complejidad estructural del genoma mediante la adquisición de cambios en genes como TP53 (45).
Por tanto, la complejidad genómica es, en parte, el resultado del cáncer, más que la causa.
(Lea También: Perspectiva Histórica de la Oncología Gastrointestinal)
También hay cierto orden en el caos de las neoplasias.
Las mutaciones en los genes conductores causan una ventaja de crecimiento selectivo, ya sea directa o indirectamente, y siempre a través de un número limitado de vías de señalización celular (todos se pueden clasificar en 12 vías). El descubrimiento de los componentes moleculares de estas vías es uno de los mayores logros de la investigación biomédica, un tributo a los investigadores que trabajan en campos que abarcan la bioquímica, la biología celular, y el cáncer.
Estas vías pueden organizarse en sí mismas en tres procesos celulares centrales incluyendo el devenir celular, la supervivencia, y el mantenimiento del genoma. Numerosos estudios han demostrado la relación opuesta entre la división y diferenciación celular. Las células activas que son responsables de poblar los tejidos normales no se diferencian, y viceversa. La ventaja de crecimiento selectivo esta favorecida por la actividad de vías que incluyen APC, HH y NOTCH, que son bien conocidas por controlar el destino celular. Los genes que codifican las enzimas modificadoras de la cromatina también pueden incluirse en esta categoría (46).
En el desarrollo normal, el cambio hereditario de la división a la diferenciación no está determinado por la mutación, como ocurre en el cáncer, sino por las alteraciones epigenéticas que afectan al ADN y las proteínas de la cromatina.
Aunque las células neoplásicas se dividen de forma anormal
Debido a sus alteraciones autónomas, las células estromales que las rodean son perfectamente normales y no siguen el mismo ritmo. La ramificación más obvia de esta asimetría es la vasculatura anormal de los tumores (47).
A diferencia de la red bien ordenada de arterias, venas y linfáticos que controlan las concentraciones de nutrientes en los tejidos normales, el sistema vascular en los cánceres es tortuoso y carece de uniformidad estructural. Las células normales están siempre a menos de 100 μm de un capilar, pero esto no es cierto para las células tumorales (48).
Como resultado, una célula neoplásica que adquiera una mutación que le permita proliferar bajo concentraciones limitantes de nutrientes y oxígeno tendrá una ventaja de crecimiento selectivo, prosperando en entornos claramente hostiles que exigen adaptación.
Las mutaciones que sustentan la supervivencia a través de vías de señalización están relacionadas con los genes EGFR, HER2, FGFR2, PDGFR, TGFbR2, MET, KIT, RAS, RAF, PIK3CA y PTEN.
Algunos de estos genes codifican receptores para los propios factores de crecimiento, mientras que otros transmiten la señal directamente al interior de la célula, estimulando el crecimiento cuando se activa.
Por ejemplo, las mutaciones en los genes KRAS o BRAF confieren a las células anormales la capacidad de crecer en concentraciones de glucosa inferiores a las requeridas para el crecimiento de células normales (49).
La progresión a través del ciclo celular (y su antítesis, la apoptosis) puede controlarse directamente mediante metabolitos intracelulares y los genes impulsores que regulan directamente el ciclo celular o la apoptosis, como CDKN2A, MYC y BCL2, a menudo están mutados en paralelo.
Otro gen cuyas mutaciones potencian la supervivencia celular es VHL, cuyo producto estimula la angiogénesis mediante la secreción del factor de crecimiento vascular endotelial (VEGF) y con el relacionado con la hipoxia (HIF1).
Las vías de conducción intracelular relacionadas con el mantenimiento del genoma son esenciales para mantener el microambiente interno de la célula tumoral y su estabilidad genómica. Por tanto, no es de extrañar que mutaciones en los genes que mantienen o anulan puntos de control, como TP53 y ATM, favorecen la proliferación (50).
Conclusiones
Aunque la secuenciación del genoma del cáncer es un esfuerzo relativamente nuevo, ha tenido un enorme impacto en la atención clínica de los pacientes con diversas neoplasias.
El reconocimiento de que ciertos tumores contienen mutaciones activadoras en genes conductores que codifican proteínas quinasas ha llevado al desarrollo de fármacos inhibidores específicos (51).
Ejemplos representativos de este tipo de medicina basada en el genoma incluyen el uso de inhibidores del EGFR, BRAF y ALK antes mencionados. Solo una fracción de los pacientes con cáncer de pulmón tienen mutaciones en el gen EGFR o translocaciones de ALK, y responderán a los medicamentos blanco dirigidos. Sin embargo, la genómica ha identificado 16 blancos potenciales en desarrollo para la misma enfermedad, alcanzando diferentes líneas para cada ámbito (52).
Un segundo tipo de medicina basada en la genómica se centra en los efectos secundarios y el metabolismo de los agentes terapéuticos, más que en las alteraciones genéticas a las que se dirigen.
En la actualidad, la dosis de los medicamentos contra el cáncer se basa en el área de superficie, pero la proporción terapéutica o biológica efectiva depende de la interacción génica.
De manera óptima, la evaluación del genoma permitirá realizar mediciones farmacocinéticas de las concentraciones biológicamente activas en cada paciente (53).
El costo adicional de tales análisis sería menor en comparación con los costos exorbitantes de los medicamentos, que se estima en US$200.000 – US$300.000 por año de calidad de vida ganado con calidad.
Referencias
-
1. Dulbecco R. A turning point in cancer research: sequencing the human genome. Science. 1986; 231(4742): 1055-6.
-
2. Robertson M. The proper study of mankind. Nature. 1986; 322(6074):11.
-
3. Futreal PA, Coin L, Marshall M, et al. A census of human cancer genes. Nat Rev Cancer. 2004; 4(3):177-83.
-
4. Vogelstein B, Papadopoulos N, Velculescu VE, et al. Cancer genome landscapes. Science. 2013; 339(6127): 1546–1558.
-
5. Herceg Z, Hainaut P. Genetic and epigenetic alterations as biomarkers for cancer detection, diagnosis and prognosis. Mol Oncol. 2007;1(1):26–41.
-
6. Sadikovic B, Al-Romaih K, Squire JA, Zielenska M. Cause and consequences of genetic and epigenetic alterations in human cancer. Curr Genomics.2008;9(6):394–408.
-
7. Stankiewicz P, Lupski JR. Structural variation in the human genome and its role in disease. Annu Rev Med. 2010;61:437–455.
-
8. Talpaz M, Silver RT, Druker BJ, Goldman JM, Gambacorti- Passerini G, Guilhot BJ et al. Imatinib induces durable hemato-logic and cytogenetic responses in patients with accelerated phase chronic myeloid leukemia: results of a phase 2 study. Blood. 2002;99(6):1928–1937.
-
9. Eckschlager T, Pilat D, Kodet R, et al. DNA ploidy in neuroblastoma. Neo-plasma. 1996;43(1):23–26.
-
10. Mandahl N, Gustafson P, Mertens F, et al. Cytogenetic aberrations and their prognostic impact in chondrosarcoma. Genes Chromosomes Cancer. 2002;33(2):188–200.
-
11. Orr LC, Fleitz J, McGavran L, et al. Cytogenetics in pediatric low-grade astrocytomas. Med Pediatr Oncol. 2002;38(3):173–177.
-
12. Biswas S, Rao CM. Epigenetics in cancer: fundamentals and beyond. Pharmacol Ther. 2017;173:118–134.
-
13. Chen ZX, Riggs AD. DNA methylation and demethylation in mammals. J Biol Chem. 2011;286(21):18347–18353.
-
14. Chakravarthi BV, Nepal S, Varambally S. Genomic and epigenomic alterations in cancer. Am J Pathol. 2016;186(7):1724–1735.
-
15. Weisenberger DJ. Characterizing DNA methylation alterations from The Cancer Genome Atlas. J Clin Invest. 2014;124(1):17–23.
-
16. Zhao R, Choi BY, Lee MH, et al. Implications of genetic and epigenetic alterations of CDKN2A (p16(INK4a)) in cancer. EBioMedicine. 2016;8:30–39.
-
17. Reddy KB. MicroRNA (miRNA) in cancer. Cancer Cell Int. 2015;15:38.
-
18. Chakraborty C, Sharma AR, Sharma G, et al. The novel strategies for next-generation cancer treatment: miRNA combined with chemotherapeutic agents for the treatment of cancer. Oncotarget. 2018;9(11):10164– 10174.
-
19. Dizdaroglu M. Oxidatively induced DNA damage and its repair in cancer. Mutat Res Rev Mutat Res. 2015;763:212–245.
-
20. Feinberg AP, Koldobskiy MA, Gondor A. Epigenetic modulators, modifiers and mediators in cancer aetiology and progression. Nat Rev Genet. 2016;17(5):284–299.
-
21. Wallace SS, Murphy DL, Sweasy JB. Base excision repair and cancer. Cancer Lett. 2012;327(1–2):73–89.
-
22. Kim YJ, Wilson DM, 3rd. Overview of base excision repair biochemistry. Curr Mol Pharmacol. 2012;5(1):3–13.
-
23. Le DT, Durham JN, Smith KN, et al. Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade. Science. 2017;357(6349):409–413.
-
24. Li SKH, Martin A. Mismatch repair and colon cancer: mechanisms and therapies explored. Trends Mol Med. 2016;22(4):274–289.
-
25. Helleday T, Eshtad S, Nik-Zainal S. Mechanisms underlying mutational signatures in human cancers. Nat Rev Genet. 2014;15(9):585–598.
-
26. Aparicio T, Baer R, Gautier J. DNA double-strand break repair pathway choice and cancer. DNA Repair (Amst). 2014;19:169–175.
-
27. Chang HHY, Pannunzio NR, Adachi N, Lieber MR. Nonhomologous DNA end joining and alternative pathways to double-strand break repair. Nat Rev Mol Cell Biol. 2017;18(8):495–506.
-
28. Katsanis SH, Katsanis N. Molecular genetic testing and the future of clinical genomics. Nat Rev Genet. 2013;14(6):415–426.
-
29. Futreal PA, Coin L, Marshall M, et al. A census of human cancer genes. Nat Rev Cancer. 2004 ; 4(3):177-83.
-
30. Tokheim CJ, Papadopoulos N, Kinzler KW, et al. Evaluating the evaluation of cancer driver genes. Proc Natl Acad Sci U S A. 2016;113(50):14330-14335..
-
31. Parsons DW, Jones S, Zhang X, et al. An integrated genomic analysis of human glioblastoma multiforme. Science. 2008; 321(5897):1807-12.
-
32. Hou AH, Tien HF. Genomic landscape in acute myeloid leukemia and its implications in risk classification and targeted therapies. J Biomed Sci. 202021;27(1):81.
-
33. Chen G, Cai Z, Dong X, et al. Genomic and Transcriptomic Landscape of Tumor Clonal Evolution in Cholangiocarcinoma. Front Genet. 2020;11:195.
-
34. Yang H, Ye D, Guan KL, et al. IDH1 and IDH2 mutations in tumorigenesis: mechanistic insights and clinical perspectives. Clin Cancer Res. 2012;18(20):5562-71.
-
35. Ley TJ, Ding L, Walter MJ, et al. DNMT3A mutations in acute myeloid leukemia. N Engl J Med. 2010;363(25):2424-33.
-
36. Varela I, Tarpey P, Raine K, et al. Exome sequencing identifies frequent mutation of the SWI/SNF complex gene PBRM1 in renal carcinoma. Nature. 2011;469(7331):539-42.
-
37. Shain AH, Pollack JR. The spectrum of SWI/SNF mutations, ubiquitous in human cancers. PLoS One. 2013; 8(1):e55119.
-
38. Kobrinski DA, Yang H, Kittaneh M. BAP1: role in carcinogenesis and clinical implications. Transl Lung Cancer Res. 2020;9(Suppl 1):S60-S66.
-
39. Li Y, Shi J, Yang J, et al. Uveal melanoma: progress in molecular biology and therapeutics. Ther Adv Med Oncol. 2020 Oct 22;12:1758835920965852.
-
40. Yoshida K, Sanada M, Shiraishi Y, Nowak D, Nagata Y, Yamamoto R et al. Frequent pathway mutations of splicing machinery in myelodysplasia. Nature. 2011;478(7367):64-9.
-
41. Dagogo-Jack I, Shaw AT. Tumour heterogeneity and resistance to cancer therapies. Nat Rev Clin Oncol. 2018;15(2):81-94.
-
42. Burrell RA, McGranahan N, Bartek J, Swanton C. The causes and consequences of genetic heterogeneity in cancer evolution. Nature. 2013;501(7467):338-45.
-
43. Turner NC, Reis-Filho JS. Genetic heterogeneity and cancer drug resistance. Lancet Oncol. 2012 ;13(4):e178- 85. Mar 30.
-
44. Venkatesan S, Swanton C, Taylor BS, Costello JF. Treatment-Induced Mutagenesis and Selective Pressures Sculpt Cancer Evolution. Cold Spring Harb Perspect Med. 2017;7(8):a026617.
-
45. Zhang Y, Ma Y, Li Y, et al. Comparative analysis of cooccurring mutations of specific tumor suppressor genes in lung adenocarcinoma between Asian and Caucasian populations. J Cancer Res Clin Oncol. 2019;145(3):747- 757.
-
46. Ljungman M, Lane DP. Transcription – guarding the genome by sensing DNA damage. Nat Rev Cancer. 2004;4(9):727-37.
-
47. Perrimon N, Pitsouli C, Shilo BZ. Signaling mechanisms controlling cell fate and embryonic patterning. Cold Spring Harb Perspect Biol. 2012;4(8):a005975.
-
48. Baish JW, Stylianopoulos T, Lanning RM, Kamoun WS, Fukumura D, Munn L et al. Scaling rules for diffusive drug delivery in tumor and normal tissues. Proc Natl Acad Sci U S A. 2011; 108(5):1799-803.
-
49. Turner N, Grose R. Fibroblast growth factor signalling: from development to cancer. Nat Rev Cancer. 2010; 10(2):116-29.
-
50. Yun J, Rago C, Cheong I, et al. Glucose deprivation contributes to the development of KRAS pathway mutations in tumor cells. Science. 2009; 325(5947):1555-9.
-
51. Medema RH, Macůrek L. Checkpoint control and cancer. Oncogene. 2012; 31(21):2601-13.
-
52. Bertier G, Carrot-Zhang J, Ragoussis V, Joly Y. Integrating precision cancer medicine into healthcare—policy, practice, and research challenges. Genome Med. 2016; 8(1):108.
-
53. Malone ER, Oliva M, Sabatini PJB, Stockley TL, Siu LL. Molecular profiling for precision cancer therapies. Genome Med. 2020;12(1): 8.
-
54. McLeod HL. Cancer pharmacogenomics: early promise, but concerted effort needed. Science. 2013; 339(6127):1563-6.
Recibido: Noviembre 26, 2020
Aceptado: Noviembre 26, 2020
Correspondencia:
Andrés F. Cardona
cardona@clinicadelcountry.com