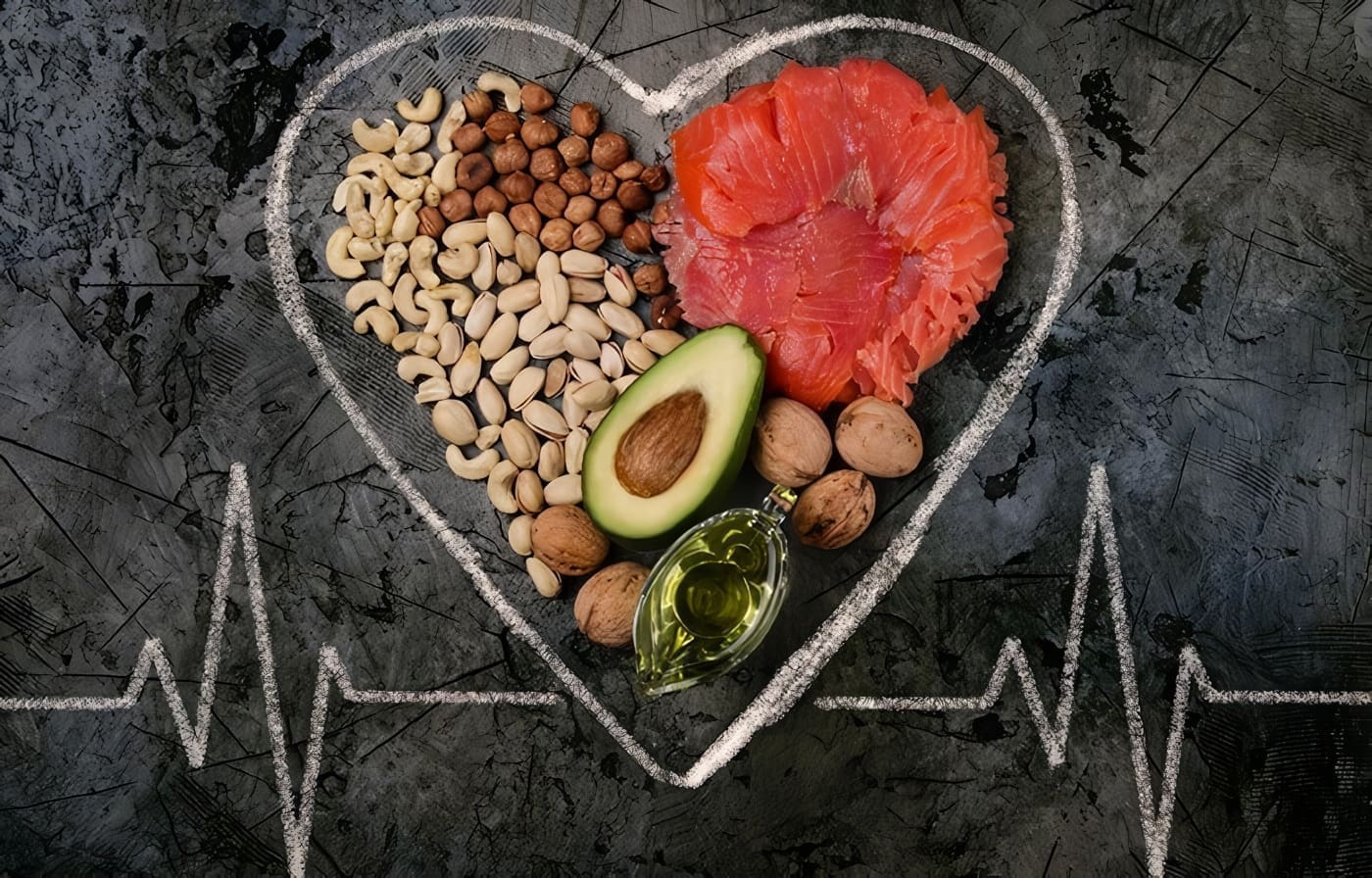Fisiología del Hipotálamo, Pineal y Neurohipófisis
Autor: Alfredo F. Jácome-Roca, MD
Existe una estrecha relación entre los sistemas nervioso y endocrino y buena parte de esta organización neuroendocrina está constituida por el hipotálamo y la hipófisis. Si bien a este último órgano se le ha llamado “la glándula maestra”, al primero se le ha denominado “el poder detrás del trono”, que a su vez se relaciona por medio de neurotransmisores y vías con estructuras nerviosas superiores. Esto hace que pequeñas señales originadas en tejido neurológico sean amplificadas enormemente cuando –primero la pituitaria, luego los órganos endocrinos periféricos y finalmente diversos tejidos del organismo- reciben el influjo de las diferentes hormonas que se van originando en cada uno de estos niveles de los diferentes ejes endocrinos.
Generalidades
Existe una estrecha relación entre los sistemas nervioso y endocrino y buena parte de esta organización neuroendocrina está constituida por el hipotálamo y la hipófisis. Si bien a este último órgano se le ha llamado “la glándula maestra”, al primero se le ha denominado “el poder detrás del trono”, que a su vez se relaciona por medio de neurotransmisores y vías con estructuras nerviosas superiores. Esto hace que pequeñas señales originadas en tejido neurológico sean amplificadas enormemente cuando –primero la pituitaria, luego los órganos endocrinos periféricos y finalmente diversos tejidos del organismo- reciben el influjo de las diferentes hormonas que se van originando en cada uno de estos niveles de los diferentes ejes endocrinos.
Anatomía
El cerebro o encéfalo tiene una gran masa superior denominada prosencèfalo, compuesto principalmente por el telencèfalo –prácticamente constituido por los dos hemisferios cerebrales y los dos ventrículos laterales- y por el diencèfalo; este último es la parte cerebral alrededor del tercer ventrículo e incluye el tálamo (dos grandes masas de sustancia gris a cada lado del tercer ventrículo), los cuerpos geniculados medio y lateral, la glándula pineal y el hipotálamo.
Otras partes cerebrales hacia abajo y atrás son el mesencèfalo (pedúnculos cerebrales y tectum), con neuronas monoaminèrgicas que se conectan con el hipotálamo y con el sistema lìmbico talàmico. También está el romboencèfalo, compuesto por el cerebelo, la protuberancia anular y el bulbo raquídeo, cuya continuación es la medula espinal.
El hipotálamo está restringido a la parte anterior del piso y la parte inferior de las paredes laterales del tercer ventrículo. Hacia delante está delimitado por el quiasma óptico, hacia atrás por los cuerpos mamilares, a los lados por los surcos formados con los lóbulos temporales y hacia arriba se separa del tálamo por el surco hipotalàmico.
La base redondeada y lisa del hipotálamo se denomina tuber cinereum, una capa de sustancia gris. El llamado infundíbulo o tallo neural está constituido por la eminencia media (o parte central del tuber, donde se producen las hormonas hipofisiotropas) y por un desprendimiento del tuber llamado pedículo infundibular; este último forma con la parte tuberal adenohipofisiaria el tallo pituitario (que como vemos, es parcialmente tejido nervioso y en parte además, tejido epitelial. La eminencia media y la neurohipòfisis constituyen -junto con la pineal, el órgano subcomisural (con su fibra de Reissner) y la medula suprarrenal- las glándulas neuroendocrinas.
Circulación Portal hipotálamo-hipofisiaria.
 La sangre de la zona túbero-infundibular proviene de la arteria hipofisiaria superior, que se origina en la carótida interna. De dicha arteria superior se forma el plexo capilar primario que rodea la eminencia media –al que se vierten las hormonas hipofisiotropas, sin pasar por la circulación general- cuyas células endoteliales son fenestradas, con diámetro suficiente como para que estos capilares se llamen sinusoides.
La sangre de la zona túbero-infundibular proviene de la arteria hipofisiaria superior, que se origina en la carótida interna. De dicha arteria superior se forma el plexo capilar primario que rodea la eminencia media –al que se vierten las hormonas hipofisiotropas, sin pasar por la circulación general- cuyas células endoteliales son fenestradas, con diámetro suficiente como para que estos capilares se llamen sinusoides.
Las terminaciones axónicas de las neuronas secretoras se sitúan muy próximas a la membrana basal de estos capilares, que luego se unen para formar venas portas largas –el sistema porta propiamente dicho- que atraviesan el tallo neural formando luego el plexo capilar secundario, que está en íntima relación con las células de la adenohipófisis.
La sangre venosa sale de la hipófisis por diversas venas que van a desembocar en los senos cavernosos. Aunque la irrigación de la neurohipòfisis proviene directamente de la arteria hipofisiaria inferior, la sangre de ambos lóbulos es drenada –a través de venas eferentes- al seno cavernoso; la de la adeno-hipófisis va a estas venas eferentes a través de las venas portas cortas. La inervación pituitaria viene del plexo carotìdeo, cumpliendo una función vasomotora.
El control neural de la hipófisis está dado por varios tipos de neuronas. Unas –que son peptidèrgicas- pertenecientes a los tractos supraòptico-hipofisiario y paraventrìculo-hipofisiario, con núcleos hipotalàmicos magnocelulares que producen sus hormonas (vasopresina y ocitocina) y con axones cuyas terminaciones nerviosas las depositan en el lóbulo neural. Otras -también peptidèrgicas- con núcleos mediales y tractos tùbero-pituitarios; de estas, unas terminan en la eminencia media y allí se depositan las hormonas hipofisiotropas -en relación anatómica con los vasos porta- y otras lo hacen en la parte baja del tallo.
Entre las neuronas monoaminèrgicas, unas terminan cerca del núcleo de otras de tipo peptidèrgico y otras -también monoaminèrgicas- al finalizar cerca de los terminales de las peptidèrgicas dan una transmisión axo-axònica. Hay las que sirven de unión funcional entre las neuronas peptidèrgicas hipotalàmicas y el resto del cerebro. El control de la neurohipòfisis es de tipo colinèrgico, mientras que el de la adenohipòfisis es adrenèrgico.
Las neuronas monoaminèrgicas segregan dopamina, nor-epinefrina y serotonina. El control del hipotálamo por centros nerviosos superiores está dado en algunos casos por fibras dopaminèrgicas que se encuentran en el núcleo arcuado (región ventromedial del hipotálamo), en otros casos por vías nor-adrenèrgicas que se originan en el núcleo tùbero-hipofisisiario y en el mesencèfalo. Los tres tipos de fibras monoaminèrgicas que van al sistema lìmbico se originan dentro de la última estructura mencionada, que contribuye además con una vía serotoninèrgica al núcleo supraquiasmàtico del hipotálamo; rutas neurales más convencionales logran el efecto del sistema lìmbico sobre el hipotálamo.
La pineal (o epífisis) es parte del sistema neuroendocrino, aunque es relativamente independiente de los ejes hormonales que se inician en el hipotálamo. La pineal es un cuerpo pequeño en forma de cono de pino (de ahì su nombre), adherido al techo del tercer ventrículo, cerca del área de la comisura posterior. Está compuesta por tejido conectivo vascularizado, neuroglia y células de tamaño variable (pinealocitos), de núcleo pálido, citoplasma argiròfilo granular y escasos procesos citoplasmáticos. Se cree que los pineocitos son un tipo de neuroglia modificada, ya que no toman los colorantes clásicos para visualizarlas. La pineal recibe fibras de la estría medular talàmica, la habènula y la comisura posterior. En la evolución, la pineal fue un órgano visual en el hombre y en los anfibios.
En el capítulo sobre el sistema neuro (inmuno) endocrino difuso mencionaremos las células APUD -de origen neuro-ectodérmico- al que pertenecen tanto las glándulas neuroendocrinas aquí mencionadas como otras células diseminadas en el organismo, particularmente en el aparato digestivo.
Hormonas hipotalámicas, neurohipofisiarias y de la pineal
Con frecuencia el hipotálamo y la hipófisis se estudian juntos, merced a su estrecha relación. En aras del equilibrio entre los capítulos de este libro, hemos resuelto discutir el tema de la pituitaria anterior por aparte, limitándonos acá a las neurohormonas como tal.
Cada hormona adeno-hipofisiaria tiene su correspondiente hormona hipofisiotropa liberadora y/o inhibidora en el hipotálamo; cada una de las hormonas hipofisiotropas está codificada por su correspondiente gen, pero este se expresa en más de un tejido, y el comportamiento de la hormona producida en tejidos extrahipotalàmicos puede ser diferente. Aunque esto se refiere a tejidos sanos, explica en parte la situación de la producción hormonal paraneoplàsica
Tanto las hormonas tròficas como otras de estructura proteica tienen presentaciones comerciales (obtenidas por medio de tecnología de DNA recombinante), pues tienen utilidad terapéutica o diagnóstica. Los ejes clásicos hipotálamo-hipófisis-glándula periférica son los de las suprarrenales, la tiroides y las gonadas. La corticorrelina o CRH regula la producción de ACTH, que a su vez controla la producción de glucocorticoides y andrógenos de la corteza suprarrenal, pero tiene poca influencia sobre los mineralocorticoides; la tirorrelina o TRH estimula la producción de TSH, la que a su vez lo hace sobre la T4 y la T3. Una sola hormona tròfica –la gonadorrelina, GnRH o LH-RH, regula las dos gonadotrofinas –FSH y LH- en ambos sexos.
La hormona del crecimiento se libera por acción de la somatorrelina o GHRH – y luego a travès del IGF-1 (antes denominada muy lógicamente “somatomedina”) actúa en los tejidos blanco; su liberación es frenada por la somatostatina o GHR-IH, mientras que la dopamina o PIH, inhibe la liberación de prolactina; estas hormonas son somatomamotropas, al igual que la somatomamotrofina coriònica (que nuevamente fue llamado inicialmente con lógica, el “lactògeno placentario”). La MSH -estrechamente ligada al ACTH- (está incluida en sus primeros 13 aminoácidos), hace parte de esta manera con esta y con una lipotropina y una endorfina, en la molécula de la pro-opio-melanocortina (POMC) o prohormona precursora de todos estos pèptidos, tiene una menor importancia en el hombre que en animales inferiores, particularmente en aquellos capaces de mimetizarse o cambiar de colores, como el camaleón; en situaciones clínicas donde el ACTH está elevada (Enfermedad de Addison, Síndrome de Nelson), se observa pigmentación.
Otras neurohormonas de carácter independiente, generadas en el hipotálamo pero depositadas en la pituitaria posterior, son la vasopresina u HAD y la ocitocina, llamada también “hormona eyecto-làctea”. Finalmente, la melatonina se genera en la epífisis. Las hormonas hipofisiotropas se producen en neuronas parvocelulares cuyo núcleo se localiza en el tuber cinereum del hipotálamo, en sitios como el núcleo arqueado y el paraventricular medial. Los axones de estas neuronas terminan en la eminencia media del hipotálamo, donde se liberan los pèptidos hipofisiotropos que son llevados a la pituitaria anterior por medio del sistema porta hipofisiario. Por otro lado las hormonas de la pituitaria posterior son producidas en neuronas magnocelulares que comienzan en el núcleo paraventricular lateral y supraòptico, y viajan a través de los axones para depositarse en la neuro-hipófisis, que –más que un órgano- es una extensión del hipotálamo.
Córtico-relina. La hormona liberadora del ACTH es conocida por la sigla CRH (de “corticotropin-releasing hormone”) y su secreción está regulada por un un mecanismo de retroalimentación negativo determinado por los niveles de cortisol plasmático libre, pero también por transeúntes neurales de asa abierta, de naturaleza circadiana, situaciones de estrés (mediante mecanismos adrenèrgicos), etc. A través del tronco (vías ascendentes) se producen estímulos adrenèrgicos sobre el núcleo paraventricular (donde se produce la CRH) durante el estrés, lo que requiere producción de cortisol, (y otras hormonas contra-reguladoras de la insulina). La CRH induce la producción de pro-opio-melanocortina (POMC), prohormona de molécula grande, que da lugar al ACTH y a la betalipotrofina (que a su vez se divide en gamma-lipotrofina y el opioide beta-endorfina). De allí la acción inhibidora de CRH por opiodes tipo morfina, inhibición que también es dada por la angiotensina, el neuropèptido Y, la interleucina-1 (interrelación del sistema inmune, estrés y liberación de CRH). La arginina-vasopresina tiene acción tipo CRH pues es liberadora de ACTH en condiciones experimentales. La còrticorrelina tiene 41 aminoácidos codificados por un gen del brazo largo del cromosoma 8.
Tiro-relina. La TRH (“Thyrotropin- releasing hormone), libera la TSH. La concentración plasmática de hormona tiroidea libre inhibe más la TSH que la TRH en la retroalimentación negativa. Es un tripèptido (ácido piroglutàmico, histina y prolinamida) cuya administración endovenosa de TRH incrementa los niveles plasmáticos tanto de TSH como de prolactina, situación que también opera en situaciones clínicas de aumento de la tirotrofina, como en el hipotiroidismo primario, en el que no sólo hay hiperprolactinemia en un porcentaje importante de casos, sino incluso galactorrea. Como la TRH hipotalàmica no se afecta por la concentración plasmática de glucosa, y la producida en el páncreas sí, esto indica que probablemente la función de esta hormona en el otro tejido es diferente. La somatostatina por otro lado inhibe la secreción de la TSH.
Gonado-relina. La GnRH (Gonadotropin- releasing hormone) libera las gonadotrofinas FSH y LH, producidas en la pituitaria anterior. Los somas de sus neuronas se encuentran diseminados en el hipotálamo, principalmente en el núcleo arcuado pero también en el área preòptica y en el núcleo paraventricular posterior; sus axones terminan en la eminencia media y bajan por el tracto tùbero-infundibular. Se trata de un decapéptido cuya molécula precursora –la pre-pro-GnRH- que es una proteína de 92 aminoácidos, 56 de los cuales constituyen el péptido asociado (con la GnRH), que tiene una acción inhibidora de prolactina mientras que el decapèptido liberador de FSH y LH lo es también de la prolactina. Otros 23 aminoácidos iniciales sirven de señal, dentro de los cuales 3 (Gli-Lis-Arg) son necesarios para el procesamiento de la molécula. Esta es de vida corta (alrededor de tres minutos) y es muy baja su concentración en la circulación general; se modula su liberación por estímulos nor-adrenèrgicos y se inhibe por retroalimentación de las gonadotrofinas, dopamina y pèptidos opioides tipo endorfinas y encefalinas. La gonadorrelina tiene receptores de membrana en los gonadotrofos, que se internalizan una vez forman un complejo hormona-receptor y después de degradarse dicho complejo, regresan a la superficie celular por un mecanismo de regulación hacia arriba, lo que permite que la GnRH -que en su fase inicial sólo libera gonadotrofinas previamente almacenadas- pueda continuar liberándolas con cantidades menores, lo que permite la liberación en pico de la LH. Durante la primera mitad del ciclo menstrual, la gonadorrelina se libera en pulsos que duran unos pocos minutos y se hacen cada hora y media; en la segunda mitad del ciclo estos pulsos se dan cada tres a cuatro horas. Por este mecanismo, la gonadorrelina administrada por medio de una bomba de infusión se ha utilizado en tratamientos de fertilidad para inducir la ovulación, mientras que sus análogos de larga acción por el contrario bloquean las gonadotrofinas, siendo de utilidad en el manejo de entidades como el cáncer de próstata, la pubertad precoz y la endometriosis. Merced a las conexiones del núcleo arcuado con el sistema lìmbico, las funciones ovulatoria y menstrual se encuentran afectadas por mùltiples factores psíquicos.
Somato-relina. Es la GH-RH (Growth hormone-releasing hormone), producida en el núcleo periventricular del hipotálamo, con axones que finalizan en la eminencia media del tuber cinereum. Actúa en la hipòfisis a travès del segundo mensajero AMPc, pero en los mayores de 40 años, la respuesta es casi nula.
Recientemente se ha descubierto un ligando que estimula la secreción de hormona del crecimiento a través de un receptor huérfano, no del receptor usual de la GHRH hipotalámica. Esta molécular se produce en el estómago y se ha denominado Ghrelina; su hallazgo muestra nuevos caminos en los mecanismos de secreción de hormona del crecimiento.
Somatostatina. Es un polipéptido de 14 aminoácidos, sintetizado por Guillemin. El origen de las neuronas productoras está entre los núcleos peri y paraventricular, y su acción es inhibitoria potente sobre la producción de hormona del crecimiento y algo sobre la TSH. Además se segrega en otros tejidos (aparato digestivo, páncreas –donde inhibe insulina y glucagòn-, gastrina, pepsina y el jugo gástrico en general, por lo que el preparado sintético (u ocreòtido) se indica en diferentes patologías, como el gastrinoma.
Dopamina.
Es una monoamina que actúa como neurotransmisor, como catecolamìnico precursor de la nor-epinefrina y como hormona inhibidora de la secreción de prolactina (PIH) y también de GnRH.
El concepto de los ligandos a los receptores huérfanos ha dado lugar al descubrimiento de nuevos neuro-péptidos como la nociceptina, la orfanina FQ, la orexina y el péptido liberador de la prolactina. Este último interactúa con un receptor huérfano localizado en la adeno-hipófisis y –además de liberar prolactina- es mediador de la respuesta de estrés, a través de la liberación de CRH y por consiguiente de ACTH.
Vasopresina.
Neuronas magno celulares de los núcleos supraòptico y paraventricular segregan tanto vasopresina como ocitocina, las que por estímulos colinèrgicos se sintetizan al tiempo con las neurofisinas I y II –sus proteínas transportadoras- y viajan en forma quántica (empaquetadas en pequeñas vesículas) para depositarse en la hipófisis posterior que tiene el 20% del volumen pituitario o unos 120 mg. La vasopresina –también llamada hormona antidiurética- se libera en esas neuronas osmorreceptoras, que tienen umbral mucho más bajo (osmolalidad por encima de 280) que las neuronas osmorreceptoras del centro de la sed. Estas células nerviosas son primordialmente sensibles a estímulos osmòticos como la deshidratación o el aumento en la concentración de solutos, lo que eleva la osmolalidad plasmática (que fluctúa en un estrecho margen entre 280 y 296 mmol/Kg ) La vasopresina es un nona péptido de 1084 daltons, que posee un anillo formado por cinco aminoácidos cerrados por puentes disulfìdicos de dos cisteìnas (que tienen el papel antidiurético), y una cola de tres aminoácidos que en unos casos es arginina o AVP (en la mayoría de los mamíferos) y otros lisina. La diuresis es máxima cuando la concentración de AVP es de < 1 pmol/L y mínima, con 5 pmol/L, cuando se empiezan a estimular los osmorreceptores de la sed.
Los estímulos no osmòticos (que actúan como factores menores en la liberación de la AVP) son la hipovolemia y la hipotensión; si se reduce el volumen plasmático en 10% se aumenta la liberación de AVP en una respuesta curvilínea, estando localizados en la aurícula izquierda y las grandes venas los barorreceptores de la hipotensión; si la disminución de la tensión arterial es del 40%, los niveles de AVP alcanzan los 100 pmol/L. También aumentan la secreción situaciones como la emesis, la hipoglicemia, la angiotensina II, el dolor intenso, el estrés o las emociones. La acetilcolina, la nicotina, los barbitúricos, la morfina, mediante un mecanismo colinèrgico- hacen (al igual que otros mediadores de la liberación de la AVP) que la hormona antidiurética deje el soma neuronal y viaje por los axones, donde bien se deposita unida a proteínas en el lóbulo posterior o se libera a la circulación para actuar en los órganos blanco; el tiempo entre producción y liberación toma como hora y media y la esta ultima requiere entrada de calcio, liberándose al tiempo con la neurofisina.
La vasopresina ejerce su acción antidiurética en el tùbulo contorneado distal y canales colectores renales, por mediación del AMPc; la reabsorción de agua se estimula por medio de la inserción de canales de agua (llamados acuaporinas), lo que logra el transporte de agua libre hacia la sangre, que lleva a una disminución de la osmolaridad plasmática y a un aumento de la concentración de la orina. Su acción vasopresora (que es mínima en adultos saludables) la logra por el sistema fosfatidil-inositol/calcio, y puede además estimular la liberación de ACTH.
Regulación renal del metabolismo hidroelectrolítico.
El 60% del peso corporal está constituido por agua y este contenido se mantiene estable a pesar de la variabilidad en la ingesta de líquidos o en su pérdida. El filtrado glomerular es isotónico con respecto al plasma; su volumen es de 180 litros en 24 horas, En el tùbulo contorneado proximal se reabsorbe el 85% del sodio por acción de la correspondiente bomba –es decir, es un proceso activo- y el agua se arrastra pues la membrana del nefròn proximal es permeable al agua. Cuando el contenido baja por el asa de Henle a la medula renal –que es hipertónica- la difusión de líquidos lo vuelve hipertónico pero cuando asciende y sale de la medula, por el mecanismo de contracorriente el sodio vuelve a salir (esta vez no acompañado de agua), manteniendo hipertónica la medula renal. En el tùbulo contorneado distal se logra la reabsorción del otro 15% del sodio, por acción de la aldosterona, que intercambia sodio por potasio (e hidrógeno). Allí y en el canal colector la membrana se hace permeable al agua por acción de la vasopresina (formación de microporos) y el agua sale, arrastrada por el sodio. Al final la orina es isotónica, y su volumen diario está alrededor del litro y medio.
Ocitocina. Es una hormona peptìdica de nueve aminoácidos, también llamada “hormona eyecto-láctea”, similar a la vasopresina, que después de un corto tiempo en la circulación es –al igual que esta- se metaboliza en el hígado. Una vez que la mama está preparada por la acción de los estrógenos, progesterona y prolactina, la ocitocina estimula las miofibrillas del pezón y hace sacar la leche, lo que facilita la lactancia. La ocitocina se libera por succión mamaria (lo que estimula también la prolactina) y por la vía colinèrgica. En cuanto a la acción sobre el útero grávido, este se vuelve sensible a la ocitocina cuando el embarazo llega a término, y de desencadenan las contracciones rítmicas del trabajo de parto; su acción sobre el cerebro facilita la conducta maternal de la lactancia, aunque estas dos últimas acciones son –más que esenciales- facilitadoras. En los hombres parece que facilita el transporte espermático en el sistema reproductor masculino. La producción y acciones de la ocitocina son moduladas por los esteroides sexuales.
Melatonina. La luz produce en la pineal un cambio adaptativo; su contenido de serotonina es alto durante el día y bajo en la noche, ocurriendo lo contrario con la concentración de nor-epinefrina. La pineal de los mamíferos responde indirectamente a los estímulos visuales.

Los fotorreceptores de la retina la excitan por medio de ramas nerviosas que se dividen en el quiasma óptico, formando el tracto óptico accesorio inferior. La melatonina es un derivado indòlico que se deriva de la serotonina (ambas aminas provenientes del triptófano) por procesos sucesivos de acetilaciòn y metilaciòn (por acciones de las enzimas N-acetilasa y hidroxi-indol-metiltransferasa), que sufre cambios con la luz. A pesar de que la serotonina se libera a un ritmo constante, se libera más durante la oscuridad, activando a su vez las enzimas mencionadas que la degradarán, las que son activadas a travès de receptores nor-adrenèrgicos, por medio de la adenilciclasa y el AMPc; de esta manera la melatonina se producirá de acuerdo a un ritmo circadiano, que permite niveles bajos mientras haya luz del día, o altos durante la noche; la liberación pre-sináptica de norepinefrina está disminuida por acción de la luz. Existen dos receptores -de membrana, acoplados a proteínas G- de melatonina en los mamíferos (Mel 1A y Mel 1B), expresados diferencialmente en diversos tejidos, posiblemente con diferentes efectos biológicos. Hay mayor densidad de estos receptores en el núcleo supraquiasmàtico del hipotálamo, en la adenohipòfisis tuberal y en la retina. La melatonina inhibe la GnRH, y por tanto la LH y la FSH; la pineal de mamíferos como caballos y ovejas, o en roedores, es capaz de medir la duración del día (más largo en el verano, más corto en el invierno), lo que se llama el “fotoperiodo”; de acuerdo a esto, la pineal regula la secreción de melatonina, aumentada en la noche. De esta manera estos animales reconocen que clase de estación está presente, pues en la estación (que para determinado animal es la reproductiva) las gonadas se rejuvenecen, y en la estación no reproductiva, las gonadas permanecen inactivas. Una oveja se reproduce una vez al año, pero merced a la melatonina, puede tener dos embarazos al año.
A pesar del interés que ha generado la melatonina en el tratamiento del insomnio, esta hormona no es un regulador del patrón normal de sueño, aunque si tiene algún efecto. En los viejos con insomnio, su secreción es menor que en los viejos que no lo padecen, por lo que cabría la melatonina como tratamiento, aunque su efecto es modesto. En las personas que hacen turnos nocturnos, la melatonina no ha resultado muy efectiva para que puedan dormir de día. En los viajeros que sufren del “jet lag”, la administración de melatonina hacia el momento cuando oscurecerá en el sitio de llegada, puede aliviar los síntomas. En dosis altas, la melatonina disminuye la actividad motora, induce cansancio e hipotermia, lo que facilitaría el sueño. En animales inferiores, la distribución del pigmento melànico se altera por la administración de pineal del ganado, aclarándose el color de su piel o volviéndose casi transparentes, este efecto no se observa en mamíferos o en los pájaros.
Funciones no hormonales del Hipotálamo
Numerosas y complejas funciones no hormonales se llevan a cabo en el hipotálamo, entre ellas la regulación del apetito y de la saciedad (y por lo tanto del peso corporal), de la temperatura (pues tiene neuronas sensibles al calor y el frío), el sueño y el sistema nervioso autónomo simpático y para simpático. Diversos pèptidos, neurotransmisores y citoquinas intervienen en la regulación de estos procesos fisiológicos, al tiempo que lesiones hipotalàmicas experimentales o patológicas pueden inducir cambios en todas estas funciones. Los cambios en la osmolaridad –manifestados por sed- también inducen su control hipotalàmico a travès de la hormona antidiurética.
Patología
La diabetes insípida (DI) o enfermedad con grandes volúmenes urinarios, donde no se produce deshidratación mientras el mecanismo de la sed se mantenga intacto, es idiopàtica en una tercera parte de los casos, debida a trauma o lesión intracraneana (transitoria) en otra tercera parte, mientras que los casos restantes son nefrogènicos, donde existe resistencia a la hormona antidiurética. Una de las causas de hiponatremia crónica es el llamado “síndrome de secreción inapropiada de ADH”, en donde la orina es hipertónica.
La destrucción de la pineal por intervención quirúrgica o por tumor produce deficiencia de la LH y pubertad precoz. Si a las mujeres con ciclos anovulatorios u oligomenorrea se les hace dormir con la luz encendida, su trastorno tiende a corregirse. Los tumores pineales son primarios o metastáticos, que se diagnostica en personas prepùberes en un 10 a 15%, en quienes sólo en un tercio se ve la pubertad precoz. Algunos dicen que la producción de este trastorno endocrino en pinealomas es debida a la compresión que ejercen sobre el hipotálamo. Otros síntomas que aparecen son somnolencia, hiperfagia, diabetes insípida, obesidad y trastornos emocionales. Estos tumores a veces producen síntomas de hipertensión endocraneana e hidrocéfalo. En los pinealomas es clásico observar el síndrome de Parinaud, en el cual el paciente es incapaz de mirar hacia arriba por esfuerzo voluntario. Hay además anormalidades pupilares, de la acomodación, retracción de párpados y nistagmo opto cinético.
Terapéutica
En las dos primeras clases de DI, el manejo es con vasopresina; para el manejo crónico en la idiopàtica se usaba la solución oleosa, y ahora la que se administra por vía nasal; para el manejo agudo en casos neurológicos, o en neurocirugía, se usa la solución acuosa para evitar la hiponatremia dilucional. En la variedad nefrogènica, la idea es causar una baja relativa de sodio por medio de dieta hiposòdica y administración de diuréticos tiazìdicos, lo que logran disminuir la poliuria en un 50%, haciéndola más tolerable.
El tratamiento de los pinealomas es quirúrgico. Como fisiológicamente la melatonina se produce durante la oscuridad, esta hormona se usa para el tratamiento del insomnio.
Historia
El sistema porta hipotálamo-hipofisiario fue descubierto en una morgue de Bucarest, cuando en 1927 el patólogo Rainer observó el plexo vascular que rodeaba el tallo y vio cómo este era especialmente prominente en personas que habían muerto súbita y violentamente; le sugirió entonces a estudiante Popa que continuara investigando, lo que él hizo removiendo el hipotálamo y la hipófisis en bloque. Wisloki encontró un sistema parecido en animales inferiores y Harris hizo estudios novedosos que le dieron impulso a la neuroendocrinología. La pineal ha sido por siglos una glándula misteriosa, ya que aunque se le han asignado muchas funciones posibles (Aristóteles la consideraba el asiento del alma), realmente es una pequeña estructura que precozmente se calcifica, y que está enclavada en el centro del cerebro aparentemente sin ningún propósito. Su vinculación con la endocrinología tiene relación con la aparición de pubertad precoz en algunos casos de pinealoma y la producción de melatonina.
Referencias seleccionadas
Van der Lely AJ, et al. Biological, physiological, pathophysiological and pharmacological aspects of Ghrelin. Endocrine Reviews. 2004 25: 426-457.
Kaltsas GA, et al. The diagnosis and medical management of advanced neuroendocrine tumors. Endocrine Reviews. 2004 25: 458-511.
Millar RP et al. Gonadotropin-releasing hormone receptors Endocrine Reviews. 2004 25: 235-275.
Ben-Jonathan N, et al. Dopamine as a prolactin (PRL) inhibitor. Endocrine Reviews. 2001 22: 724-763.
Smith KA, Schoen MW, Czeisler CA. Adaptation of human pineal melatonin suppression by recent photic history.Journal of Clinical Endocrinology and Metabolism. 2004; 89(7):3610-4
Kiss A, Adameova A, et al. Effect of immobilization on in vitro thyrotropin-releasing hormone release from brain septum in wild-type and corticotropin-releasing hormone knock-out mice. Annals of the New York Academy of Sciences. 2004;1018:207-13.
Racine MS, et al. Augmentation of growth hormone secretion after testosterone treatment in boys with constitutional delay of growth and adolescence: evidence against an increase in hypothalamic secretion of growth hormone-releasing hormone. Journal of Clinical Endocrinology and Metabolism. 2004; 89(7):3326-31.
Dunser MW, Werner ER, et al. Arginine vasopressin and serum nitrite/nitrate concentrations in advanced vasodilatory shock. Acta Anaesthesiologica Scandinavica. 2004;48(7):814-9.
Cassoni P, et al. Oxytocin and oxytocin receptors in cancer cells and proliferation. Journal of Neuroendocrinology. 2004;16(4):362-4.
Kalliomaki ML, et al. Prolactin-releasing peptide affects pain, allodynia and autonomic reflexes through medullary mechanisms.Neuropharmacology. 2004;46(3):412-24.
Barón-Castañeda G. Fundamentos de endocrinología ginecológica.Contacto Gráfico, Bogotá, 1998.
Bowen R. The pineal gland and melatonin. 2003. https://arbl.cvmbs.colostate.edu/
Raff H. Secretos de la Fisiología. Editorial McGraw-Hill Interamericana. México, 2000.
Strbak V, et al. Comparison of pancreatic and hypophysiotropic TRH systems. Physiol Res 2000. 49(S1): S71-S78.