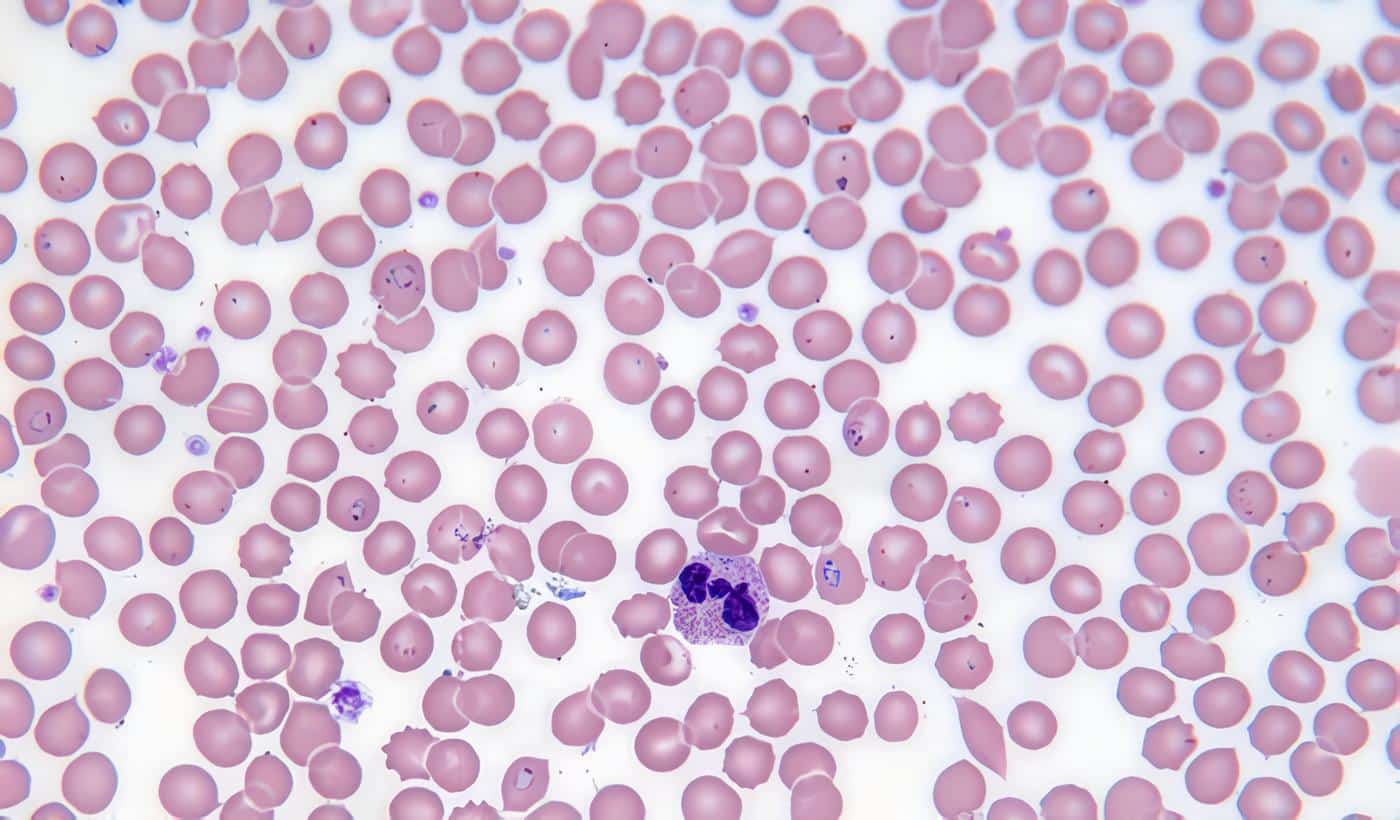
Técnicas y Procedimientos de Laboratorio en Malaria
Las siguientes son las recomendaciones mínimas necesarias para el diagnóstico de la malaria por el laboratorio. (Lea también: Procedimientos en Salud Pública de la Malaria)
• El área de toma de muestras debe permanecer idealmente limpia, ordenada y libre de polvo
• La toma de muestras debe hacerse siguiendo las normas generales de asepsia y antisepsia
• Las láminas de vidrio a emplear deben estar meticulosamente limpias con agua y jabón, así como desengrasadas con alcohol
• La solución colorante de trabajo será siempre de preparación reciente, a diferencia de las soluciones madre, las cuales pueden almacenarse durante mucho tiempo
• El momento de toma de la muestra de sangre es independiente de la presencia del pico febril en el paciente
• El diagnostico idealmente se realiza por medio de gota gruesa y extendido, en los cuales se debe visualizar el parasito. Sin embargo, el examen de rutina debe ser la gota gruesa debido a su mayor sensibilidad, pues concentra la muestra de seis a veinte veces más que el extendido; por tanto, es posible detectar entre 5 y 10 parásitos/ul de sangre. Esto lo hace muy adecuado en el caso de parasitemias bajas.
También facilita el diagnostico de infecciones mixtas o asociaciones parasitarias
• En algunas ocasiones en que las parasitemias son muy bajas (pacientes seminmunes, tratamiento previo, etc.), es necesario el examen de sangre periférica diario seriado (aun hasta cada seis horas) para poder establecer el diagnostico
• Es preferible el uso de un microscopio binocular con fuente de luz halógena incorporada, con filtro azul, óptica no brillante y objetivos planacromáticos, ya que la iluminación es un factor crítico cuando se usa el objetivo de inmersión
• En los casos de pacientes de la Costa Pacifica o procedentes de esta región es conveniente elaborar, además de la gota gruesa, el extendido de sangre periférica para descartar una infección por P. malariae.
2.1 Toma de Muestras
• Llenar ficha epidemiológica
• Tomar muestra en un área física ordenada
• Marcar la lamina en el borde esmerilado o rotular con cinta de enmascarar
• Con manos enguantadas realizar la limpieza del dedo del corazón o índice del paciente, con algodón mojado en alcohol (en el caso de niños se puede tomar el dedo gordo del pie, el talón o el lóbulo de la oreja) dejar secar y puncionar con lanceta estéril desechable el borde lateral del dedo a la altura del nacimiento de la una
• Limpiar la primera gota de sangre con algodón seco; presionar el dedo y colocar la siguiente gota a un centímetro de la marca de la lámina portaobjetos; poner en contacto la lamina con la gota de sangre, de manera delicada, evitando que la lamina toque el dedo del paciente. Realizar dos láminas de gota gruesa por paciente
• Extender la gota de sangre para formar un cuadrado de aproximadamente 1 cm x 1 cm y un grosor y homogeneidad adecuados y así obtener un mayor número de campos microscópicos ideales. Para realizar un extendido, presionar el dedo para obtener una nueva gota de sangre del paciente
• Dejar secar la gota de sangre a la temperatura ambiente en una superficie plana y libre de polvo. Limpiar con alcohol la lamina utilizada para realizar las gotas gruesas para evitar contaminar las siguientes muestras.
• Colorear con alguna de las coloraciones derivadas de Romanowsky
• Observar al microscopio con objetivo de 10x y 40x para la selección de los campos donde se encuentre mayor número de glóbulos blancos. Posteriormente, mirar con objetivo de 100x y buscar las formas parasitarias propias del plasmodium. De no visualizar el parasito, se deben observar por lo menos 200 campos microscópicos antes de calificar la muestra como negativa
• Debe tenerse presente que un buen campo microscópico es aquel en el cual se observan de diez a veinte leucocitos por campo.
2.2 Coloración de Romanowsky
Los colorantes derivados del método original de Romanowsky sirven para la diferenciación de la mayoría de estructuras normales y anormales de la sangre.
Los componentes básicos del colorante tipo Romanowsky son las tiacinas y los componentes ácidos son las eosinas, razón por la cual se denominan eosinatos de tiacina. Las tiacinas están constituidas por azul de metileno y por diversas proporciones de sus análogos producidos por desmetilación oxidativa: azur B, azur A y azur C. La mayoría de ellos se disuelve en alcohol metílico.
Entre los colorantes de Romanowsky se encuentran: la coloración de Field, Giemsa, Wright y Romanowsky modificada.
La coloración de Romanowsky modificada es indicada para trabajar en climas cálidos ya que no es higroscopica, es decir, que no absorbe la humedad del ambiente como lo son Giemsa y Wright, razón que la hace más estable en climas con alta humedad relativa. Los componentes de la coloración de Romanowsky modificada la hacen la más económica.