7.3 (Pregunta 3)
En pacientes con patología general, ¿cuál es el efecto de las intervenciones no transfusionales para aumentar la concentración de Hb sobre la morbilidad, la mortalidad y la necesidad de transfusión sanguínea de GR?
Evidencia
La transfusión de glóbulos rojos demanda muchos recursos y se ha asociado con morbilidad a corto y largo plazo en los receptores. Los agentes estimulantes de eritropoyesis recombinantes (AEE) promueven la producción de glóbulos rojos en la medula ósea. Sin embargo, los AEE se han asociado con complicaciones en algunos pacientes. Particularmente donde la Hb basal es casi normal. En algunos pacientes, la administración de hierro también puede ser eficaz. La revisión sistemática examinó la efectividad de los AEE o la suplementación con hierro en subgrupos de pacientes anémicos.
La eritropoyetina es secretada por los riñones en respuesta a la hipoxia y estimula la eritropoyesis en la médula. Una reducción de la masa renal puede contribuir a reducir los niveles de eritropoyetina y, por lo tanto, la anemia. Los AEE son moléculas sintéticas que replican esta función. Son eficaces en el aumento de la Hb en individuos con función renal gravemente deteriorada. Aunque también se han utilizado en otros escenarios clínicos donde la eritropoyesis está disminuida, como cáncer, neoplasias malignas hematológicas y otras enfermedades crónicas. La respuesta eritropoyética a los AEE se reduce en los trastornos de la médula ósea primaria y donde la inflamación crónica contribuye a la anemia.
La eficacia de los AEE en el tratamiento de la anemia y su consecuente efecto potencial sobre el estado funcional debe equilibrarse con los riesgos asociados con la terapia. Tanto la eficacia como los riesgos varían en los diferentes subgrupos de diagnóstico.
Deficiencia de hierro
La deficiencia de hierro resulta cuando las pérdidas de hierro o los requerimientos exceden la absorción. A menudo es multifactorial y puede ser absoluta o relativa. La deficiencia relativa de hierro se conoce comúnmente como deficiencia funcional de hierro (DFH). Un paciente con DFH tiene reservas adecuadas de hierro. Pero el hierro no puede ser movilizado para la eritropoyesis, que es mediada por la hepcidina elevada. La DFH se observa comúnmente en pacientes con enfermedad renal terminal. Pero también puede contribuir a la anemia en pacientes con enfermedades inflamatorias, falla cardíaca crónica y cáncer.
El nivel de ferritina sérica es el índice de deficiencia de hierro más fácilmente disponible y útil (80). En un adulto con anemia, un nivel de ferritina inferior a 15 μg/L es un diagnóstico de deficiencia de hierro, y los niveles entre 15 a 30 μg/L son altamente sugestivos de la condición. Sin embargo, la ferritina es también una proteína de fase aguda y está elevada en inflamación, infección, enfermedad hepática y malignidad. Esto puede dar lugar a niveles de ferritina falsamente elevada en pacientes deficientes en hierro con enfermedad sistémica coexistente.
La terapia con hierro puede usarse como tratamiento primario para la deficiencia de hierro anémica o no anémica, o para aumentar la respuesta a los AEE.
Cuando se administra con AEE, la terapia con hierro previene tanto la deficiencia absoluta de hierro como la DFH, y minimiza la dosis de AEE necesaria para alcanzar las concentraciones objetivo de Hb.
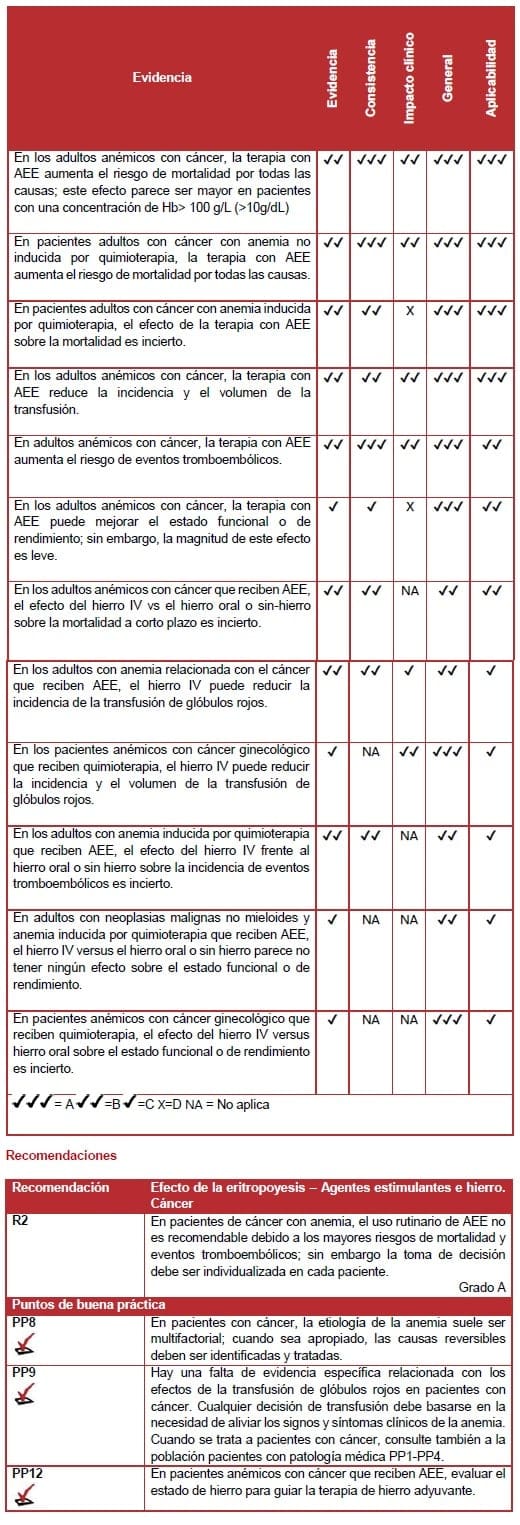
7.3.1 Cáncer
AEE y Cáncer
En pacientes con cáncer, la anemia puede deberse a inflamación, quimioterapia, infiltración de médula ósea por malignidad o deficiencia hematínica (ej. deficiencia de hierro). Los pacientes con neoplasias malignas hematológicas forman un subgrupo separado. Debido a que tienen una eritropoyesis potencialmente defectuosa y por lo tanto una capacidad reducida para responder a los AEE.
Una revisión sistemática de ECA (nivel I) (81) evaluó la efectividad de los AEE en individuos con neoplasias no hematológicas. El estudio documentó un aumento significativo en el riesgo de mortalidad con tratamiento con AEE entre pacientes con cáncer. Esto fue confirmado por un metaanálisis que incluyó cinco estudios publicados posteriormente. Hubo una tendencia no significativa a un mayor riesgo de mortalidad entre el grupo con una Hb basal más alta que recibió tratamiento de AEE.
Estudios de Tonelli et al
Los metaanálisis de los estudios de Tonelli et al (81) y dos ECA de moderada a baja calidad (nivel II) (82-83) identificaron beneficios en pacientes con cáncer que recibieron AEE. Hubo una probabilidad significativamente inferior de transfusión entre los pacientes tratados con AEE si la Hb basal era 120 g/L (12 g/dL) o menor. Adicionalmente, el volumen medio de transfusión de glóbulos rojos entre todos los pacientes que recibieron AEE fue 0,8 unidades menos que en pacientes no tratados. Hubo un efecto favorable sobre el estado funcional o de rendimiento. Sin embargo, un meta análisis de estudios – incluyendo aquellos identificados por Bohlius et al (84), Tonelli et al (81), Hoskin (82) y Tsuboi (83) – encontró un mayor riesgo de eventos tromboembólicos entre pacientes con cáncer tratados con AEE.
Con base en estos análisis, no es posible obtener conclusiones para pacientes con subtipos específicos de cáncer. Tampoco es posible distinguir entre pacientes con diferentes concentraciones de Hb pre-transfusión, o entre pacientes tratados con intención curativa en lugar de intención paliativa. En vista del aumento de la mortalidad y la incidencia de eventos tromboembólicos entre los pacientes con cáncer tratados con AEE, la toma de decisiones debe ser individualizada en pacientes con cáncer.
Hierro intravenoso-cáncer
La revisión de la literatura identificó cinco ECA (nivel II) que evaluaron el uso de la terapia con hierro en pacientes anémicos con cáncer. Todos los estudios compararon el hierro intravenoso (IV) con hierro oral o sin hierro. Los participantes recibieron darbepoetina adyuvante en tres de los estudios, que fueron de moderada a buena calidad (85-87) y eritropoyetina adyuvante en un estudio (88) que fue de baja calidad.
De los cuatro ECA que informaron mortalidad (85-88), no se encontró diferencia significativa en los pacientes tratados con hierro IV en comparación con los pacientes que recibieron terapia oral o sin hierro. Sin embargo, los estudios fueron insuficientes. No se encontraron diferencias significativas después del meta-análisis.
Dos estudios (86-89), encontraron que en comparación con los pacientes que no recibieron hierro IV, los pacientes tratados con hierro IV presentaron una incidencia significativamente menor y un volumen medio menor de transfusión de glóbulos rojos. No hubo diferencias significativas en el estado funcional (Valoración Funcional de la Terapia de Cáncer (FACT)) entre los grupos en ambos estudios. Uno de estos estudios (89) comparó el hierro intravenoso solo con el hierro oral en pacientes con cáncer ginecológico con anemia (Hb <100 g/L – <10g/dL) sometidos a cirugía primaria y que recibían quimioterapia basada en platino.
De los tres estudios que informaron eventos tromboembólicos, no hubo diferencias significativas entre los pacientes tratados con darbepoetina más el hierro IV y los tratados con darbepoetina más hierro oral o sin hierro, incluso después del metanálisis (85-87).
Riesgos asociados con los AEE
Los riesgos asociados con los AEE incluyen aumento de la mortalidad, tromboembolismo venoso, progresión tumoral e infarto. Con el aumento en el conocimiento de estos riesgos, el papel de la terapia con hierro (solo o en combinación con dosis más bajas de AEE) en pacientes seleccionados requiere un estudio adicional. Mientras que la terapia con hierro se recomienda generalmente para aumentar la respuesta en los receptores de los AEE con deficiencia de hierro, no hay pruebas suficientes para recomendar el uso rutinario de hierro IV. Los pacientes con cáncer y anemia deben ser evaluados y tratados para la deficiencia de hierro antes de que se inicien los AEE. Estos pacientes deben ser reevaluados periódicamente durante el curso de la terapia. El hierro IV puede ser necesario cuando la administración oral no es posible o es ineficaz.
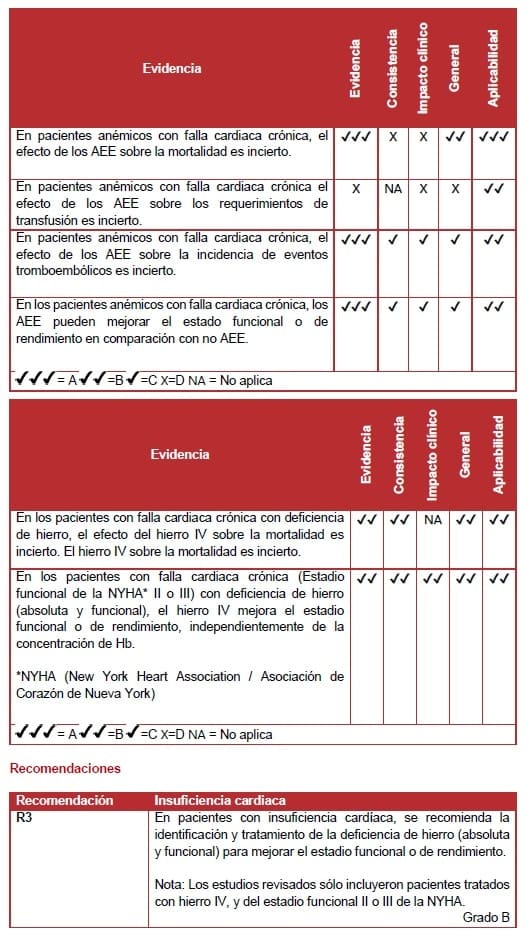
7.3.2 Falla cardiaca crónica
Agentes estimulantes de la eritropoyesis – falla cardíaca crónica
Una revisión sistemática (nivel I), que incluía un gran subconjunto de pacientes con diabetes y falla cardiaca congestiva, encontró que el tratamiento con AEE se asoció con una reducción de la mortalidad (90). En una revisión sistemática separada, la incidencia de eventos tromboembólicos, las hospitalizaciones relacionadas con mortalidad y falla cardiaca no fueron afectadas por los AEE (91), pero hubo una mejoría significativa en la tolerancia al ejercicio.
Hierro intravenoso – falla cardíaca crónica
La deficiencia de hierro es común en los pacientes con insuficiencia cardiaca congestiva, y suele asociarse con anemia.
Dos ECA (nivel II), uno de buena calidad (2) y uno de baja calidad (92), evaluaron el uso de la terapia con hierro IV en pacientes con insuficiencia cardiaca congestiva (Estadio funcional II o III de la NYHA). Ambos estudios incluyeron pacientes anémicos y no anémicos que tenían una deficiencia absoluta de hierro (ferritina <100 μg/L) o DFH (ferritina 100 – 300 μg/L con una saturación de transferrina del 20%).
No hubo diferencias significativas en la mortalidad entre los pacientes tratados con hierro intravenoso y los pacientes que no recibieron hierro intravenoso, incluso tras el meta análisis. Sin embargo, los estudios fueron insuficientes. Ningún estudio informó la incidencia o el volumen de la transfusión de sangre. Ambos estudios mostraron una mejoría significativa en la clasificación de la NYHA con hierro IV.
El ECA multicéntrico de buena calidad de Anker et al incluyó a pacientes con insuficiencia cardiaca congestiva con deficiencia absoluta de hierro y DFH, con concentraciones de Hb entre 95 – 135 g/L (9.5 – 13.5 g/dL) (2). El estudio demostró síntomas reducidos y mejoró la tolerancia al ejercicio submáximo y la calidad de vida con el uso de carboximaltosa férrica IV en comparación con placebo. Las mejoras fueron independientes de las concentraciones de Hb. No hubo diferencias significativas entre el hierro IV y el placebo en las tasas de hospitalización por cualquier causa cardiovascular o por trastornos vasculares.
7.3.3 Enfermedad renal crónica (Agentes estimulantes de la eritropoyesis)
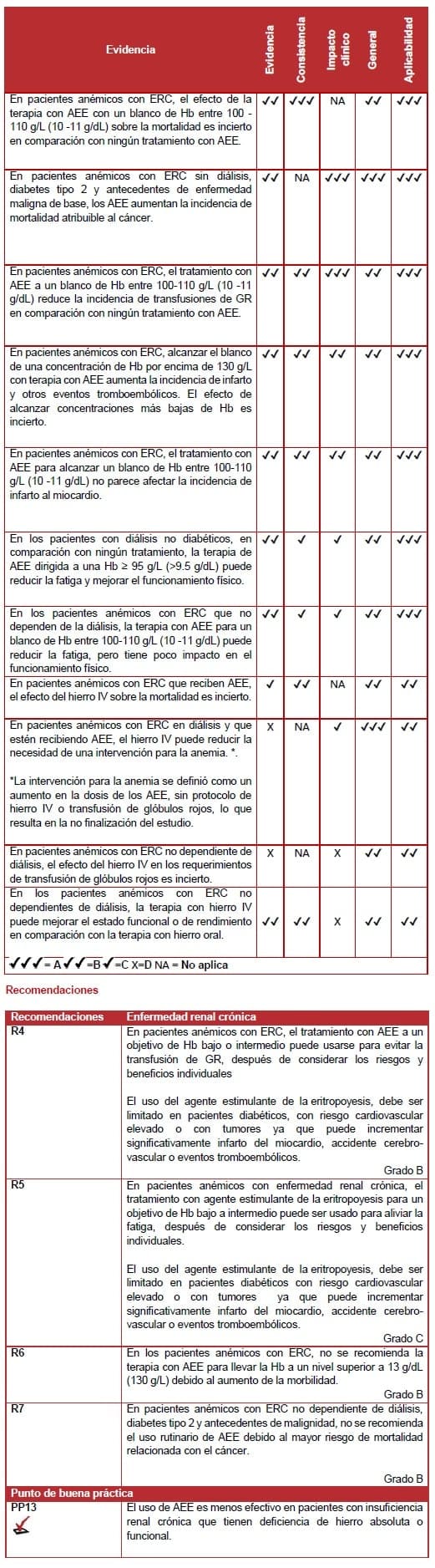
Agentes estimulantes de la eritropoyesis AEE – enfermedad renal crónica ERC
La revisión de literatura identificó cuatro revisiones sistemáticas (nivel I) sobre el uso de AEE para pacientes anémicos con ERC (93-96). Solo aquellas revisiones que compararon el tratamiento con AEE y sin AEE fueron incluidos (97). De manera similar, al discutir los resultados de Tonelli et al, sólo los estudios definidos por la revisión que compararon AEE con no- AEE, en lugar de comparar los protocolos relacionados con un nivel de Hb alto con intermedio o bajo, fueron elegibles para la inclusión (94).
Se ha identificado una incidencia significativamente menor de mortalidad cardiovascular, pero no de mortalidad global, en pacientes con ERC tratados con AEE (94). Se ha informado un aumento de la mortalidad en pacientes con ERC tratados con AEE con antecedentes de malignidad (98). Adicionalmente, un aumento significativo se ha encontrado en el infarto de miocardio, isquemia y otros eventos tromboembólicos en pacientes diabéticos con ERC (99).
Incidencia de transfusión de glóbulos rojos en pacientes con ERC
La incidencia de transfusión de glóbulos rojos en pacientes con ERC que no dependen de la diálisis (108) y los pacientes con hemodiálisis (94) se reduce con los AEE. La calidad de vida en los pacientes dializados mejora con los AEE (100,101). Aunque los pacientes con ERC que no dependen de la diálisis tenían una puntuación mejorada de la prueba FACT-de fatiga, no hubo diferencias significativas en la energía y las puntuaciones de funcionamiento y la gravedad de la falla cardíaca en los que recibieron AEE (98, 99,102).
Estos hallazgos sugieren que los AEE pueden utilizarse para reducir la incidencia de la transfusión de glóbulos rojos en pacientes con ERC que no dependen de la diálisis y en pacientes ERC con diálisis. El uso de AEE también puede resultar en una mejor calidad de vida en pacientes diabéticos con ERC dializados y no dializados. Sin embargo, en vista del aumento del riesgo de infarto al miocardio, y otros eventos tromboembólicos en algunos pacientes, los AEE deben utilizarse con precaución en esta población. La Administración de Drogas y Alimentos de los Estados Unidos ha destacado un mayor riesgo para los pacientes con una Hb blanco >110 g/L (>11 g/dL). No se ha definido un blanco apropiado de Hb para el tratamiento con AEE en pacientes con ERC, pero se recomienda precaución en pacientes con una Hb >100g/L (>10 g/dL).
Hierro intravenoso – enfermedad renal crónica (ERC)
La revisión de literatura identificó una revisión sistemática (nivel I) (103) y cinco ECA (nivel II) sobre el uso de hierro intravenoso para pacientes anémicos con ERC.
La revisión sistemática (103) comparó el uso de hierro IV vs hierro oral en pacientes anémicos con ERC (estadios III a V). Esta revisión incluyó estudios que evaluaron la terapia con hierro en pacientes con ERC no dependientes de diálisis y pacientes ERC con diálisis, con o sin tratamiento con AEE.
Dos ECA informaron la mortalidad como un desenlace, pero no encontraron ninguna diferencia significativa, incluso después del meta-análisis (104-105). No hay estudios que hayan reportado la incidencia de transfusiones. Dos ECA informaron la proporción de pacientes que requirieron una intervención para la anemia (es decir, aumento de la dosis de AEE, iniciación de hierro IV sin protocolo o transfusión de glóbulos rojos) (106-107). Uno de estos ECA no encontró diferencias significativas en la necesidad de una intervención anémica con hierro IV (comparado con el hierro oral) (106). Sin embargo, el otro ECA encontró una diferencia significativa con el hierro IV comparado con no hierro (107).
El meta análisis de los datos de los dos estudios de pacientes que requirieron una intervención para la anemia no mostró una diferencia significativa en las tasas de mortalidad de pacientes con ERC tratados con hierro IV o con terapia de hierro o sin hierro (106-107).
Ninguno de los estudios incluidos informó la incidencia de eventos tromboembólicos.
Dos de los ECA incluidos (106-108) reportaron el estado funcional o de desempeño. Uno de estos estudios (108) mostró una mejora. Los pacientes tratados con hierro IV experimentaron mejoras significativamente mayores en dos medidas de calidad de vida (Cuestionario sobre Síntomas y Efectos de la Enfermedad Renal en la Calidad de Vida, KDQoL) en comparación con los pacientes tratados con hierro oral.
7.3.4 Pacientes adultos mayores
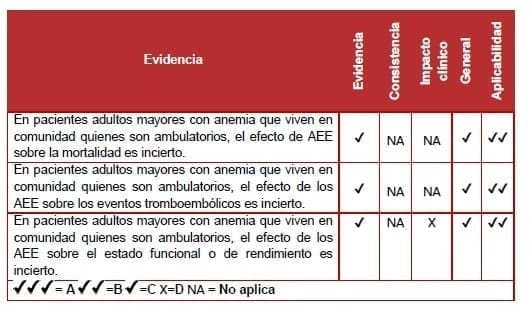
Eritropoyesis – agentes estimulantes – pacientes adultos mayores
Un único ECA de moderada calidad (nivel II) de pacientes adultos mayores anémicos que recibieron AEE no identificó un efecto sobre la mortalidad o la incidencia de complicaciones tromboembólicas (109). El tratamiento con AEE se asoció con mejoría funcional.
(Lea También: Efecto de los Componentes Sanguíneos en los Desenlaces)
7.3.5 Enfermedad inflamatoria intestinal
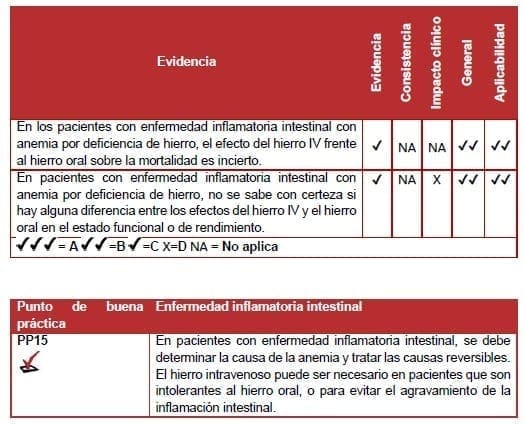
Hierro intravenoso – Enfermedad intestinal inflamatoria
Aunque la anemia en la enfermedad inflamatoria intestinal (EII) es multifactorial, la deficiencia de hierro y la anemia de la enfermedad crónica son factores etiológicos comunes. La terapia con hierro intravenoso se usa frecuentemente en pacientes con enfermedad inflamatoria intestinal porque el hierro oral tiene inconvenientes (ej. intolerancia, falta de adherencia, mala absorción y empeoramiento de la inflamación).
La revisión identificó dos ECA (nivel II) que evaluaron el uso de la terapia con hierro en pacientes con enfermedad inflamatoria intestinal con anemia por deficiencia de hierro (110,111).
Kulnigg et al no encontraron diferencias significativas en la mortalidad entre el hierro IV y el hierro oral, pero el estudio fue insuficiente (111). Ningún estudio informó sobre la incidencia o el volumen de la transfusión de sangre o eventos tromboembólicos.
En el estudio de Kulnigg et al, los pacientes tratados con hierro IV tuvieron una mejoría mayor en el SF-36 desde el inicio del seguimiento en comparación con los pacientes tratados con hierro oral (110). En el de Schroder et al, hubo mejoras similares desde las mediciones basales en el seguimiento del hierro intravenoso comparado con el hierro oral para el índice de actividad de la enfermedad de Crohn, el índice de actividad de la colitis y el SF-36 (111). Estos dos estudios proporcionaron detalles insuficientes para determinar si el efecto del tratamiento en este resultado fue estadísticamente significativo.
7.3.6 Síndrome mielodisplásico (SMD)
Agentes Estimulantes de la Eritropoyesis AEE – síndrome mielodisplásico SMD
La revisión identificó tres ECA (nivel II) (112-114) que evaluaban el uso de AEE en pacientes con síndrome mielodisplásico (SMD).
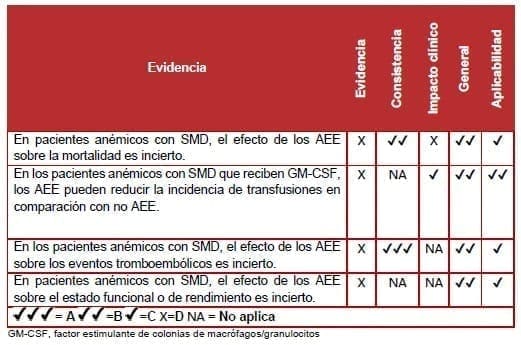
El SMD es un grupo heterogéneo de trastornos caracterizados por diversos grados de diseritropoyesis e infiltración de la médula por células hematopoyéticas anormales. Existe evidencia proveniente de un ECA (nivel II), que demuestra un impacto favorable en la mortalidad entre los pacientes con anemia refractaria con sideroblastos anillados, pero no en otros subgrupos de SMD tratados con AEE (112).
Se requirieron menos transfusiones de glóbulos rojos entre los pacientes con SMD cuando se incluyeron los AEE en el tratamiento con factor estimulante de colonias de granulocitos / macrófagos (GM-CSF), siempre y cuando el nivel basal de eritropoyetina endógena fuera ≤500 mUI/ml (113). No hubo diferencias significativas en la incidencia de las complicaciones tromboembólicas, incluyendo infarto. Los pacientes en los que se había observado una respuesta eritroide en cuatro meses mostraron mejoras en el bienestar físico, emocional y funcional, fatiga y calidad de vida en general (112).
7.3.7 Otras poblaciones
La revisión bibliográfica no encontró evidencia suficiente para brindar recomendaciones para pacientes con SCA, enfermedad cerebrovascular y enfermedad respiratoria, hepatitis C, virus de inmunodeficiencia humana (VIH) o síndrome de inmunodeficiencia adquirida (SIDA) y para pacientes sometidos a radioterapia.