Conclusión
Conclusión
“Estudio de biodisponibilidad relativa entre dos formulaciones de Oxalato de Escitalopram en comprimidos recubiertos de 10 mg, administrados en ayunas a voluntarios sanos de ambos sexos, con la formulación experimental producida por Sanofi-Aventis de Colombia, S.A. para Winthrop Pharmaceuticals de Colombia, S.A., y la formulación de referencia (Lexapro®) fabricada por H. Lundbeck A/S e importada a Colombia por Lundbeck Colombia, S.A.”.

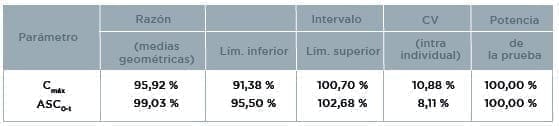
“En el análisis estadístico se determinaron los intervalos de confianza. Los CV intraindividuales y la potencia de la prueba para los parámetros Cmáx y ASC0-1, como se aprecia en el resumen a continuación:
Resumen Estadístico
 Centro Clínico/Analítico/Estadístico: UNIFAG
Centro Clínico/Analítico/Estadístico: UNIFAG
Protocolo: OXALATO DE ESCITALOPRAM en comprimidos recubiertos de 10 mg – JPJ 07/12
Patrocinador: Medley Indústria Farmacêutica Ltda.
Observando los resultados del estudio, se verifica que las formulaciones experimental y de referencia son estadísticamente Bioequivalentes, pues satisfacen el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006, es decir, los valores extremos del intervalo de confianza de 90 % de la razón de las medías geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 80 % y menores que 125 %.
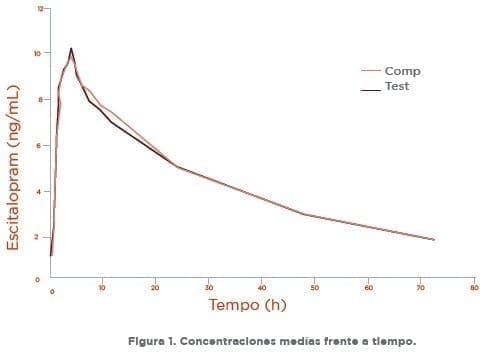
En la Figura 1 se presentan las curvas de las concentraciones plasmáticas medias del Oxalato de Escitalopram (medicamentos de referencia y experimental) frente al tiempo, de los 29 voluntarios que concluyeron el estudio.
* En estudio por INVIMA
MATERIAL DISEÑADO CON FINES EDUCATIVOS Y DIRIGIDOS AL CUERPO MEDICO.
Información prescriptiva completa a disposición del médico, en la Dirección Medica de Sanofi Aventis de Colombia S.A.
Transversal 23 N 97-73, Ed.City Business, Pisos 8 y 9, Bogotá D.C. Tel: (1) 6214400 – Fax: (1) 7444237


 Conclusión
Conclusión