Todos los pacientes fueron diagnosticados con biopsias por octantes y evaluados histológicamente bajo la modalidad de sumatoria de Gleason.
El primer implante fué realizado el 21 de Julio de 1998; el presente estudio analiza los resultados con un periodo de seguimiento de 4 años y 9 meses. Se han implantado 53 pacientes y en el análisis estadístico se excluye un paciente por muerte, secundaria a un Infarto agudo al miocardio, a los 9 meses del implante.
Tabla 3 Características clínicas de los 52 pacientes
| Gleason | No de pacientes | % de pacientes |
| 3 | 1 | 1.9 |
| 4 | 8 | 15.3 |
| 5 | 13 | 25.0 |
| 6 | 25 | 48.0 |
| 7 | 5 | 9.6 |
| Estado Clínico TNM (1977) |
||
| Tic | 18 | 34.6 |
| T2a | 24 | 46.1 |
| T2b | 7 | 13.4 |
| T3a | 3 | 5.7 |
| Niveles PSA (ng/ml) |
||
| 0-10 | 37 | 71.1 |
| 10.1-15 | 9 | 17.3 |
| 15.1-20 | 2 | 3.8 |
| Mas de 20 | 14 | 7.6 |
| RTUP previa | ||
| Si | 6 | 11.5 |
| No | 46 | 88.4 |
| Hormonoterapia Previa |
||
| Si | 18 | 34.2 |
| No | 34 | 65.3 |
| Radioterapia Previa |
||
| Si | 14 | 26.9 |
| No | 38 | 73.0 |
En promedio se utilizan 98 semillas, 23 agujas y un tiempo de 55 minutos para realizar el implante.
Ochenta y uno por ciento (80.77%) de los pacientes se presentan con tumores estado T2a o menos, al tacto rectal.
Ocho pacientes, quince por ciento (15%), requieren bloqueo hormonal, por 3 a 6 meses, con el fin de disminuir el volumen de la próstata o para corregir la interferencia del arco púbico. Todos los pacientes requieren llegar al volumen ideal para el implante de menos de 50 cc. Para este fin se utiliza bloqueo con Acetato de Leuprolide 11.25 miligramos por dosis.
Treinta y siete pacientes (71.1%) de los casos, tienen al inicio de la terapia los niveles de PSA en 10 ng/ml o menos.
La Tabla 4, muestra la distribución de los pacientes implantados de acuerdo al riesgo.
Tabla No 4
| RIESGO | Número | % |
| Bajo | 32 | 61.5 |
| Intermedio | 12 | 23.0 |
| Alto | 8 | 15.3 |
De los pacientes de bajo riesgo, se encuentra hasta la fecha recaída en 2 casos; 2 de los pacientes de riesgo intermedio muestran recurrencia de la enfermedad y no hay recaídas observadas hasta el momento en los pacientes de riesgo alto.
De la totalidad de los pacientes con recaída, en uno se confirmó tener enfermedad recurrente, mediante biopsias de la próstata y gamagrafía ósea positiva para enfermedad metastásica. Adicionalmente, tres pacientes mostraron incremento en tres controles consecutivos en los niveles de PSA, cumpliendo con la definición de recaída bioquímica. Por lo tanto 4 (7.69%) de 52 pacientes muestran recurrencia de la enfermedad.
Todos los 4 pacientes en los que ha fallado en tratamiento, presentan la recaída bioquímica antes de los 2 años del implante. En tres de ellos, los niveles de antígeno prostático específico disminuyeron progresivamente, pero al año se observó el incremento de esta glicoproteina, sin disminución posterior de estos niveles, hasta que cumplieron con la definición de recaída bioquímica de la ASTRO. El otro paciente tiene niveles de PSA por debajo de 0.5 ng/ml, hasta los 3 años de seguimiento, después de esto inició el incremento progresivo del marcador.
Hasta la fecha no se registra mortalidad secundaria a la enfermedad.
La Tabla 5 documenta el último análisis clínico de los 52 pacientes.
Tabla 5 Estado actual en el último seguimiento con PSA
| Número (%) | |
| Sin Enfermedad | 48 (92.3%) |
| Progresión del PSA | 3 (5.7%) |
| Enfermedad a distancia | 1 (1.9%) |
La Tabla 6, muestra la evolución en los niveles de antígeno prostático específico.
Tabla 6 Evolución en los niveles de antígeno prostático específico
| PSA Nadir |
Basal | 1 Mes | 3 Meses | 6 Meses | 12 Meses | 18 Meses | 24 Meses |
| 0 – 0,5 | 0 | 6 | 8 | 10 | 10 | 12 | 6 |
| 0,51 – 1,0 |
0 | 1 | 5 | 7 | 8 | 1 | 0 |
| 1,1 o más |
52 | 42 | 27 | 17 | 13 | 10 | 6 |
| Total | 52 | 49 | 40 | 34 | 31 | 23 | 12 |
De la totalidad de los pacientes implantados, cuatro (7.69%), han presentado retención urinaria que requerió sonda uretral a permanencia. La duración del cateterismo fue uno por 1 semana, dos por 1 mes y el restante la requirió por 3 meses, por lo que se manejó con sonda de cistostomia.
Se definió la evolución de la sintomatología Urinaria, de acuerdo al cuestionario de la IPSS. El cuestionario se entregó en forma dirigida al paciente a los 8 días del implante, al mes, seis meses y un año. Grafica 1.
La sintomatología urinaria se observa como una constante en los paciente sometidos a braquiterapia, síntomas caracterizados por polaquiuria, disuria y tenesmo vesical. Estos síntomas se relacionan directamente con el puntaje IPSS pre-operatorio y con el volumen de la próstata.
Los cuatro pacientes que presentaron retención urinaria, tenían un puntaje pre-operatorio de la IPSS superior a 15.
Se observa que el puntaje regresa a los niveles registrados antes del tratamiento hasta 12 meses después del procedimiento. El pico máximo en el incremento de los síntomas urinarios se aprecia en el primer mes del implante. Gráfica No. 2.
[enc_su_row][enc_su_column size=”1/2″ center=”no” class=””]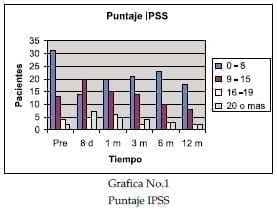 [/enc_su_column] [enc_su_column size=”1/2″ center=”no” class=””]
[/enc_su_column] [enc_su_column size=”1/2″ center=”no” class=””]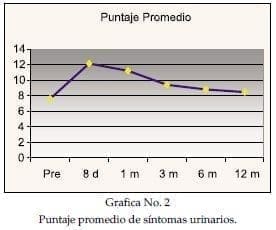 [/enc_su_column][/enc_su_row]
[/enc_su_column][/enc_su_row]
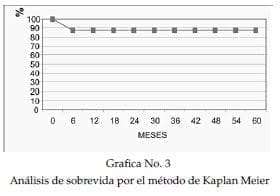
Se analliza la sobrevida libre de enfermedad a 5 años de acuerdo al método de Kaplan Meier. Gráfica No. 3
Se presentó un caso con hematuria macroscópica tardía, a los 5 días del implante que se manejó con lavado de vejiga y sonda durante 48 horas.
Se presentaron dos casos con infección urinaria, cuadro clínico confirmado con parcial de orina y urocultivo, los dos casos manejados con Ciprofloxacina por 7 días.
Hay dos casos de estrechez uretral, uno de ellos con estrechez leve la cual se ha resuelto con dos sesiones de dilatación de uretra, y en la actualidad se encuentra sin evidencia clínica de estrechez; la uroflujometria libre muestra un pico máximo de 17.3 ml/segundo. El segundo caso ha presentado una estrechez de uretra bulbo-membranosa severa que requiere dilataciones periódicas.
No se reportan casos de incontinencia urinaria permanente.
Conclusión
Se concluye que la Braquiterapia moderna como monoterapia y en su forma combinada muestra altos porcentajes de control bioquímico y clínico de la enfermedad. Se identifican complicaciones menores. Los resultados deben continuar en evaluación ya que se requiere de mayor tiempo en el seguimiento de los pacientes para comparar esta serie con las que muestra la comunidad científica internacional.
Bibliografía
1. Stock RG, Kao J, Stone NN. Penile erectile func¬tion after permanent radioactive seed implan¬tation for treatment of prostate cancer. J.Urol 2001: 165: 436-9
2. Bates TS, Wright MP, Guillat DA. Prevalence and impact of incontinence and impotence following total prostatectomy assessed anonymously by the ICS-male questionarie. Eur Urol 1988: 33: 165-9
3. Blasko JC, Wallner K, Grimm PD, et al. Pros¬tate specific antigen based disease control fo¬llowing ultrasound guided I-125 implantation for stage T1/T2 prostatic carcinoma. J Urol 1995;154:1096-1099
4. Barringer BS. Radium in the treatment of Carci¬noma of the Bladder and prostate. JAMA 1917; 68:1227-1230
5. Flocks RH, Kerr HD, Elkins HB et al. Treatment of carcinoma of the prostaste by intersticial radia¬tion with radioactive gold (Au-198): a preliminary report. J Urol 1952 ;68:510-522
6. Whitmore WF Jr, Hilaris B, Grabstald H. Retro¬pubic implantation of iodine-125 in the treatment of prostatic cancer. J Urol 1972; 108:908-920
7. Kuban D. El Mahdi AM, Schellhammer PF. I-125 intersticial implantation for prostate cancer: What have we learned 10 years later? Cancer 1989; 63:2415-2420
8. Schellhammer PF, El Mahdi AM, Wright GL, Kolm P, Ragle R. Prostate-specific antigen to determine progression-free survival after radiation therapy for localized carcinoma of the prostate. Urology 1993¸42:13-20
9. Kratochwill A, Puncture guided by ultrasound. (Abstract) In First Ultrasound World Meeting Program; 1969 June 2-7; Viena, Austria. 1969; 297
10. Watanabe H, Igari D, Tamahashi Y, Harada K, Saitoh M. Transrectal ultrasonotomografhy of the prostate. J. Urol 1975; 114: 734-739
11. Holm HH. The history of intersticial brachythe¬rapy of prostatic cancer. 1977, Semin Surg Oncol 13(6): 431-437
12. Holm HH, Juul N, Pedersen JF, et al. Transperineal 125 Iodine seed implantation in prostatic cancer guided by transrectal ultrasonography. J Urol 1983; 130:283-286
13. Blasko JC, Ragde H, Schumacher D. Transperineal percutaneous Iodine – 125 implantation for prostatic carcinoma using transrectal ultrasound and template guidance. Endocurietherapy Hypertermia Oncology 1987; 3: 131-139
14. Ragde H, Blasko JC, Schumacher D, et al. Use of transrectal in transperineal Iodine – 125 seeding for prostate cancer: methodology. J Endourol 1989; 3:209-218
15. Ramos CG, Calvalhal GF, Smith DS, Mager DE, Catalona WJ. Retropsective comparision of ra¬dical retropubic prostatectomy and 125 iodine brachyteraphy for localized prostate cancer. J Urol 1999; 161: 1212-1215
16. Ragde H, Korb L. Brachytherapy for clinically localized prostate cancer. Semin Surg Oncol 2000, 18: 45-51
17. Bise W.S, Prestidge BR. A review of post-implant quality assessment in permanent transperineal in¬tersticial prostate brachytherapy. J Brachytherapy Int 1997; 13:297-313
18. Nag S, Baird M, Blasko J et al. American Bra¬chytherapy Society (ABS) survey of current clinical practice for permanent brachytherapy of prostate cancer. J Brachyther Int 1997; 13:243-251
19. Nag S, Beyer D, Friedland J, Grimm P, Nath R. American Brachytherapy society recommend¬ations for transperineal permanent brachytherapy of prostate cancer. Int. J. Radiation Oncology Biol. Phys, 1999; 44: 789-799.
20. Partin AW, Yoo J, Carter HB et al. The use of pros¬tate specific antigen, clinical stage and Gleason to predict pathological stage in men with localized prostate cancer. J. Urol 1993; 150:110-114
21. Blasko JC, Lange PH. Prostate cancer-the the¬rapeutic challenge of locally advanced disease. NEJM 1997; 337:340-341
22. Blasko JC, Ragde H, Grimm PD, Sylvester John Cavanagh W. Potential for Neoadjuvant Hor¬monal Theraphy with Brachytherapy for Prostate Cancer. Molecular Urology 1997; 1:207-214
23. Grimm PD, Blasko JC, Ragde H. Ultrasound-gui¬ded transperineal implantation of iodine-125 and palladium-103 for the treatment of early prostate cancer-technical concepts in planning, operative technique, and evaluation. Atlas Urol Clin N Am 1994;2: 113-125
24. Stone NN, Stock RG, DeWyngaert JK, et,al. Pros¬tate Brachytherapy: Improvements in Prostate Vo¬lume measurements and dose distribution using interactive ultrasound guided implantation and three-dimensional dosimetry. Radiat Oncol Invest 1995;3:185-195
25. Stock RG, Stone NN, Wesson MF et al. A modi¬fied technique allowing interactive ultrasound-guided three dimensional transperineal prostate implantation. Int J Radiation Oncology Biol Phys 1995;32: 219-225
26. Quimby EH. The grouping of radium tubes in packs and plaques to produce the desired distri¬bution of irradiation. AJR 1932; 27:18
27. Paterson R, Parker HM. A dosage system for ga¬mma-ray therapy, Parts 1 and 2. Brit J Rad 1943;7:592
28. Wallner K, Roy J, Harrison L. Dosimetry guide¬lines to minimize uretrhal and rectal morbidity following transperineal I-125 prostate brachythe¬rapy. Int. J Radiation Oncology Biol Phys 1995; 32:465-471
29. Dattoli M, Wallner KA. Single method of stabi¬lize the prostate during transperineal prostate brachytherapy. Int J Radiation Oncology Biol Phys 1996; 38: 341-342
30. Butler WM, Merrick GS. I-125 Rapid Strand loading technique. Radiat Oncol Invest 1996; 4:48-49
31. Zelefsky MJ, Whitmore WF Jr. Long-term results of retropubic permanent 125 iodine implantation of the prostate for clinically localized prostatic cancer. J Urol 1997; 158:23-29
32. Stock RG, Stone, Talbert A et al. A dose-res¬ponse study for iodine-125 prostate implants Int. J radiation Oncology Biol Phys 1998; 41:101-108
33. Nath R, Anderson LL, Luxton G, et al. Dosimetry of intersticial Brachytherapy soursces: Recom¬mendations of the AAPM Radiation Theraphy Committee Task Group No. 43. Med Phys 1995; 22:209-233
34. Ragde H, Blasko JC, Grimm PD et al. Brachythe¬rapy for Clinically Localized Prostate Cancer: Results at 7 and 8 year Follow-up. Semin Surg Oncol 1997; 13:438-443
35. Nag S, Scaperoth DD, Badalament R et al. Trans¬perineal palladium-103 prostate Brachytherapy: Analysis of morbidity and seed migration. Uro¬logy 1995; 45:87-92
36. Hu K, Wallner K. Rectal and urinary morbidity in patients undergoing prostate I-125 implant (Abstr.) Int J Radiation Oncology Biol Phys 1997; 39: 292
37. Prestidge BR, Bice ES, Kiefer EJ et al. Ti¬ming of computed tomography-based pos¬timplant assessment following permanent transperineal prostate brachytherapy. Int J Radiation Oncology Biol Phys 1988; 40:1111-1115
38. Amdur RJ, Gladstone ScD, Leopold KA et al. Pros¬tate seed implant quality assessment using MR and CT image fusion. Int J Radiation Oncology Biol Phys 199;43:67-72
39. Roy JN, Wallner K, Harrington PJ et al. CT-ba¬sed evaluation method for permanent implants: Application to prostate. Int J Radiation Oncology Biol Phys 1993; 39: 347-353
40. Vijverberg PLM, Blank LECM, Dabhoiwala NF et al. Analysis of Biopsy findings and implant quality following ultrasonically-guided I-125 implantation for localized prostatic Carcinoma. Br J Urol 1993; 72:470-477
41. Ragde H, Elgannal AAA, Snow PB et al. Ten-Year disease free survival after transperineal sono-graphy-guided iodine-125 brachytherapy with or without 45-Gray external bean irradiation in the treatment of patients with clinically localized, low to high Gleason grade prostatic carcinoma. Cancer 1988; 83:989-1001
42. Critz FA, Williams WH, Halladay CT et al. Post-treatment PSA < or = 0.2 ng/mL defines disease freedom after radiotheraphy for prostate cancer using modern techniques. Urology 1999; 54: 968-971
43. American Society for Therapeutic Radiology and Oncology Consensus panel. Consensus statement: Guidelines for PSA following Radiation Therapy. Int J Radiation Oncology Biol Phys 1997; 37: 103
44. Consensus statement. Guidelines for PSA follo¬wing radiation therapy. Int J Radiat Oncol Biol Phys 1997;37:1035-1041.
