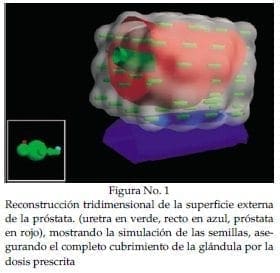
Las recomendaciones del comité y de los sub-comités son con carácter técnico y de orientación clínica, pero la responsabilidad final esta en las manos del médico tratante.
Recomendaciones
Criterios de exclusión de pacientes:
- Expectativa de vida menor de 5 años.
- Defecto por resección transuretral y/o prostatectomía retropúbica, grande o no completamente cicatrizado.
- Riesgo quirúrgico alto.
- Metástasis a distancia.
Contraindicaciones relativas para la braquiterapia:
Se aplica para pacientes que no son considerados casos ideales para la braquiterapia, pero que han sido tratados con éxito en algunos centros. Se recomienda a los especialistas en periodo de entrenamiento, que no traten a este grupo de pacientes.
- Pacientes con riesgo aumentado para complicaciones:
- Lóbulo medio grande.
- Irradiación pélvica previa.
- Puntuación alta de síntomas urinarios de acuerdo a la Asociación Americana de Urología.
- Cirugías pélvicas múltiples.
- Diabetes no compensada.
- Dificultades técnicas que impiden una buena dosimetría:
- Resección transuretral previa.
- Glándula mayor de 60 cc.
- Lóbulo medio prominente.
- Biopsias de vesículas seminales positivas.
Indicaciones de la Braquiterapia como Monoterapia:
- Estadios clínicos T1a- T2a y
- Gleason 2 a 6 y
- PSA < 10 ng/ml.
Indicaciones de la Braquiterapia con Radioterapia Externa (Combinada):
- Estadios clínicos T2b- T2c o
- Gleason 8 a 10 o
- PSA > 20 ng/ml.
- Invasión Perineural.
- Múltiples biopsias positivas.
- Bilateralidad de las biopsias positivas.
- Invasión de la cápsula demostrada por resonancia magnética.
Indicaciones del tratamiento integrado: comprende radioterapia externa, Braquiterapia y bloqueo andrógeno completo.
- Pacientes con glándulas mayores de 60 cc que respondieron al tratamiento hormonal, además de las características previamente enumeradas.
Con el uso de las tablas de Partin20, que son consideradas como el mas grande acumulo de información que permite identificar a los pacientes con enfermedad extraprostática, haciendo una correlación entre estadio, grado del tumor y nivel de PSA, se pueden ayudar a confirmar las recomendaciones de la Asociación Americana de Braquiterapia (ABS), definiendo cuales son los pacientes que se pueden beneficiar de la braquiterapia sola, o en combinación con radioterapia externa. Los pacientes que se encuentran entre los dos grupos establecidos, deben ser evaluados en forma individual y tomarse en cuenta otros factores como son: invasión perineural en la biopsia, localización del tumor, número de biopsias positivas y hallazgos aportados por la resonancia magnética, que permitirán tomar la decisión de si se tratan además con radioterapia externa, con o sin bloqueo androgénico completo21,22.
Planificación pre-implante:
La sociedad de Braquiterapia Americana (ABS) recomienda que se realice un” pre-plan” del implante antes de la inserción de las semillas. Generalmente se practica algunas semanas antes del acto quirúrgico23, y está basado en imágenes de ultrasonido por vía transrectal, previamente adquiridas, y que permiten determinar el volumen de la próstata.
Hay otro método que ha tomado auge, y que consiste en la realización del plan del implante, el mismo día del procedimiento, en tiempo real, o también denominada “técnica interactiva”, introducido en el medio Americano por el Dr. Stone y colaboradores, en Nueva York, y adoptado por otros24,25.
Su implementación fue consecuencia de las dificultades encontradas en el momento operatorio, de reproducir el pre-plan, debido a cambios de forma de tamaño de la próstata por uso de hormonas, presencia de orina en la vejiga, gas en el recto, y diferencias en el ángulo del transductor de ultrasonido. Con la técnica interactiva no es necesario duplicar un pre-plan, lo que da mayor flexibilidad en la ejecución del implante. Se puede cambiar la posición del paciente o el ángulo de incidencia del transductor de ultrasonido en caso que se detecte interferencia del arco púbico. Ambas técnicas tienen defensores y detractores. Hay mucha similitud entre ellas, fundamentalmente por el hecho de que son basadas en las imágenes de la próstata adquiridas por ultrasonido transrectal, el plan se elabora de manera que se administre una dosis de radiación mayor en la periferia de la glándula, y se calcula para administrar la misma dosis. Mediante el uso de un sistema de cálculo computarizado, se determina el número y posición de las semillas para obtener cobertura de la glándula dentro de la isodosis establecida (dosis tumoral periférica mínima).
Hay dos modelos de cálculo en la dosis en braquiterapia. En su comienzo, se utilizaba el sistema de Quimby26 que se basa en la distribución uniforme de las semillas radioactivas en la próstata, para disminuir la dosis deseada al volumen implantado (próstata). En este caso, el centro de la glándula, y por ende, la uretra; recibe 2 a 3 veces mas dosis de radiación que la prescrita a la periferia de la glándula, produciendo mayor incidencia de complicaciones urinarias. El otro sistema, y que es la base de los sistemas modernos de calculo computarizado, es el de Patterson y Parker27, y consiste en la distribución uniforme de la dosis de radiación en el volumen implantado, y usando una distribución no uniforme de las semillas radioactivas, y de esta manera colocar la mayoría de las semillas en la periferia de la glándula, y menor cantidad en el centro de la misma, minimizando la dosis a la uretra, y por ende, disminuyendo la intensidad de los síntomas urinarios. Se debe mantener a un mínimo el segmento de uretra que recibe mas del 200% de la dosis prescrita23,28.
El paciente se coloca en posición de litotomía. La técnica usada para implantar las semillas es mediante la vía transperineal, con una guía de coordenadas y del ultrasonido. Debe tratarse de reproducir la misma posición, y ángulo usado en el pre-plan, al menos que se este haciendo el procedimiento en tiempo real. Debe usarse el transductor de alta resolución y biplanar para poder adquirir imágenes tanto transversales como longitudinales. El detector de ultrasonido debe fijarse en una plataforma con corredera de movimiento, que permita pasos en incrementos de cinco en cinco milímetros en ambas direcciones. En casa posición se delimita el contorno de la glándula prostática, y de la sumatoria de todas las imágenes adquiridas, se determina el volumen tri-dimensional de la próstata, y se define posición, y cantidad de semillas necesarias para obtener la dosis mínima periférica necesaria. Durante la inserción de las semillas se pueden usar agujas de inmovilización de la próstata con el objeto de minimizar el desplazamiento de la glándula durante la introducción de las agujas cargadas con las semillas y antes de ser depositadas en la glándula29. Otra forma de presentación de las semillas, es fijada en material de sutura reabsorbible (RAPID strand)30 o en cartuchos pre-cargados como en el equipo de Mick6.
Dosis de irradiación a ser administrada
Desafortunadamente, la dosis precisa de irradiación necesaria a ser administrada por la braquiterapia para erradicar el cáncer prostático es controversial. La mayoría de los reportes disponibles en la literatura informan de la dosis prescrita, y no la dosis realmente recibida por el tumor. Esto se deduce de la forma variada en que se han emitido los reportes de estas dosis, que fueron correlacionadas con el resultado del tratamiento basado en la respuesta y control del PSA31,32. En 1.995 la Asociación Americana de Físicos Médicos (AAPM)= creó un grupo de trabajo (TG-43) para el estudio de los algoritmos de calculo de dosis para el I-125, y el Pd-10333. Para el I-125 la dosis a ser administrada como tratamiento único debe ser 144 Gy en vez de la acostumbrada 160 Gy (Tabla 1). En la Tabla 1 se especifican las dosis de braquiterapia dependiendo de estos factores, y si se asocia o no con la radioterapia externa.
Tabla 1. Dosis recomendadas por la Asociación Americana de Braquiterapia
| ISOTOPOS | BRAQUITERAPIA SOLA Gy |
BRAQUITERAPIA COMO “BOOST” de 40-5 Gy RADIOTERAPIA EXTERNA Gy |
| I-125 (pre TG-43) |
169 | 110 – 120 |
| I.125 (TG-43) |
144 | 100-110 |
| Pd-103 | 115-120 | 80-90 |
La actividad de los isótopos oscila entre 0.3 a 0.5 mCi/semilla para el I-125, y de 1.0 a 1.5 mCi/semilla para el Pd-103. El grupo del Hospital Memorial de Nueva York, usa semillas de actividad mayor. No hay recomendación formal en cuanto al intervalo de tiempo entre la radioterapia externa y la braquiterapia, pero por regla general, la tendencia es entre 2 a 6 semanas. Otros informes recomiendan dosis diferentes, así como también del uso de la braquiterapia previa a la radioterapia externa34. (Figura 1).
Pasos a seguir después del implante
La mayoría de los pacientes son sometidos a una cistoscopia después del implante. Esto es con el objeto de extraer coágulos sanguíneos, o semillas que hubiesen caído en la vejiga o uretra durante el implante, y para evaluar si el paciente tiene riesgo de desarrollar retención aguda de orina por obstrucción. En años recientes esta practica ha caído en desuso.
Se sugiere seguir las recomendaciones de protección radiológica previamente establecidas por cada institución, específicamente en lo que se relaciona a la cercanía de niños pequeños y de mujeres embarazadas. Existe la posibilidad de migración de las semillas, y quedar en el pulmón35.
Cuando esto sucede, es por regla general después del segundo día del implante; por eso se recomienda tomar una Radiografía de Tórax en la primera visita de seguimiento, sobre todo cuando la cuenta de las semillas no coincide con las imágenes obtenidas inmediatamente post-implante. No se han descrito complicaciones serias como consecuencia de la presencia de las semillas en el pulmón. El uso de antibióticos, anti-inflamatorios, analgésicos y bloqueadores alfa es de rutina, pero algunos grupos prefieren esperar a la aparición de los síntomas para iniciar su administración. Si hay aparición de síntomas obstructivos podría ser necesario el uso prolongado de una sonda. Si son de larga duración, en ocasiones pudiera ser necesario una resección transuretral o una incisión transuretral de próstata. Cualquiera que sea, recomiendan esperar por lo menos 6 meses después del implante, para evitar complicaciones serias, sobre todo de incontinencia urinaria36.