Para el seminoma puro se ha ensayado dosis efectivas más bajas de radioterapia y quimioterapia adyuvante con una o dos dosis de carboplatino.
En el teratoma metatásico de buen pronóstico se dan cuatro cursos de BEP cada 21 días o 2 a 5 días con cisplatino, la supervivencia libre de enfermedad a los dos años es de 90.4%. Tener en cuenta la toxicidad pulmonar de la Bleomicina, en pacientes mayores de 40 años o en insuficientes renales. El cisplatino a pesar de riesgo de ototoxicidad se prefiere como medicamento único o combinado con Etoposide. Pacientes con pobre pronóstico: 4 cursos de BEP cada 21 días. No se encuentra beneficio aplicando más cursos o añadiendo otros agentes quimioterapeúticos diferentes a los anteriormente descritos.
Carcinoma in situ (CIS): El significado de la presencia del cis en el testículo contralateral no ha sido totalmente resuelto. Indudablemente no todos los pacientes con cis contralateral desarrollan evidentes tumores testiculares. Su incidencia como ya lo habíamos anotado anteriormente es del 5.2%. Se recomienda radioterapia del lecho tumoral.
Cáncer testicular bilateral (sincrónicos): Históricamente se ha tratado con orquidectomía inguinal bilateral. Actualmente se recomienda la enucleación en cánceres pequeños asociados con márgenes negativos para pacientes obedientes con lesiones bilaterales o testículo único. El riesgo de desarrollar C.T. contralateral es raro en hombres tratados con orquidectomía pero se deben practicar ecografías anuales para detectarlo.
Criptorquidia: El criptorquidismo es un factor de riesgo de C.T. y pacientes que fueron sometidos a orquidopexia requieren exámenes periódicos a conciencia. Cambios impalpables en la túnica albugínea tales como calcificaciones (29%) de los casos, fueron comúnmente observados por ecografía después de la orquidopexia. Sin embargo lesiones parenquimatosas deben ser consideradas como anormales.
Tumores de células de Sertoli yLeydig: Son considerados benignos, recurrencias retroperitoneales tardías fueron notadas en 25 y 8% de pacientes tratados con vigilancia, recomendándose entonces la L.R.P.
Cánceres puros del saco vitelino: El de los adultos difiere de aquellos de los niños en que un 33% están asociados con estadio patológico II de la enfermedad y, por consiguiente se les considerará para L.P.R. primaria.
Teratoma (T): Aquellos pacientes con T. En su espécimen de L.R.P.Q. tienen más probabilidad de recaída que aquellos sin T. Los que recaen con T, después de la L.R.P.Q., la mitad recaerá nuevamente con T. Y la mitad recaerán con carcinoma. Una teoría es que la recurrencia como cáncer representa una diferenciación del T.
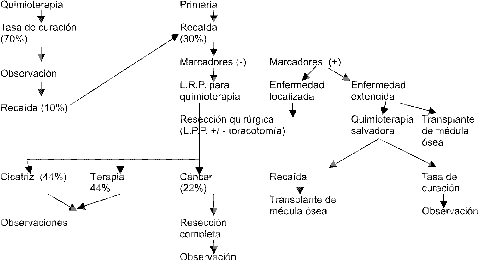
Esquema de la Quimioterapia del C.T. no Seminomatoso
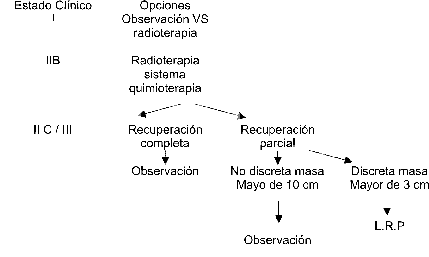
Estado clínico lic /III
Seminoma puro
Raros elementos patológicos
Adenocarcinomas, sarcomas y otros elementos de tumor son ocasionalmente encontrados como tumor primario testicular, al igual que las metástasis y tumores recurrentes. En general, estos tumores no responden bien a la quimioterapia. Completa extirpación quirúrgica parece ser la mejor opción de tratamiento para estos difíciles tumores. El pronóstico de estos pacientes es generalmente pobre.
Cáncer testicular y fertilidad
¿El C.T. causa infertilidad o es la infertilidad un factor de riesgo para el C.T?
El 50% de hombres tenían concentración anormal de espermios (menos de 20 millones) al momento de su diagnóstico.
Causas potenciales para infertilidad en hombres con C.T.: ambiental, genética, hormonal, autoinmune, carcinoma in situ contralateral, quimioterapia, cirugía, psicológico.
Ambiental: Disminución global del recuento espermático. Aumento de la incidencia de cáncer de células germinales. ¿Es una disminución real o una manipulación estadística? Existen diferentes modelos de laboratorio desde hace 40 años.
Genético: La infertilidad remotamente es de un rasgo genéticamente trasmitido. Números estudios dejan de mostrarlo y por incidencia de aneuploidía de espermatozoides en hombres con C.T. con FISH. Parece haber un mayor porcentaje de aneuploidía en casos de más severa infertilidad.
Hormonas intrínsecas: Carrol y col. En 1987, en 15 pacientes: el 66% tenían desproporción hormonal: aumento de estrógeno. LH, gonadotrofina beta-coriónica y disminución de la F.S.H. Hansen y col en 1989 con 97 pacientes: el 38% tenían aumento de la alfa-feto proteína y aumento de estrógeno.
Proceso autoinmune: Sangre. La barrera del testículo puede estar comprometida por el C.T. resultando en anticuerpos antiespermas. Dos estudios revelaron aumentos de dichos A.C. en un 21 a 73% en 67 hombres, versus 8% vistos en normales.
Carcinoma in situ: Encontrado en el testículo contralateral en un 5,2% de pacientes. La progresión a cáncer es del 36 al 70%. En hombres con infertilidad es el 5%. Berthelsen y col. En 200 hombres después de la orquidectomía encontraron promedio de recuento de 7,5 millones, 25% tenían interrupción de la espermatogénesis. El 97% de biopsias con espermatogénesis no CIS. El 54% de biopsias con CIS tuvieron espermatogénesis.
Radiación y espermatogénesis: Brenner y col. En 1983 en un estudio con prisioneros voluntarios, encontraron que 15 rads, afectaban el recuento espermático, 50% abolían la espermatogénesis, 400 rads causaban azoopermia, 9,7 rads era una dosis letal para el 50% de espermatogonias.
Después de las 3.600 rads con protección a los rayos X, la exposición fue de 78 rads. El 25% de hombres llegaron a ser estériles. No hubo aumento de las malformaciones en la descendencia después de los rayos X.
Quimioterapia e infertilidad: Los agentes quimioterapeúticos afectan rápidamente el crecimiento celular (la espermatogonia). En cuanto a la función testicular endocrina hay una elevación de la FSH en un 64% y la LH en un 59%.
No se presentan malformaciones en la descendencia.
Psicológico: Después de un año NED. El 20 a 30% pérdida de la conducta sexual. El 20 al 50% disfunción eréctil. El 20 al 40% disminución de la sensación orgánica. El 30% pérdida de la autoestima (imagen del cuerpo) aún en hombres casados.
Tratamiento de la aneyaculación: Medicamentos: los alfa-estimulantes: 15% de efectividad: imipramina 25 a 50 mgs 2 v/d. Ornade: 75 mgs 2v/d. Pseudoefedrina 60 mgs. 4 v/d- La electroeyaculación por vía rectal alcanza solamente un 20% de embarazo con inseminación asistida (fertilización in vitro).
Fertilidad natural: No se alcanzaron embarazos con ciclo natural o inseminación intrauterina,
Reproducción asistida y fertilidad: Inseminación intracitosplasmática (ICI): el porcentaje fue de 55,6% para recuperación del espermatozoide y el porcentaje de implantación fue de 33.3% por embrión.
Resumen: Las causas de infertilidad por C.T. son multifactoriales. El alto porcentaje de supervivencia y la juventud de los pacientes es un problema que frecuentemente persiste después de que el cáncer es curado.
Con las modernas técnicas de reproducción asistida se pueden lograr embarazos pero con un altísimo costo monetario: aproximadamente unos diez millones de pesos por ciclo y se puede necesitar mas de uno con ICI.
Riesgos a desarrollar segundas enfermedades malignas
Se han presentado recientes informaciones de aumento en la incidencia de malignidades hematológicas, melanomas, tumores del tracto gastrointestinal y el tiroides. Estos resultados son vistos en pacientes sometidos a previa radiación o quimioterapia.
Actualmente se está utilizando la tomografía de emisión de positrones (P.E.T.) para detectar metástasis que no han podido ser visualizadas con el TAC convencional. Esto es una gran ayuda para quimioterapias innecesarias y para el control de las recaídas sospechadas por el aumento de la cifra de marcadores tumorales. Se está haciendo profilaxis con antibióticos para prevenir la sepsis neutropénica. Medicamentos como el taxol, se están añadiendo al tratamiento quimioterápico para mejorar el pronóstico de pacientes en estado crítico. También se está ensayando aumentar la dosis de los agentes terapéuticos, en aquellos enfermos que no han respondido a las dosis convencionales.
Se hace hincapié sobre la importancia de la cirugía extirpativa de masas metastásicas en aquellos pacientes que no han respondido a la quimioterapia. Actualmente se está investigando genes causantes de C.T. hereditario. Por ejemplo se ha identificado 18q y Xq 13 como sitios de susceptibilidad potencial de genes. Estamos a la espera de grandes acontecimientos en el campo del genoma humano y de la clonación, para erradicar enfermedades hereditarias y llegar a la curación de aquellas patologías que actualmente permanecen sin resolver.
Bibliografía
1. Journal of urology vol 149 – 1993 – 237. Retroperitoneal limphadenectomy for clinical stage a tests cancer (1965 to 1989) modifications of technique and impact on ejaculation. J.p. Donohue departament of urology, Indiana university school of medicine, Indianapolis, indian.
2. A.U.A. today. August. 1993: some problems in treating testicular cancer remain unsolved. John P. Donohue, m.d. and Richard S. Foster, m.d. Indianapolis, In.
3. A.U.A. today. November. 1993: what are the risks of morbidity from testicular cancer treatment? Richard S. Foster, m.d. and John P. Donohue, m.d. Indianapolis, in.
4. THE Journal of urology vol 152 – 1994 – 1139: the fertility of patients with clinical stage I testes cancer managed by nerve sparing retroperitoneal lymph node dessection. Richard S. Foster Indian university medical center, Indianapolis, Indian
5. A.U.A. today. October 1994: what is the best treatment for patients with nonseminomatous germ cell testis tumors when elevated serum tumor markers are the only evidence of disease? Pramod C. Sogani, m. d. New York, Ny
6. A. U. A. today: march: 1996 laparoscopic retroperitoneal lymphadrnectomy may be an option for high – risk stage 1 non seminomatous germ cell tumors. Dr. Laurence Klotz. Toronto.
7. A.U. A. news september – october 1996 tricks of the trade retroperitoneal lymph node dissection for testis cancer:templates, tips and traps. Dr. Jerome P. Richie. Boston, Massachusetts
8. A. U. A. news: january / february 1997-is retroperitoneal lymph node dissection necessary for stage 1 nonseminomatous testis cancer?. Dr. Robert C. Flanigan. Hines, Illinois.
9. A. U. A. news may june 1997 take home messages Dr. James E. Montie Ann Arbor Michigan
10. A. U. A. News: january / february 1999-15: surveillance for stage 1 nonseminomatous testis cancer selection and management of apropriate candidates Drs. Michael J Morris and George J. Bosl. New York, New York.
11. A. U. A. news july august 1999 take home messages testicular cancer . Dr. Peter R. Carroll. San Francisco California.
12. CURSO DICTADO POR LA Escuela de Medicina Universidad de New York. Diciembre 9-11 de 1999
Moderador: Samir Taneja M.D.
Profesor asistente de Urología Co-Director de Oncología Urológica.
Manejo de las masas Post-Quimioterapia
Randal G. Rouland, M.D. PHD
División de Urología, Universidad de Kentucky, Lexington, Kentucky.
Cancer Testicular y Fertilidad
Andrew R. Mc Cuelough, M.D. FACS
Director de Salud Sexual y Sexualidad.
13. Congreso sobre progreso y controversia en Urología Oncológica realizado en Rotterdam Holanda año 2000
14. FUNDAMENTOS de cirugía. Urología 2ª edición Dres Feres Flórez Silva y Juan Fernando Uribe Arcila Página 163. Año 2000
15. MANUAL of Urology. diagnosis and therapy. edited by Mike B. Siroky, md Robert J. Krane página 179.
16. QUIMIOTERAPIA hoy para el C.T. Abraham Cachoua. M.D. Profesor asistente de la Escuela de Medicina. Editado por S.b. Kaye. Del departamento de Oncología Médica del Hospital Royal, Arsden. Down Road Sulton Sm25PT. Reino Unido.