Fabián Alberto Jaimes Barragán MD. MSc. ( c ).
Especialista en Medicina Interna. Candidato a Magister en Epidemiología Clínica.
Profesor Departamento de Medicina Interna Universidad de Antioquia
En las últimas dos décadas hemos presenciado avances asombrosos en todos los campos del saber y obviamente el conocimiento médico no escapa a esta avalancha de ciencia y tecnología: todos y cada uno de los actos que envuelven nuestra práctica médica, y por lo tanto nuestra relación con los pacientes, están rodeados de un cuerpo conceptual que está en continua renovación y mejoramiento. El derecho al conocimiento y el deber de ofrecer siempre las mejores respuestas a nuestros pacientes nos obligan a estar frente a frente, con una mirada crítica y escrutadora, con el inmenso volumen de información médica que se produce diariamente en el mundo.
La corriente epistemológica de la Medicina Basada en la Evidencia (MBE) ha surgido como un complemento necesario a la aproximación tradicional de la enseñanza y la práctica de la medicina, buscando integrar la experiencia clínica individual con la mejor evidencia externa disponible; siempre en beneficio de la razón de ser de nuestra vida profesional: El paciente(1).
Este artículo busca mostrar, con un ejemplo práctico del área a la que pertenece la mayoría de lectores de esta revista, una visión muy general de los fundamentos de la MBE –que debe ser complementada con la literatura disponible(2-3)– y las bondades que se pueden derivar de implementar esta estrategia en nuestra práctica profesional cotidiana.
Nuestro paciente
En la revista académica del servicio de Medicina Interna de un hospital universitario se presenta el siguiente caso: una mujer de 50 años de edad con 14 meses de evolución de fenómeno de Raynaud, edema de manos y cara, pirosis y malestar general. Sus pruebas de laboratorio evidencian un patrón restrictivo en la espirometría y unos anticuerpos antinucleares positivos 1:160 con patrón homogéneo. Se plantea el diagnóstico de Esclerosis Sistémica Progresiva (ESP) variedad difusa y se empiezan a hacer conjeturas sobre el mejor tratamiento:
1. Penicilamina: la paciente había sido tratada previamente con este medicamento con muy mala tolerancia y en la ronda se discute que no ha sido aceptada plenamente la eficacia del mismo.
2. Fotoquimioterapia extracorpórea: se menciona como una alternativa prometedora para el compromiso cutáneo exclusivamente pero que no está disponible en nuestro medio.
3. Esteroides: considerados como un tratamiento complementario o sintomático en este tipo de pacientes. Se le suministran a la paciente irregularmente y en la actualidad con una dosis de 10 mg por día de prednisona.
4. Análogos de la prostaciclina: un residente recuerda haber leído un artículo al respecto pero no tiene claridad sobre los resultados.
5. Inmunosupresores: entre las muchas alternativas probables mencionadas ninguno de los presentes sabe a ciencia cierta si este tipo de fármacos tiene alguna indicación o utilidad en la enfermedad.
Con este antecedente práctico, se ve la necesidad de ofrecer la mejor solución disponible al problema del paciente, en este caso la mejor opción terapéutica, y vemos la posibilidad de utilizar de manera secuencial los cuatro contenidos básicos de la MBE:
1. Formulación de preguntas clínicas relevantes y susceptibles de ser resueltas
Este es el punto con el cual estamos más familiarizados los clínicos; especialmente en nuestro medio académico, donde surgen de manera constante y espontánea (aunque casi nunca precisas) las inquietudes acerca de áreas específicas de la práctica médica: hallazgos clínicos, etiología, diagnóstico diferencial, pruebas diagnósticas, pronóstico, tratamiento y prevención. Cualquiera de estas áreas de interés debe producir preguntas pertinentes al problema del paciente, formuladas de manera que dirijan la búsqueda hacia respuestas precisas y relevantes. Una pregunta clínica bien construida debe tener cuatro elementos que se presentan a continuación tomando las características del caso que nos ocupa:
1. El paciente o el problema: ¿cómo podría describir un grupo de pacientes que sean similares a mi paciente? “En pacientes con ESP variedad difusa de menos de dos años de evolución….”.
2. La intervención (una causa, un factor de pronóstico, un tratamiento, etc.): ¿cuál intervención principal voy a considerar? “….cuál tratamiento…”
3. La comparación de intervenciones (si es necesario): ¿cuál es la principal alternativa para comparar con la intervención? “…comparado con placebo..”
4. El desenlace: ¿Qué es lo que espero lograr? “…disminuye el compromiso cutáneo y visceral..”.
Con las anteriores consideraciones hemos construido una pregunta clínica significativa y debemos pasar al proceso de intentar resolverla.
2. Búsqueda de la mejor evidencia
En este punto, usualmente, comienzan nuestras debilidades, ya que el poco tiempo disponible y la falta de familiaridad con las herramientas de búsqueda (Medline, Current Contents, Cochrane Collaboration, etc.) limitan substancialmente, acá y en otras partes del mundo, la recolección de información(4). El uso constante de algunos de esos medios ha demostrado, no solo que se mejora la eficiencia en la búsqueda y el uso de la información médica, sino también, lo más importante, que mejora el cuidado de los pacientes y su pronóstico(5).
Para nuestra pregunta acudimos a la biblioteca médica de la institución y utilizamos el sistema Medline (la versión electrónica del Index Medicus) por medio del programa de búsqueda Winspirs®. Seleccionamos la base de datos correspondiente a los artículos publicados entre 1992 y 1998 y activamos el comando “Thesaurus”, que nos muestra términos y entidades definidos, identificados y clasificados en orden alfabético. La exploración del término “Scleroderma,-systemic” y todos los ítems del mismo relacionados con “therapy” nos ofrece un conjunto de 301 artículos publicados. Sabemos y aceptamos que la mejor estrategia de investigación para evaluar la eficacia de una intervención es el experimento clínico controlado(6), por lo tanto, limitamos los anteriores hallazgos por tipo de publicación (PT = “Randomized-Controlled-Trial”), lo que reduce el número de estudios a 18. Una segunda limitación para el lenguaje de la publicación (LA = “English”), nos permite un número final y razonable de investigaciones: 12.
La revisión de los resúmenes nos permite descartar, por resultados negativos, el uso de penicilamina o ciclofenil(7), así como el activador tisular del plasminógeno(8,13), el clorambucil(9), los pulsos de dexametasona(10), el aminobenzoato(11), la urokinasa(12), o el iloprost, un análogo de la prostaciclina , oral o en infusión(14-15). Igualmente se corrobora la utilidad de la fotoquimioterapia para el compromiso cutáneo(16), y llama la atención el hecho de encontrar un resultado alentador con el uso de metotrexate, para lo cual no se tenía referencia(17). Para confirmar los hallazgos anteriores, se repite la búsqueda por el comando de términos libres (“search”) cruzando “Scleroderma” con “Therapy” y, de esta manera, se obtiene un resultado similar; además de la detección de un estudio no controlado, lo cual le resta la validez necesaria para considerarlo aplicable, con interferón gamma(18).
Con el precedente de que la fotoquimioterapia extracorpórea no está disponible en el medio y su utilidad está restringida al compromiso cutáneo, nos queda la posibilidad de analizar el artículo que propone el uso de metotrexate(17).
3. Apreciación crítica de la evidencia
A través de esta se busca determinar la validez de los hallazgos; es decir comprobar si estos son cercanos a la verdad y su importancia, o sea, si son potencialmente útiles para los clínicos. Estas dos consideraciones (validez e importancia) se aplican, entre otros, para pruebas diagnósticas, marcadores pronósticos o tratamientos (ya sea evaluados por experimentos clínicos controlados, revisiones sistemáticas, análisis económicos o análisis de decisiones clínicas). El grupo de trabajo en Medicina Basada en la Evidencia ha venido publicando en JAMA desde 1993 las Guías para Usuarios de Literatura Médica, que proponen los elementos necesarios para hacer una evaluación crítica de los diversos tipos de publicaciones médicas. Especialmente se recomiendan, por sus conceptos básicos de uso diario, las primeras guías, que tratan de investigaciones primarias o no integrativas(19-25), entendiéndose por integrativas aquellas que se basan en evidencia previa como los metanálisis o los análisis de decisiones clínicas.
Para evaluar el estudio acerca del uso de metotrexate en el tratamiento de la esclerosis sistémica, tomaremos como referencia las guías sobre cómo usar un artículo acerca de terapia o prevención(20-21):
1. ¿Fueron los pacientes asignados de una manera aleatoria a los grupos de tratamiento?, es decir, ¿únicamente determinada por el azar? SÍ. La asignación aleatoria permite que los diferentes factores que pueden determinar el pronóstico o la respuesta al tratamiento estén distribuidos de manera equivalente en los grupos de estudio.
2. ¿Se hizo un seguimiento completo de los pacientes? SÍ. Los estudios que finalizan el período de observación rápidamente respecto a la enfermedad en cuestión, pueden mostrar resultados benéficos que el tiempo se encarga de confirmar como incorrectos. En este caso, un tiempo de seguimiento de 48 semanas es considerado prudencial para la ESP.
3. ¿Se hizo un “análisis por intención de tratar?” SÍ. Es decir que los pacientes y sus resultados finales sean analizados como correspondientes al grupo al que originalmente fueron asignados, independientemente de las suspensiones o cambios de tratamiento. Esto permite el análisis de la intervención en su contexto real (un estudio pragmático) al considerar las modificaciones posteriores del tratamiento como debidas a las condiciones y características del mismo.
4. ¿Se hizo un “cegamiento” de los pacientes y los evaluadores ante el tratamiento?. SÍ. Ni el paciente ni el evaluador del desenlace deben saber el tipo de tratamiento que se está recibiendo, para evitar que de manera deliberada o involuntaria se inclinen los hallazgos hacia un resultado.
5. ¿Los grupos fueron comparables o similares en cuanto a factores de pronóstico y a otros tratamientos diferentes de la intervención en estudio? Parcialmente. No hay diferencias en cuanto a las cointervenciones, pero la composición por sexo y la proporción de pacientes con ESP variedad difusa difiere en los grupos. Esta diferencia debe tenerse en cuenta al analizar los resultados por que puede favorecer la respuesta al tratamiento (Tabla 1).
Tabla 1. Proporción de hombres y de casos de ESP variedad difusa en los grupos de tratamiento

Metotrexate Placebo
Variedad difusa 5 / 17 (29%) 6 / 12 (50%) Hombres 7 / 17 (41%) 2 / 12 (17%)
6. ¿Cuáles son los resultados y cuál es su precisión?. Los principales desenlaces evaluados son el puntaje total de piel (PTP), que es la suma de los puntajes de 0 a 4 obtenidos manualmente en 26 sitios anatómicos y descrito por Steen y cols(26), La sensación de bienestar del paciente determinada por una escala visual análoga (EVA) donde 100 mm representa un bienestar general óptimo, y la capacidad de difusión pulmonar reflejada por la difusión pulmonar de monóxido de carbono (DLco). Los resultados a las 48 semanas de tratamiento se muestran en la Tabla 2.
Tabla 2. Resultados finales del estudio (desenlaces principales)
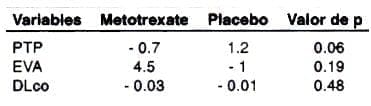
Aunque no fue contemplado como un objetivo inicial, también se detectó un aumento en la tasa de depuración de creatinina de 4 ml/min con un valor de p de 0.07.
Para efectos de facilitar la comprensión de los resultados debemos recordar que el valor de p, que arbitrariamente se predetermina como significativo si es menor de 0.05 o menor de 0.01, expresa simplemente la probabilidad de que el resultado esperado sea únicamente debido al azar y no expresa de ninguna forma la magnitud de ese resultado(27).
De lo anterior podemos apreciar que para este estudio, aunque todos los resultados superen el valor de p de 0.05, los hallazgos de PTP, depuración de creatinina y EVA muestran una discreta mejoría en el grupo de metotrexate, que en el peor de los casos puede ser dada por el azar en el 20% o en 1 de cada 5 veces. La DLco, por el contrario, con una p de 0.48 nos evidencia que en el punto específico de la capacidad de difusión pulmonar el tratamiento con metotrexate se comporta igual que la suerte de lanzar una moneda al aire (0.5 es la probabilidad de obtener cara o sello).
4. ¿Puede aplicarse esta evidencia, válida e importante, en el cuidado de nuestros pacientes?
En este momento son esenciales la habilidad y el arte para integrar dicha evidencia con la experiencia y el juicio clínicos, y decidir como incorporar, si está indicado, estos elementos en la práctica diaria. Las guías mencionadas, que no sustituyen la integridad y la complejidad del acto médico, ofrecen algunas sugerencias para decidir la aplicación de los resultados en nuestros pacientes en cuanto a pruebas diagnósticas, pronósticos y tratamientos, entre otros.
1. ¿Son aplicables los resultados en mi (nuestros) paciente (s)? Probablemente sí. Acá buscamos definir si las características de los pacientes de la investigación, es decir los criterios de inclusión y exclusión, los hacen similares o comparables a un paciente como el nuestro. En este caso, con las precauciones debidas a las diferencias en sexo y tipo de compromiso, podemos considerar aceptable la aplicabilidad de los resultados en nuestra paciente.
2. ¿Se evaluaron desenlaces clínicamente relevantes? Sí y no. El compromiso de piel y la sensación de bienestar son componentes fundamentales del curso clínico de estos pacientes, pero no hay detalles acerca del compromiso visceral diferente del pulmonar ni de la frecuencia y severidad del fenómeno de Raynaud.
3. ¿Se ha considerado el riesgo y el beneficio de la intervención? Sí. En el estudio se pudo apreciar una disminución discreta y temporal en los valores de leucocitos (1200 en promedio) y plaquetas (53000 en promedio). Ninguna fue causa de suspensión o retiro del tratamiento. Un paciente tuvo que descontinuar el metotrexate por la cefalea intensa inducida por cada dosis del medicamento.
Con todas las anteriores consideraciones, regresamos a la revista académica y asistencial del servicio con la mejor evidencia disponible para el tratamiento de nuestra paciente, mostrando las opciones y las limitaciones que le permitan a ella definir sus preferencias y tomar sus propias decisiones:
– No existe un tratamiento que demuestre plena eficacia y efectividad para su enfermedad.
– Entre las opciones disponibles, consideramos que puede ofrecer algún beneficio el uso de metotrexate en una dosis inicial de 15 mg intramuscular cada semana.
– Es probable, al menos con un 80% de certeza, que este tratamiento mejore el compromiso cutáneo y de su estado general.
– No sabemos si este tratamiento también puede servir para la frecuencia o severidad del fenómeno de Raynaud.
– No existe una evidencia para afirmar que este mismo tratamiento pueda mejorar sustancialmente el compromiso visceral. Sin embargo esta posibilidad no se descarta y puede verse alguna respuesta en el compromiso renal.
– Tendrá una disminución discreta y transitoria en sus leucocitos y plaquetas, con una certeza cercana al 100% de que esto no le producirá complicaciones mayores ni le obligará a suspender el tratamiento.
– Uno de cada 30 pacientes, con una enfermedad como la suya y un tratamiento como el que se le ofrece, puede tener un dolor de cabeza muy intenso que obligue a la suspensión del tratamiento.
Podemos trasladar, con este ejemplo, el concepto de MBE a una definición operativa y práctica: MBE es integrar la experiencia clínica individual con la mejor evidencia externa disponible, a través de un autoaprendizaje de toda la vida, para ofrecer las mejores soluciones a los problemas y expectativas de nuestros pacientes.
Bibliografía
1. Evidence-Based Medicine Working Group. Evidence-Based Medicine. A new approach to teaching the practice of medicine. JAMA 1992; 268: 2420-2425.
2. Jaimes FA. Medicina basada en la evidencia: Por qué y cómo llegar a ella. IATREIA 1998; 11: 113-118.
3. Sackett DL, Richardson WS, Rosemberg W, Haynes RB. Evidence-Based Medicine. How to practice and teach EBM. New York: Churchill Livingstone; 1997.
4. Covell DG, Uman GC, Manning PR. Informartion needs in office practice: are they being met?. Ann Intern Med 1985; 103: 596-599.
5. Lindberg DAB, Siegel ER, Rapp BA, Morris FR. Use of MEDLINE by physicians for clinical problem solving. JAMA 1993; 269: 3124-3129.
6. Fletcher RH, Fletcher SW, Wagner EH. Epidemiología Clínica. Barcelona: Ediciones consulta; 1989.
7. Akesson A, Blom Bulow B, Scheja A, Wollmer P, Valind S, Wolheim FA. Long term evaluation of penicillamine or cyclofenil in systemic sclerosis. Results from a two year randomized study. Scand J Rheumatol (abs). 1992; 21: 238-244.
8. Klimiuk PS, Kay EA, Illingworth KJ, Gush RJ, Taylor LJ, Baker RD et al. A double blind, placebo controlled trial of recombinant tissue plasminogen activator in the treatment of digital ischemia in systemic sclerosis. J Rheumatol (abs). 1992; 19: 716-720.
9. Clements P, Lachenbruch P, Furst D, Paulus H. The course of skin involvement in systemic sclerosis over three years in a trial of chlorambucil versus placebo. Arthritis Rheum (abs). 1993; 36: 1575-1579.
10. Sharada B, Kumar A, Kakker R, Adya CM, Pande I, Uppal SS et al. Intravenous dexamethasone pulse therapy in diffuse systemic sclerosis. A randomized placebo controlled study. Rheumatol Int (abs). 1994; 14: 91-94.
11. Clegg DO, Reading JC, Mayes MD, Seibold JR, Harris C, Wigley FM et al. Comparison of aminobenzoate potassium and placebo in the treatment of scleroderma. J. Rheumatol (abs). 1994; 21: 105-110.
12. Ciompi ML, Bazzichi L, Melchiorre D, De Giorgio F, Bondi F, Puccetti L. A placebo controlled study if urokinase in sysemic sclerosis. Biomed Pharmacother (abs). 1996; 50: 363-368.
13. Wilson D, Edworthy SM, Hart DA, Fritzler MJ. The safety and efficacy of low dose tissue plasminogen activator in the treatment of systemic sclerosis. J Dermatol (abs). 1995; 22: 637-642.
14. Wigley FM, Korn JH, Csuka ME, Medsger TA, Rothfield NF, Ellman M et al. Oral iloprost treatment in patients with Raynaud’s phenomenon secondary to systemic sclerosis: a multicenter placebo controlled double blind study. Arthritis Rheum (abs). 1998; 41: 670-677.
15. Scorza R, Rivolta R, Mascagni B, Berruti V, Bazzi S, Castagnone D et al. Effect of iloprost infusion on the resitance index of renal vesels of patients with systemic sclerosis. J Rheumatol (abs). 1997; 24: 1944-1948.
16. Rook AH, Freundlich B, Jegasothy BV, Perez MI, Barr WG, Jimenez SA et al. Treatment of systemic sclerosis with extracorporeal photochemoterapy. Results of a multicenter trial. Arch Dermatol (abs). 1992; 128: 337-346.
17. Van Den Hoogen FH, Boerbooms AM, Swaak AJ, Rasker JJ, Van Lier HJ, Van De Putte LB. Comparison of methotrexate with placebo in the tratment of systemic sclerosis: a 24 week randomized double blind trial, followed by a 24 week observational trial. Br J Rheumatol. 1996; 35: 364-372.
18. Hunzelmann N, Anders S, Fierbelck G, Hein R, Herrman k, Albretch M et al. Systemic scleroderma. Multicenter trial of 1 year of treatment with recombinant interferon gamma. Arch Dermatol. 1997; 133: 609-613.
19. Oxman AD, Sackett DL, Guyatt GH. I. How to get started. JAMA 1993; 270: 2093-2095.
20. Guyatt GH, Sackett DL, Cook DJ. II. How to use an article about therapy or prevention. A. Are the results of the study valid? JAMA 1993; 270: 2598-2601.
21. Guyatt GH, Sackett DL, Cook DJ. II. How to use an article about therapy or prevention. B. What were the results and will they help me in caring for my patients? JAMA 1994; 271: 59-63.
22. Jaeschke R, Guyatt GH, Sackett DL. III. How to use an article about a diagnostic test. A. Are the results of the study valid? JAMA 1994; 271: 703-707.
23. Jaeschke R, Guyatt GH, Sackett DL. III. How to use an article about a diagnostic test. B. What are the results and will they help me in caring for my patients? JAMA 1994; 271: 703-707.
24. Levine M, Walter S, Lee H, Laupacis A, Cook DH. IV. How to use an article about harm. JAMA 1994; 271: 1615-1619.
25. Laupacis A, Wells G, Richardson WS, Sackett DL, Cook DH. V. How to use an article about prognosis. JAMA 1994; 272: 234-237.
26. Steen VD, Medsger TA, Rodnan GP. D-penicillamine therapy in progressive systemic sclerosis (scleroderma). Ann Intern Med. 1982; 97: 652-659.
27.Jaimes FA. Consideraciones epidemiológicas y estadísticas para el estudio del cáncer. En: Olarte F. Gómez LR (ed): Oncología Quirúrgica, colección Fundamentos de Cirugía. Medellín: Universidad de Antioquia (en imprenta).