Dr. Luis Fernando Pinto Peñaranda
Médico lnternista Reumatólogo. Profesor Universidad Pontificia Bolivariana. Reumatólogo ISS, Fundación Santa María
La Artritis Reumatoide (AR) y la osteoartrosis (OA) son entidades muy frecuentes con incidencia de 0.8% para la primera y 32% para la segunda. En ambas entidades, y por mecanismos diferentes hay alteraciones del metabolismo esquelético que pueden llevar a osteoporosis secundaria(1).
Artritis Reumatoide
La composición corporal, tanto la masa ósea como la masa magra, son influenciadas por citoquinas liberadas durante la actividad reumatoidea, la inmovilización y por el tratamiento. La disminución de la masa ósea y de la masa magra son marcadores de severidad e indicadores tempranos de pronóstico desfavorable.
Westhonens(2) publica un estudio de composición corporal en pacientes con AR encontrando que tanto en hombres como en mujeres había una disminución de la masa magra y un aumento de la masa grasa con relación a los controles sanos y con una diferencia estadísticamente significativa. Como dato interesante no demostraron diferencias entre los pacientes tratados o no con esteroides. La distribución de la grasa corporal mostró un carácter claramente centrípeto más marcado en el grupo que utilizó esteroides (Z-Score en el tronco).
En el grupo de mujeres con AR se encontró una disminución significativa de Densidad Mineral Osea (DMO) con relación a los controles y con excepción de la medición L2-L4. En los hombres con AR la diferencia no fue tan marcada como en las mujeres, pero, de nuevo, fue menor que en los controles en todos los sitios de medición. Para ambos grupos no hubo diferencia entre los tratados con esteroides o sin éstos.
La osteoporosis es una bien conocida complicación de la AR y es de 2 tipos: yuxtaarticular (temprana y secundaria a factores locales) y generalizada (más tardía y de origen multicausal: reposo, drogas, actividad reumatoidea, grado de alteración funcional y deterioro de la masa muscular).
La evaluación del metabolismo óseo en pacientes con AR se ve dificultada por la multiplicidad de factores que influyen. Para obviar esto se seleccionaron los estudios longitudinales con poblaciones homogéneas en su status hormonal y en el uso de esteroides; se escogieron además aquellos que comparasen poblaciones con diferentes estados funcionales y duración de la enfermedad, y para evaluar el papel de los corticosteroides se consideraron solo los estudios de casos y controles.
La Osteoporosis como manifestación extraarticular de la AR
Los estudios de la década anterior muestran un claro aumento de los marcadores de resorción ósea con correlación con los índices de actividad reumatoidea (3, 4) sugiriendo que la pérdida ósea temprana se debe a un aumento de la resorción determinado por citoquinas producidas por el sinovio reumatoideo, Goug y Sambrook(5) publican el estudio con mejor diseño metodológico para evaluar correlación entre actividad reumatoidea, marcadores de resorción ósea y pérdida de DMO por DEXA, excluyendo los pacientes que recibieron corticosteroides concluyen:
1. La DMO basal fue menor en los casos que en los controles en todos los sitios de medición (P < 0.005); al año y a los dos años de evolución de la AR estas diferencias se mantenían (P < 0.005).
2. Al inicio de la enfermedad los marcadores de formación ósea (fosfatasa alcalina específica de hueso y procolágeno o fueron menores en los pacientes que en los controles pero durante el seguimiento no hubo correlación entre éstos y los cambios porcentuales en la masa ósea. Sugieren estos resultados que la disminución de DMO en pacientes con AR no depende de una menor formación ósea.
3. Los niveles de Cross Links estuvieron elevados durante el seguimiento con relación a los controles (P < 0.005 y P < 0.001) y se correlacionaron con la VSG, la PCR y la pérdida porcentual de masa ósea. Por análisis de regresión se determinó que la PCR fue mejor predictor de pérdida de masa ósea que los Cross Links y que la VSG.
En resumen estos datos demuestran que el proceso que determina la pérdida de DMO en AR es un aumento de la resorción ósea. La correlación entre resorción y actividad reumatoidea está de acuerdo con estudios previos(6) que plantean que esta se debe a citoquinas proinflamatorias (IL6, IL1, TNF) secretadas por la membrana sinovial reumatoidea. La rata de pérdida ósea fue mayor en etapas tempranas y fue mayor en pacientes con AR activa sugiriendo una mayor propensión a fracturas, a largo plazo, en pacientes mal controlados de su proceso inflamatorio.
Lane y Goldring(7) enfatizan en que numerosos estudios demuestran que los pacientes de AR tienen menor DMO y mayor riesgo de fracturas y que la pérdida es Unto yuxtaarticular como axial sugiriendo una naturaleza sistémica, secundaria, por lo menos en parte, a mediadores producidos en la sinovia reumatoidea. Hay una compleja interacción entre inflamación y resorción ósea y un desacoplamiento entre formación y resorción.
En un estudio posterior(8) Cortet y Flipo demuestran correlación entre marcadores de resorción ósea, índices de actividad reumatoidea y DMO en el cuello femoral pero no en la columna lumbar. Hubo una disminución de DMO femoral entre 6.9 y 8.2% con relación a los controles y correlacionada con la actividad reumatoidea. La pérdida lumbar (y también la femoral) se vieron aumentadas en el grupo que utilizó esteroides (femoral: -10.5%/P < 0.0001 y lumbar -11.1%/P < 0.0023).
La demostración de resorción ósea por células sinoviales fue ilustrada por Fujikawa y colaboradores(9) quienes aislaron de muestras sinoviales de articulaciones reumatoideas, células capaces de producir resorción sobre placas de dentina. Estas células satisfacían criterios para ser consideradas osteoclastos (multinuclearidad, teñían positivamente para fosfatasa ácida tartratoresistente, tenían receptores para vitronectina y ocasionaban resorción lacunar sobre placas de dentina).
La conclusión que resulta de estos estudios es que la osteoporosis yuxtaarticular es un evento temprano en AR y que precede cambios radiológicos como las erosiones, los quistes subcondrales y el colapso articular. Probablemente resulta de la liberación de citoquinas inductoras de resorción ósea como IL1, IL6 o TNF y del papel de células sinoviales con funciones de osteoclastos.
El efecto nocivo sobre la DMO tiene una importancia grande en niños con artritis reumatoide juvenil (ARJ) por su influencia en el pico de masa ósea y las implicaciones posteriores de una pobre masa ósea máxima. Los pacientes con ARJ como grupo tienen una menor DMO que los controles sanos(10-11) pero los diferentes tipos muestran diferencias. Los pacientes con ARJ pauciarticular no muestran diferencia con los controles ni en DMO ni en talla. La mayor pérdida de DMO la muestran los pacientes con enfermedad de Still (-2,4 SD con relación a los controles) seguidos por los niños con ARJ poliarticular (-0,5 SD).
La DMO del radio distal fue significativamente menor en niños con ARJ con afección permanente de la muñeca corroborando el efecto local de citoquinas y otros mediadores inflamatorios. Sin embargo la DMO del radio distal también disminuyó en niños con ARJ sin compromiso de muñecas en comparación con los controles indicando un efecto sistémico de la enfermedad.
Estos hallazgos se observan en niños sin uso de corticosteroides; el efecto de estos es aditivo.
Se ha planteado que el polimorfismo del gen que codifica el receptor de vitamina D (VDR) puede predisponer a osteoporosis en mujeres postmenopáusicas(13). Gough y Sambrook demuestran que mujeres con el genotipo tt tuvieron mayor rata de pérdida ósea durante los primeros 3 años de artritis reumatoide que las mujeres con el genotipo TT (P < 0.05 en columna lumbar y P < 0.01 en cuello femoral). Este marcador genético podría ayudar a seleccionar las mujeres con mayor riesgo de osteoporosis y fracturas.
La pérdida de DMO del esqueleto axial, específicamente vertebral, ha sido considerada multifactorial y varios estudios(14-15) la atribuyen a edad, duración de la AK estado funcional (grado de incapacidad), la talla y el uso de corticosteroides. La DMO femoral se correlaciona mejor con el compromiso funcional y anatómico de rodilla, tobillo y pie.
A diferencia de la pérdida apendicular que es mayor m las etapas iniciales de la AR y que disminuye con la evolución, la pérdida axial es más tardía a no ser que haya una severa alteración funcional (postración) o que se usen dosis altas de esteroides(16).
Papel de dosis bajas de corticosteroides en la DMO de pacientes con AR
Hay una clara controversia en la literatura mundial sobre si dosis bajas de esteroides causan mayor osteoporosis en pacientes con AR o si, por el contrario, disminuyen el riesgo de esta al mejorar la inflamación y el estado funcional. Múltiples estudios evalúan este tópico (Tabla 1).
Lems y Jahangeir(15) publican un estudio que incluye hombres y mujeres postmenopáusicas con AK comparan usadores y no usadores de prednisona estratificándolos de acuerdo al tiempo de utilización y comparan esta población con individuos sanos. El 13% de los usadores de esteroides tuvieron fracturas vertebrales sintomáticas contra 2% de los no usadores (P < 0.003), además el 58% de las mujeres con AR tratadas con esteroides tuvieron deformidad vertebral lo que es muy superior al 15% de deformidad vertebral en mujeres de la población general(22).
Peel y Moore(21) encuentran que la DMO fue significativamente menor, en todos los sitios de medición, m mujeres con AR usadoras de esteroides, que en las no usadoras de estos; 27% de estas mujeres tuvieron deformidad vertebral contra el 5.8% de los controles. Sin embargo el hallazgo más importante de este estudio fue que el riesgo de fracturas fue mayor al esperado para el grado de pérdida mineral ósea lo que se explica por el efecto de los esteroides sobre la calidad ósea.
Tabla 1. Estudio de casos y controles para evaluar DMO en pacientes con AR y uso de esteroides
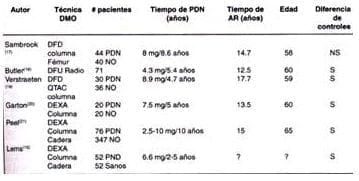
La mayoría de los estudios que evalúan el efecto esteroideo en la DMO de pacientes con AR se centran en evaluar DMO axial; Martín y Munro(23) evalúan DMO del radio ultradistal total, cortical y trabecular (Q TAC), DMO lumbar y femoral (DEXA) y eco de calcáneo BUA y SOS) en pacientes con AR y comparan pacientes con y sin dosis bajas de corticosteroides. El estudio demostró mayor pérdida apendicular que axial, específicamente no hubo una pérdida lumbar significativa, además la pérdida apendicular fue más trabecular (36%) que cortical (15%).
No hubo diferencia en la DMO vertebral entre casos y controles; la DMO femoral fue significativamente menor en los casos que en los controles, pero no hubo diferencias entre usadores y no usadores de esteroides. Esto refuerza la propuesta de utilizar mediciones de DMO apendicular como un marcador de mal pronóstico y de daño anatómico temprano en AR(24) más sensible y posiblemente más específico que la PCR, la VSG y los títulos de factor reumatoide.
Osteoartrosis
Los grandes estudios epidemiológicos(25) no concluyen que los pacientes con osteoartrosis nodular tengan mayor DMO apendicular que los controles sanos. Con la osteartrosis de cadera si se demuestra que los pacientes que la padecen tienen mayor DMO axial y apendicular que los controles. Hay 3 hipótesis para explicar esto:
1. Asociación causal (que la mayor DMO ocasione la coxartrosis) es la hipótesis con mayor respaldo experimental. La mayor rigidez del hueso subcondral que se presenta en personas con mayor DMO puede llevar a daño del cartílago con cargas de compresión axial normales.
2. Asociación indirecta (factores adicionales, como la obesidad, por ejemplo, ocasionen tanto la coxartrosis como el aumento de DMO).
3. Que la remodelación del hueso subcondral por la osteoartrosis ocasione una mayor DMO.
Espondilitis Anquilosante
Los estudios en conjunto(26) muestran que tempranamente hay una disminución de la DMO lumbar y femoral con DMO del carpo normal (trabecular). Tardíamente también disminuye la masa ósea del carpo (cortical) y la DMO espinal tiende a aumentar con la formación de sindesmofitos.
Bibliografía
1. Star V, Hochberg M. Osteoporosis in patients with rheumatic Diseases. Rheum. Dis. Clin. North Am. 1994; 20: 561-576.
2. Westhonens R, Nijs J, Taelman V. et al. Body composition in rheumatoid arthritis. Br J, Rheum. 1997; 36: 444-448.
3. Rajapakse J. Bone turnoner in early rheumatoid arthritis. Ann Rheum Dis. 1983; 46: 852- 857.
4. Sambrook P, Ansell B, Foster S. et al. Bone turnoner in early rheumatoid arthritis, 1 Biochemical and kinetics indexes. Ann Rheum Dis, 1985; 44: 575-579.
5. Gough A, Sambrook P, Devlin J. et al. Osteoclastic activation is the principal mechanism leading to secundary osteoporosis in RA. J Rheum. 1998; 25: 1282-1289.
6. Sambrook P, Ansell B, Foster S. et al. Bone turnoner in early rheumatoid arthritis. 2 longitudinal bone density studies. Ann Rheum Dis. 1985; 44: 580-584.
7. Lane N, Goldring S. Bone loss in RA: What role does inflamation play?. J. Rheum. 1998; 25: 1251-1253.
8. Cortet B, Flipo RM, Pigny P. et al. Isturnoner a determinant of bone mass in RA?. J. Rheum. 1998; 25: 2339-2344.
9. Fujikawa Y, Shingu M, Torisu T. et al. Bone resorption by tartrate-resistant acid phosphatase-positive multinuclear cells insolated from rheumatoid sinovium. Br J. Rheum. 1996; 35: 213-217.
10. Brik R, Keidar Z, Schapira D. et al. Bone mineral density and turnoner in children with sistemic juvenil chronic arthritis. J Rheum; 1998; 25: 990-992.
11. Polito C, Strano C, Rea L. et al. Reduced bone mineral content and serum osteocalcin in non-steroid treated patients with juvenile rheumatoid arthritis. Ann Rheum Dis 1995; 54: 193-196.
12. Gough A, Sambrook P, Devlin J. et al. Effect of vitamin D receptor gene alleles on bone loss in early RA. J. Rheum. 1998; 25: 864-868.
13. Patel MS, Cole DEC, Rubin LA. The golem for osteoporosis genetics. J Rheum. 1998; 25: 831-833.
14. Sambrook P, Eisman J, Champion D. et al. Determinants in axial bone loss in rheumatoid arthritis. Arth Rheum. 1987; 30: 721-728.
15. Lems WF, Jahangier ZN, Jacobs FW, et al. Vertebral fractures in patients with rheumatoid arthritis treated with corticosteroids. Clin. Exp. Rheum. 1995; 13: 293- 297.
16. Als O, Gotfredsen A, Riis B. et al. Are disease duration and degree of functional imparirment determinants of bone loss in rheumatoid arthritis?. Ann Rheum Dis. 1985; 44: 406-411.
17. Sambrook P, Eastman J, Jeates M. et al. Osteoporosis in rheumatoid arthritis: Safety or low dose o corticosteroids. Ann Rheum Dis. 1986; 45: 950-954.
18. Butler R, Davie M, Worsfold M. et al. Bone mineral content in patient with rheumatoid arthritis: Relation ship to low-dose steroid therapy. Br J. Rheum. 1991; 30: 86-90.
19. Verstraeten A, Degueker J. Vertebral and periferical bone density content and fracture incidence in postmenopausal patients with rheumatoid arthritis: effects of low dose of corticosteroids. Ann Rheum Diss 1986; 45: 852-856.
20. Garton MJ, Reid DM. Bone mineral density of the hip and the anteroposterior and lateral dimensions of the spine of men with rheumatoid arthritis: effects of low dose of corticosteroids. Arthritis Rheumatism. 1993; 36: 222-227.
21. Peel N, Moore D, Barrington N. et al. Risk of vertebral fracture and relation ship to bone mineral density in steroid treated rheumatoid arthritis. Am Rheum Dis. 1995; 54: 801-806.
22. Melton LJ, Khan SH, Wahner HW. et al. Epidemiology of vertebral fractures in women. Am J Epidem. 1989;129: 1000-1010.
23. Martin J, Munro R, Campbell M. et al. Effects of disease and corticosteroids on appendicular bone mass in postmenopausal women with rheumatoid arthritis: comparison with axial measuraments. Br J. Rheum, 1997; 36: 43-49.
24. Reid D, England A. Peripheral bone mass measuraments- is there any clinical value in rheumatoid arthritis? Br J Rheum. 1996; 35: 109-111
25. Hordon L, Curigth V, Smith M. Bone mass in osteoarthritis. Br J. Rheumatol, 1992; 31: 823-827.
26. Bronson W, Walkers Hillman L. et al. Bone mineral density and biochemical markers of bone metabolism in ankilosing spondylitis. J Rheumatol. 1998; 25: 929-935.