La tasa de refutar el participar en el estudio fue apenas del 5%. Se entrevistaron un total de 4.100 mujeres. De ellas, 235 (5.6%) se excluye-ron por datos incompletos, dejando un total de 3.965 para el análisis. La característica de la muestra se resume en la Tabla 1. La edad promedio de las participantes fue de 54.3±5.1 años (rango de 45 a 64 años) y el promedio de tiempo trascurrido desde la menopausia fue de 6.6±5.0 años. El porcentaje de fumadoras actuales fue del 11.8%, en un rango de 1.3 (Lima, Perú) a 77.3% (La Habana, Cuba). El porcentaje de usuarias actuales de TH en toda la muestra fue del 24.7%, en un rango de 3.6% (Santiago de los Caballeros, República Dominicana) a 69.9% (Cochabamba, Bolivia).
Encontramos que 87.6; 62.5; 35.1; 13.5 y 3.2% de la población tenía al menos 1, 2, 3, 4, o 5 componentes respectivamente (Tabla 2). El NCEP ATP III considera que los sujetos que tienen SM tienen tres o más componentes; por lo tanto, casi una tercera parte de la población posmenopáusica latinoamericana entrevistada en este estudio puede clasificarse como que tiene esta condición.
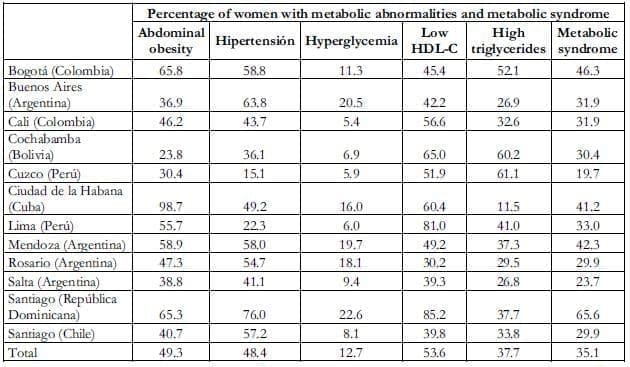
Un alto porcentaje de mujeres tienen al menos un factor de riesgo de SM (Tabla 2). Además, más de un tercio de toda la muestra (35.1%) presentó tres o más factores de riesgo simultáneamente y por lo tanto fue diagnosticada como SM. Todos los cinco factores de riesgo se encontraron en 3.2% de las mujeres encuestadas. Se observaron grandes diferencias entre los diferentes centros en la prevalencia del SM (Tabla 3). El factor de riesgo más prevalente fue el HDL-C bajo, afectando el 53.6% de las mujeres.
Otros factores de riesgo, tales como obesidad abdominal, hipertensión nivel de triglicéridos altos e hiperglicemia se presentaron en un 49.3%, 48.4%, 37.7% y 12.7%, respectivamente.
Tabla 2. Prevalencia en cada Centro de las 3.965 mujeres latinoamericanas posmenopáusicascon uno o más componentes del SM, basados en el National Cholesterol EducationAdult Treatment Panel III (NCEP ATP III)
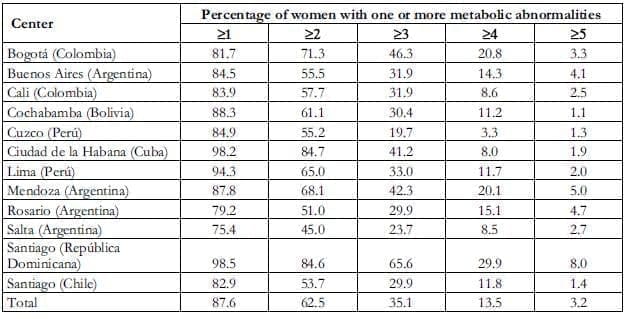
Tabla 3. Prevalencia de componentes individuales del SM basados en las guías del National Cholesterol Education Adult Treatment Panel III (NCEP ATP III) en 3.965 mujeres posmenopáusicas latinoamericanas
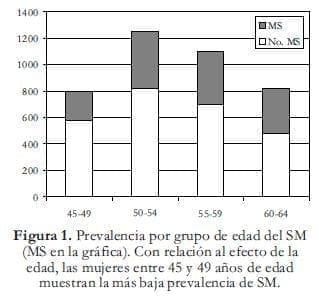
Acerca del efecto de la edad en la prevalencia del SM, mujeres entre 45 y 49 años de edad mostraron una prevalencia del 28.1%, más bajo que el 34.1%, 35.6% y 42.9% observado en los grupos de edad de 50-54, 55-59 y 60-64 años respectivamente (Figura 1). Análisis univarible ha mostrado que mujeres de 55 años de edad, con cinco o más años de menopausia y fumado-ras corrientes fueron las de más alto riesgo de SM (RR, 1.35, IC 95% 1.19-1.56. RR 1.32, IC 95% 1.1.5-1.51; y RR 1.24, IC 95% 1.05-1.466, respectivamente). En contraste, las usuarias corrientes de TH se asociaron con una significante disminución del riesgo (RR 0.61, IC 95% 0.52-0.70) El análisis multivariado de esos factores se muestra en la Tabla 4.
Tabla 4. Factores de riesgo de SM: análisis de regresión logística (multivariada)
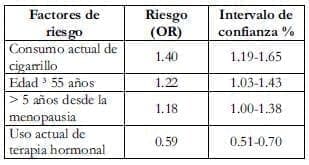
La obesidad abdominal implica un aumento del riesgo para SM (RR 13.01, IC 95% 0.52-0.70). Una circunferencia abdominal de ± 88 cm en el diagnóstico de SM tiene 84.4% de sensibilidad y 69.9% de especificidad y 60.4% de valor predictivo positivo. Un índice de masa corporal IMC de 30 (obesa) determinó también un riesgo alto para SM (RR 5.30, IC 95% 4.51-6.24), presión sanguínea ± 130/85 mmHg se asoció con un riesgo más alto de SM (RR 9.30, IC 95% 7.91-10.94). Este parámetro presentó 80.7% de sensibilidad, 69% de especificidad y 58.5% de valor predictivo positivo en el diagnóstico de SM. Finalmente, cuando ambos parámetros, obesidad abdominal e hipertensión, se juntan, el riesgo de SM se encontró extremadamente aumentado (RR 20.57, IC 95% 17.16-24.67). Esta asociación dio una sensibilidad del 66.7%, especificidad del 91.1% y 80.3 de valor predictivo positivo en el diagnóstico de SM.
Discusión
El principal hallazgo de este estudio fue la alta prevalencia del SM observado en mujeres posmenopáusicas latinoamericanas que se atendían en
centros de cuidado de la salud. Aunque los resultados no pueden ser transferidos a la población general, son muy similares a los encontrados por Ford y sus colegas en el estudio NHANES III (33%) y por Santos y su colegas11 en Portugal (35%) en estudios que incluían mujeres de edad media. Adicionalmente nuestros datos están de acuerdo con los observados en este pequeño número de poblaciones estudiadas realizado en Latinoamérica acerca de la prevalencia del SM12,13.
La mayor limitación de nuestro estudio es la comentada previamente acerca de la posible restricción de la generalización de los resultados a otras comunidades, puesto que nosotros solo evaluamos mujeres latinoamericanas; sin embargo, hay otros inconvenientes. Así, para una interpretación balanceada de los datos, la natural cortada-cruzada del presente estudio puede limitar la interpretación de las inferencias causales. Por ejemplo, nuestros datos sugieren que las usuarias de TH fueron menos propensas a tener SM; sin embargo, nos es claro si esto es porque aquellas con SM son menos posibles que sean formuladas con TH o si la TH protege contra el SM. Además, como este estudio es una muestra de conveniencia y no un estudio a escala nacional, no es posible controlarlo por sesgos debido a la autoselección en la encuesta o dentro de las clínicas donde la encuesta se terminó, y final-mente, importantes factores de conflicto tales como diferentes estilos de vida no fueron controlados. A pesar de las limitaciones, este es el primer estudio grande en Latinoamérica para explorar la prevalencia del SM.
La prevalencia del SM varía grandemente en el mundo en un rango de 12% en Ho Chi Minh, Vietnam14 y 18% en Hong Kong15 a 33.7% y 41.1% en países de Este Medio16,17. Además, la gente que vive en las áreas urbanas16 y los consumidores de dieta ricas en ácidos grasos saturados18 está a un riesgo mayor de SM, mientras aquellos que realizan intensa actividad física están a bajo riesgo18. Similarmente en nuestro estudio, la prevalencia de SM difiere ampliamente entre diferentes centros participantes, sugiriendo diferencias étnicas y de estilo de vida entre los países de latinoamérica.
El HDL-C fue el parámetro más frecuente-mente alterado, afectando el 53.6% de las mujeres en el estudio. Estos hallazgos están en concordancia con los datos de estudios hechos en la India19 e Irán17 pero en desacuerdo con los resultados del estudio NHANES III donde este desorden involucraba el 39.3% y 46.3% de las mujeres americanas de origen europeo y mexicano, respectivamente6.
La obesidad abdominal y la hipertensión afectaron al 49.3% y 48.4% de las mujeres encuestadas, respectivamente. Los datos fue-ron muy similares a los encontrados en el estu-dio NHANES III. La alta prevalencia de restos marcadores y su buen valor predicativo positi-vo cuando se combinaron podrían alertar a los doctores a buscar el diagnóstico de SM en todos los pacientes obesos abdominales. Reciente-mente, la International Diabetes Federation (IDF) ha determinado nuevos criterios diagnós-ticos de SM para mujeres (circunferencia abdo-minal de ≥ 80 cm y glucosa en ayunas de 100 mg/dL20). En el presente estudio aplicando esos criterios, la prevalencia de SM podría ha-ber sido de 50.2% en lugar de 35.1%. Estos datos están en desacuerdo con los de Ford y col., quienes no encontraron diferencia en la prevalencia de SM entre mujeres incluidas en el estudio NHANES III usando los criterios de la IDF de ATP III (34.5% a 37.1%).
El consumo de cigarrillo fue el factor de riesgo más importante relacionado con SM. Esta asociación ha sido ya descrita y posiblemente sugiere estilos de vida negativos22,23. Los sujetos que presentan estilos de vida negativos muy a menudo tienen más de un factor de riesgo: sedentarismo, obesidad, consumo de cigarrillo, alcohol, etc. En el presente estudio, como también en otros, el aumento de edad6,11-18 y el tiempo transcurrido desde la menopausia24 fueron otros factores de riesgo independientes para SM. En contraste, la TH aparece como un fuerte factor de riesgo protector. Por lo que sabemos, otros estudios acerca del efecto de la TH sobre la prevalencia del SM son limitados.
Varios estudios y meta-análisis han demostrado que el SM es un fuerte predictor de enfermedades crónicas tales como diabetes, infarto del miocardio y ACV25,26. Sin embargo, más que un buen predictor de enfermedad severa, esta entidad es un precursor de condiciones que pueden ser prevenidas. En este sentido, el estudio Finnish Diabetes Prevntion demostró una reducción significante en la incidencia de nuevos casos de diabetes después de un programa de cuatro años de estilos de vida saludable que incluye reducción de peso, disminución del con-sumo de las grasas saturadas y aumento de la ingesta de fibra y actividad física27.
En conclusión, el estudio sugiere que la prevalencia de SM entre mujeres posmenopáusicas latinoamericanas es alta y que la obesidad abdominal y la hipertensión son fuertes predictores. Cuando el SM se confirme, es esencial aconsejar a las pacientes e inculcarles inmediatamente cambios en el estilo de vida.
No se declaran conflictos de interés.
No se declaran fuentes de financiación.
Referencias
1. Haffner SM, Valdez RA, Hazuda HP, Mitchell BD, Morales PA, Stern MP. Prospective analysis of the insulin resistance syndrome (syndrome X). Diabetes 1992; 41: 715-722.
2. Isomaa B, Almgren P, Tuomi T, et al. Cardiovascular morbidity and mortality associated with the metabolic syndrome. Dia-betes Care 2001; 24: 683-689.
3. Trevisan M, Liu J, Bahsas FB, Menotti A. Syndrome X and mortality: a population-based study. Risk Factor and Life Expectancy Research Group. Am J Epidemiol 1998; 148: 958-966.
4. World Health Organization. Definition, diag-nosis and classification of diabetes mellitus and its complications. Report of a WHO Consultation. Part 1. Diagnosis and classifi-cation of diabetes mellitus. Geneva: WHO, 1999 (document WHO/NCD/NCS/99.2)
5. Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP). JAMA 2001; 285: 2486-2497. Metabolic syn-drome prevalence in Latin American postme-nopausal women Royer et al. Climacteric 169.
6. Ford ES, Giles WH, Dietz WH. Prevalence of the metabolic syndrome among US adults: findings from the Third National Health and Nutrition Examination Survey. JAMA 2002; 287: 356-359.
7. Carr MC. The emergence of the metabolic syndrome with menopause. J Clin Endocrinol Metab 2003; 88: 2404-2411.
8. Hurd WW, Barhan SM, Rogers RE. Obste-trician- gynecologist as primary care provider. Am J Manag Care 2001; 7 Spec No: SP19-24.
9. Brett KM, Chong Y. Hormone Replacement Therapy: Knowledge and Use in the United States. Hyattsville, Maryland: National Center for Health Statistics, 2001.
10. Ninomiya JK, L.Italien G, Criqui MH, Whyte JL, GaMetst A, Chen RS. Association of the metabolic syndrome with history of myocardial infarction and stroke in The Third National Health and Nutrition Examination Survey. Circulation 2004; 109: 42-46.
11. Santos AC, Lopes C, Barros H. Prevalence of metabolic syndrome in the city of Porto. Ver Port Cardiol 2004; 23: 45-52.
12. Aguilar-Salinas CA, Rojas R, Gomez-Perez FJ, et al. High prevalence of metabolic syndrome in Mexico. Arch Med Res 2004; 35: 76-81.
13. Ministerio de Salud (República de Chile). Pontificia Universidad Católica de Chile. Universidad de Chile. Encuesta Nacional de Salud Chile 2003. https://www.emol.com/ noticias/ documentos/informe_salud.pdf (accessed Feb 2006)
14. Son le NT, Kunii D, Hung NT, Sakai T, Yamamoto S. The metabolic syndrome: prevalence and risk factors in the urban population of Ho Chi Minh City. Diabetes Res Clin Pract 2005; 67: 243-250.
15. Thomas GN, Ho SY, Janus ED, Lam KS, Hedley AJ, Lam TH. Hong Kong Cardiovascu-lar Risk Factor Prevalence Study Steering Committee. The USNational Cholesterol Education Programme Adult Treatment Pa-nel III (NCEP ATP III) prevalence of the metabolic syndrome in a Chinese population. Diabetes Res Clin Pract 2005; 67: 251-257.
16. Al-Nozha M, Al-Khadra A, Arafah MR, et al. Metabolic syndrome in Saudi Arabia. Saudi Med J 2005; 26: 1918-1925.
17. Azizi F, Salehi P, Etemadi A, Zahedi-Asl S. Prevalence of metabolic syndrome in an urban population: Tehran Lipid and Glucose Study. Diabetes Res Clin Pract 2003; 61: 29-37.
18. Athyros VG, Bouloukos VI, Pehlivanidis AN, et al. MetS-Greece Collaborative Group. The prevalence of the metabolic syndrome in Greece: the MetS-Greece Multicentre Study. Diabetes Obes Metab 2005; 7: 397-405.
19. Gupta R, Deedwania PC, Gupta A, Rastogi S, Panwar RB, Kothari K. Prevalence of metabolic syndrome in an Indian urban population. Int J Cardiol 2004; 97: 257-261.
20. International Diabetes Federation. The IDF consensus worldwide definition of the metabolic syndrome. Brussels: IDF 2005. Available at: https:// www.idf.org/webdata/docs/IDF_Meta syndrome_definition.pdf (accessed May 2005).
21. Ford ES. Prevalence of the metabolic syndrome defined by the International Dia-betes Federation among adults in the U.S. Diabetes Care 2005; 28: 2745-2749.
22. Ishizaka N, Ishizaka Y, Toda E, Hashimoto H, Nagai R, Yamakado M. Association between cigarette smoking, metabolic syndrome, and carotid arteriosclerosis in Japanese individuals. Atherosclerosis 2005; 181: 381-388.
23. Park YW, Zhu S, Palaniappan L, Heshka S, Carnethon MR, HeyMetsfield SB. The metabolic syndrome: prevalence and associa-ted risk factor findings in the US population from the Third National Health and Nutrition Examination Survey, 1988-1994. Arch Intern Med 2003; 163: 427-436.
24. Mesch VR, Boero LE, Siseles NO, et al. Metabolic syndrome throughout the menopausal transition: influence of age and menopausal status. Climacteric 2006; 9: 40-48.
25. Ford ES. Risks for all-cause mortality, cardio-vascular disease, and diabetes associated with the metabolic syndrome: a summary of the evidence. Diabetes Care 2005; 28: 1769-1778.
26. Najarian RM, Sullivan LM, Kannel WB, Wilson PW, D.Agostino RB, Wolf PA. Metabolic syndrome compared with type 2 diabetes mellitus as a risk factor for stroke: the Framingham Offspring Study. Arch Intern Med 2006; 166: 106-111.
27. Tuomilehto J, Lindstrom J, Eriksson JG, et al. Finnish Diabetes Prevention Study Group. Prevention of type 2 diabetes mellitus by changes in lifestyle among subjects with impaired glucose tolerance. N Engl J Med 2001; 344: 1343-1350.
