william Otero, Fernando Sierra
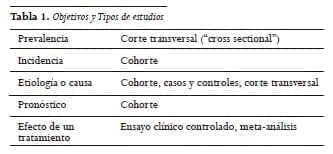
Cada tipo de estudio está diseñado para responder diferentes preguntas. Los estudios observacionales, analíticos, (cohorte, corte transversal, meta-análisis y casos y controles) en los cuales el investigador solamente “observa”, tienen objetivos diferentes de los estudios de intervención (1) (Tabla 1), por lo cual sus resultados y conclusiones se expresan estadísticamente de manera diferente.
El meta-análisis, es una técnica estadística para evaluar la eficacia clínica de intervenciones en salud, combinando los hallazgos de dos o más ensayos clínicos independientes y por ello se le puede considerar un “estudio de estudios”.
Los ensayos clínicos aleatorizados (“randomized controlled trials”) bien diseñados, son la mejor estrategia para evaluar el beneficio de un tratamiento y por ello se consideran la mejor evidencia sobre la eficacia de las intervenciones médicas (2).
Sin embargo, para que sus resultados puedan ser adecuadamente evaluados y no generen confusión, es necesario que sean expresados de manera comprensible, y para que el lector pueda hacer a adecuada interpretación de los mismos es necesario que esté familiarizado con las diferentes medidas del impacto o efectos de ese tratamiento.
Las medidas de impacto que mejor expresan las magnitud del efecto son las siguientes: reducción de riesgo relativo (RRR), reducción absoluta del riesgo (RAR), número necesario de tratar (NNT), número necesario para producir daños o efectos adversos (NND “NNH”).
Reducción del riesgo relativo
También llamada fracción atribuible. Esta medida compara el riesgo de un resultado desfavorable en el grupo de pacientes que reciben un tratamiento, con el riesgo de ese desenlace en los que reciben placebo o un nuevo medicamento, que se está comparando con tratamiento que se venía utilizando (3-6).
En un ensayo clínico, lo más frecuente es que en cada paciente ese resultado se represente mediante una variable binaria o dicotómica (del tipo si o no), como por ejemplo, recidiva tumoral, curación de una enfermedad, erradicación de una infección, etc.
El resultado para un grupo de pacientes es la proporción de pacientes en los que el evento ocurre.
Esta proporción estima la probabilidad o riesgo del evento en ese grupo y para evaluar el efecto de ese tratamiento, hay que comparar el riesgo en el grupo tratado con el riesgo en el grupo control (7), que, en resumen, se trata de comparar dos números. Esta comparación se hace de la siguiente manera:

Ejemplo: en un ensayo clínico doble ciego, aleatorizado, se comparó la incidencia de primer sangrado por várices esofágicas (SVE), entre pacientes tratados con ß bloqueadores versus tratados con placebo (8). En el primer grupo se produjo SVE 2/51 (4%) y en el segundo grupo 11/51 (22%).
La RRR = 22% – 4% /22%= 82%.
Este resultado significa que en los pacientes que reciben beta bloqueador (BB) y tienen várices esofágicas es 82% menos probable que desarrollen SVE si se compara con los que tienen VE y toman placebo.
Como puede verse, con esta medida no se percibe muy claramente el verdadero impacto que se pudiera tener cuando se aplican tales resultados a nuestros pacientes, puesto que compara el riesgo de eventos entre pacientes con tratamientos y con placebo, es decir, ilustra el beneficio del tratamiento en términos relativos.
Posiblemente, en la práctica diaria lo que realmente se desearía determinar es el desenlace en los pacientes tratados, es decir, la reducción del riesgo absoluto o disminución absoluta del riesgo (RAR).
Posiblemente la utilidad de la RRR es cuando se aplica a subgrupos de pacientes con diferentes riesgos intrínsecos de desenlaces desfavorables, que en el ejemplo que nos ocupa, pudiera expresarse teniendo en cuenta la clase funcional de la cirrosis con base en la clasificación de Child-Turcotte.
Sin embargo, algunos autores definitivamente consideran que esa variación puede ser clínicamente irrelevante (9).
Cuando se evalúa la RRR en subgrupos de alto riesgo, ésta es consistente en los diferentes subgrupos de pacientes. Otra forma de expresar la RRR es 1-RR (riesgo relativo) X 100.
El riesgo relativo (RR), es el cociente entre el grupo placebo y el del grupo tratado (4, 5) o al contrario, dependiendo del evento que se esté estudiando y el diseño del estudio ya que si se está estudiando la exposición a un tóxico para observar la aparición de un desenlace específico, el RR será el cociente entre la incidencia del evento en el grupo expuesto, sobre la incidencia en el grupo no expuesto, y el RR se expresará como las veces en que es más probable que el evento ocurra entre los expuestos, comparados con los no expuestos.
El RR es la medida de asociación que se utiliza en ensayos clínicos o estudios de intervención y estudios de cohorte, como la OR se utiliza en estudios de casos y controles y de prevalencia analítica (1).
Reducción absoluta del riesgo
Esta medida estima la disminución real de desenlaces desfavorables entre los pacientes que reciben un determinado tratamiento y se calcula sencillamente mediante una resta entre la diferencia absoluta del riesgo entre el grupo tratado y el grupo control (3-6).
RAR = Incidencia en el grupo con placebo _ incidencia en el grupo tratado.
En el ejemplo anterior sería: 22%_4%=18%. Este resultado se interpreta de la siguiente manera: los pacientes con VE que reciben beta bloqueador disminuyen el riesgo de SVE en 18% o dicho de otra manera, por cada 100 pacientes con cirrosis y VE tratados con beta bloqueador durante el periodo que duró el estudio, se evitan 18 SVE con respecto a los que se hubieran evitado si se utilizara placebo.
Esta medida expresa las consecuencias de dar ese tratamiento y por ello también se le llama reducción atribuible del riesgo o riesgo atribuible (6).
En ocasiones se habla de diferencia absoluta de riesgo (DAR) (9) y la resta se hace al revés: incidencia del efecto adverso en el grupo tratado, menos la incidencia en el grupo control, dando lugar a un cambio de signo, es decir dando un valor negativo si el tratamiento reduce el riesgo y positivo si lo aumenta. En el ejemplo que traemos sería:
4%-22% = – 18%.
No obstante, la ventaja interpretativa con respecto a la RRR, la RAR tiene inconvenientes para ser recordada e incluso interpretada cuando es menor de 1 y por lo tanto, la mejor estimación actualmente considerada es el número necesario de tratar o NNT.
Número necesario de tratar
Este índice es otra forma de expresar la RAR y es el número estimado de pacientes que se necesita tratar con un tratamiento definido (nuevo, experimental, etc.) para que se beneficie un paciente adicional o se prevenga un desenlace indeseable en comparación con el grupo control (10-12). Se calcula como el recíproco de la RRA, o sea: NNT = 1/RAR (10-12).
Debe tenerse en cuenta la palabra “adicional” de la definición. En el ejemplo que nos ocupa, el riesgo de SVE en el grupo control es 22% y en el grupo con BB, 4% y por lo tanto RAR es 18% lo que significa que por cada 100 paciente que sigan el tratamiento con BB se evitarían 18 SVE con respecto al grupo placebo y por lo tanto para evitar un episodio de SVE se necesitará tratar 1/0,18 ó 100/18 = 5,6.
En el numerador se utiliza 1 si la RAR se expresa como proporción (decimales) o 100 si se utilizan porcentajes (12). Entre mayor sea el beneficio del tratamiento, menor será el NNT y por lo tanto si el tratamiento no tuviera ningún efecto, la RAR sería cero y el NNT infinito (1/0) y esto trae inconvenientes para calcular su intervalo de confianza (12).
El NNT es específico de cada tratamiento, siempre se refiere a comparaciones con otro grupo (que recibe placebo, ningún tratamiento u otro tratamiento), un desenlace particular y un período definido de tratamiento (13) y por lo tanto para que el NNT y el NND (véase más adelante) sean claramente interpretados, siempre se les debe especificar su comparador, el desenlace terapéutico y la duración del tratamiento para que se produzca ese desenlace (13).
No hay un valor absoluto para un NNT que diga si determinado tratamiento es útil o no.
Un NNT de 1 significa que el desenlace en estudio se produce en cada paciente que recibe el tratamiento.
Teniendo en cuenta que pocos tratamientos tienen eficacia de 100% y pocos controles (placebos o no tratamiento) no tienen ningún efecto, los tratamientos por muy eficaces que sean, usualmente están en el rango de 2-4, excepto los antibióticos y por ejemplo la terapia triple para erradicar H. pylori tiene un NNT de 1,1 (14).
El NNT es solo una parte de la información requerida para tomar decisiones y aunque sea un término clínico concreto, a la hora de decidir una conducta terapéutica, también se deben tener en cuenta otros factores como costos, efectos adversos, características de los pacientes y prioridades sociales y de los servicios médicos.
El NNT es el índice con más popularidad por su simplicidad y capacidad para resumir el efecto de una intervención y el que en la actualidad se está utilizando con más frecuencia, aunque también existen quejas sobre su mal uso en los meta-análisis (15). Sin embargo, otros expertos consideran que sí pueden ser utilizados en estos últimos (13,16).
No se debe olvidar que los NNTs son una representación o herramienta y como tal cuando se usa adecuadamente tendrá utilidad y como otras medidas estadísticas, es una estimación de la verdad que debe estar acompañada de sus respectivos intervalos de confianza, que especifican los límites dentro de los cuales se puede considerar con seguridad los valores que están expresando (12).
A pesar de la claridad de estas últimas medidas:
Es sorprendente que hasta hace poco tiempo un mínimo número de investigadores las empezaron a utilizar para exponer los resultados de sus estudios.
Recientemente, se revisaron 4 años (1989, 92, 95, 98) de las cinco revistas más frecuentemente citadas: New England Journal of Medicine, Lancet, Annals of Internal Medicine, JAMA y British Medical Journal y se encontró que de 359 artículos elegibles, el NNT fue utilizado en 8 artículos y seis de estos fueron de 1998 y la RRA en 18 artículos, 10 de los cuales de 1998 (17).
Si el NNT no es proporcionado en un ensayo clínico, el lector puede calcularlo, teniendo en cuenta la incidencia del evento en estudio en los dos grupos de tratamiento, con los cuales puede calcular la RAR y aplicar la fórmula. Lo mismo se puede hacer con el NND. Cuando los meta-análisis no sintetizan sus resultados en forma de NNT (sobre todo los de hace algu
nos años), sino como OR o RR, estos pueden convertirse en NNT o NND utilizando fórmulas para ello (16).
Un NNT negativo significa que el tratamiento tiene un efecto peligroso o perjudicial.
Un NNT de _15 indica que si 15 pacientes son tratados con el nuevo medicamento, uno menos podría tener un buen resultado que si todos ellos recibieran el tratamiento estándar o convencional. Este NNT negativo, también se conoce como NND (NNH de “harm”).
Para algunos el NNT y NND no son buenas abreviaturas y sería más apropiado que el número necesario para tratar para que un paciente adicional se beneficie o se perjudique, sería NNTB (número necesario de tratar para producir un beneficio) y NNTH (número necesario de tratar para producir un perjuicio) respectivamente (12).
Una apreciación de la relación riesgo/beneficio, puede ser representada por la relación NNT/NND (14). Una relación menor de 1 podría indicar que los riesgos clínicos sobrepasan los beneficios (14).
Número necesario para dañar o lesionar (NND, NNH)
Si la intervención, en vez de producir beneficio produce efectos adversos, se utiliza el NND y se siguen los mismos pasos que para el NNT teniendo en cuenta que en vez de utilizar la RAR se utiliza el aumento absoluto del riesgo (AAR) y el inverso de este, será el NND que se expresa como el número de pacientes tratados que se necesitan para producir un efecto adverso adicional (16).
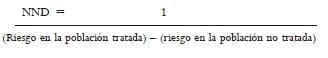
Referencias
- 1. Mann CJ. Observational research methods. Research design II: cohort, cross sectional, and case-control studies. Emerg Med J 2003;20:54-60.
- 2. Gray JAM. Evidence-based healthcare. NY: Churchil Livingstone; 1997.
- 3. Friedland DJ. Guide for assessing the validity of a study. In Friedland DJ (ed). Evidence-based Medicine. London: Appeton & Lange; 1998:153-182.
- 4. Guyatt GH, Sackett DL, Cook DJ. User´s guides to the medical literature. II. How to use an article about therapy or prevention. JAMA 1994;271:59-63.
- 5. Maya JM, Torres Y. Concepto de causa, medición de riesgos y sus aplicaciones. En: Blanco JH, Maya JM (eds). Fundamentos de salud pública, Medellín: CIB; 2000:36-46.
- 6. Abraira V. Medidas del efecto de un tratamiento (I): reducción absoluta del riesgo, reducción relativa del riesgo y riesgo relativo. Semergen 2000;26:535-536.
- 7. Oxman A, Guyatt G. A consumer´s guide to subgroup análisis. Ann Intern Med 1992;116:78-81.
- 8. Conn HO, Grace ND, Bosh J. Propranolol in the prevention of the first hemorrhage from esophagogastric varices. Hepatology 1991;13:902-911.
- 9. Feinstein AR. Individual comparisons and unmet clinical challenges. Am J Med 1992;92:117-120.
- 10. Laupacis A, Sackett DL, Roberts RS. An assessment of clinically useful measures of the consequences of treatment. N Engl J Med 1988; 318:1728-1733.
Bibliografías
- 11. Cook RJ, Sackett DL. The number needed to treat: a clinically useful measure of treatment effect. Br Med J 1995;310: 452-454.
- 12. Altman DG. Confidence intervals for the number hended to treta. Br Med J 1998;317:1309-1312.
- 13. McQuay HJ, Moore RA. Using numerical results from systematic reviews in clinical practice. Ann Intern Med 1997;126:712-720.
- 14. Moore A, McQuay HJ. www.evidence based medicine co.uk
- 15. Smeeth L, Haines A, Ebrahim S. Numbers needed to treat derived from meta-analysis sometimes informative, usually misleading. Br Med J 1999;318:1548-51
- 16. Sackett DL, Strauss SE, Richardson WS, et al. Medicina basada en la evidencia. 2ª Edición, Madrid, 2001.
- 17. Nuovo J, Melnikov J, Chang D. Reporting number need to treatment and absolute risk reduction in randomized controlled trials. JAMA 2002;287:2813-2814.
Autores:
William Otero, MD, gastroenterólogo, Internista, Epidemiólogo, Profesor asistente de medicina, Universidad Nacional de Colombia. Jefe de Gastroenterología Clínica Fundadores.
Fernando Sierra, MD, gastroenterólogo, Internista, Epidemiólogo Clínico. Profesor de Medicina Escuela Colombiana de Medicina. Jefe de Gastroenterología Fundación SantaFé. Presidente Asociación Latinoamericana de Hepatología. Bogotá, DC. Rev Colomb Gastroenterol 2003;18:46-48.