Conceptos para la Identificación y Abordaje de la Gangrena de Fournier
Concepts for the Identification and Approach of Fournier’s Gangrene
Resumen
Introducción. La gangrena de Fournier es una fasciitis necrosante fulminante y progresiva, de origen infeccioso sinérgico polimicrobiano, que afecta las regiones perianal, perineal, genital y abdominal.
Su incidencia es mayor en hombres, la edad promedio de presentación reportada está en los 54,7 ± 15,6 años, su mortalidad es del 3-67 %, aunque hay estudios que informan una mortalidad en hombres del 7,5 % y en las mujeres del 12,8 %.
Métodos. Se hizo una revisión de la literatura en las bases de datos y fuentes de información PubMed, Scielo y Google Scholar, publicados entre 1950 y 2018, utilizando términos como “fournier gangrene”, “fasciitis, necrotizing”, “wound infection”, “therapy”[subheading] y “GRADE approach”.
Se realizó una segunda revisión para artículos latinoamericanos en español hasta 2020 usando las mismas fuentes y palabras claves.
Resultados. Se seleccionaron artículos que reportaron definiciones, datos históricos, actualizaciones en diagnóstico y terapéutica para hacer una revisión actualizada. Para el uso de las imágenes se solicitó consentimiento informado.
Conclusión. La gangrena de Fournier continúa siendo una emergencia quirúrgica potencialmente letal. Gracias a las investigaciones realizadas se ha avanzado en su tratamiento, mejorando los resultados. Es importante analizar los factores de riesgo en cada paciente y su etiología para establecer el tratamiento más adecuado.
Palabras clave: fascitis necrotizante; gangrena de Fournier; infección; tejidos blandos; tratamiento.
Abstract
Introduction. Fournier’s gangrene is a fulminant and progressive necrotizing fasciitis of synergistic polymicrobial infectious origin that affects the perianal, perineal, genital and abdominal regions. Its incidence is greater in men, the average age of reported presentation is 54.7 ± 15.6 years; its mortality is 3-67%, although there are studies that report a mortality of 7.5% in men and 12.8% in women.
Methodology. A review of the literature was carried out in the databases and information sources: PubMed, Scielo, and Google Scholar, published between 1950 and 2018 using terms such as “Fournier Gangrene”, “Fasciitis, Necrotizing”, Wound Infection, “therapy”[Subheading] and “GRADE Approach”.
A second review was performed for articles in Latin American Spanish up to 2020 using the same sources and keywords.
Results. Articles that reported definitions, historical data, diagnostic and therapeutic updates were selected, performing an updated review. Informed consent was requested for the use of images.
Conclusion. Fournier’s gangrene continues to be a potentially lethal surgical emergency, thanks to the research carried out, progress has been made in its treatment, improving results. It is important to analyze the risk factors for each patient and its etiology to establish the most appropriate treatment.
Keywords: necrotizing fasciitis; Fournier’s gangrene; infection; soft tissues; treatment.
Introducción
La gangrena de Fournier (GF) es una fasciitis necrosante rápidamente progresiva, de origen polimicrobiano, potencialmente mortal, que afecta principalmente las regiones perianal, perineal, genital o abdominal, conduciendo a trombosis de los pequeños vasos subcutáneos que lleva a la necrosis de la piel adyacente.
La literatura reciente informa que la GF tiene una menor mortalidad y letalidad, con una etiología más frecuentemente identificada, y una edad media de presentación más alta, pero con un inicio más insidioso 1–3.
Fue descrita por primera vez en 1764 por Baurienne, quien informó el caso de un niño que había sido herido por el cuerno de un buey 4, sin embargo, lleva el nombre del dermatólogo y venereólogo francés Jean Alfred Fournier, quien en 1883 presentó cinco casos de gangrena escrotal rápidamente progresiva, de etiología desconocida, caracterizados por una necrosis extensa del tejido subcutáneo y la fascia superficial con acúmulos de exudado, edema y gas en pacientes masculinos jóvenes previamente sanos 1–5.
Se han empleado diversos términos para describir esta condición clínica tales como:
Gangrena estreptocócica, fascitis necrosante, flegmón peri-ureteral, celulitis sinérgica necrotizante, síndrome idiopático del pene, escroto y erisipela gangrenosa perineal 2 e incluso infección bacteriana “come-carne” en la literatura sensacionalista 6.
Meleney en 1924, la denominó gangrena estreptocócica hemolítica aguda, al identificar al estreptococo betahemolítico como agente causal 7; Wilson en 1952 acuñó el término de fasciitis necrosante, al describir que esta infección afectaba los tejidos blandos superficiales, como la fascia de Camper y Scarpa, sin comprometer la aponeurosis de los músculos 8.
Actualmente se reconoce a la gangrena de Fournier como una emergencia quirúrgica potencialmente letal, que afecta a ambos sexos y en todas las edades, con mayor incidencia en pacientes con enfermedades crónicas cardiacas, diabéticos mal controlados y pacientes inmunodeprimidos. Su etiología puede ser identificada en un 95 % de los casos y requiere un manejo oportuno, agresivo y multidisciplinario 2,3,9.
Epidemiología
Se estima que en todo el mundo 13 millones de personas al año son hospitalizadas por fasciitis necrosante 6. Esta patología afecta tanto a hombres como a mujeres, con una relación 9-10/1. La edad promedio de presentación es de 54,7 ± 15,6 años 10,11, siendo más frecuente en edades avanzadas 2,5,10. En Estados Unidos la incidencia es de 1,6 casos por cada 100.000 hombres por año y representa el 0,02 % de las admisiones hospitalarias.
Tiene un pico de incidencia a los 50 años, con 3,3 casos por 100.000 varones por año, y se incrementa 0,2 casos por 100.000 pacientes por cada aumento regional del 1 % de la prevalencia de diabetes mellitus 4,5,10,11.
La tasa de mortalidad varía entre 20-40 %. Reino Unido reporta una mortalidad global de 18-20 % 4, la cual ha ido disminuyendo según los reportes más recientes de series de casos, aunque hay pocos datos poblacionales sobre la incidencia de esta patología. Estos pacientes representan el 0,02 % de los ingresos hospitalarios 12.
Un estudio poblacional realizado por Sorensen y colaboradores en Estados Unidos, publicado en el 2009, se encontró una mortalidad del 7,5 % (n=1641), que fue mayor en las mujeres (12,8 %), sin una diferencia estadísticamente significativa, mientras en el estudio de Eke (n=1726) describieron una mortalidad del 16 % 12.
Otros trabajos se informó una mortalidad entre el 3-67 % 13-15. En un estudio realizado en Argentina entre el 2005 y el 2007 se observó que la tasa de mortalidad era del 23 %, siendo la causa más frecuente la sepsis (83,3 %) 16. En dos estudios realizados en Colombia, se encontró una mortalidad del 26 % 17,18.
Las comorbilidades que predisponen a su aparición y empeoran su pronóstico son diabetes mellitus, senilidad, alcoholismo crónico, enfermedad vascular periférica, terapia con corticoides, desnutrición severa, radioterapia, quimioterapia, defectos sensitivo neuronales, cardiopatía orgánica, insuficiencia cardiaca congestiva, hipertensión arterial, cirrosis, lupus eritematoso, promiscuidad, drogadicción, inmunosupresión, falla renal y vasculitis 6,19,20.
La diabetes mellitus está presente en 20-70 % y el alcoholismo crónico en 25-50 % de los pacientes 21.
En un estudio realizado en Chile se encontró como comorbilidad más frecuente la diabetes mellitus en un 58 %, seguido por el tabaquismo 41,1 %, alcoholismo crónico 35,4 %, hipertensión arterial 32,2 %, obesidad 25,8 % y patología anorrectal 19 % 22.
Otro estudio publicado en Chile mostró una asociación con la diabetes mellitus del 66,6 %23. En México un estudio reportó el alcoholismo crónico como la comorbilidad más frecuente (70,5 %), seguido por la diabetes mellitus (52,3 %), 24.
Los pocos estudios que han evaluado la mortalidad y el momento quirúrgico, definido como el intervalo desde el inicio de los síntomas hasta la primera intervención quirúrgica, sugieren que una intervención temprana entre el segundo y séptimo día puede reducir significativamente la mortalidad, por lo que es importante seleccionar adecuadamente a los pacientes con mayor riesgo mediante un sistema de puntuación para definir un diagnóstico inicial que permita decidir el momento quirúrgico más apropiado 20.
Etiopatogenia
Esta patología tiene un origen infeccioso poli microbiano y sinérgico 2,3,5,6,24-26 (tabla 1).
Tabla 1. Agentes microbianos implicados como agentes
etiológicos de la gangrena de Fournier.
——————————————
Aeróbicos gramnegativos
Escherichia coli (48-61,4 %)
Pseudomonas aeruginosa
Proteus mirabilis
Klebsiella pneumoniae
Providencia sturtii
Cocos aeróbicos grampositivos
Enterococos faecalis (28 %)
Estafilococos aureus (33-34,8 %)
Estafilococos epidermidis (10-30 %)
Bacterias anaeróbicas
Bacteris fragilis
Bacteroides malaninogenicus
Estreptococo (13,1 %)
Clostridum
Organismos micóticos
Candida spp
Rhizopus mucor
Rhizopus arrihzus
—————————————————
Fuente: elaboración propia.
Los organismos aeróbicos se encuentran en el 10 % de los casos, los anaeróbicos en 20 % y el 70 % está constituido por flora microbiana mixta (aerobia y anaerobia). Un único organismo se aísla en menos del 10 % y en el 90 % de los casos se encuentran entre tres y cinco microorganismos 25.
En dos estudios realizados en Argentina los microorganismos más frecuentemente aislados fueron Escherichia coli en más del 50 % de los casos 16 y Escherichia coli 50 %, Bacteroides spp. 47 %, Estreptococo spp. 42 %, Estafilococo spp. 27 % y Enterobacter spp. 27 % 27. En un estudio realizado en Colombia los gérmenes más aislados fueron Escherichia coli 63 %, Bacteroides spp. 55 % y Peptostreptococcus spp. 42 %17. En un estudio realizado en Chile se encontró Escherichia coli como el agente causal en el 51,8 % 23.
Un gran número de estos gérmenes forman parte de la flora habitual de la vía digestiva y del periné 28. Actualmente la etiología se logra establecer hasta en el 95 % de los casos 29. Dentro de las causas más comunes se encuentran las infecciones anorrectales (30-50 %), genitourinarias (20-40 %) y cutáneas (20 %) 30.
El origen anorrectal es la etiología más frecuente y tiende a presentar un peor pronóstico en relación con las causas urológicas 31,32; se deben tener también en cuenta las causas ginecológicas y las de origen abdominal 6,33–35 (tabla 2).
Tabla 2. Origen anatómico de la gangrena de Fournier.
——————————————————————————————————————
|
Causas de origen anorrectal Causas de origen ginecológicas |
Causas de origen urogenital Estenosis uretral Usuario de sonda Litiasis uretral Biopsia prostática Cateterización traumática Trauma perineal Inserción de prótesis peneana Absceso escrotal Masaje prostático en relaciones sexuales Neoplasias Divertículos ureterales Ruptura traumática de la uretra Infección genitourinaria Causas de origen abdominal Apéndicitis aguda Enfermedad diverticular complicada Cáncer colorrectal Enfermedad de Crohn Hernias estranguladas |
——————————————————————————————————————
Fuente: elaboración propia.
Fisiopatología – Identificación y Abordaje de la Gangrena de Fournier
Fournier enfatizo tres características importantes en este proceso: iniciación brusca en hombres jóvenes saludables, progresión rápida y etiología desconocida 5.
La infección bacteriana conduce a trombosis de vasos subcutáneos pequeños y necrosis tisular, lo que produce bajas concentraciones de oxígeno y permite el crecimiento de anaerobios 36; la hipoxia y el consecuente infarto de los nervios de la región afectada inicialmente causa dolor, seguido de una hipoestesia regional 4. La microangiopatía diabética limita aún más la oxigenación tisular.
Los aerobios y los anaerobios actúan sinérgicamente y producen enzimas como colagenasa, heparinasa, hialuronidasa, estreptoquinasa y estreptodornasa, que destruyen los tejidos. La trombosis vascular y la necrosis dérmica se deben a la actividad de la heparinasa y la colagenasa producida por los aerobios. (Le puede interesar: Absceso en glúteo posterior a inyección intramuscular)
La actividad alterada de los leucocitos fagocíticos en el tejido necrótico es responsable de la propagación de la infección, ya que requieren oxígeno para la producción de radicales antibacterianos de alta energía 26,36,37.
El deterioro de la inmunidad celular provoca que la infección se disemine a una velocidad alarmante, de aproximadamente 2-3cm/h 6,38, por lo que una infección perianal puede penetrar la fascia de Colles, tomar anteriormente la fascia de Buck, la fascia de Dartos y alcanzar con rapidez la fascia de Scarpa y propagarse por la pared abdominal hasta la clavícula 4,39.
Presentación clínica – Identificación y Abordaje de la Gangrena de Fournier
La presentación clínica suele ser variable, desde un inicio insidioso, hasta lo que reportan algunas series como inicio rápido o abrupto. Incluso en algunas ocasiones se puede llegar a presentar como una sepsis sin foco aparente 40. En el 30–50 % de los casos hay síntomas urinarios, siendo la retención el más frecuente 5.
La presentación insidiosa se caracteriza por la presencia de síntomas prodrómicos no específicos como malestar general o regional, imposibilidad para sentarse y limitación de movimientos amplios.
Posteriormente evoluciona a dolor, tumefacción y eritema, configurando un cuadro de celulitis que puede comprometer por separado o en conjunto pene, escroto y periné.
En la presentación de inicio rápido o abrupto, pueden existir síntomas peri-rectales inespecíficos, con fiebre, edema, dolor genital o perineal, rubor, tumefacción de la zona afectada, eritema, escalofrío, necrosis, crepitación, retención aguda de orina, náusea y vómito (figura 1).
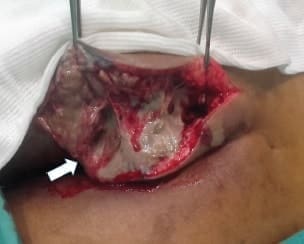
Figura 1. Femenina adulta joven, diabética, con proceso inflamatorio,
necrótico y enfisematoso del glúteo izquierdo.
La flecha blanca señala el tejido con necrosis.
Todos los pacientes presentan una combinación de cuatro o más de estos síntomas 19,32,40.
En su evolución clínica se pueden distinguir cuatro fases: la primera (24-48 horas), caracterizada por ser inespecífica, semejante a un cuadro gripal, asociada a un endurecimiento local con prurito, edema y eritema de los tejidos afectados 2,6.
La segunda o invasiva (48-72 horas), de corta duración y con manifestaciones inflamatorias locales, como dolor perineal, eritema escrotal o peneano y fiebre 6. En la tercera fase o de necrosis (4-10 días) ocurre un deterioro rápido del estado general, con evolución a shock séptico en el 50 % de los casos.
A nivel local, aumenta la tensión de los tejidos con flictenas hemorrágicas que evolucionan rápidamente a necrosis. Inicialmente hay disminución del dolor por la necrosis de los nervios y entre el octavo y décimo días el tejido necrótico es separado por un proceso supurativo de los tejidos adyacentes 2,5,40.
En la cuarta fase o de restauración, los pacientes que han sido tratados adecuadamente inician la restauración de los tejidos necrosados, con cicatrización lenta, granulación profunda y posteriormente epitelización. Ocurre también un restablecimiento progresivo de los parámetros generales 41.
En cuanto a las manifestaciones sistémicas, éstas suelen estar dadas por deterioro del estado general, marcada postración, náuseas y vómitos, progresando a alteraciones hidroelectrolíticas, sepsis, coagulopatía, choque y muerte 42.
Ersay et al. encontró que la presentación más común fue el dolor perianal o escrotal (78,6 %), seguido de taquicardia (61,4 %), crepitación (54,3 %) y fiebre (41,4 %) 43.
De acuerdo a su microbiología, la fasciitis necrosante se puede clasificar en cuatro tipos: El tipo I, es más frecuente, polimicrobiano, con gérmenes aeróbicos y anaeróbicos.
El tipo II es causado por un solo germen, generalmente Estreptococo del grupo A hemolítico beta o Estafilococo aureus. El tipo III es causada por organismos gramnegativos y el tipo IV por hongos 4.
Diagnóstico – Identificación y Abordaje de la Gangrena de Fournier
Se basa en una historia clínica completa, que incluya antecedentes por medio de los cuales se puede sospechar o establecer el origen de la infección en la mayoría de los pacientes.
Se debe diferenciar de la gangrena de origen no infeccioso y secundaria a enfermedad vascular causada por diabetes mellitus o enfermedad renal, al igual que de las infección dermatológicas 29,31,44.
En 1995 Laor et al. desarrolló el Índice de Severidad de Gangrena de Fournier (FGSI, por sus siglas en inglés) en un intento de evaluar la gravedad de la enfermedad.
En este índice se miden nueve parámetros: temperatura corporal, frecuencia cardíaca, frecuencia respiratoria, y niveles plasmáticos de sodio, potasio, creatinina, bicarbonato, hematocrito y recuento de leucocitos.
El grado de desviación de la normal se clasifica de 0 a 4. A continuación se suman los valores para obtener la puntuación o score (FGSIS, por sus siglas en inglés) 4,45.
El FGSI es una herramienta que nos entrega información sobre el pronóstico de estos pacientes.
Si el índice es > 9, la mortalidad es cercana al 75 %; si el índice es < 9, la tasa de supervivencia alcanza el 78 % 45. La adición de la edad del paciente y la extensión del proceso infeccioso aumentan aún más el valor predictivo del índice, con una puntuación >9 la probabilidad de muerte es del 94 %, y con puntuación <9, la probabilidad de supervivencia es del 81 % 4.
Varios de estos índices predicen la mortalidad en pacientes con GF, pero requieren de al menos nueve parámetros clínicos, por lo que Lin et al., sugieren un índice simplificado (SFGSI) con mayor utilidad en la práctica diaria, que consta de tres parámetros: creatinina, hematocrito y niveles de potasio 20.
En el SFGSI el valor normal de cada parámetro se establece como “0” y la desviación del valor normal se puntúa de 1 hasta 4 puntos, por lo que la puntuación de este índice varía de 0 a 12 puntos 20.
Los autores categorizan la puntuación en bajo riesgo (1 a 2 puntos), con una mortalidad de 1,3 % y alto riesgo (puntuación mayor de 2), con una mortalidad del 41 %.
En el análisis del tiempo quirúrgico y la mortalidad para el grupo de bajo riesgo, no se ha observado diferencia significativa, pero en el grupo de alto riesgo, para los pacientes que tuvieron un tiempo quirúrgico de 12 horas la mortalidad fue del 26,3 %, entre 12-24 horas del 40 % y mayor de 24 horas del 69,2 %, por lo que sugieren como tiempo quirúrgico óptimo 861 minutos (14,35 horas) con una sensibilidad de 0,68 y especificidad del 0,76 20.
El indicador de riesgo de laboratorio de fasciitis necrosante (LRINEC, por sus siglas en inglés) sirve para distinguir la fasciitis necrosante de otras infecciones de tejidos blandos.
Utiliza marcadores de laboratorio que incluyen la proteína C reactiva, el recuento total de glóbulos blancos, la hemoglobina, el sodio, la creatinina y glucosa plasmáticos. Una puntuación mayor a seis conlleva sospecha de fasciitis necrosante y la puntuación mayor a ocho es altamente predictiva 4.
Otro importante y controversial factor es el área de superficie corporal total comprometida (ASC), que es análoga al cálculo del área de superficie corporal en quemados, donde el pene, el escroto y el periné tendrían un valor del 1% y cada fosa isquiorrectal 2,5 %.
Tuncel et al. reportaron un 2,3 % y 4,8 % de compromiso de ASC entre sobrevivientes y no sobrevivientes (p=0,001) 46. Corcoran et al. encontraron una asociación de ASC con la mortalidad, 4,4 % vs. 5,9 % en sobrevivientes y no sobrevivientes, para el compromiso del muslo (16,7 % vs. 71,4 %, p=0,005) y para la pared abdominal (26,7 % vs. 85,7 %, p=0,004) 47.
Dahm et al. estadificaron el compromiso del área de superficie corporal por tamaños: pequeño de un 0,5-3 %; medio de 3,5-5 % y grande >5 %, representando una enfermedad localizada, parcialmente extendida y extendida. La mortalidad para cada grupo fue: compromiso extenso 36 %, parcialmente extendida 11 % y localizada 0 % (p=0,0262) 45,48,49.
Estudios imagenológicos – Identificación y Abordaje de la Gangrena de Fournier
Aunque el diagnóstico de la gangrena de Fournier es clínico, su estudio se puede complementar mediante el uso de imágenes.
La radiografía simple de abdomen o pelvis es el estudio más simple y menos costoso, y permite observar la presencia de gas en la pared abdominal 4,50,51, con la indicación absoluta de cirugía 26.
La ecografía permite delimitar el compromiso de los tejidos blandos a nivel genital, dado por el incremento del grosor de la pared escrotal, además ayuda a diferenciar anomalías de la pared escrotal o de su contenido 50,51.
Se ha convertido en una primera línea en el diagnóstico de esta patología, particularmente en los hombres, evitando el retraso en el diagnóstico y diferenciando de otras emergencias quirúrgicas o diagnósticos como la torsión testicular 52, además permite realizar el estudio doppler del área genital 26.
La tomografía computarizada es considerada actualmente la principal herramienta imagenológica 26; es útil cuando se sospecha compromiso de los tejidos profundos o del espacio retroperitoneal. Es específica para determinar la extensión de la enfermedad, etiología subyacente, engrosamiento de los planos faciales con presencia de gas e infiltración de la grasa (figuras 2 y 3) 32,53.
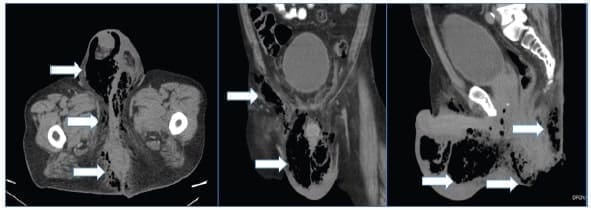
Figura 2. Tomografía computarizada que muestra el proceso inflamatorio enfisematoso que afecta la región perianal, genital, glútea e inguinal derecha. Se observa proceso enfisematoso a nivel de la grasa peri-rectal. Las flechas blancas señalan las áreas de enfisema.
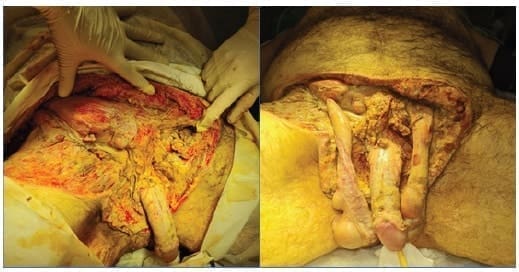
Figura 3. Tratamiento quirúrgico con un desbridamiento agresivo en el paciente de las imágenes mostradas previamente.
También sirve para evaluar las vías anatómicas de diseminación y la presencia de colecciones líquidas o abscesos, incluyendo las extensiones retroperitoneal, intraabdominal o torácica 54.
La resonancia magnética puede definir mejor la extensión de la infección necrosante, pero es costosa y no está siempre disponible. Tiene una sensibilidad diagnóstica del 93-100 % 26,55.
Tratamiento – Identificación y Abordaje de la Gangrena de Fournier
Los pilares del tratamiento son el manejo hidroelectrolítico y nutricional, la estabilización hemodinámica, antibioticoterapia de amplio espectro que debe incluir cobertura contra bacterias aeróbicas y anaeróbicas, grampositivas y gramnegativas, y el desbridamiento quirúrgico amplio 3–5.
Por ser una emergencia quirúrgica, la remoción de los tejidos desvitalizados no debe ser retrasada 56.
El tratamiento hidroelectrolítico se debe basar en las guías del programa “Surviving Sepsis Campaing” desarrollado en el 2002, que utilizando medicina basada en la evidencia establece una guía práctica para el manejo del paciente y la reducción de la mortalidad.
Estas guías se revisaron en el 2013 y dan unas pautas en el tratamiento inicial del paciente séptico: resucitación temprana durante las primeras seis horas de reconocimiento de la sepsis; hemocultivos antes del tratamiento con antibióticos; administración de antibióticos de amplio espectro dentro de la primera hora, una vez reconocido el choque séptico o la sepsis grave sin choque séptico; rápida realización de estudios de imagen para confirmar la posible fuente de infección; reanimación inicial con cristaloides y considerar la administración de albúmina para mantener la presión arterial media; evitar los esteroides intravenosos si la reanimación con líquidos y los vasopresores son capaces de restablecer la estabilidad hemodinámica 57.
Tratamiento antibiótico
El tratamiento antibiótico debe ser parenteral, de inicio precoz, cubriendo flora mixta, tanto aerobia como anaerobia, por lo que se recomienda la administración de tres medicamentos, como por ejemplo: Cefalosporina de primera o tercera generación + Metronidazol o clindamicina + aminoglucósido 57,58.
Aunque debe ajustarse al protocolo de sepsis de cada institución, estos esquemas antibióticos son utilizados en Argentina desde hace más de dos décadas 59.
Otros ejemplos son: Meropenem 1 g c/8 hora IV o piperacilina-tazobactam 3,37 g c/8 horas IV + clindamicina 900 mg c/8 horas IV + vancomicina 15 mg/kg c/12 horas IV o linezolid 600 mg c/12 horas IV o daptomicina 6 mg/kg c/24 horas.
Otros esquemas incluyen: Ciprofloxacina + clindamicina; ampicilina/sulbactam; Ticarcilina/ clavulanato + aminoglucósido (por ejemplo, gentamicina) o metronidazol o clindamicina; y la administración de penicilina (para estreptococos), metronidazol o clindamicina (anaerobios), cefotaxima y gentamicina (gramnegativos), meropenem y piperacilina/tazobactam 6.
Desbridamiento quirúrgico – Identificación y Abordaje de la Gangrena de Fournier
Una vez estabilizado el paciente y con cobertura triple antibiótica de amplio espectro, se debe realizar el desbridamiento quirúrgico del tejido necrótico y no viable, de forma amplia, hasta encontrar zonas de tejido sano, removiendo cualquier área sospechosa de infección.
La resección radical del tejido necrótico, el uso de antibióticos de amplio espectro y la atención en la unidad de cuidados intensivos, se conoce como el tratamiento clásico 60, evitando así la progresión de la infección y reduciendo la mortalidad. El objetivo es controlar la progresión de la infección local y aliviar la toxicidad sistémica. A nivel del ano es importante dejar un puente de piel para evitar el ano flotante 2,29,35.
El lavado se puede realizar con solución de Dakin (hipoclorito de sodio) 18. De forma clara se ha documentado que aquellos pacientes que recibieron un manejo quirúrgico dentro de las primeras 12 horas tuvieron resultados significativamente mejores 4.
Es frecuente que se requiera de nuevas exploraciones para manejar el proceso infeccioso, con un promedio de tres reintervenciones por paciente.
Debe sospecharse el origen abdominal si no se encuentra un claro origen perineal, por lo que en este caso, debe considerarse una exploración abdominal 3.
El manejo integral incluye el soporte nutricional, buscando mantener un balance nitrogenado positivo, debido a que estos pacientes aumentan los requerimientos metabólicos por el estrés y a la pérdida de proteínas por la exposición de los tejidos, que cerraran por segunda intención, obteniendo un tejido adecuado de granulación. En algunos casos se requiere el uso de injertos y colgajos para cubrir estos defectos 35,44.
La cistotomía debe realizarse solo cuando el origen de la infección es urológico, en casos de estenosis uretral, de extravasación de orina, o cuando ha sido necesario el desbridamiento perineal posterior y genital extenso 32,35.
La colostomía en casos de perforación o compromiso del esfínter anal, incontinencia fecal definitiva o clínica, o cuando ha sido necesario el desbridamiento perineal posterior y genital extenso 61,62. Estos procedimientos no deben realizarse de manera sistemática.
Se ha visto que la realización de la enterostomía o colostomía puede disminuir la tasa de mortalidad en pacientes con GF, como se presentó en la seria de Yang-Dong et al. donde la tasa de mortalidad en el grupo de pacientes con enterostomía/colostomía fue de 3,6 % en comparación con el grupo de control con un 21,7 % 63. La necesidad de realizar una colostomía queda a discreción del cirujano general y tiene por objeto la prevención de la contaminación de la herida 4.
En un estudio mexicano se realizó colostomía al 31,73 % de los pacientes por las siguientes indicaciones: 40,9 % por destrucción de esfínteres anales, 28,7 % por amplia extensión de la patología y 30,3 % sin causa explicada. La colostomía se realizó durante la primera cirugía en el 9,0 % y durante lavados subsecuentes en el 90,9 % de los pacientes 61.
En la mayoría de los casos los testículos no se ven comprometidos, debido a que su irrigación proviene de la arteria testicular, cuyo origen es intraabdominal. Los testículos se necrosan cuando la fuente infecciosa es retroperitoneal, intraabdominal, o cuando aumenta la extensión de la lesión.
La orquiectomía puede ser necesaria hasta en un 24 % de los casos 6.
En un trabajo se encontró que los pacientes requieren múltiples cirugías (2,2 ± 1,6) y desbridamiento múltiple (1,5 ± 1,0), con manejo en UCI y requerimiento de ventilación mecánica en el 10 % de los casos y de hemodiálisis en el 1,4 %.
El 7 % de los pacientes se sometieron a reconstrucción de la herida con o sin injerto de piel durante la hospitalización. La mediana de estancia hospitalaria fue de ocho días 64.
Las heridas suelen permanecer expuestas durante mucho tiempo, por lo que requieren curaciones y vendajes frecuentemente. Se han propuesto diferentes protocolos para la atención postoperatoria de este tipo de herida: la miel sin procesar, oxigenación hiperbárica, hormonas cultivadas, agentes de crecimiento y las tecnologías de apósito al vacío 60.
Nuevos enfoques – Identificación y Abordaje de la Gangrena de Fournier
El oxígeno hiperbárico ha demostrado su eficacia al disminuir la diseminación de la fasciitis, promover la granulación después del desbridamiento, mejorar el proceso de fagocitosis de los polimorfonucleares, estimular la angiogénesis capilar, reducir el edema, aumentar el transporte intracelular de los antibióticos y ser tóxica para gérmenes anaerobios, principalmente en infecciones por Clostridium, aumentando la supervivencia en un 95 % 53. Se recomiendan al menos 10 sesiones de 90 minutos cada una 4.
La terapia de cierre asistido por vacío (VAC: Vacuum-Assisted Closure), es una técnica relativamente nueva para el manejo de las heridas, la cual ha comenzado a ser utilizada en los casos de gangrena de Fournier, obteniendo heridas mucho más limpias sin exudados, aún en el caso de heridas extremadamente problemáticas y con bolsillos profundos.
Es un sistema de cuidado de la herida que funciona sobre la base de la aspiración de presión negativa, elimina el exudado y materiales infecciosos, reduce el edema y promueve la curación. Ofrece un menor número de cambios de apósito, menos dolor y una mayor movilidad en comparación con los apósitos convencionales 4,60,62.
El VAC puede ser útil en la curación de heridas, reduciendo así la necesidad de cirugía adicional o injerto de piel 65. La hidrocirugía con Versajet®, el sistema de aspiración-tracción72 y el uso de Integratm, son otros sistemas que se pueden asociar a este manejo 6.
Conclusiones – Identificación y Abordaje de la Gangrena de Fournier
Se llevó a cabo una revisión de la literatura abordando los elementos más importantes en la identificación y manejo de la gangrena de Fournier, que continúa siendo una patología potencialmente letal que requiere un tratamiento quirúrgico de urgencias.
Gracias a las últimas investigaciones realizadas, se ha avanzado en su tratamiento, mejorando los resultados, pero siempre es importante analizar los factores de riesgo en cada paciente y establecer su etiología para definir el tratamiento más adecuado.
Cumplimiento de normas éticas
Consentimiento informado: el presente estudio se adhiere a los lineamientos de la Resolución 008430 de 1993 del Ministerio de Salud de Colombia, y no requirió consentimiento informado ni aprobación por parte de un comité de ética dado que se basa en una revisión de la literatura
Conflicto de interés: los autores declararon no tener conflictos de interés.
Fuente de financiación: los recursos de financiación de este proyecto de investigación provienen en su totalidad de aportes de los autores.
Contribución de los autores
Concepción y diseño del estudio: Andrés Felipe Escudero- Sepúlveda, Julián Camilo Cala-Duran, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti, Raúl Abularach-Borda, Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre.
Adquisición de datos: Andrés Felipe Escudero-Sepúlveda, Julián Camilo Cala-Duran, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti, Raúl Abularach-Borda, Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre.
Análisis e interpretación de datos: Andrés Felipe Escudero- Sepúlveda, Julián Camilo Cala-Duran, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti, Raúl Abularach-Borda, Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre.
Redacción del manuscrito: Andrés Felipe Escudero- Sepúlveda, Julián Camilo Cala-Duran, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti, Raúl Abularach-Borda, Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre.
Revisión crítica: Andrés Felipe Escudero-Sepúlveda, Julián Camilo Cala-Duran, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti, Raúl Abularach-Borda, Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre.
Agradecimientos: A la Universidad de Buenos Aires por inculcar la labor investigativa en sus residentes.
Referencias – Identificación y Abordaje de la Gangrena de Fournier
1. Wróblewska M, Kuzaka B, Borkowski T, Kuzaka P, Kawecki D, Radziszewski P. Fournier’s gangrene, current concepts. Polish J Microbiol. 2014;63:267-73. https://doi.org/10.33073/pjm-2014-036
2. Cancino C, Avendaño R, Poblete Andrade C, Guerra K. Gangrena de Fournier. Cuad Cir. 2010;24:28-33. https://doi.org/10.4206/cuad.cir.2010.v24n1-05
3. Sroczyński M, Sebastian M, Rudnicki J, Sebastian A, Agrawal AK. A complex approach to the treatment of fournier’s gangrene. Adv Clin Exp Med. 2013;22:131-5.
4. Virasoro R. Manejo contemporáneo de la gangrena de Fournier. Revis Argentina Urol. 2020;85:7-12.
5. Navarro-Vera JA. Gangrena de fournier. Rev Eviden Invest Clin. 2010;3:51-7.
6. Martinez-Ubieto F, Rodriguez-Coello J, Solano-Murillo J, Albiac-Andreu M, Resa-Bienzobas J, Perez-Salinas V, et al. Testicular necrosis caused by Fournier’s gangrene: an exceptional case. Arch españoles Urol. 2002;55: 309-11.
7. McHenry CR, Brandt CP, Piotrowski JJ, Jacobs DG, Malangoni MA. Idiopathic necrotizing fasciitis: recognition, incidence, and outcome of therapy. Am Surg. 1994;60:490-4.
Otras Referencias – Identificación y Abordaje de la Gangrena de Fournier
8. Wilson B. Necrotizing fasciitis. Am Surg. 1952;18:416-31.
9. Kaufmann JA, Ramponi D. Recognition of Risk Factors and Prognostic Indicators in Fournier’s Gangrene. Crit Care Nurs Q. 2015;38:143-53. https://doi.org/10.1097/CNQ.0000000000000055
10. Unalp HR, Kamer E, Derici H, Atahan K, Balci U, Demirdoven C, et al. Fournier’s gangrene: evaluation of 68 patients and analysis of prognostic variables. J Postgrad Med. 2008;54:102-5. https://doi.org/10.4103/0022-3859.40775
11. Eke N. Fournier’s gangrene: a review of 1726 cases. 2000;718-28. https://doi.org/10.1046/j.1365-2168.2000.01497.x
12. Sorensen MD, Krieger JN, Rivara FP, Broghammer JA, Klein MB, Mack CD, et al. Fournier’s Gangrene: population based epidemiology and outcomes. J Urol. 2009;181:2120-6. https://doi.org/10.1016/j.juro.2009.01.034
13. Kiran RP. Fournier’s gangrene: a review of 1726 cases. The British journal of surgery. 2000;87:1596. https://doi.org/10.1046/j.1365-2168.2000.01679-9.x
14. Ersay A, Yilmaz G, Akgun Y, Celik Y. Factors affecting mortality of Fournier’s gangrene: review of 70 patients. ANZ J Surg. 2007;77:43-8. https://doi.org/10.1111/j.1445-2197.2006.03975.x
Bibliografías – Identificación y Abordaje de la Gangrena de Fournier
15. Nathan B. Fournier’s gangrene: a historical vignette. Canadian journal of surgery. 1998;41:72.
16. Esponda A, Amarilla A, Díaz F, Aguirre C, Hugo O. Gangrena de Fournier veintiséis casos en dos años. Rev Arg Urol. 2008;73:180-4.
17. García A, Turégano F, Martín J, Vaquero A, Camarero C, Pérez M. Gangrena de Fournier: análisis de una serie de 34 casos. Rev Colomb Cirugía. 2010;25:151-7.
18. Montoya-chinchilla R, Pietricica BN, Rosino-sánchez A. Gangrena de Fourier: estudio descriptivo de 30 casos y análisis de factores pronósticos más allá de la escala de Laor. Rev Urol Colomb. 2012;21:39-47.
19. Ahrenholz DH. Necrotizing soft-tissue infections. Surg Infect. 1988;68:199-214. https://doi.org/10.1016/S0039-6109(16)44440-3
20. Lin T-Y, Cheng I-H, Ou C-H, Tsai Y-S, Tong Y-C, Cheng H-L, et al. Incorporating Simplified Fournier’s Gangrene Severity Index with early surgical intervention can maximize survival in high-risk Fournier’s gangrene patients. Int J Urol. 2019;26:737-43.
21. Mallikarjuna MN, Vijayakumar A, Patil VS, Shivswamy BS. Fournier’s Gangrene: Current Practices. ISRN Surg. 2012;2012:1-8. https://doi.org/10.5402/2012/942437
Otras Bibliografías -Identificación y Abordaje de la Gangrena de Fournier
22. Azolas M R. Factores de riesgo para mortalidad en gangrena de Fournier. Rev Chil cirugía. 2011;63:270-5. https://doi.org/10.4067/S0718-40262011000300006
23. Castillo H F, Moraga C J, Pérez C P, Álvarez Z C, Iglesias B A. Diagnóstico y manejo precoz de la gangrena de Fournier. Rev Chil cirugía. 2015;67:181-4. https://doi.org/10.4067/S0718-40262015000200011
24. Sedano-Basilio JE, Cornejo-Dávila V, Trujillo-Ortiz L, Cantellano-Orozco M, Fernández-Noyola G, Martínez- Arroyo C, et al. Experiencia y revisión de la literatura en el manejo de gangrena de Fournier en una institución, 2008-2015. Rev Mex Urol. 2016;76:29-35. https://doi.org/10.1016/j.uromx.2015.12.003
25. Durlach R, Fischer M, Heindenreich A, Peczan C. Fascitis necrotizante perineal. Prensa Med Argent. 1996;73:442.
26. Rodríguez-Vera AM, Larios-García CA, García-Casilimas GA, Rodríguez-Sabogal IA, López-Pérez JL. Gangrena de Fournier. Rev Medica Sanitas. 2015;18:212-9.
27. Mecca R, Malawka S, Marottoli N, Macías F, Ambrosetti F. Gangrena de fournier. Rev Arg Urol. 2010;75:22-7.
28. Church JM, Yaghan RJ, A-jaberi TM, Bani-hani I. Fournier ‘ s Gangrene Changing Face of the Disease. 1998;1300-8.
Lecturas Recomendadas – Identificación y Abordaje de la Gangrena de Fournier
29. Planelles-Gómez J, Vergés-Prósper A, Rubio-Tortosa I, Beltrán JR. Gangrena de fournier. Arch Esp Urol. 2006;59:767-71. https://doi.org/10.4321/S0004-06142006000800002
30. Thwaini A, Khan A, Malik A, Cherian J, Barua J, Shergill I, et al. Fournier’s gangrene and its emergency management. Postgr Med J. 2006;82:516-9. https://doi.org/10.1136/pgmj.2005.042069
31. Benizri E, Fabiani P, Migliori G, Chevallier D, Peyrottes A, Amiel J, et al. Gangrene of the perineum. Urology. 1996;47:935-9. https://doi.org/10.1016/S0090-4295(96)00058-1}
32. Baskin LS, Carroll PR, Cattolica E V, McAninch JW. Necrotising soft tissue infections of the perineum and genitalia. Bacteriology, treatment and risk assessment. Br J Urol. 1990;65:524-9. https://doi.org/10.1111/j.1464-410X.1990.tb14801.x
33. Mallikarjuna MN, Vijayakumar A, Patil VS, Shivswamy BS. Fournier ‘ s Gangrene : Current Practices. 2012;e942437. https://doi.org/10.5402/2012/942437
34. Muñiz J. Gangrena de Fournier, casos poco frecuentes. SITUA. 2002;21:23-6.
35. Morpurgo E, Galandiuk S. Fournier ‘ s gangrene. 2002;82: 1213-24. Surgical Clinics of North America https://doi.org/10.1016/S0039-6109(02)00058-0
Otras Lecturas Recomendadas – Identificación y Abordaje de la Gangrena de Fournier
36. Janane A, Hajji F, Ismail TO, Chafiqui J, Ghadouane M. Terapia de oxígeno hiperbárico complementaria al desbridamiento en el control de la gangrena de Fournier: utilidad de la puntuación de un índice de severidad en la predicción de la gravedad de la enfermedad y la supervivencia del paciente. Actas Urológicas Españolas. 2011;35:332-8. https://doi.org/10.1016/j.acuro.2011.01.019
37. Martínez-Rodríguez R, Ponce de León J, Caparrós J, Villavicencio H. Fournier’s Gangrene: A Monographic Urology Center Experience with Twenty. Urol Int. 2009;83:323-8. https://doi.org/10.1159/000241676
38. Urdaneta-Carruyo E, Méndez-Parra A, Urdaneta-Contreras A. Gangrena de Fournier. Perspectivas actuales. AN MED INTERNA. 2007;24:190-4. https://doi.org/10.4321/S0212-71992007000400009
39. Saijo S, Kuramoto Y, Yoshinari M, Tagami H. Extremely extended Fournier’s gangrene. Dermatologica. 1990;181:228-32. https://doi.org/10.1159/000247930
40. Paty, R; Smith A. Fournier’s Gangrene secondary to intraabdominal processes. Urol Clin North Am. 1992;19:149-62. https://doi.org/10.1016/S0094-0143(21)00855-7
41. Kouadio L, Kouadio G, Anoh A, Turquin H. Perineal gangrene: an experience of digestive and proctologic surgical unit, university hospital of treichville. Gomal J Med Sc. 2014;12:110-4.
42. Gerber GS, Guss SP, Pielet RW. Fournier’s gangrene secondary to intra-abdominal processes. Urology. 1994;44(5):779-82. https://doi.org/10.1016/S0090-4295(94)80230-0
Fuentes Bibliográficas – Identificación y Abordaje de la Gangrena de Fournier
43. Ersay A, Yilmaz G, Akgun Y, Celik Y. Factors affecting mortality of Fournier’s gangrene: Review of 70 patients. ANZ J Surg. 2007;77(1-2):43-8. https://doi.org/10.1111/j.1445-2197.2006.03975.x
44. Horta R, Cerqueira M, Marques M, Ferreira P. Gangrena de Fournier: de urgencia urológica hasta el departamento de cirugía plástica. Actas Urol Esp. 2009;33:925- 9. https://doi.org/10.1016/S0210-4806(09)72884-0
45. Laor E, Palmer LS, Tolia BM, Reid RE, Winter HI. Outcome prediction in patients with Fournier’s gangrene. J Urol. 1995;154:89-92. https://doi.org/10.1016/S0022-5347(01)67236-7
46. Tuncel A, Aydin O, Tekdogan U, Nalcacioglu V, Capar Y, Atan A. Fournier’s Gangrene: three years of experience with 20 patients and validity of the Fournier’s Gangrene Severity Index Score. Eur Urol. 2006;50:838-43. https://doi.org/10.1016/j.eururo.2006.01.030
47. Corcoran AT, Smaldone MC, Gibbons EP, Walsh TJ, Davies BJ. Validation of the Fournier’s Gangrene Severity Index in a Large Contemporary Series. J Urol. 2008;180:944- 8. https://doi.org/10.1016/j.juro.2008.05.021
48. Camargoa L, García-Perdomo HA. Mortality risk factors in fournier gangrene. A literature review. Rev Chil Cir. 2016;68:273-7. https://doi.org/10.1016/j.rchic.2015.11.003
49. Dahm P, Roland FH, Vaslef SN, Moon RE, Price DT, Georgiade GS, et al. Necrotizing Fasciitis of the Male Genitalia. Urology. 2000;56:31-6. https://doi.org/10.1016/S0090-4295(00)00604-X
Otras Fuentes Bibliográficas – Identificación y Abordaje de la Gangrena de Fournier
50. Kane CJ, Nash P, Mcaninch JW. Ultrasonographic appearence of necrotizing gangrene: Aid in early diagnosis. Urology. 1996;5:42-4.
51. Levenson RB, Singh AK, Novelline RA. Fournier Gangrene : Role of Imaging 1. RadioGraphic. 2008;01655:519- 29. https://doi.org/10.1148/rg.282075048
52. Weatherspoon K, Polansky S, Catanzano T. Ultrasound emergencies of the male pelvis. semin ultrasound, CT MRI. 2017;38:327-44. https://doi.org/10.1053/j.sult.2017.02.002
53. Chang I-J, Lee C-C, Chen S-Y. Fulminant gangrenous and crepitating scrotum. Archives of dermatology. 2006;142:797-8. https://doi.org/10.1001/archderm.142.6.797
54. López-Bravo MW, Francisco de Alba-Celedón J, Guerrero-Avendaño GML, Améndola MA, Casillas del Moral J. La gangrena de Fournier: evaluación con tomografía computada. An Radiol Mex. 2012;2:98-103.
55. Vayvada H, Demirdover C, Menderes A, Karaca C. Necrotising fasciitis in the central part of the body: diagnosis, management and review of the literature. Int Wound J. 2013;10:466-72. https://doi.org/10.1111/j.1742-481X.2012.01006.x
56. Xeropotamos NS, Nousias VE, Kappas AM. Fournier‘s Gangrene: diagnostic approach and therapeutic challenge. Eur J Surg. 2002;168:91-5. https://doi.org/10.1080/11024150252884304
57. Dellinger RP, Levy MM, Rhodes A, Bs MB, Annane D, Gerlach H, et al. Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock. 2013;39:165-228. https://doi.org/10.1007/s00134-012-2769-8
Reseñas Bibliográficas – Identificación y Abordaje de la Gangrena de Fournier
58. Vayvada H, Demirdover C, Menderes A, Karaca C. Necrotising fasciitis in the central part of the body : diagnosis, management and review of the literature. Int Wound J. 2012;e1-8. https://doi.org/10.1111/j.1742-481X.2012.01006.x
59. Fiorentino AN, Biso NA, Leo RP, Loza CA. Gangrena de Fournier. Rev Argent Urol. 1996;55(4):173.
60. Yanaral F, Balci C, Ozgor F, Simsek A, Onuk O, Aydin M, et al. Comparison of conventional dressings and vacuum- assisted closure in the wound therapy of Fournier’s gangrene. Arch Ital di Urol Androl organo Uff [di] Soc Ital di Ecogr Urol e Nefrol. 2017;89:208-11. https://doi.org/10.4081/aiua.2017.3.208
61. Jiménez-Bobadilla B, Santillán-Ruvalcaba JH, Idhaly-Legorreta C, Villanueva-Herrero AJ, Charúa-Guindic L. Utilidad de la colostomía en la gangrena de Fournier y su valor predictivo de mortalidad. Cir Gen. 2008;30:141-8.
62. Zagli G, Cianchi G, Degl’Innocenti S, Parodo J, Bonetti L, Prosperi P, et al. Treatment of Fournier’s Gangrene with combination of vacuum-assisted closure therapy, hyperbaric oxygen therapy, and protective colostomy. Case Rep Anesthesiol. 2011;2011:1-4. https://doi.org/10.1155/2011/430983
63. Li YD, Zhu WF, Qiao JJ, Lin JJ. Enterostomy can decrease the mortality of patients with Fournier gangrene. World J Gastroenterol. 2014;20:7950-4. https://doi.org/10.3748/wjg.v20.i24.7950
64. Sorensen MD, Krieger JN. Fournier’s Gangrene: Epidemiology and outcomes in the General US Population. Urol Int. 2016;97:249-59. https://doi.org/10.1159/000445695
65. Hong KS, Yi HJ, Lee R-A, Kim KH, Chung SS. Prognostic factors and treatment outcomes for patients with Fournier’s gangrene: a retrospective study. Int Wound J. 2017;14:1352-8. https://doi.org/10.1111/iwj.12812
Autores – Identificación y Abordaje de la Gangrena de Fournier
1 Andrés Felipe Escudero-Sepúlveda, María Belén-Jurado, Silvio Emilio Tomasone, Vicente Mario Carlino-Currenti. Médico, especialista en Cirugía general, Hospital de Trauma y Emergencias Dr. Federico Abete, Buenos Aires, Argentina.
2 Julián Camilo Cala-Duran, Médico, especialista en Epidemiologia, Hospital Universitario de Santander, Bucaramanga, Santander, Colombia.
3 Raúl Abularach-Borda , Carla Roccuzzo, José Felipe de Jesús Puche-Burgos, José Enrique Acosta-Maestre, Médico, residente de Cirugía general, Universidad de Buenos Aires, Hospital de Trauma y Emergencias Dr. Federico Abete, Buenos Aires, Argentina.
Fecha de recibido: 13/05/2021 – Fecha de aceptación: 27/02/2022 – Publicación en línea: 25/08/2022
Correspondencia: Andrés Felipe Escudero-Sepúlveda, Dirección postal: Libertad 844 4E Buenos Aires, Argentina.
Teléfono: +54 11 62327368. Dirección electrónica: dr.andresescudero@gmail.com
Citar como: Escudero-Sepúlveda AF, Cala-Duran JC, María Belén-Jurado M, Tomasone SE, Carlino-Currenti VM, Abularach-Borda R, et al. Conceptos para la identificación y abordaje de la gangrena de Fournier. Rev Colomb Cir. 2022;37:653-64. https://doi.org/10.30944/20117582.930
Este es un artículo de acceso abierto bajo una Licencia Creative Commons – BY-NC-ND https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es