Durante el periodo de estudio, se revisaron 210 historias clínicas que cumplían con rango de edad establecido y códigos CIE-10 del diagnóstico relacionados; de estas, en 41 se cumplieron todos los criterios de inclusión. Hubo 27 (65,9 %) hombres, con una edad media de 41,9 años en el momento del diagnóstico del tumor, sin diferencias en la aparición por sexo (42,7 mujeres y 41,52 hombres) y con un rango etario entre los 26 y los 50 años.
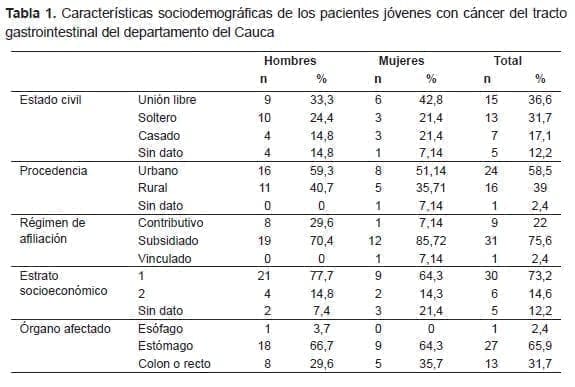
Como se describe en la tabla 1, el cáncer más frecuente en este estudio fue el de estómago, seguido por el colorrectal y, por último, el de esófago (un solo caso en un paciente masculino), sin diferencias por sexo en el orden de presentación.
 En general, la estadificación del cáncer se hizo antes de la cirugía en 38 (92,7 %) de los pacientes y, durante la cirugía, en 3 (7,3 %). El estudio más utilizado en esta institución fue la tomografía computadorizada (TC) en 32 (78,0 %), seguida de la laparoscopia en 4 (9,7 %), que solo fue utilizada para el cáncer gástrico, al igual que la ecografía abdominal. De los tres casos cuya estadificación fue intraoperatoria, a uno se le practicó derivación gastroentérica paliativa por cáncer gástrico en estadio IV; los otros dos, ambos con cáncer de colon en estadio IV, requirieron colostomía, uno por obstrucción y otro por perforación.
En general, la estadificación del cáncer se hizo antes de la cirugía en 38 (92,7 %) de los pacientes y, durante la cirugía, en 3 (7,3 %). El estudio más utilizado en esta institución fue la tomografía computadorizada (TC) en 32 (78,0 %), seguida de la laparoscopia en 4 (9,7 %), que solo fue utilizada para el cáncer gástrico, al igual que la ecografía abdominal. De los tres casos cuya estadificación fue intraoperatoria, a uno se le practicó derivación gastroentérica paliativa por cáncer gástrico en estadio IV; los otros dos, ambos con cáncer de colon en estadio IV, requirieron colostomía, uno por obstrucción y otro por perforación.
Esófago
De los 41 pacientes incluidos en el estudio, uno de 45 años presentó cáncer esofágico. Los síntomas cardinales fueron disfagia y pérdida de peso, además de otros como dispepsia y pirosis.
Se encontró con bajo peso (índice de masa corporal, IMC=16,4 kg/m2), calificación de C (desnutrición) en la valoración global subjetiva (Subjective Global Assessment, SGA), y con estadio clínico II (localmente avanzado). No hubo datos sobre antecedentes familiares y refirió el antecedente de tabaquismo.
El estudio histopatológico demostró un carcinoma esofágico escamocelular moderadamente diferenciado. En la endoscopia de vías digestivas altas, se encontró estenosis lisa en el tercio medio del esófago. La estadificación se hizo con TC de tórax. Se le colocó una endoprótesis como tratamiento paliativo, debido al compromiso del estado nutricional. La supervivencia fue de 15 meses a partir del momento del diagnóstico.
Estómago
El cáncer gástrico fue el más frecuentemente diagnosticado con un total del 65,9%. Se presentó más en hombres (18 hombres y 9 mujeres). Se encontró existencia de antecedente familiar de cáncer gástrico en el 15,8% (n=3, sin información 8 casos), los síntomas cardinales de presentación fueron dolor abdominal 88,5% (n=23), pérdida de peso 80,8% (n=21) y dispepsia 63,3% (n=14); el sangrado digestivo correspondió al 48% (n=12).
En cuanto al estado nutricional, en el 58,3 % el IMC fue normal y en el 25 % hubo bajo peso; en la valoración global subjetiva, 14 (53 %) se encontraban en riesgo y 12 (46,2%) se consideraron desnutridos.
La histopatología demostró que todos los 27 casos de cáncer gástrico correspondían a adenocarcinoma, de los cuales, 7 (26,9 %) (n=7) fueron de subtipo difuso; no hubo casos de linfoma, sarcoma o tumores del estroma.
En todos los casos, se practicó endoscopia de vías digestivas altas como método diagnóstico y, en 22 (91,7 %) TC de abdomen. En 12 (51,7 %) pacientes se practicó ecografía abdominal y, en 4 (14,8 %), laparoscopia diagnóstica. Por medio de la TC abdominal, se estadificó la neoplasia: en 7 (31,8 %) se encontró enfermedad metastásica y, en 8 (36,4 %), el tumor estaba localmente avanzado.
En 17 (63 %) pacientes, se determinó un estadio IV, y en 7 (25,9 %) un estadio III; en ningún caso se encontró enfermedad in situ o estadio I.
Se sometieron a cirugía 16 (59,3 %) de 27 pacientes:
Como medida diagnóstica, para resección o como tratamiento paliativo, según el caso. En 16 (64,5 %) se administró radioterapia, quimioterapia (adyuvante o paliativa), o ambas; en 5 (19,2 %) de los que recibieron paliación, esta consistió en la colocación de endoprótesis.
El 66,6% (n=18) de los pacientes falleció dentro de los 5 años que correspondió el estudio,
sobrevivieron 7,4% (n=2 y sin datos de 7 pacientes); el tiempo de supervivencia fue mayor en el estadio II, 32 meses (17,5 meses para los que no se operaron) y 2 a 3,7 meses para el estadio IV. En el estadio III la supervivencia promedio varió 6,5 meses a favor de los que se operaron vs los que no (23,5 vs 30 meses).
Colon
El cáncer colorrectal fue el segundo en frecuencia y se presentó en 13 (31,7 %) de los 41 pacientes.
En 6 de ellos (46,2 %) se encontraron antecedentes familiares de cáncer de colon (sin poder establecer síndrome genético asociado).
Los síntomas de presentación más frecuentes fueron dolor abdominal en 12 (92,3 %), cambio del hábito intestinal en 11 (84,6 %) y pérdida de peso en 8 (66,7 %). En 6 (46,2 %) casos, hubo sangrado digestivo bajo.
El estado nutricional valorado con el IMC, fue normal en 9 (69,2 %) y bajo solo en uno (7,7 %) de los casos. En la valoración global subjetiva, 11 (84,6 %) se encontraban en clasificación B, en riesgo de desnutrición, y dos (15,4 %) en la C, correspondiente a desnutrición; ninguno tenía un buen estado nutricional según esta escala.
El diagnóstico se apoyó en la colonoscopia total en 11 (84,6 %) y fue intraoperatorio como
urgencia oncológica en los dos restantes. La estadificación del tumor se estableció por medio de TC abdominal en 12 (92,3 %) pacientes, y solo en uno (7,7 %) se practicó laparoscopia para hacerlo (10 %).
Según el estudio de histopatología:
Predominó el adenocarcinoma no mucinoso, con 10 (76,9 %); además, hubo 2 (15,4 %) casos de adenocarcinoma mucinoso y 1 (7,7 %) de melanoma en el recto distal. La graduación del estadio clínico en el momento del diagnóstico fue: un (7,7 %) caso en estadio I, 5 (38,5 %) en estadio II, 5 (38,5 %) en estadio III y 2 (15,4 %) con metastasis.
En 12 (92,3 %) pacientes la intervención quirúrgica se llevó a cabo como una urgencia oncológica o en plan de resección, y 11 (84,6 %) recibieron tratamiento adyuvante con quimioterapia, radioterapia o ambas.
Durante el seguimiento fallecieron 6 (46,1 %) pacientes. La supervivencia fue de 46 meses para casos en estadio I y de 2 meses para aquellos en estadio IV; en los estadios II y III, estuvo entre 30 y 34 meses, siendo el rango mayor en los operados.
Discusión
Este es un estudio caracterizado por la inclusión de las neoplasias malignas de todo el tracto gastrointestinal, en pacientes clasificados por la OMS como jóvenes. La mayoría de la población de este estudio fueron hombres (65,8 %), lo cual coincide con lo publicado correspondiente a este grupo etario 17,32–34. En la población de mayor edad, la prevalencia es superada por el cáncer de mama y el de cuello uterino en mujeres, y el de próstata en hombres; en algunos países, como el nuestro, el cáncer de próstata es la primera causa de mortalidad por cáncer.
El promedio de la edad de presentación fue un poco mayor que lo informado en otros estudios similares, en los cuales estuvo entre los 25 y los 33 años en casos de cáncer de esófago o estómago, y en 38 años, en los del cáncer gástrico difuso hereditario 9,33,35–37.
La estadificación en esta población se hizo mediante TC, según lo indicado en la mayoría de guías internacionales, como la National Comprehensive Cancer Network (NCCN), la European Society for Medical Oncology (ESMO) y las guías japonesas 13,14.
El cáncer de esófago en este estudio fue un carcinoma escamocelular del tercio medio:
Similar a lo encontrado en la población mayor de 50 años 37 en países con alta prevalencia, a diferencia de los Estados Unidos donde el adenocarcinoma predomina (aparición entre 40 a 55 años) y el carcinoma escamocelular es de aparición más tardía (10 años más) 38. Se presentó en estadio II, diferente a lo encontrado en otras poblaciones, en las cuales el estadio III para mayores o menores de 45 años, que constituye la presentación más frecuente 35,39. Solo 5 a 15 % de este tipo de neoplasias se presentan en menores de 40 años 7,33,34,38. La disfagia y la pérdida de peso fueron los síntomas cardinales, sin diferencia con lo encontrado en los mayores de 50 años.
La supervivencia fue de 15 meses en el presente caso; en general, a los cinco años, esta es de 17 %, y en estadio II, de 39 % 39.
El cáncer más frecuente en la población joven fue el gástrico, similar a lo encontrado en otros países, como los de Latinoamérica y Asia, donde es alta la prevalencia de esta enfermedad, así como en las estadísticas de la OMS 5,12,14,23,40. Esto contrasta con los estudios en Europa occidental y Estados Unidos, donde el cáncer del tubo digestivo más frecuente es el de colon, en el rango de 15 a 39 años 28,41.
El tipo histológico más frecuente de cáncer gástrico fue el adenocarcinoma intestinal, algo
que contradice un poco lo encontrado en la literatura científica mundial, en la cual, en jóvenes, corresponde al adenocarcinoma de tipo difuso 18.
La excepción se presenta en poblaciones con alta prevalencia:
Como la de nuestro departamento, en las cuales las inadecuadas condiciones sanitarias promueven la exposición a H. pilory desde temprana edad (presente en más del 50 % de los niños); además, el nivel socioeconómico era bajo en nuestra población 13,22,42.
En la presente muestra, la sintomatología no fue específica para cáncer gástrico y consistió en dolor abdominal, dispepsia y pérdida de peso, como también sucede en población de mayor edad. Se presentó sangrado digestivo evidente en 48 % de los pacientes jóvenes, a diferencia del 20 % en otros grupos etarios 43.
En este grupo con cáncer de estómago, el 63 % presentó enfermedad metastásica; en la población no discriminada por edad, se espera un porcentaje de 32 % en casos en estadio III o IV (43,44). Los diagnósticos tardíos se pueden explicar por circunstancias como el difícil acceso a la red pública en salud en el departamento (y en Colombia, en general) y porque nuestra población pertenecía a los estratos 1 y 2; cuentan la propia idiosincrasia, la gran cantidad de población indígena con sus creencias sobre la enfermedad, y la terapéutica local o tradicional.
Se incluyó la clasificación de la valoración global subjetiva como estándar del estado nutricional.
Llama la atención que en los artículos revisados, no se menciona ninguna calificación de este tipo. Se estableció que la valoración global subjetiva es mejor que el índice de masa corporal para calificar el estado nutricional. Si la neoplasia es proximal, del esófago, la nutrición se verá gravemente comprometida, como es de esperarse debido a la propia fisiología de la absorción de nutrientes en el tubo digestivo proximal.
Con respecto a la herencia, la asociación familiar del cáncer fue más acentuada en el carcinoma de colon:
Comparativamente con el de estómago (60,0 Vs. 15,8 %), sin que se hubiera podido determinar la presencia de ningún síndrome genético mediante criterios clínicos específicos; no hubo datos sobre antecedentes familiares en el único paciente con cáncer esofágico.
Por la propia historia natural de la enfermedad en pacientes jóvenes, el cáncer de colon es
menos agresivo que en el adulto mayor, lo cual favorece una mayor supervivencia en ellos (30).
Los síntomas más frecuentes en jóvenes, fueron dolor abdominal, cambio del hábito intestinal y pérdida de peso (más importante en la enfermedad avanzada), similar a lo que sucede en los adultos mayores 5.
Al cáncer gástrico le corresponde una supervivencia promedio de menos del 10 % a los cinco años, en los pacientes adultos jóvenes 20,21. La supervivencia en el presente grupo de estudio, varió de 2 a 3,7 meses en casos de cáncer gástrico en estadio IV; la media de supervivencia es del 25 % a los cinco años y solo del 5 % en casos en estadio IV. En casos en estadio II, la supervivencia en los sometidos a cirugía fue de 32 meses y, para para los que no se operaron, de 17,5 meses; el rango de supervivencia fue de 3 a 11 meses, sin cirugía.
En el cáncer de colon en estadio I, la media de supervivencia fue de 46 meses. A diferencia de lo observado en otros grupos etarios, la supervivencia no ha mejorado notoriamente en los últimos 30 años para el adulto joven o adolescente, y es equiparable a la del adulto mayor 38,43,45,46.
No se presentaron casos de carcinoma de intestino delgado.
Conclusión
Este estudio descriptivo y retrospectivo, en el que se incluyeron pacientes jóvenes con neoplasias de cualquier parte del tubo digestivo (único en este tipo de inclusión), mostró que el pronóstico es peor o igual al de otros grupos etarios, según algunas situaciones o el tipo de tumor.
En cuanto a la supervivencia, siendo más agresiva para el cáncer de estómago a pesar de no dominar el adenocarcinoma difuso, tiene un pobre pronóstico, todo esto es secundario a una consulta tardía (en casi dos terceras partes de la población, el estadio clínico era IV), al difícil acceso a los centros de alta complejidad, y a la idiosincrasia y creencias sobre tratamientos alternativos regionales o locales.
El cáncer de esófago y el de intestino delgado tuvieron una mínima presentación en este grupo poblacional. Es importante resaltar que la valoración integral de la nutrición, como se hace con la valoración global subjetiva, permite obtener un mejor resultado y más real que el del índice de masa corporal. El cáncer de colon sigue teniendo el mejor pronóstico y el mayor tiempo de supervivencia.
Los vacíos en los datos clínicos, el bajo nivel socioeconómico y la falta de profundización de
los estudios genéticos, impidieron identificar síndromes de cáncer del tubo digestivo en esta población.
Se requieren más estudios como este, que abarquen múltiples instituciones y colaboraciones interdepartamentales, para saber a qué problema real nos enfrentamos en la población productiva con cáncer del país.
Es importante considerar la búsqueda activa de síntomas que puedan sugerir estadios iniciales de estas entidades en la población adulta joven y, de esta manera, evitar la consulta en estadios avanzados.
Agradecimientos.
Al Hospital Universitario San José de Popayán y a su comité de ética.
Conflicto de interés.
Los autores declaran no tener conflictos de interés.
Referencias
- 1. Organización mundial de la salud. Datos y cifras sobre el cáncer. WHO [Internet]. 2014 Disponible en: https://www.who.int/cancer/about/facts/es/ Fecha de descarga: Febrero 14 de 2019
- 2. Mork ME, You YN, Ying J, Bannon SA, Lynch PM, Rodriguez-Bigas MA, et al. High prevalence of hereditary cancer syndromes in adolescents and young adults with colorectal cancer. J Clin Oncol. 2015;33:3544-9. doi: 10.1200/JCO.2015.61.4503.
- 3. Levi F. Cancer incidence in five continents. IARC Scientific Publications. 2014. Disponible en http://ci5.iarc.fr/CI5I-X/old/vol10/CI5vol10.pdf Fecha de descarga: Febrero 14 de 2019
- 4. Liu L, Moke DJ, Tsai K-Y, Hwang A, Freyer DR, Hamilton AS, et al. A Reappraisal of Sex-Specific Cancer Survival Trends Among Adolescents and Young Adults in the United States. J Natl Cancer Inst. 2018 Oct 15. doi: 10.1093/jnci/djy140.
- 5. Instituto Nacional del Cáncer. Adolescentes y adultos jóvenes con cáncer – National Cancer Institute [Internet] 2018. Fecha de descarga: Febrero 14 de 2019. Disponible en: https://www.cancer.gov/espanol/tipos/adolescentes-adultos-jovenes.
- 6. Instituto Nacional del Cáncer. Tratamiento de los cánceres poco comunes en la niñez (PDQ®)—Versión para pacientes – National Cancer Institute [Internet]. 2019 Fecha de consulta: 14 de febrero de 2019. Disponible en: https://www.cancer.gov/espanol/tipos/infantil/paciente/canceres-infantiles-poco-comunes-pdq.
- 7. Rozen P. Cancer of the gastrointestinal tract: Early detection or early prevention? Eur J Cancer Prev. 2004;13:71-5.
- 8. OPS Chile. OPS/OMS Chile – Expertos hayan que consumo de bebidas muy calientes probablemente cause cáncer del esófago en los seres humanos. [Internet]. 2016 Disponible en: https://www.paho.org/chi/index.php?option=com_content&view=article&id=755:expe
rtos-hayan-que-consumo-de-bebidas-muy-calientesprobablemente-cause-cancer-del-esofago-en-los-seres-humanos&Itemid=1005 Fecha de descarga: Febrero 14 de 2019 - 9. Organización Panamericana de la Salud. Cancer [Internet]. 2018. Fecha de consulta: 14 de febrero de 2019. Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/cancer
- 10. Barrios E, Sierra MS, Musetti C, Forman D. The burden of oesophageal cancer in Central and South America. Cancer Epidemiol. 2016;44 Suppl 1:S53-S61. doi: 10.1016/j.canep.2016.03.013.
Bibliografía
- 11. Borráez-Segura BA, Montoya-Botero JA, Meneses PA, Abadía M, Pinilla RE, Oliveros R. Esofagectomía en un centro suramericano de tratamiento del cáncer. Rev Colomb Cir. 2018;33:71-8.
- 12. Herszényi L, Tulassay Z. Epidemiology of gastrointestinal and liver tumors. Eur Rev Med Pharmacol Sci. 2010;14:249-58.
- 13. Suárez R, Wiesner C, González C, Cortés C, Shinchi A. Antropología del cáncer e investigación aplicada en salud pública. Revista de Estudios Sociales. 2004;17:42- 55
- 14. Adrada JC, Calambás FH, Díaz JE, Delgado DO, Sierra CH. The socio-demographic and clinical characteristics in gastric cancer population in the department of Cauca, Colombia. Rev Colomb Gastroenterol. 2008;23:309-14
- 15. Uehara G, Nago A, Espinoza R, Vargas G, Astete M, Morán L, et al. Edad óptima para el despistaje endoscópico de cáncer gástrico en pacientes con dispepsia sin síntomas de alarma. Rev Gastroenterol Perú. 2007;27:339-48
- 16. Jurado Ciro A. Cáncer gástrico: visión y misión de un cirujano endoscopista Rev Colomb Cir. 2008;23:85-99.
- 17. Torres MM, Acosta CP, Sicard DM, Restrepo D, Groot H. Genetic susceptibility and risk of gastric cancer in human population of Cauca, Colombia. Biomédica. 2004;24:153-6.
- 18. Takatsu Y, Hiki N, Nunobe S, Ohashi M, Honda M, Yamaguchi T, et al. Clinicopathological features of gastric cancer in young patients. Gastric Cancer. 2016;19:472-8. doi: 10.1007/s10120-015-0484-1
- 19. Dhobi MA, Wani KA, Parray FQ, Wani RA, Wani ML, Peer GQ, et al. Gastric cancer in young patients, Clinical Study. Int J Surg Oncol. 2013;2013:981654. doi: 10.1155/2013/981654
- 20. Piñeros M, Ferlay J, Murillo R. Cancer incidence estimates at the nation and district levels in Colombia. Salud Pública Mex. 2006;48:455-65
Fuentes
- 21. Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer J Clin. 2011;61:69-90
- 22. Bravo LE, Cortés A, Carrascal E, Correa P, Ordóñez N. Seroprevalencia de anticuerpos anti-Helicobacter pylori en donantes de sangre de regiones colombianas con diferencias en la mortalidad por cáncer gástrico. Colombia Médica. 2000;31:122-30.
- 23. Parsonnet J. Bacterial infection as a cause of cancer. Environ Health Perspect. 1995;103(Suppl.8):263-8. doi: 0.1289/ehp.95103s8263
- 24. Correa P, Potter A, Professor W. Cáncer gástrico: una enfermedad infecciosa. Rev Colomb Cir. 2011;26:111-7.
- 25. Ayala JC, Lotero JD. Tamización de cáncer gástrico. Universitas Med. 2013;54:209-22
- 26. Fondo Colombiano de Enfermedades de Alto Costo. Situación del cáncer de la población atendida en el SGSSS en Colombia 2015. Registro de información para el año 2016. Cuenta de Alto Costo. 2016;1:páginas?. Fecha de consulta: 14 de febrero de 2019. 2016. Disponible en: https://cuentadealtocosto.org/site/images/Libro%20C%C3%A1ncer%202015/Situaci%C3%B3n%20del%20c%C3%A1ncer%202015%20-%20Aug22-2%20(1).pdf.
- 27. Orozco, C; Benavides, E; Bastidas, B; Gómez C. Registro de cáncer de dos instituciones de referencia en el departamento del Cauca 2011 Cancer registry of two reference institutions in the department of Cauca 2011. Revista de la Facultad de Ciencias de la Salud de la Universidad del Cauca 2018;20:16–21
- 28. Ferlay J1, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136:E359-86. doi: 10.1002/ijc.29210.
- 29. Martínez CI, Pérez LF, Baquero D, Barco A. Cáncer colorrectal hereditario no asociado a poliposis o síndrome de Lynch. Rev Colomb Cir. 2017;32:297-303. doi: 10.30944/20117582.38.
- 30. Fernández CV, Barr RD. Adolescents and young adults with cancer: An orphaned population. Paediatr Child Health. 2006;11:103-6
Referencias Bibliográficas
- 31. Sierra R. Cáncer gástrico , epidemiología y prevención. Acta Med Costarric. 2002;44:55-61.
- 32. Wu Q-J, Vogtmann E, Zhang W, Xie L, Yang W-S, Tan Y-T, et al. Cancer incidence among adolescents and young adults in urban Shanghai, 1973-2005. PLoS ONE. 2012;7:e42607. doi: 10.1371/journal.pone.0042607
- 33. De Stefani E, Deneo-Pellegrini H, Ronco AL, Boffetta P, Correa P, Mendilaharsu M, et al. Diet patterns and risk of squamous cell oesophageal carcinoma: A casecontrol study in Uruguay. Asian Pac J Cancer Prev. 2014;15:2765-9.
- 34. Pohl H, Wrobel K, Bojarski C, Voderholzer W, Sonnenberg A, Rösch T, et al. Risk factors in the development of esophageal adenocarcinoma. Am J Gastroenterol. 2013;108:200-7.
- 35. Oezcelik A, Ayazi S, DeMeester SR, Zehetner J, Abate E, Dunn J, et al. Adenocarcinoma of the esophagus in the young. J Gastrointest Surg. 2013;17:1032-5. doi: 10.1007/s11605-013-2177-6.
- 36. Sun X, Zhao D, Liu Y, Liu Y, Yuan Z, Wang J. The longterm spatial-temporal trends and burden of esophageal cancer in one high-risk area: A population-registered study in Feicheng, China. PLoS One. 2017;12:e0173211. doi: 10.1371/journal.pone.0173211.
- 37. Gómez M, Otero W, Caminos J. Cáncer gástrico en pacientes jóvenes en Colombia. Rev Col Gastroenterol. 2012; 27:166-72.
- 38. Ajani JA, Barthel JS, Bentrem DJ, D’Amico TA, Das P, Denlinger CS, et al. Esophageal and esophagogastric junction cancers. J Natl Compr Canc Netw. 2011;9:830-87..
- 39. Rustgi AK, El-Serag HB. Esophageal carcinoma. N Engl J Med. 2014;371:2499-509.
Otras Bibliográficas
- 40. Medina-Franco H. Cáncer gástrico hereditario. Genética y manejo clínico. Rev Gastroenterol Mex. 2003;68:51-54.
- 41. Bleyer A, O’Leary M, Barr R, Ries L. Cancer epidemiology in older adolescents and young adults 15-29 years of age, including SEER incidence and survival: 1975-2000. In: National Cancer Institute, NIH Pub No 06-5767. 2006. Fecha de consulta: 14 de febrero de 2019. Disponible en: https://seer.cancer.gov/archive/publications/aya/
- 42. Arias-Sosa LA, Cuspoca-Orduz AF, Siabato-Barrios JA, Eslava-Roa JS. Incidencia y mortalidad del cáncer gástrico en el departamento de Boyacá-Colombia. Acta Gastroenterol Latinoam. 2018;48:181–9.
43. Kantarjian Hagop M. Manual de Oncología Médica MD Anderson (2Tomos) . 2nd ed. Amolca, editor. 2014. 1489 p. - 44. Ajani JA, Bentrem DJ, Besh S, D’Amico TA, Das P, Denlinger C, et al. Gastric cancer, version 2. J Natl Compr Canc Netw. 2013;11:531-46. doi: 10.6004/jnccn.2013.0070
- 45. OMS; Organización Mundial de la Salud. WHO Global Urban Ambient Air Pollution Database (update 2018). Air. 2018. Fecha de Consulta: 14 de febrero de 2019. Disponible en: https://www.who.int/airpollution/data/cities/en/
- 46. Ahnen DJ, Wade SW, Jones WF, Sifri R, Silveiras JM, Greenamyer J, et al. The increasing incidence of young-onset colorectal cancer: A call to action. Mayo Clin Proc. 2014;89:216-24. doi: 10.1016/j.mayocp. 2013.09.006.