El Síndrome de Chediak-Higashi (SCH) es un trastorno heredado como un rasgo autosómico recesivo, que se origina por mutaciones en el gen CHS1 localizado en el cromosoma 1q42-q43. Este gen codifica para una proteína, aún en proceso de caracterización, pero se tienen evidencias de su requerimiento para la generación normal, la estructura y la función de una variedad de organelas intracelulares como los lisosomas y los gránulos secretorios (22).
Estas alteraciones llevan a la fusión anormal de los gránulos intracitoplasmáticos, originando granulaciones gigantes observadas en los leucocitos circulantes, las neuronas, los melanocitos, las células tubulares renales, los fibroblastos y el cabello.
Adicionalmente, otras consecuencias del defecto molecular son la neutropenia, por una destrucción intramedular de estos granulocitos; una disminución marcada de la quimiotaxis de los neutrófilos al parecer por un impedimento mecánico debido a los gránulos gigantes y una deficiente acción citotóxica de las células NK.
El cuadro clínico del Síndrome de Chediak-Higashi (SCH) es característico y comprende manifestaciones dermatológicas que van desde una dilución pigmentaria moderada de la piel y el cabello, hasta una hipopigmentación severa comparable al albinismo óculo-cutáneo tirosinasa positiva.
Se puede presentar hiperpigmentación en áreas expuestas al sol. Además: fotofobia, infecciones recurrentes piógenas severas en la piel y aparato respiratorio, deterioro neurológico gradual con retardo mental, convulsiones, neuropatía periférica y debilidad muscular.
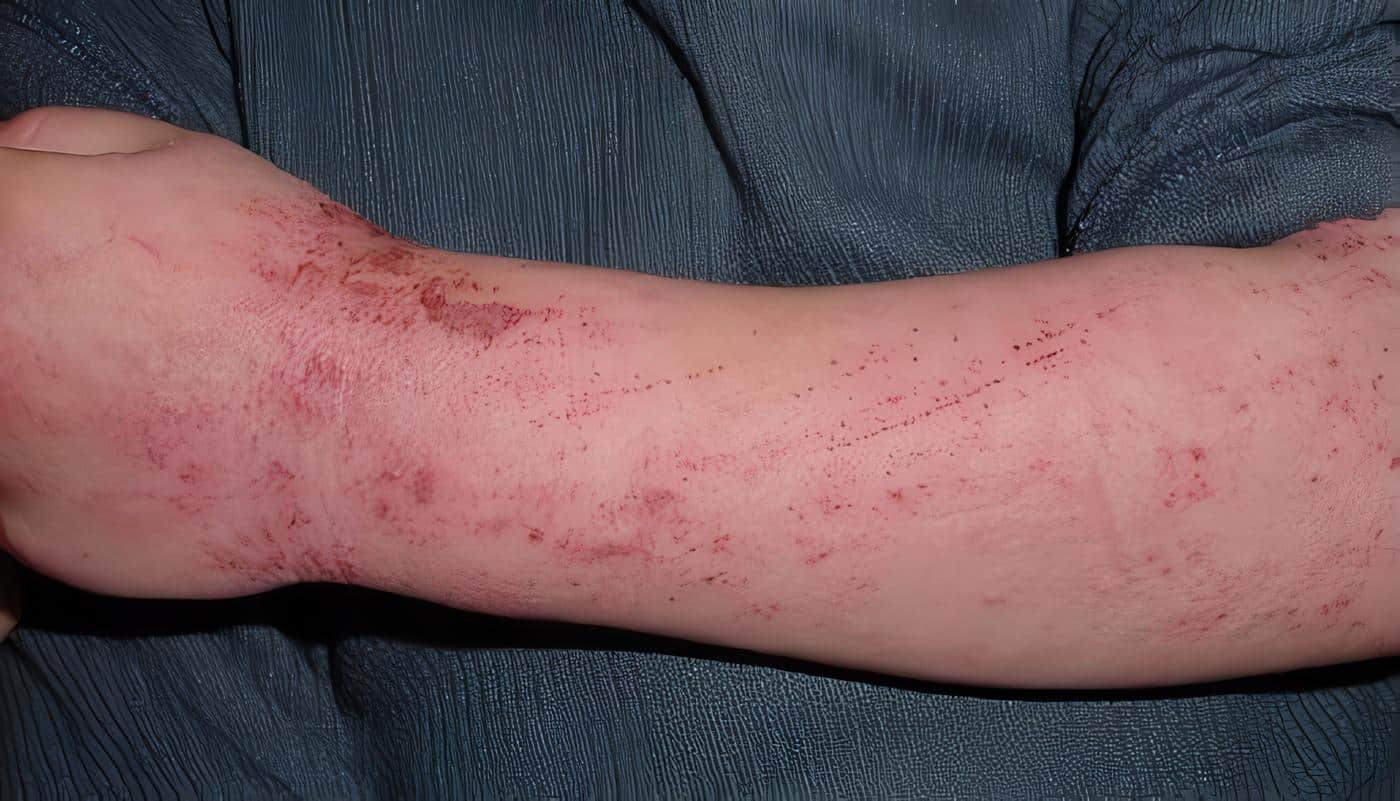
Luego de varios años de evolución, la enfermedad presenta en el 85% de los casos episodios agudos, denominados “fase acelerada” similares a un linfoma, y se caracterizan por la infiltración visceral del hígado y el bazo por linfocitos atípicos e histiocitos, con hepatoesplenomegalia, poliadenopatías, ictericia, pancitopenia y gingivoestomatitis. Por la trombocitopenia, se encuentran petequias y equimosis (16) (Foto 9).
Granulomas cutáneos
Enfermedad Granulomatosa Crónica (EGC)
La EGC es causada por un defecto profundo en la explosión respiratoria que acompaña a la fagocitosis de todas las células mieloides (neutrófilos, eosinófilos, monocitos, macrófagos).
Durante la explosión respiratoria se produce la conversión catalítica del oxígeno molecular (O2) en anión superóxido (O-2), el cual se convierte en peróxido de hidrógeno (H2O2), ácido hipocloroso y radicales hidroxilo (.OH); estos derivados del O2 son importantes para la reacción microbicida contra bacterias y hongos.
El complejo enzimático que cataliza la explosión respiratoria se conoce como NADPH oxidasa, compuesto por lo menos por cuatro proteínas, dos se encuentran en la membrana plasmática, las subunidades del citocromo b558, la gp91-phox y la p22-phox, (phox: oxidasa de los fagocitos), y dos proteínas citosólicas, la p47-phox y la p67-phox (23).

Foto 9. Síndrome de Chediak-Higashi. Albinismo moderado del cabello y marcada hiperpigmentación de la cara.
El defecto molecular en la EGC es bastante heterogéneo y se origina a partir de las mutaciones en cualquiera de los cuatro genes que codifican para las proteínas del sistema. Así, mutaciones localizadas en el gen que codifica para la gp91phox (ubicado en el cromosoma X, Xp21-1) producen la variedad ligada al sexo que afecta el 60% de todos los pacientes.
El otro 40%, se transmite como un rasgo autosómico recesivo debido a que los genes que codifican para p47phox, p67 phox y p22 phox se encuentran en los cromosomas somáticos.
La principal característica clínica de la EGC es la aparición en el primer año de vida del síndrome de infección recurrente anormal con compromiso de la piel, los aparatos gastrointestinal y respiratorio, los ganglios y algunos órganos profundos como el hígado.
En la piel, las manifestaciones más frecuentes son las infecciones por Staphylococcus aureus: piodermitis, forunculosis, abscesos, granulomas cutáneos; fístulas perianales; úlceras crónicas por fistulización de una adenitis supurada a nivel del cuello, gingivoestomatitis crónica, úlceras orales y una dermatitis similar a la atópica (4, 16, 24, 25) (Foto 10).
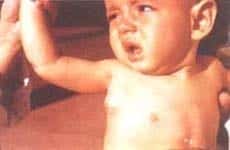
Foto 10. Enfermedad granulomatosa crónica. Granuloma cutáneo en tercio superior del tórax.
Con frecuencia se presentan: neumonía, osteomielitis, enfermedad diarreica recurrente o crónica, septicemia y hallazgos no infecciosos como la hepatoesplenomegalia y las adenopatías múltiples.
Las mujeres heterocigóticas portadoras de mutaciones para la EGC ligada al cromosoma X no tienen un riesgo anormal de infecciones, pero pueden presentar un lupus discoide o sistémico y afecciones de la cavidad oral como estomatitis aftosa y queilitis granulomatosa (16).
Infecciones cutáneas por Candida albicans
Candidiasis Mucocutánea Crónica (CMC)
La CMC es una inmunodeficiencia de origen desconocido que se inicia por lo general en los primeros años de la vida, pero existen también casos en la vida adulta. Se caracteriza por una susceptibilidad anormalmente elevada a las infecciones de la piel y las mucosas por Candida albicans, que rara vez se acompaña de compromiso sistémico o de infecciones por otros microorganismos (hongos y bacterias). En algunos casos se asocia con endocrinopatías como el hipotiroidismo, el hipoparatiroidismo, la disfunción gonadal y el hipoadrenalismo. La presencia de autoanticuerpos dirigidos contra diferentes órganos endocrinos ha llevado a proponer una etiología autoinmune (26).
En los pacientes con CMC las diferentes subpoblaciones de LT son normales, pero las pruebas de hipersensibilidad retardada para Candida albicans son negativas. La función de los LB y la producción de anticuerpos específicos está conservada.
La intensidad de las lesiones varía en cada paciente y se observa desde moderado compromiso de las uñas o la mucosa oral hasta formas difusas con gran hipertrofia de las mucosas y formación de granulomas en la piel y en las uñas (16) (Foto 11).
Infecciones virales de la piel
Inmunodeficiencia celular con inmunoglobulinas y anticuerpos normales
Es una inmunodeficiencia primaria de origen molecular desconocido, en la cual se aprecia una disminución profunda y sostenida en el número de LT CD4+ circulantes. Se afectan además los LB y las células NK, pero los granulocitos son normales (2, 27).
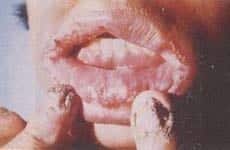
Foto 11. Candidiasis mucocutánea crónica. Lesiones crónicas por Candida albicans en labios y mucosa yugal. Queilitis angular. Lesiones granulomatosas crónicas con destrucción de uñas de los dedos.
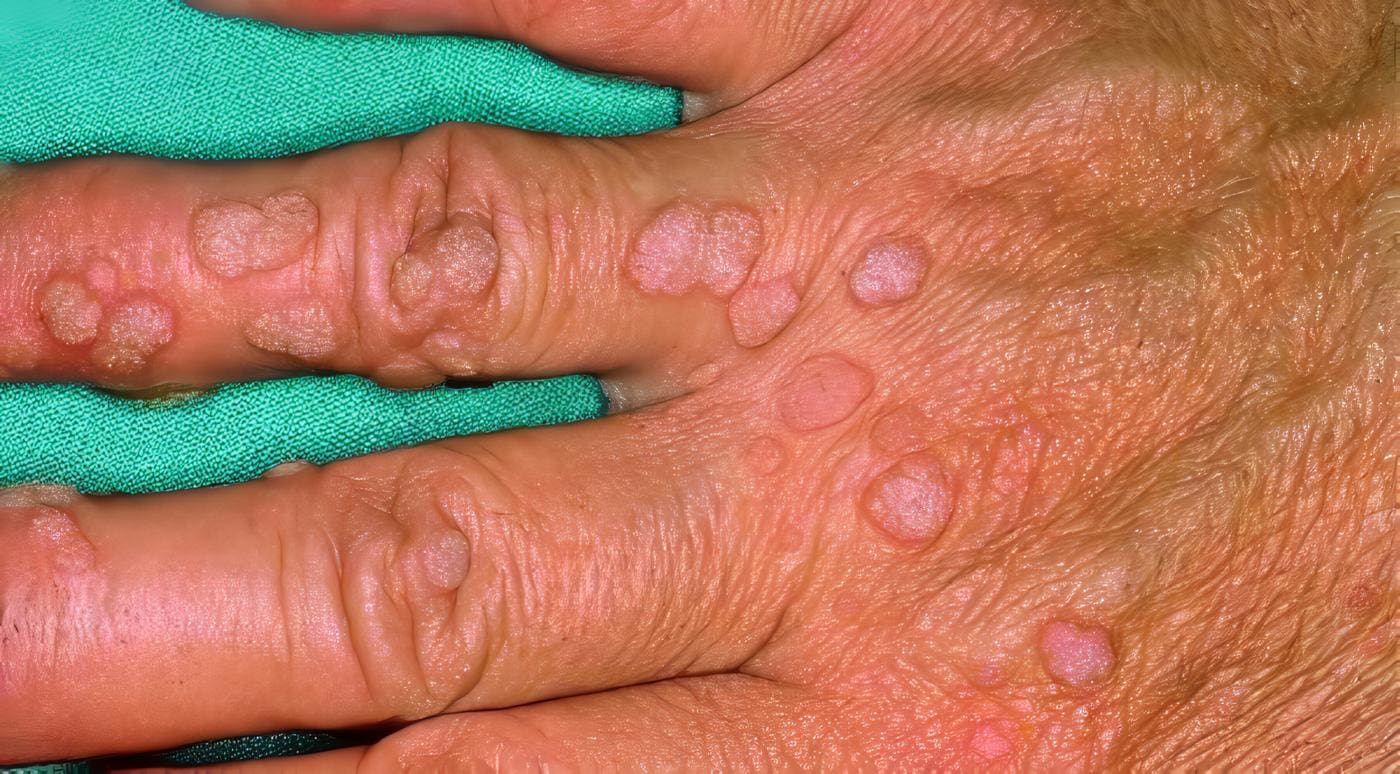
Los síntomas se presentan en la pubertad con afecciones por papilomavirus, los cuales producen verrugas extensas diseminadas y resistentes a todo tipo de tratamiento, en ocasiones semejan una epidermodisplasia verruciforme. Además, manifiestan infecciones por gérmenes intracelulares como la meningitis por Cryptococcus neoformans, la tuberculosis pulmonar y miliar, la neumonía por Pneumocystis carinii, y las infecciones mucocutáneas y diseminadas por Candida albicans. En estos pacientes no se observan infecciones por bacterias extracelulares porque tienen normales los niveles de inmunoglobulinas séricas y la producción de anticuerpos específicos está conservada (28) (Foto 12).
Reacciones inflamatorias agudas de la piel y las mucosas
Edema Angioneurótico Hereditario (EAH)
El EAH es una enfermedad autosómica recesiva generada por la deficiencia de una de las proteínas reguladoras del complemento conocida como Inhibidor de la C1 esterasa (C1INH), la cual es codificada por un gen localizado en el cromosoma 11 (29).
La C1INH se encuentra normalmente en bajas concentraciones en el suero y controla la activación espontánea de las enzimas C1r y C1s al unirse en forma covalente a ellas e impedir la formación de un complejo C1 macromolecular activo. Además, el C1INH controla la actividad de otras proteínas como el C2, el C4 y el Factor de Hageman.
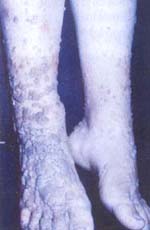
Foto 12. Inmunodeficiencia celular con inmunoglobulinas y anticuerpos normales. Extensas lesiones de verrugas planas, confluentes (semejante a la epidermodisplasia verruciforme), en piernas y pies.
En ausencia del C1INH, aún con traumas mínimos se induce la cascada de la coagulación con la activación del factor de Hageman y las calicreínas, para generar sustancias vasoactivas que producen el angioedema. Éste se puede localizar en áreas cutáneas y mucosas, pero es más frecuente en la piel de la cara produciendo un edema severo de ella, los párpados y los labios; ocasionalmente hay compromiso laringofaríngeo que obstruye las vías aéreas y puede causar la muerte. El angioedema es indoloro, no hay prurito ni signos inflamatorios, y generalmente desaparece en 2 a 4 días. Cuando compromete la mucosa digestiva se presenta con dolor abdominal recurrente (Foto 13).
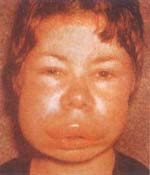
Foto 13. Angioedema hereditario (Deficiencia C1INH). Angioedema severo que compromete: párpados, cara y labios.
Este tipo de angioedema no responde al tratamiento con antihistamínicos, esteroides ni antiinflamatorios generales, solo mejora con terapia basada en sustancias que incrementan la síntesis hepática del C1INH.
Correspondencia: Diana García de Olarte. AA. 1226 de Medellín. Teléfono: 510 60 57. Email: dolarte@epm.net .co
Referencias Bibliográficas
- Smith CIE, Ochs HD, Puck JM. Genetically Determined Immunodeficiency Diseases: A Perspective. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:3-11.
- WHO Scientific Group. Primary Immunodeficiency Diseases. Clin Exp Immunol 1997;109 (suppl. 1):1-28.
- Latinoamerican Group of Primary Immunodeficiency Diseases (LAGID). Clasificación fenotípica de las inmunodeficiencias primarias. Boletín LAGID 1997;1:11-13.
- García de OD, Patiño PJ, Salgado H, López JA, Montoya CJ, Pérez JE. Evaluación del paciente con inmunodeficiencia. Síndrome de infección recurrente patológica. Medicina y Laboratorio 1997;7:545-575.
- García de OD. Que tan lejos se ha llegado en el conocimiento de las inmunodeficiencias primarias. Rev Asoc Colomb Alerg Asma e Inmunol 2000;9:51-61.
- Grimbacher B, Holland SM, Gallin JI, et al. Hyper-IgE Syndrome with recurrent infections. An autosomal dominant multisystem disorder. N Engl J Med 1999;340:692-702.
- Buckley RH. Disorders of the IgE system. In: Stiehm RE, ed. Immunologic disorders in infants and children. 4th ed. Philadelphia: WB Saunders Company, 1996:409-422.
- Montoya CJ, García de OD, Butler B, Leiva LE, Rodríguez J, Sorensen RU. Abnormal IgG antobidy response to Streptococcus pneumoniae polysaccharide and defective immunological memory in patients with the Hyper-IgE recurrent infection syndrome. (Sometido para publicación en Journal of Clinical Immunology).
- Montoya CJ, García de OD, Butler B, Leiva LE, Sorensen RU. Cytokine and CD40 ligand mRNA expression by resting and stimulated peripheral blood mononuclear cell of patients with the Hyper-IgE recurrent infection syndrome. (Manuscrito en preparación).
- Geha RS, Leung DYM. Hyper immunoglobulin E syndrome. Immunodef Rev 1989;1:155-172.
- Borges WG, Hensley T, Carey JC, Petrak BA, Hill HR. The face of Job. J Pediatr 1998;133:303-305.
- Buckley RH, Schiff IR, Schiff SE, et al. Human severe combined immunodeficiency: Genetic, phenotypic, and functional diversity in one hundred eigth infants. J Pediatr 1997;130:378-387.
- IUIS Scientific Group. Primary Immunodeficiency Diseases. Clin Exp Immunol 1999;118 (Suppl. 1):1-28.
- Schwarz K, Notarangelo LD, Spanopoulou E, Vezzoni P, Villa A. Recombination Defects. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:155-166.
- Stephan JL, Vlekova V, Le Deist F, et al. Severe Combined Immunodeficiency: A retrospective single-center study of clinical presentation and outcome in 117 patients. J Pediatr 1993;123:564-572.
- Paller AS. Cutaneous Changes in Disorders of Altered Reactivity. Genetic Immunodeficiency Diseases. In: Freedberg I, Eisen A, Wolff K, Austen F, Goldsmith L, Katz S, Fritzpatrick T, eds. Fritzpatrick’s Dermatology in General Medicine. 5th ed. New York: McGraw-Hill, 1999:1397-1408.
- Etzioni A, Harlan JM. Cell Adhesion and Leukocyte Adhesion Defects. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:375-388.
- Rosen FS, Geha RS. Leukocyte Adhesion Deficiency. In: Rosen FS, Geha RS, eds. Case Studies in Immunology. A Clinical Companion. Second ed. New York: Current Biology Publications – Garland Publishing, 1999:87-94.
- Ochs HD, Rosen FS. The Wiskott-Aldrich Syndrome. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:292-305.
- Lavin MF, Shiloh Y. Ataxia-Telangiectasia. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:305-323.
- Cohen LE, Tanner DJ, Schaefer HG, Levis WR. Common and uncommon cutaneous findings in patients with ataxia-telangiectasia. J Am Acad Dermatol 1984;10:431-438.
- Spritz RA. Chediak-Higashi Syndrome. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:389-396.
- Segal BH, Leto TL, Gallin JI, Malech HL, Holland SM. Genetic, Biochemical, and Clinical Features of Chronic Granulomatous Disease. Medicine 2000;79:170-200.
- Winkelstein JA, Marino MC, Johnston RB, et al. Chronic Granulomatous Disease. Report on a National Registry of 368 Patients. Medicine 2000;79:155-169.
- Dohil M, Prendiville JS, Crawford RI, Speert DP. Cutaneous manifestations of chronic granulomatous disease. J Am Acad Dermatol 1997;36:899-907.
- Hong R, Clement LT, Gatti RA, Kirkpatrick CH. Disorders of the T-cell System. In: Stiehm ER, ed. Immunologic Disorders in Infants and Children. Philadelphia: W.B. Saunders Company, 1996:339-408.
- Latinoamerican Group of Primary Immunodeficiency Diseases (LAGID). Clasificación fenotípica de las inmunodeficiencias primarias. Boletín LAGID 1997;1:11-13.
- Lowy DR, Androphy EJ. Wartz. In: Freedberg I, Eisen A, Wolff K, Austen F, Goldsmith L, Katz S, Fritzpatrick T, eds. Fritzpatrick’s Dermatology in General Medicine. 5th ed. New York: McGraw-Hill, 1999:2484-2497.
- Sullivan KE, Winkelstein JA. Genetically Determined Deficiencies of the Complement System. In: Ochs HD, Smith CIE, Puck JM, eds. Primary immunodeficiency Diseases. A Molecular and Genetic Approach. New York: Oxford University Press, 1999:397-417.