Ana María Segura R. MD.1
Universidad Metropolitana
Laboratorio de Inmunología y Genética
Calle 76 N° 52-78 Barranquilla, Colombia
1 Carrera 43 N° 72-122 Oficina 706
Tel.: 3587935 Telefax: 3581473
Email: asegurar@usa.net
Abstract
After reviewing the literature on mucosal immunology produced in the last decade in various research centers around the world, it was possible to compile all the information regarding the discoveries made in the twentieth century in this area.
At the end of this review, it was concluded that the advances obtained up to now have great applicability in various forms of immunomodulation. For instance, the induction of immunoprophylaxis, immunotolerance, immunopotentiation, immunosupression and anergy.
These advances could play a fundamental role in the desensitization treatment of allergic patients, the treatment of rheumatological and autoimmune processes in general. As well as for tolerance in organ transplantation and vaccination processes. With regard to allergies, protocols in sublingual immunotherapy have already been developed in humans.
Although findings in this area are still on an experimental level, research indicates that a promising future awaits for the mucosal immunitary system as far as the immunomodulation processes are concerned, as shown by the results obtained so far.
Marco teórico
Recuento histórico
La obtención de inmunidad a través de las mucosas fue sospechada y confirmada desde hace aproximadamente 300 años (109, 131, 175). Pero sólo hasta las dos últimas décadas se han aclarado, aunque parcialmente, los mecanismos de tipo celular, humoral y molecular que participan en este tipo de respuesta (9-10, 14, 19, 40, 48-50, 75, 81, 90, 92, 97, 108, 129, 138, 139, 142, 149-152).
Fue en 1910 cuando se intentó inducir inmunotolerancia a diferentes alimentos en roedores (109).
En 1922 se tuvo la primera evidencia de que la inmunidad en mucosas era de tipo humoral y se señaló a la Inmunoglobulina A secretora (IgAs) como el mecanismo de defensa más importante a este nivel (109). Pero fue en la década de los años 60 a 70, cuando se intensificó esta investigación. Explorando todo lo concerniente a los diferentes elementos humorales y celulares que participan en la respuesta inmunitaria de mucosas. Y dándosele desde entonces el nombre de respuesta inmunitaria local para distinguirla de la respuesta inmunitaria obtenida por vía parenteral.
En 1970 se propuso el factor secretor o componente secretor que actúa como un receptor polimérico transmembrana de inmunoglobulinas como son la IgA y la IgM dimérica y pentamérica, respectivamente (10, 39, 109).
En la actualidad este mecanismo de transporte de anticuerpos transmembrana ha sido plenamente comprobado gracias a nuevas metodologías de biología molecular que han dilucidado aspectos de tipo celular y humoral (10, 23, 39, 151).
Desde hace aproximadamente 10 años existe en la comunidad científica médica gran interés en la inducción de métodos de inmunotolerancia, inmunosupresión e inmunoprofilaxis por vía oral, nasal, bronquial y sublingual.
Durante algún tiempo a estos procedimientos se les llamó métodos alternativos:
Sin embargo, debido a que este término se utiliza para designar procedimientos de la medicina tradicional como la homeopatía, acupuntura, etc. Se adoptó últimamente el término inmunoterapia local, ya que ésta, es una práctica ortodoxa dentro de la medicina alopática (173, 174).
Son muchos los centros de investigación en donde se ha venido trabajando experimentalmente con animales y humanos a nivel de mucosas. Con resultados que van desde el fracaso hasta éxitos tan relevantes que sus autores los han calificado de asombrosos (131, 175, 176).
Según algunos autores la vía parenteral, tradicionalmente utilizada para inducir desensibilización de procesos alérgicos, la inducción de tolerancia, inmunosupresión, anergia o para lograr inmunidad. Es un procedimiento cuyos resultados dejan mucho que desear, ya que después de su uso indiscriminado durante muchos años. Ha puesto al descubierto muchos efectos colaterales nocivos, algunos de los cuales, podrían poner en riesgo la vida de los pacientes (6, 24).
A continuación se describen algunas de esas desventajas:
- Su efecto a muy largo plazo, en el caso de desensibilización de procesos alérgicos.
- El trauma, pues son muchas las inyecciones que debe recibir el paciente, lo cual es especialmente molesto en niños.
- El costo elevado.
- El alto riesgo de producir reacciones anafilácticas, algunas veces letales.
- Efectos colaterales en el sitio de la punción.
- El resultado no siempre es exitoso.
- La tolerancia inducida no es persistente.
Todo lo anterior ha llevado a la búsqueda de otras vías para abordar al sistema inmunitario, utilizando para ello las mucosas. Lográndose por esta vía, respuestas no sólo de tipo local sino también sistémicas que es lo ideal cuando se trata de inducir tolerancia, inmunosupresión o inmunidad.
A lo largo de estas investigaciones se ha ido ampliando. Cada vez más, el uso de las mucosas para diferentes procedimientos en el campo profiláctico, terapéutico y preventivo de la inmunología clínica a lo cual nos referiremos a continuación:
En inmunoprofilaxis
En este campo se ha trabajado con gran interés en el diseño de vacunas que puedan administrarse por vía oral (11, 13, 21, 25, 32-34, 42, 54, 65, 94, 135,).
Este sentido ya se tiene una buena experiencia con el plan de vacunación contra la poliomielitis que se sigue a nivel mundial y con el cual se aspira erradicar esta enfermedad del planeta tierra, tal como sucedió con la viruela.
Una vacuna aplicada por vía de mucosas digestivas, produce una inmunidad sistémica y local, lográndose una protección de un 100%, porcentaje que casi nunca se logra con las vacunas aplicadas parenteralmente.
Vacuna oral antipoliomielitis
Esta experiencia con la vacuna oral antipoliomielitis nos demuestra que la vía de las mucosas es la ideal para inducir inmunidad y se está trabajando con gran interés en la búsqueda de:
- Antígenos apropiados (25, 33, 34, 94).
- Coadyuvantes y sustancias de transporte de antígenos (11, 13, 21, 25, 65).
- Sustancias que bloquean la tolerancia inmunitaria (32, 42, 54).
Después de obtener el antígeno apropiado, encontrando a su vez el elemento que lo transporte y proteja de las enzimas y acidez gástricas, faltaría únicamente adicionar una sustancia inhibidora de tolerancia inmunitaria en mucosas para obtener la vacuna ideal para administración oral (67, 113, 114, 135).
En inmunotolerancia
Hasta este momento ha tenido su mayor aplicación en la desensibilización de procesos alérgicos (58, 89, 102, 111, 128, 130, 131, 105-159, 160-172, 176) y de las dermatitis por contacto (4, 12, 45). Las vías oral y sublingual han sido las más empleadas, pero también se ha explorado la vía nasal y bronquial. Los antígenos utilizados son proteínas hidrosolubles y péptidos preparados en extractos biológicos estandarizados (7, 176).
Los resultados satisfactorios, obtenidos en la inmunoterapia de enfermedades alérgicas a través de las mucosas, suscitaron a algunos investigadores a aplicar protocolos similares en el tratamiento de procesos autoinmunitarios en el campo experimental; con el uso del autoantígeno “responsable” del proceso autoin-munitario, se trata de desensibilizar a los “individuos” (animales o ratones) a los cuales se les indujo la enfermedad autoinmune experimentalmente.
Los resultados obtenidos han sido excelentes constituyéndose este procedimiento en una gran esperanza para el futuro de los pacientes con enfermedades autoinmunitarias; sin embargo, para obtener éxito a nivel humano y en patologías no inducidas experimentalmente se requiere identificar y purificar los autoantígenos “responsables”; este hecho constituye el eje central de las investigaciones actuales (2, 3, 5, 14, 16, 26, 27, 29, 35-38, 41-44, 57, 59, 60, 63, 66, 73-80, 91, 96, 100, 101, 105, 106, 115, 117-119, 125-127, 133, 136, 140-143).
En tolerancia a trasplantes de órganos
Múltiples investigaciones en este campo han tratado de resolver el problema del rechazo de un órgano trasplantado que proceda de un animal de la misma especie o de especie diferente; en este sentido los trabajos experimentales pretenden inducir un estado de tolerancia, supresión o anergia sistémica que evite el rechazo de un tejido alogénico o de cualquier agente extraño (49, 51, 59-62, 65-67, 71, 82, 86, 88, 103, 113, 114, 134).
Un estado de anergia clonal se puede inducir experimentalmente con la Enterotoxina B del Stafilococcus dorado, sustancia responsable de infecciones graves en pacientes con algún tipo de inmunodeficiencia (8, 61).
Además, se han realizado trabajos con el propósito de inducir inmunosupresión o tolerancia ante antígenos HLA clase II (HLAII), que permita una buena aceptación de tejidos alogénicos procedentes de otros seres humanos. Estos trabajos son realmente los que han resultado de mayor trascendencia por los éxitos obtenidos en el plano experimental.
Los antígenos utilizados son péptidos sintéticos HLAII administrados por vía oral-sublingual.
Lo más sorprendente de estos resultados es que no sólo se ha obtenido un estado de supresión, sino verdaderos estados de tolerancia a tejidos alogénicos. Estos estudios son alentadores, ya que se ha logrado evitar el desarrollo de una enfermedad injerto versus huésped o GVsH (Rechazo del receptor contra el trasplante o viceversa) y más aún, la aceptación del trasplante de un órgano alogénico en un animal retrasplantado; esto último es de suma importancia porque lo normal es que la persona o animal que ha rechazado un primer trasplante, en un segundo intento, existe gran probabilidad de encontrarse sensibilizado contra los antígenos HLAII y puede producir un rechazo agudo o hiperagudo del tejido trasplantado (15, 20, 50, 72, 124).
En inmunomodulación
Para la reactivación o intensificación de la respuesta inmunitaria se han utilizado diferentes sustancias que administradas por vía oral, a dosis e intervalos adecuados de aplicación, estimulan al sistema inmunitario.
Este procedimiento es útil en ciertos tipos de inmunodeficiencia adquirida (no SIDA), como en el cáncer, la tuberculosis etc., o para mejorar la respuesta a una vacuna actuando como coadyuvantes.
El descubrimiento de nuevas sustancias inmunomoduladoras se convierte en un pilar fundamental para la inmunoterapia ya sea porque éstas activen la inmunidad o impidan la tolerancia (11, 13, 25, 32-34, 42, 94).
La dosis e intervalos de aplicación del antígeno son factores fundamentales, por consiguiente, la mayoría de investigaciones apuntan a establecer estas dos variables. Cada antígeno se comporta en forma muy particular, puede inducir inmunidad o contrario como sería su tolerancia, supresión o anergia (67, 113, 114, 135).
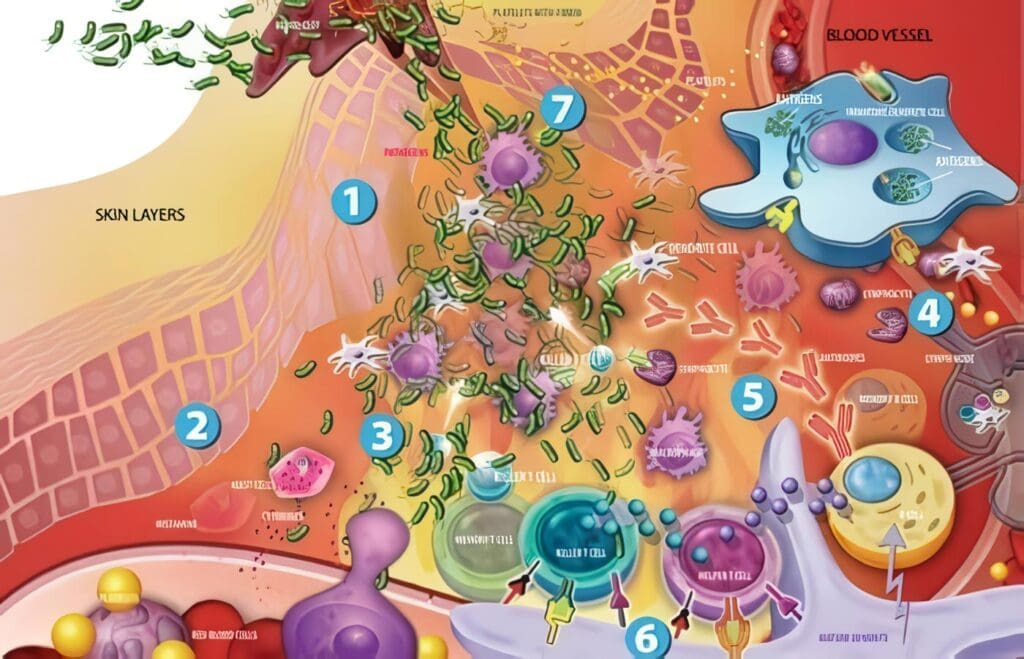
Estructura tisular, celular y molecular de las mucosas y su participación en la respuesta inmunitaria local y sistémica
En la búsqueda de los elementos que propician la respuesta inmunitaria a nivel de las mucosas, se han aclarado aspectos de tipo tisular, celular, humoral y molecular (9, 10, 14, 17-19, 35, 48-50, 104, 110, 115, 146, 149, 152). En cuanto a la dinámica con que operan esos elementos, también se han logrado importantes adelantos (35, 72, 75, 76, 81, 90, 132, 137, 138, 142, 150).
A continuación se hará una descripción de los principales aspectos anatómicos y de la dinámica con que se desarrolla una respuesta inmunitaria en mucosas.
Es importante aclarar que cuando se suministra un antígeno por vía oral su destino puede ser muy diferente si su deglución es inmediata o si, por el contrario, es sostenido por escasos minutos en la cavidad oral y debajo de la lengua.
(Lea También: Estudios en Autoinmunidad Inducida Experimentalmente)
Nivel de mucosa oral sublingual
El sistema inmunitario que opera a nivel de mucosa oral sublingual es muy rico en células dendríticas portadoras a gran escala de antígenos HLAII (81, 111, 138, 149, 152, 176).
Estas células pueden procesar enzimáticamente al antígeno, migrar a los nódulos linfoides locales y actuar como presentadoras de antígenos a los linfocitos T-CD4 (81).
La célula dendrítica de mucosas produce la interleucina IL-12, la cual promueve la derivación de un LT-CD4 indiferenciado hacia la línea TH1; de esta manera favorece la respuesta celular aferente activando LTh1 y no los LTh2 (151), esto equivale a crear inmunidad específica y no tolerancia.
Una demostración de lo anterior fue realizada neutralizando la IL-12 con un anticuerpo monoclonal. Lo cual produjo un aumento en la secreción del Factor Transformante de Crecimiento b1 (TGF-b1) induciendo tolerancia (144). Esto nos explica el hecho de que los antígenos administrados por vía sublingual inducen inicialmente inmunidad y solo después. Cuando se continúa su administración en pequeñas dosis y por un período de tiempo prolongado. Se logra un estado de tolerancia estable sobre este antígeno (113, 114, 135, 176).
Se confirmó recientemente la absorción de antígenos a nivel de mucosa oral, pues al aplicar el polen Parietaria Judaica, éste persistió en la mucosa por más de 12 horas (174), tiempo suficiente para que un antígeno sea detectado por el sistema inmunitario.
Si un antígeno logra llegar al intestino estará sometido a diferentes acciones de la inmunidad local de mucosas; puede ser neutralizado por la Inmunoglobulina A secretora (IgAs) que lo inhabilita, hasta ser retirado. Los autores coinciden en que la IgAs prima en todas las mucosas y que es el factor esencial para adquirir tolerancia, mediada por anticuerpos, a este nivel (1, 9, 10, 23, 92, 110, 176).
Si un antígeno no es neutralizado por la IgAs:
En el intestino delgado es tomado por las células M estas células, las cuales están presentes en toda la superficie de la mucosa digestiva y cuya función es endocitar y transportar el antígeno al sistema linfoide de mucosas o Placas de Peyer (63, 176); es ahí donde se inicia la respuesta inmunitaria específica cuando las células dendríticas o los macrófagos, captan y procesan el antígeno y lo presentan al linfocito T CD4, se inicia, de esta manera, una respuesta celular que culmina con una expansión clonal antígeno específica en la cual participan linfocitos T y B (48-50).
Los linfocitos T activados migran a través de la linfa y sangre hasta llegar al epitelio intestinal formando parte de la población linfocitaria intraepitelial (9, 19).
Los linfocitos B migran a su vez a la lámina propia, a otras mucosas y a las glándulas exocrinas; allí se transforman en células secretantes de anticuerpos IgAs (Plasmocitos) (14).
Estos anticuerpos, después de unirse al factor secretor poli-inmunoglobulinas transmembrana son transportados por las células epiteliales y excretados a la luz intestinal (1, 9, 10, 23, 49).
En lo que respecta a la producción de interleucinas en la obtención de inmunotolerancia por vía oral existe un consenso general acerca de la participación del TGF-b1. Como el elemento humoral fundamental que modula la obtención de tolerancia ante un determinado antígeno (18, 43, 44, 62-64, 68, 69, 137, 138, 175, 176).
Este factor es producido en mucosas por los linfocitos T entre los cuales figura una nueva subpoblación linfocitaria CD4TH3 que está en estrecha relación con procesos de tolerancia a nivel de mucosas pues es el « botón de encendido» de la producción de IgAs (175-177).
En trabajos experimentales con animales a los cuales se les indujo una encefalomielitis autoinmunitaria con la MBP o proteína básica de mielina:
Se logró posteriormente, por vía de mucosas, una inmunotolerancia a esta proteína (59, 60, 63). Esto se ha relacionado con la presencia de la interleucina TGFb1 secretada por los LTh2 y LTh3 (59, 63, 175, 176).
El factor TGF b1 es de acción no restringida al sistema inmunitario en el cual se produce. Por tanto, puede transferir acción tolerante a un animal virgen o a un cultivo celular con estimulación linfoblástica (174-176).
Este factor es tan importante y definitivo en la inmunidad de mucosas que al aplicar un anticuerpo monoclonal anti TGF b1 se suprime la respuesta tolerante ante un antígeno determinado (175, 176).
La inmunidad de mucosas puede ser manipulada y es así como existen ya sustancias capaces de activar inmunidad o inducir tolerancia.
La sustancia Flt3L activa la expansión de las células dendríticas induciendo tolerancia si se administra antes del antígeno. El CT (subunidad beta del Vibrium cólera) es un activador de la inmunidad en células T (177).
Complejo Mayor de Histocompatibilidad
En cuanto a la expresión del MHC (Complejo Mayor de Histocompatibilidad) en las células de la respuesta local de mucosas se han aclarado los siguientes conceptos:
- Los antígenos HLA I y factor secretor SC aparecen en etapas muy tempranas de la gestación (10).
- Los antígenos HLA II se expresan en las células del intestino delgado y en glándulas salivares después del nacimiento, por acción del INF-g o interferón gamma (10).
La expresión de estos antígenos en las células inmunocompetentes es fundamental, pues hacen posible la respuesta inmunitaria celular y la restricción inmunogenética, mediada. Ya sea, por antígenos HLAI y LT-CD8 para respuestas de tipo citotóxica y antiviral, o por antígenos HLAII y LT-CD4 que posibilitan respuestas de tipo aferente, de inmunidad específica y de tolerancia. Todo lo descrito capacita a un neonato para defenderse de la agresión microbiológica y de agentes extraños a los cuales se ve enfrentado al abandonar del vientre materno.
Existe una relación directamente proporcional entre los antígenos de histocompatibilidad mayor HLA II y la producción del factor secretor poliinmunoglobulinas.
A su vez, el aumento en la expresión epitelial del factor secretor y antígenos HLA II depende del interferón gamma (INF); la producción de este último depende de la estimulación temprana del sistema inmunitario del neonato cuando se ve expuesto a agentes infecciosos o por antígenos extraños. Esta relación de dependencia se sigue sucediendo durante toda la vida del ser humano (10, 174-176).
El INF-g y el TNFa (factor de necrosis tumoral alfa) son moléculas muy representativas en los procesos de confrontación ante agentes extraños. Especialmente en enfermedades de tipo infecciosas o inflamatorias, verbigracia, la enfermedad de Sjogren, la gastritis crónica, la enfermedad celíaca, etc.
Las células epiteliales de mucosas portadores de antígenos HLA II:
Parecen tener funciones de células presentadoras de antígenos (20), ya que se encuentran aumentadas en enfermedades inflamatorias y en inducción de autoinmunidad experimental. Igualmente se han relacionado con el aborto de la tolerancia oral llevando a un estado contrario de inmunidad. Esto es aún materia de investigación (10, 20).
En definitiva, hasta este momento, son los LTh2, con la interleucina IL4 y el LTh3 con la interleucina TGFb1, y la IgAs (Inmunoglobulina A secretora). Los elementos más involucrados en la inducción de respuesta inmunitaria de tolerancia a nivel de mucosas (175- 176).
En lo relacionado a órganos, el bazo parece tener gran importancia, en trabajos experimentales. Al ser extirpado este órgano no es posible inducir un estado de tolerancia ante un antígeno determinado (35).
El hígado también puede inducir respuestas de tolerancia, propiciada por los linfocitos T que se encuentran en él y que también circulan en las mucosas digestivas. Esto hace pensar que este órgano también es importante para desarrollar en forma adecuada una respuesta inmunitaria en las mucosas (146).
Objetivos
Objetivo general
Revisar en forma exhaustiva la investigación que, sobre la respuesta inmunitaria de mucosas, se sucedió durante el siglo XX.
Objetivos específicos
- Presentar los adelantos en el conocimiento de los elementos tisulares, celulares, humorales y moleculares que intervienen en la respuesta inmunitaria de mucosas.
- Detallar las diferentes formas de respuesta inmunitaria que se pueden dar a nivel de mucosas.
- Revisar los métodos concebidos por diferentes investigadores para obtener respuestas inmunitarias, a través de las mucosas, a saber:
- La conformación molecular del antígeno.
- Las dosis empleadas.
- Los intervalos de las dosis.
- La duración del procedimiento.
- El sitio de la mucosa intervenida (nasal, sublingual, oral, bronquial, etc.).
- Revisar las diferentes formas de respuesta inmunitaria que se dan a través de las mucosas como:
- Inmunotolerancia.
- Inmunoprofilaxis.
- Inmunopotenciación.
- Inmunosupresión.
- Anergia.
- Relacionar la utilidad sugerida por diferentes investigadores de las mencionadas respuestas inmunitarias en las prácticas de:
- Desensibilización de pacientes alérgicos (en humanos).
- Desensibilización de procesos autoinmunitarios y reumatológicos (experimental).
- Desarrollo de nuevas vacunas por vía de mucosas (experimental).
- Inducción de tolerancia a trasplantes de órganos alogénicos (experimental).
- Inducción de respuestas anérgicas y supresoras de utilidad en trasplante de órganos y en estados alérgicos (experimental).
- Destacar las ventajas de la respuesta inmunitaria obtenida a través de las mucosas comparándola con la vía parenteral.
- Incentivar la utilización de la vía de las mucosas en reemplazo de la vía parenteral cuando se trate de inmunomodular al sistema inmunitario.