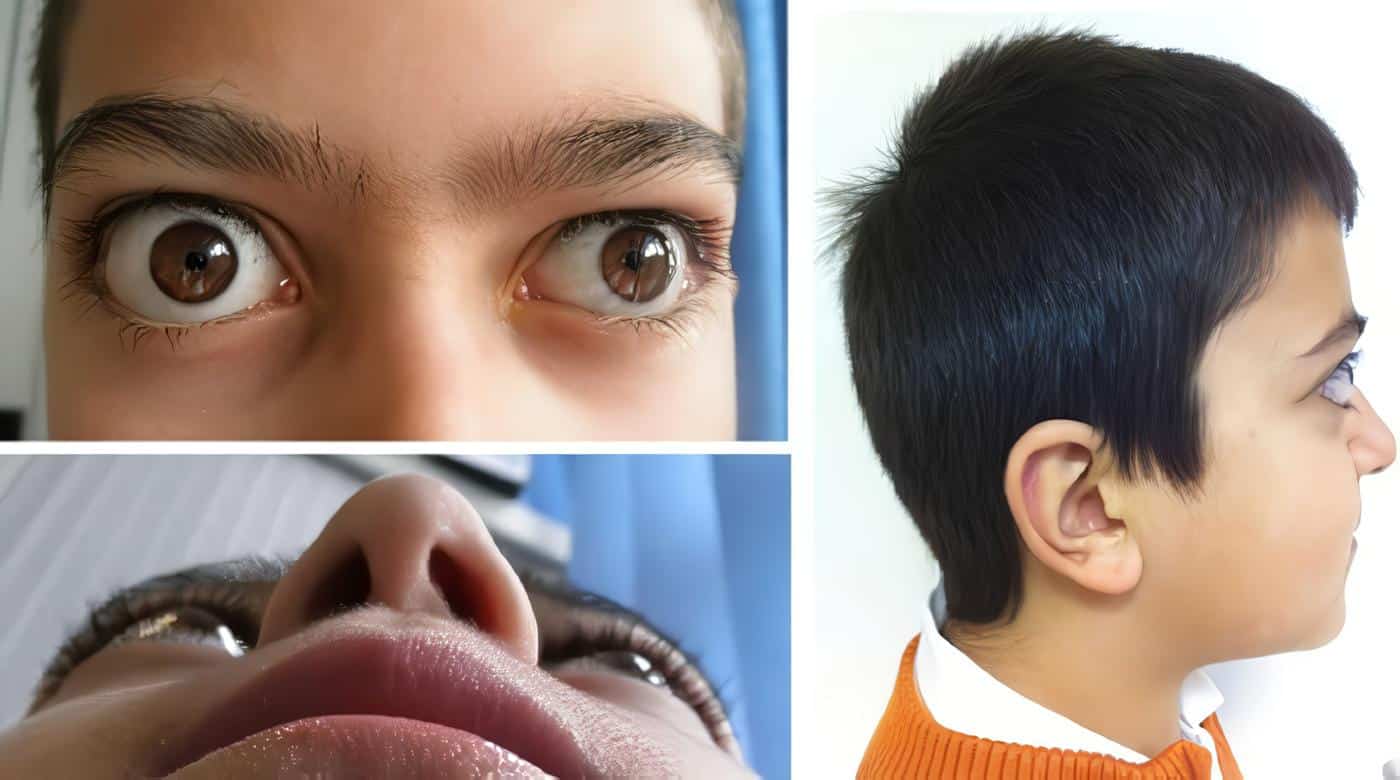
Shokery Awadalla MD.1; elizabeth mora MD.2; gemma jacques MD.3
1 Endocrinología Pediátrica, Profesor Asistente Universidad El Rosario, hospital san josé
2 Pediatría
3 Inmunología
Para valorar el efecto de la hormona de crecimiento (GH) sobre el sistema inmune se realizó un trabajo prospectivo, abierto, experimental en el cual se incluyeron 16 pacientes con talla baja familiar en el cual se realizaron pruebas cutáneas y se cuantificaron los linfocitos CD3, CD4 Y CD8 antes y después de 4 semanas de la aplicación diaria de la GH.
La edad fue de 7.5 ± 2.4 años. Hubo aumento significativo en la respuesta cutánea con la PPD y la DPT (P = 0.001, 0.002).
No hubo cambios significativos en el recuento de los CD3. Hubo aumento significativo en el recuento de los CD4. La relación CD4/CD8 aumentó después de la aplicación de la GH en forma significativa (p < =.001).
En conclusión la aplicación de la GH podría tener un efecto positivo sobre el sistema inmune.
Palabras claves: hormona de crecimiento, sistema inmune.
Introducción
La hormona de crecimiento (GH), es una pequeña molécula proteínica de cadena única que contiene 191 aminoácidos. Aparte de su efecto específico en el crecimiento, esta hormona tiene muchos efectos metabólicos generales como son el aumento de la síntesis de proteínas, el aumento en la lipólisis con mayor liberación de ácidos grasos (1).
Su secreción es controlada por dos factores que se producen en el hipotálamo que son la hormona liberadora de de la hormona de crecimiento (GHRH) y la hormona inhibidora de la hormona de crecimiento llamada somatostatina.
La GH inicialmente era extraída de los hipófisis de cadáveres y actualmente gracias a las técnicas de DNA recombinante su producción es más abundante y por esto su uso se ha ampliado a otros procesos que no son el crecimiento, y entre ellos se encuentra el sistema inmune (2-4 ).
La GH no actúa en forma directa sino a través de la producción de unas sustancias llamadas los factores de crecimiento similar a la insulina espacialmente el tipo I ( IGF-I ) (5).
Varios estudios han mostrado que facilita los procesos quimiotácticos, estimula los monocitos, por ende la actividad fagocitaria, activa el factor estimulador de las plaquetas, aumenta las subpoblaciones linfocitarias como los CD3, CD4, CD8 y mejora la respuesta de los linfocitos T.
Los CD3 y CD4 se encuentran en todas las células T periféricas:
Mientras que otras subpoblaciones CD4 y CD8 aparecen en sitios diferentes a los periféricos. Los CD4 corresponden al 60% y los CD8 al 30% de los linfocitos circulantes, con un valor ideal de 1.5 a 2 para la relación CD4/CD8 en individuos sanos (6-8).
Existen varios métodos para valorar la respuesta de inmunidad celular, siendo el más fácil pero también el más costoso, el practicar el recuento de linfocitos T y las subpoblaciones. La forma de valorar la calidad de la respuesta celular es a través de las pruebas cutáneas. En éstas se explora la respuesta de hipersensibilidad retardada intacta en la cual debe haber un reconocimiento del antígeno seguido de una respuesta inflamatoria y migración celular (9,10 ).
Por lo anterior se realizó el sigiuente trabajo con el objetivo de valorar el efecto de la hormona de crecimiento sobre el sistema inmunitario celular.
Materiales y métodos
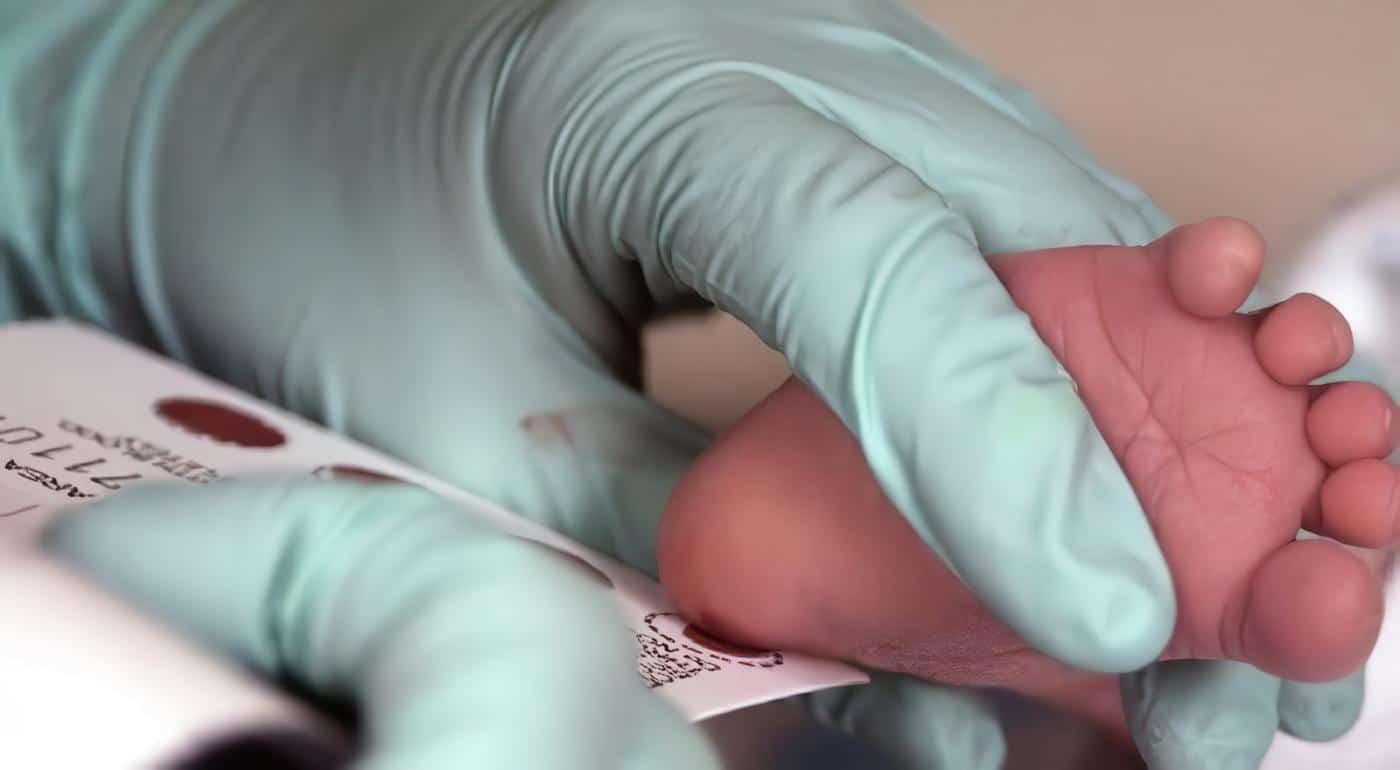
En un estudio prospectivo experimental se incluyeron niños con talla baja familiar sanos a quienes previa autorización de los padres (después de dar toda la información necesaria), se les tomó una muestra de sangre para el análisis numérico y funcional de las células inmunitarias.
La forma como se practicó el análisis celular cuantitativamente y cualitativamente fue a través de las pruebas antígeno cutáneas que midieron la calidad de la respuesta celular; estas pruebas cutáneas son: antígeno de tuberculina y antígeno de sarampión y toxoide tetánico más diftérico, la cual se aplicó intradérmica con una aguja 26 en sentido transversal de la piel, 0.5 a 10 ml (5 a 10 unidades internacionales), en la parte anterodorsal del antebrazo izquierdo a nivel del tercio medio proximal con el tercio medio; debe quedar una pápula de 5 mm, se tomó medición de la induración seis horas después de aplicada la prueba y se registró el diámetro de la misma.
Las medidas cuantitativas se realizaron por medio de cuantificación de subpoblaciones de linfocitos T CD3, CD4 y CD8.
Se aplicó la hormona de crecimiento recombinante humana a dosis de 0.1 unidades por kilogramo día subcutánea; dosis única matinal, a las cuatro semanas de aplicación se tomó una nueva muestra sanguínea para los mismos análisis anteriores y se realizaron de nuevo las pruebas cutáneas.
Aspectos Éticos
La hormona de crecimiento es un medicamento seguro a las dosis mencionadas, utilizada en niños sanos con talla baja hasta por 3 a 5 años sin efectos colaterales conocidos, además, los padres fueron informados detalladamente sobre el protocolo y se les solicitó su autorización escrita.
Los pacientes incluidos fueron los niños sin déficit de hormona de crecimiento (GH) en el cual se utilizó la hormona de crecimiento para mejorar el pronóstico estatural.
Lea También: Déficit de la Hormona de Crecimiento en los Niños
Análisis Estadístico
Los resultados se presentan en medias y desviaciones estándar (M ± DS), se utilizó la prueba del t- student para el análisis estadístico; considerando significativo p menor de 0.05. se confirmó la normalidad de la distribución de los datos.
Resultados
16 pacientes en total fueron incluidos nueve del sexo femenino, y siete del sexo masculino. No se encontró diferencia por sexo por lo cual se analizaron en un solo grupo.
La edad de los pacientes fue de 7.5 ± 2.4 años.
Los pacientes recibieron la hormona de crecimiento humana producida en las células de los mamíferos (SAIZEN) a dosis de 0.1 unidad / kg / día, y no se observó ningún efecto secundario a la aplicación del medicamento.
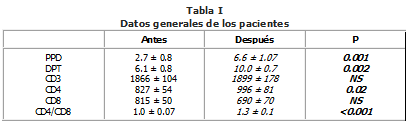
La respuesta cutánea inicial a la PPD y a la DPT fue de 2.7 ± 0.8 y 6.1 ± 0.8 mm, respectivamente. Esta respuesta aumentó en forma significativa después de la aplicación de la GH hasta 6.6 ± 1.07 y 10.0 ± 2.7 ( p = 0.001, 0.002).
No hubo cambios significativos en el número de los CD3 que fue 1866 ± 104 antes y 1899 ± 178 después.
El recuento de los CD4 aumentó en forma significativa de 827 ± 54 hasta 996 ± 81 (p = 0.02).
El número de los CD8 disminuyó de 815 ± 50 hasta 690 ± 70 pero sin llegar a la significancia estadística (p = 0.1).
La relación CD4/CD8 aumentó en forma significativa de 1.0 ± 0.07 hasta 1.3 ± 0.1 (p < 0.001) .
Tabla 1, Gráficas 1, 2, 3.
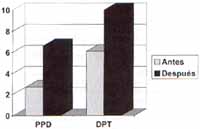
Gráfica 1. La respuesta cutánea antes y después de la gh.
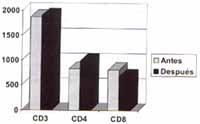
Gráfica 2. El recuento de cd3, cd4 y cd8 antes y después de la gh.
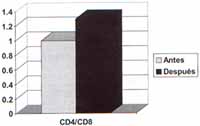
Gráfica 3. La relación cd4/cd8 antes y después de la gh.
Discusión y Conclusiones
La hormona de crecimiento es conocida por sus características anabólicas y mitóticas. Su efecto sobre los procesos catabólicos han sido bien estudiados y demostrados en trabajos nuestros anteriores (11, 12).
En este trabajo hemos querido demostrar su efecto sobre el sistema inmune desde el punto de vista cuantitativo y cualitativo. La respuesta cutánea obtenida nos muestra la mejoría importante en la actividad enzimática de los linfocitos después de la aplicación de la GH .
Aunque no hubo cambios significativos en el recuento total CD3 pero los cambios diferenciales han sido significativos, especialmente el aumento en los CD4 y el aumento en la relación CD4/CD8 que nos muestra una mejoría en la respuesta inmunitaria que aumenta la capacidad funcional del sistema inmune.
En conclusión nuestro trabajo nos muestra que la hormona de crecimiento humana podría ser efectiva para mejorar la respuesta inmune en los niños, esto podría ser benéfico en condiciones especiales de inmunosupresión.
Agradecimientos
Al laboraorio “SERONO DE COLOMBIA” por donación de la hormona de crecimiento y al laboratorio “QUALITAS” por la ayuda en el análisis de las muestras.
Referencias Bibliográficas
- 1. Jansson C Rosberg. Circulating non 22kDa growth hormone isoforms in healthy children of normal stature: relation to height, body mass and pubertal development. Eur J Endocr (1997) 137: 246-253.
- 2. Caroll P, Littlewood R. The effects of two doses of replacement growth hormone on the biochemical, body composition and psychological profiles of growth hormone-deficient adults. Eur J Endocr, (1997) 137: 146-153.
- 3. Wollman, Ranke M. Metabolic effects of growth hormone in child. Metabolism Vol 4 No 10. suppl 4 1995, 97-102.
- 4. Shonau E. Growth Prediction with biochemical markers and its consequences. Eur J Endocr (1997) 137: 603-604.
- 5. Dutour A, Briard N. Another viewof GH neuroregulation: lessons from the sheep. Eur J Endocr (1997) 136: 553-565.
- 6. Donath M, Gosteli M. Insulin-like growth factor-I stimulates myofibrillar genes and modulates atrial natriuretic factor mRNA in rat heart. Eur J Endocr (1997) 137: 309-315.
- 7. Rouget C, Marchand P. Comparative Study of Biosynthetic Human Griowth Hormone Immunogenicity in Growth Hormone Deficient Children. Horm Res 1991; 35: 76-81.
- 8. Blackburn A, Blum W. Interactions of insulin-like growth factor (IGF)-II and growth hormone in vivo: circulating levels of IGF-I and IGF-binding proteins in transgenic mice. Eur J Endocr (1997) 137: 701-708.
Fuentes Bibliográficas
- 9. Schonau E. Growth prediction with biochemical markers and its consequences. Eur J Endocr (1997) 137: 603-604.
- 10. Soliman A. Growth Hormone secretion and Circulating Insulion-Like Growth Factor-I (IGF-I) and IGF Binding Protein-3 Concentrations in Children with Sickle Cell Disease. Metabolism, Vol 46, No 11, 1997: 1241-1245.
- 11. Awadalla S, Pachón C, Agudelo M, Gómez R: El uso de la hormona de crecimiento como coadyuvante en el tratamiento de las quemaduras en niños: Actual Pediatr FSFB 1998 , 8 ( 2) 63-67.
- 12. Awadalla S, Cabeza N, Pachón C, Medina H, Alvarez A: Uso de la hormona de crecimiento humana como coadyuvante en el manejo de la sepsis en los niños: Actual Pediatr FSFB 2000, 10 ( 3 ): 118 121.