Tradicionalmente, los tipos de cáncer se han definido y asociado con la edad de aparición, el origen anatómico, la histología, y las características inmunohistoquímicas.
Actualmente, se emplean varias técnicas moleculares para detectar aberraciones genéticas, como la PCR, la secuenciación Sanger, la secuenciación de próxima generación (NGS), la hibridación por fluorescencia in situ (FISH), y otros (26).
La elección del método de detección utilizado depende de una variedad de factores, como el tipo de muestra (tejido, sangre, fluidos), volumen de la muestra, genes a analizar y tipo de mutaciones en el gen de interés (27). La PCR o reacción de cadena de polimerasa, por sus siglas en inglés. Es una técnica molecular de uso común para amplificar directamente segmentos específicos de ADN mediante ciclos repetidos de desnaturalización, hibridación y alargamiento.
El producto amplificado se puede utilizar posteriormente para diversas aplicaciones. La PCR alelo-específica es un método basado en tiempo real que detecta mutaciones conocidas con alta sensibilidad.
Requiere dos sondas fluorescentes, una para el alelo de tipo salvaje y otra para el alelo mutante.
Puede detectar ADN mutante incluso si el contenido de tumor en una muestra es solo del 1 a 5%. Por otro lado, y similar a su contraparte previamente mencionada, la PCR de microfluido digital (digital droplet PCR, ddPCR) se usa para detectar mutaciones conocidas. Incluida las variaciones de un solo nucleótido, pequeñas inserciones, deleciones, y reordenamientos con alta sensibilidad y especificidad.
La ddPCR
Permite un análisis más preciso y cuantitativo que la PCR convencional o en tiempo real. Su función en la detección de mutaciones en el ctADN (circulating tumor DNA) ha sido esencial en el desarrollo de la biopsia líquida, como estrategia diagnóstica y para el seguimiento. A diferencia de la PCR, la secuenciación Sanger se utilizó para detectar nuevas alteraciones.
Esta técnica utiliza un producto de PCR para detectar mutaciones nuevas o establecidas, incluida la variación de un solo nucleótido, pequeñas duplicaciones, inserciones y deleciones. Pero no detecta cambios en el número de copias. Requiere que el ADN mutante esté presente en al menos el 20 a 25% de las células de la muestra.
La lógica detrás de esta radica en replicar los productos de la PCR por medio de una polimerasa. Con el fin de determinar que nucleótido es incluido se emplean didesoxinucleótidos (ddNTP) marcados con un tinte fluorescente único. Los cuales al carecer de un grupo hidroxilo en la posición 3´del anillo de ribosa, inhiben el proceso de replicación.
De esta manera, se generan fragmentos de diferentes tamaños cuyo extremo contiene precisamente ese marcaje fluorescente. Al separar estos fragmentos de ADN por tamaño y leer el tinte fluorescente cuando cada uno pasa por un detector. Los nucleótidos se pueden leer de forma secuencial con una alta precisión, estableciendo la secuencia (27).
Debido a la complejidad del proceso, los costos y la velocidad de reacción se desarrollaron nuevas técnicas, conocidas como secuenciación de próxima generación.
Las plataformas de NGS
Permiten una secuenciación profunda y paralela masiva de cadenas de oligonucleótidos durante una sola serie de secuenciación. Necesitando menos material para el análisis, lo que es útil para los entornos tumorales donde la muestra de tejido es limitada.
Se basa en la fragmentación del ADN; sin embargo, en lugar de requerir una configuración separada para cada reacción como en la secuenciación Sanger. La NGS utiliza bibliotecas de ADN molde fijadas en una superficie que permite la amplificación por PCR paralela a gran escala con una cantidad relativamente pequeña de reactivo.
Dependiendo de la plataforma NGS, se utilizan varios mecanismos bioquímicos diferentes para determinar la secuencia del fragmento. La NGS puede detectar simultáneamente sustituciones de bases únicas, duplicaciones,inserciones, deleciones, y variaciones en el número de copias de múltiples genes en un solo ensayo.
Al considerar los resultados de los estudios actuales, es importante comprender que se puede realizar estudios del genoma completo, del exoma (la totalidad del material codificante) o genes específicos de interés en muestra tumorales.
La interpretación de estos hallazgos es un poco más compleja que las otras técnicas debido a que por la química de reacción pueden introducirse artefactos que pueden ser anómalamente interpretados como mutaciones con impacto sobre la biología tumoral.
Sobre este aspecto al igual que analizar la gran cantidad de datos involucrados en obtener secuencias de forma masiva. Se requirieron grandes avances en la bioinfomática y biología computacional.
Para la detección de rearrelos o cambios en el número de copias, el FISH es un buen método diagnóstico. Este utiliza sondas marcadas con fluorescencia unidas a secuencias de interés los cuales se van a hibridar con su región correspondiente en el genoma a indagar. En el caso de obtener aumento de las señales de fluorescencia sobre lo esperado, se podría estimar una ganancia de número de copias.
Por otro lado, las pérdidas de información se traducirían en ausencia de la señal de interés. Adicionalmente, mediante el diseño de sondas específicas como sondas de fusión o de ruptura. Se pueden identificar estos tales como el cromosoma Filadelfia (27).
Las micromatrices de ADN (DNA microarrays) o microarreglos se utilizan para identificar múltiples alteraciones conocidas, usando un chip sólido que contiene miles de cadenas simples de ADN para hibridar con la muestra de ADN del tumor.
Es importante destacar que el ADN monocatenario es sintético y puede prepararse para cualquier secuencia de ADN deseada. Por tanto, se puede crear una matriz con diferentes objetivos de interés.
La muestra de ADN se etiqueta con un tinte fluorescente y se hibrida con las hebras de ADN del chip. Se utiliza detección fluorescente para la detección y cuantificación, más un sistema operativo especializado para determinar la expresión, cantidad y secuencia de la muestra de ADN proveniente del tumor (27).
Alteraciones genómicas más frecuentes
La frecuencia media de mutaciones puntuales varía en más de tres órdenes de magnitud en los cánceres más comunes. Dentro de un tipo de tumor particular, la variación en la frecuencia mutacional es de un orden de magnitud (Figura 2). La variación en la frecuencia de las mutaciones es una función del número de divisiones de las células somáticas antes de la iniciación del tumor.
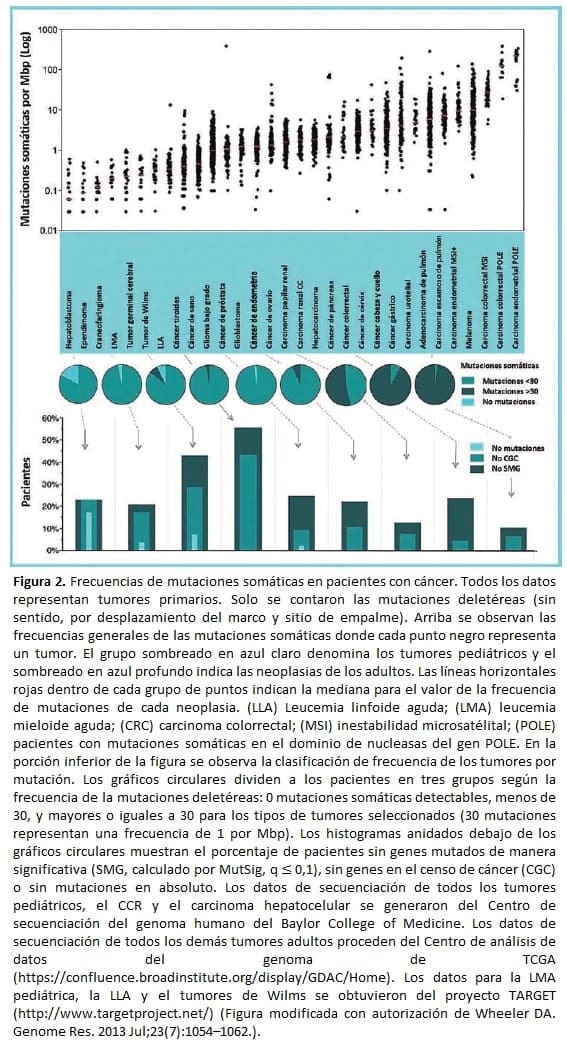
En el extremo inferior de la escala se encuentran las neoplasias pediátricas, seguidas de las leucemias agudas en adultos y de los tumores sólidos. Los tumores que superan las 10 mutaciones por Megapar de bases (Mbp) a menudo tienen deficiencias en la reparación de errores propios del apareamiento, ya sea por una mutación o silenciamiento epigenético (por ejemplo, MLH1).
Los tumores con más de 100 mutaciones por Mbp suelen tener mutaciones en la exonucleasa POLE, una de las dos enzimas de replicación del ADN (The Cancer Genome Atlas Research Network). Estos patrones pueden tener implicaciones importantes para la clínica, como ocurre para los pacientes con carcinoma colorrectal que tienen disfunción replicativa por daños en la reparación, evento que condiciona un mejor pronóstico en especial tras la exposición a la inmunoterapia.
En el otro extremo de la escala, se encuentran la mayoría de los tumores pediátricos que presentan pocas mutaciones, hallazgo que limita las posibilidades terapéuticas.
El censo inicial de los genes relacionados con el desarrollo del cáncer dio paso a COSMIC:
El Catálogo de mutaciones somáticas en el cáncer (28). En los tumores sólidos más comunes un promedio de 33 a 65 genes presenta mutaciones somáticas que modifican sus productos proteicos. Aproximadamente el 95% de estas mutaciones son sustituciones de una sola base (como C> G), mientras que el resto son deleciones o inserciones de una o pocas bases (como CTT> CT).
De las sustituciones de bases, el 91 % dan como resultado cambios sin sentido, el 7,6% dan como resultado cambios sin sentido, y el 1,7% generan alteraciones de los sitios de empalme o regiones no traducidas inmediatamente adyacentes a los codones de inicio y finalización. Información actualizada ha permitido elucidar que la mejor manera de identificar genes mutados que actúan como conductores es valorando el patrón mutacional en lugar de su frecuencia de alteración.
Los patrones de mutaciones entre los oncogenes y genes supresores de tumores bien estudiados son característicos y no aleatorios. Los oncogenes mutan de manera recurrente en las mismas posiciones de aminoácidos.
Mientras que los genes supresores de tumores mutan
A través de alteraciones que truncan proteínas en toda su longitud. Sobre la base de estos patrones de mutación en lugar de frecuencias, ha sido posible determinar cuáles de los 18.306 genes mutados que contienen un total de 404.863 alteraciones registradas en COSMIC actúan como conductores.
Para ser clasificado como un oncogén es necesario que más del 20% de las mutaciones registradas en el gen estén en posiciones recurrentes y no tengan sentido.
Por otra parte, para ser clasificado como un gen supresor de tumores, análogamente se requiere que más del 20% de las mutaciones registradas en el gen sean inactivadoras.
Esta regla 20/20 es indulgente en el sentido de que todos los genes del cáncer bien documentados superan con creces estos criterios (4,29).
El inventario más reciente de mutaciones en cáncer incluidas en COSMIC (http://www.sanger.ac.uk/genetics/ CGP/Census/) incluye más de 900.000 eventos somáticos.
Sin embargo, hasta la fecha solo se han descubierto 125 genes con mutaciones conductoras, 71 son genes supresores de tumor y 54 son oncogenes (4). Cada tipo de neoplasia tiene una colección característica de genes alterados, como lo ejemplifica el cáncer colorrectal (Figura 3).
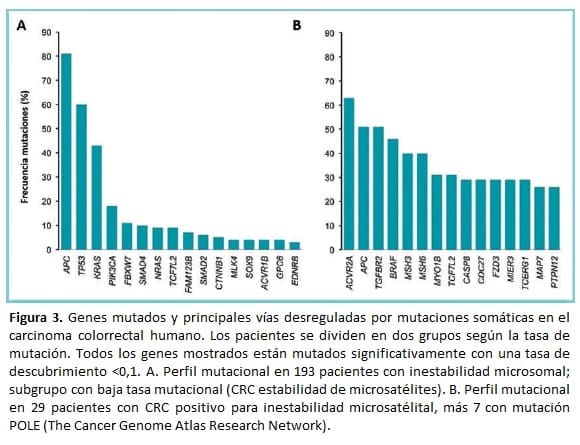
El patrón establecido desde la primera evaluación exómica del cáncer colorrectal y de seno demostró desde 2007 que un tercio de los genes están mutados en más del 20% de los tumores. De estos, un 10% tienen mayor compromiso, y el resto generan una menor carga genómica.
Los proyectos a gran escala como el TCGA y el ICGC han tenido como objetivo secuenciar más de 500 pacientes por cada tipo de tumor. Con la expectativa de recolectar una fracción considerable de los genes mutados en un rango menor al 3% (Figura 3).
Los genes alterados en menor frecuencia tienen gran importancia para la comprensión de la biología tumoral dado que pueden presentar redundancia mutacional en una vía específica de señalización.
Esta característica se hace evidente en el cáncer colorrectal donde APC es el mayor impulsor de la vía canónica WNT. Sin embargo, otros 10 genes presentan cambios deletéreos en el 1-15%, hallazgo que influye en la regulación positiva de MYC y de múltiples factores de transducción relacionados con PI3K (Figura 4).
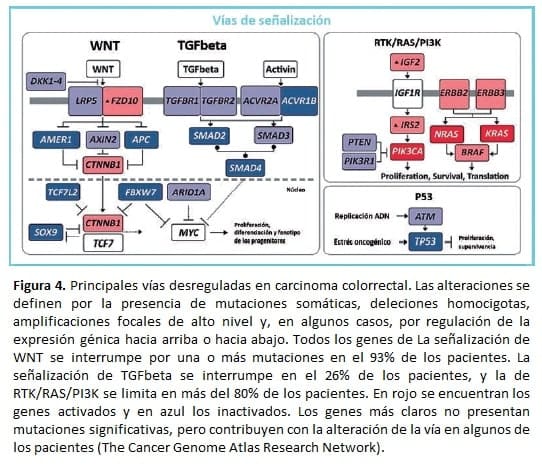
Los genes alterados con baja frecuencia revelan una complejidad adicional en relación a la heterogeneidad clonal que favorece la resistencia a medicamentos como los inhibidores de tirosin-quinasa, hallazgo común en los adenocarcinomas de pulmón EGFR (receptor para el factor de crecimiento epidérmico) positivos.
Cuando se amplía la secuenciación del ADN incluyendo análisis del número de copias, de expresión de ARN, y perfiles epigéneticos, se modifica la información basal que se obtiene.
En general, la mayoría de los perfiles mutacionales (como el que se muestra en la Figura 3) identifican entre 15 y 20 genes mutados, el análisis del número de copias agrega otros 20 genes amplificados o con deleciones focales recurrentes, y los perfiles epigenéticos y de expresión anormal refuerzan los datos sobre las mutaciones somáticas agregando usualmente algunos genes más.
Según los resultados obtenidos hasta ahora, parece probable que el repertorio de genes implicados en cualquier tipo de cáncer sea del orden de 50 a 100, en lugar de 500 a 1.000 como se creía previamente.
(Lea También: Heterogeneidad Tumoral)
Nuevas alteraciones genómicas de alta y baja frecuencia
Desde el 2004 se han encontrado una multiplicidad de alteraciones de baja frecuencia (menor del 20%) que promueven la generación y sostenibilidad de neoplasias sólidas y hematológicas. Los avances más notables proporcionaron información sobre el papel de la remodelación de la cromatina en la tumorigénesis.
La isocitrato deshidrogenasa 1 y 2 (IDH1 y 2) fueron adiciones significativas a la lista de impulsores del glioblastoma, la LMA y el colangiocarcinoma (30-32). Ambas enzimas convierten el isocitrato en α-cetoglutarato (α- KG), un cofactor de las dioxigenasas α-KG. Incluidas las ADN demetilasas de la familia TET, las histonas demetilasas de la familia KDM y muchas otras proteínas (33).
Cuando IDH1 o 2 están mutados producen 2-oxiglutarato, un análogo estructural del α-KG que actúa como potente inhibidor de enzimas dependientes de α-KG. Las metiltransferasas involucradas en la metilación del ADN y la cromatina. Estos inhibidores dan como resultado una modificación epigenética aberrante que se transfiere a la desregulación de muchas vías celulares.
La ADN demetilasa, DNMT3A
Está mutada en el 22% de los pacientes con LMA, lo que sugirió que su papel era importante para la regulación transcripcional a través de la modificación epigenética del ADN (34).
Las mutaciones en este gen son clínicamente importantes en los pacientes con LMA, ya que se asocian a reducción en la supervivencia global. Desde su descubrimiento inicial, las alteraciones en DNMT3A se han relacionado con la transformación de casi todas las neoplasias mieloides.
De manera similar, las alteraciones en el gen PBRM1 se documentaron en el 41% de los carcinomas renales de células claras, y este fue el primer miembro del complejo para remodelado de cromatina SWI/SNF que se encontró alterado en cáncer (35).
Desde entonces, las mutaciones en muchos de los otros componentes de SWI/SNF se han ido acumulando de manera constante en muestras de pacientes con cáncer de ovario, hepatocelular, gástrico y otros (36).
El gen para la proteína 1 asociada a BRCA (BAP1)
Tiene una función enzimática que desubiquitina la histona H2A y otras proteínas involucradas en la remodelación de la cromatina. Presenta mutaciones inactivantes en el 23% de los mesoteliomas (37) y en los melanomas uveales, donde el 84% de los pacientes portadores tiene alto riesgo de metástasis (38).
También se encuentra mutado en el 15% de los carcinomas renales de células claras, en los que está anticorrelacionado con las mutaciones más frecuentes de PBRM1, mencionadas anteriormente. Una mutación inactivante en BAP1 define una subclase molecular de tumores agresivos de alto grado.
En el otro extremo del perfil mutacional están los genes del cáncer que contribuyen al 10% o menos de los tumores. Quizás los más interesantes en el ámbito de la baja carga y frecuencia son aquellos relacionados con el procesamiento del ARN.
Descubiertos por primera vez en el síndrome mielodisplásico, los genes U2AF1, U2AF2, SF3B1 y SRSF2 (39), están involucrados en el reconocimiento del aceptor de empalme en la maquinaria del ARN, mutaron acumulativamente en más del 50% de los pacientes.