Análisis con FISH
El análisis FISH se llevó a cabo utilizando la sonda LSI EGFR SpectrumOrange / CEP 7 SpectrumGreen (Vysis, Abbott Laboratories) de acuerdo con las indicaciones del fabricante. Las secciones se incubaron a 56°C durante la noche, se desparafinizaron mediante lavado en CitriSolv (Fisher Scientific, Pittsburgh, PA) y se deshidrataron en etanol al 100%.
Después de la incubación en tampón de citrato sódico 2 × solución salina (2 × SSC, pH 7,0) a 75°C durante 15-25 minutos, las secciones se digirieron con proteinasa K (0,25 mg / ml en 2 × SSC, pH 7,0) a 37°C durante 15-25 minutos, se lavaron en 2 × SSC a temperatura ambiente durante 5 minutos y se deshidrataron en una serie de concentraciones crecientes de etanol (70%, 85% y 100%).
El conjunto de sondas EGFR / CEP 7 se aplicó al área seleccionada basándose en la presencia de focos tumorales en cada portaobjetos. El área de hibridación se cubrió con un cubreobjetos de vidrio y se selló con esmalte de uñas.
Los portaobjetos se incubaron a 80 ° C durante 8-10 minutos para la codesnaturalización del ADN cromosómico y de la sonda. Luego se hibridaron a 37 ° C durante 20-24 horas. Se realizaron lavados posteriores a la hibridación en urea 1,5 M y SSC 0,1 × (pH 7,0 – 7,5) a 45 ° C durante 30 minutos, y en 2 x SSC durante 2 minutos a temperatura ambiente.
Variables moleculares
Después de que las muestras se deshidrataran en etanol como se indicó anteriormente. Se aplicó 4 ‘, 6’-diamidino-2-fenilindol (DAPI) en solución salina tamponada con fosfato y glicerol (Vysis) para la contratinción de la cromatina. Los análisis de FISH se realizaron de forma independiente por dos autores que estaban cegados a las características clínicas de los pacientes y a todas las demás variables moleculares.
Para los análisis de FISH, se anotaron 60 núcleos para señales de ambas sondas de ADN usando un microscopio Olympus BX51TRF (Olympus, Tokio, Japón) equipado con un filtro de triple paso (DAPI / Verde / Naranja; Vysis) con un aumento final de 1000×. La polisomía y monosomía del cromosoma 7 se definieron como la presencia de ≥ tres señales y una señal, respectivamente, en más del 20% de las células tumorales.
El estado del gen EGFR se clasificó en seis categorías según la frecuencia de células tumorales con números de copia específicos del gen EGFR y el centrómero del cromosoma 7:
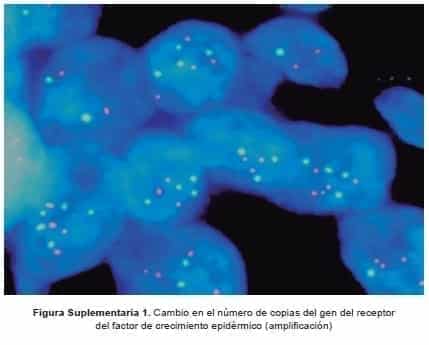
Disomía (≤ 2 copias en ≥ 90% de las células), trisomía baja (≤ 2 copias en ≥ 40% de las células, 3 copias en 10 – 40% de las células y ≥ 4 copias en <10% de las células), trisomía alta (≤ 2 copias en ≥ 40% de las células, 3 copias en ≥ 40% de las células, y ≥ 4 copias en <10% de las células), polisomía baja (≥ 4 copias en 10 – 40% de las células), polisomía alta (≥ 4 copias en ≥ 40% de las células) y amplificación génica (a: presencia de grupos de genes EGFR estrechos (≥4 puntos) en ≥10% de células tumorales b: una relación del gen EGFR al cromosoma 7 de ≥ 2, c: ≥ 15 copias de EGFR por célula en ≥ 10% de células) (Figura suplementaria 1).
 En función del estado del gen EGFR:
En función del estado del gen EGFR:
Los pacientes se clasificaron en dos grupos: 1) EGFR negativa o baja (disomía, trisomía baja, trisomía alta y polisomía baja) y 2) EGFR positiva o alta (polisomía alta y amplificación génica). Para cada preparación de FISH, se usaron células conocidas positivas y negativas como controles.
Análisis de mutación EGFR
La prueba de tejido Cobas® EGFR (qPCR) se utilizó para la detección de mutaciones. Dicha prueba está diseñada para detectar sustituciones las G719A / C / S en el exón 18, 29 deleciones en el exón 19, 5 inserciones en el exón 20, entre ellas, S768I y T790M y la sustitución L858R en el exón 21.
Además de las mutaciones detectadas en la prueba de tejido, se realizó análisis de sangre buscando la sustitución L861Q en el exón 21. Para las muestras FFPE. Se usaron 50 ng de ADN genómico para cada reacción de PCR y para las muestras de plasma. Se usaron 25 μL del eluato de ADN para cada reacción de PCR. El software del sistema Cobas® 4800 SR2 v2.0 y el software de paquete de análisis EGFR v1.0 se usaron para el análisis de resultados.
Análisis estadístico
Para fines descriptivos, las variables continuas se resumieron como medias aritméticas. Medianas y desviaciones estándar. Las variables categóricas se informaron como proporciones con intervalos de confianza del 95% (IC del 95%).
Las comparaciones se realizaron utilizando la prueba t de Student. χ2 o la prueba exacta de Fisher, se usaron para evaluar la significancia entre las variables categóricas.
Las variables de tiempo evento, obtenidas del método de Kaplan Meier. Se determinaron mediante pruebas de log rank. Para probar la asociación entre la expresión de ARNm (variables continuas) y las características clinicopatológicas (variables dicotómicas), se utilizaron las pruebas U de Kruskal Wallis y Mann-Whitney.
La significancia estadística se determinó como p≤0,05 usando una prueba a dos colas. Todos los análisis estadísticos se realizaron con SPSS versión 19.0 (SPSS, Inc., Chicago, IL, EE. UU.).

 En función del estado del gen EGFR:
En función del estado del gen EGFR: