Evaluación del Impacto Presupuestal de una Nueva Técnica Diagnóstica para la Vigilancia Epidemiológica de la Enfermedad Respiratoria Aguda en un Laboratorio de Referencia en Bogotá, Colombia
Liliana Patricia Díaz Cuevas1, Sandra L. Gómez2, Hernán A. Vargas3, Zulema Jiménez4, Juan David Rueda5
Resumen
Objetivo: Evaluar el impacto presupuestal de introducir una nueva técnica diagnóstica para la vigilancia epidemiológica en la enfermedad respiratoria aguda en un laboratorio de referencia en Bogotá, Colombia. Materiales y métodos: Estudio de impacto presupuestario desde la perspectiva del tercero pagador, para la patología de ERA con criterios de Infección respiratoria aguda grave (IRAG), con un horizonte temporal de 5 años (2013-2017), determinando los costos directos de las pruebas y su impacto en la población. Resultados: Al introducir la nueva técnica en forma progresiva hasta llegar al 75%, a los cinco años, el impacto fue un incremento del presupuesto en un 27% ($203.463.717) más que con el costo de las pruebas actuales. El análisis de sensibilidad univariado, modifi cando la variable porcentaje de introducción de la nueva prueba, permitió establecer que a un menor porcentaje de inversión de las pruebas actuales y un porcentaje mayor de introducción de la nueva prueba, el impacto en el costo del presupuesto al término de los cinco años será mayor. Conclusiones: La introducción de la nueva técnica diagnóstica hasta el 75% en el horizonte temporal de 5 años, tendrá un impacto del 27% en el presupuesto, comparado con la utilización de las pruebas actuales. La ampliación del perfi l viral y el acercamiento a la realidad, permitirá formular nuevas políticas públicas en el tratamiento y pronóstico de la ERA en la población de Bogotá.
Palabras clave: Enfermedad del tracto respiratorio, prueba diagnóstica, control presupuestal.
Budget Impact Assessment of a New Diagnostic Technique for Surveillance of Acute Respiratory Desease in a Laboratory Reference in Bogota-Colombia
Abstract
Objective: To evaluate the budget impact of the introduction of a new diagnostic test for epidemiological surveillance for acute respiratory illness in a reference laboratory in Bogota, Colombia. Materials and methods: Budget impact, from the perspective of third-party payer for pathology ARI, with criteria for severe acute infection (SARI) with a time horizon of fi ve years (2013-2017), determining the direct costs of testing and its impact in the population. Results: The introduction of the new test progressively to reach 75% at fi ve years, the impact will be an increase of $203.463.717 budget (27%) more than the cost of current evidence. Univariate sensitivity analysis, changing the variable percentage of introduction of new evidence, established that a smaller percentage of reversal of current evidence and a higher percentage of introductions of the new test, the impact on the cost of the budget at the end fi ve years will be higher. Conclusions: The introduction of new diagnostic technique up to 75% in the time horizon of 5 years will have an impact of 27% in the budget compared to the use of current evidence. Extending the viral profi le and be closer to reality, will reshape public policies in the treatment and prognosis of the ARI in the population of Bogota.
Key words: Respiratory Tract Infections, diagnostic test, budget impact.
Introducción
La Enfermedad Respiratoria Aguda (ERA) es una de las patologías más prevalentes en la población a nivel mundial, y se defi ne como un conjunto de síntomas asociados con afecciones del aparato respiratorio, por un tiempo menor a quince días (1). En Colombia, la prevalencia en el año 2010 fue de 9% en menores de 5 años, según los datos obtenidos por la Organización Panamericana de la Salud (OPS) sobre la situación de salud de las Américas en el año 2012. La ERA provoca alta mortalidad asociada a neumonía, principalmente en niños, con aproximadamente cuatro millones anuales a nivel mundial por esta causa, de los cuales 1,8 millones sucede en menores de 5 años (2,4).
En Colombia, la tasa de mortalidad registrada en menores de 5 años para el año 2011 fue 15,94 por cada 100.000 habitantes (3). Se evidencia que por grupos de edad, estos menores registran en países en vías de desarrollo por lo menos 0,28 episodios de neumonía por año, para un total de 150,7 millones de casos nuevos en el mundo y de ellos, entre el 7 y el 13% requieren hospitalización (5). En su etiología, pueden estar involucradas bacterias o virus, dándose mayor importancia a estos últimos desde la pandemia del virus Infl uenza A H1N1/09, y muchos de ellos determinantes en la severidad de la infección. Se ha observado la presencia de nuevos virus llamados emergentes tales como rinovirus, metapneumovirus, coronavirus, bocavirus humanos, entre otros, que se asocian en gran medida a otros virus causantes de la infección (2).
Para el Ministerio de Protección Social de Colombia, en su Plan Decenal de Salud 2012-2021, en la dimensión de vida saludable y enfermedades transmisibles, uno de sus objetivos consiste en reducir la carga de enfermedad por vía aérea y de contacto directo, buscando como meta, la disminución en la mortalidad por esta patología a 8,9 casos por 100.000 menores de 5 años (6).
Siendo una patología de interés en salud pública, se han expedido políticas públicas distritales para controlar su contagio, que vinculan a todos los estamentos garantes de la salud de la población como las aseguradoras, instituciones prestadoras de servicios de salud, profesionales de la salud, entre otros, emitiendo planes de contingencia en fases pico de la enfermedad asociadas a las temporadas invernales en la ciudad, intensificando las estrategias para el manejo ambulatorio de la enfermedad, la notificación oportuna de brotes y el monitoreo constante a través de la vigilancia centinela en las instituciones (7).
El Laboratorio de Salud Pública de la Secretaría Distrital de Salud tiene participación activa en la investigación de brotes y epidemias y en otros problemas de interés en salud pública (8); colabora en la vigilancia para las enfermedades que se presentan en la población, realiza exámenes de laboratorio y de esta manera, se hace apoyo diagnóstico para la ERA con criterios de infección respiratoria aguda grave (IRAG), cuya característica principal es la severidad de la enfermedad que requiere hospitalización. También con la detección de siete virus respiratorios por la técnica de inmunofluorescencia indirecta (IFI) y la confirmación del Influenza A H1N1 por otra técnica de biología molecular llamada reacción en cadena de la polimerasa en tiempo real (RT-PCR).
La IFI, ha sido utilizada como diagnóstico de virus respiratorios en el distrito capital, debido a la rapidez del montaje de la técnica y su bajo costo, detectando los siete virus de notificación obligatoria (adenovirus, Influenza A, Influenza B, parainfluenza 1, 2, 3, virus sincitial respiratorio), evidenciándose una sensibilidad del 55,5% y especificidad del 99,2% (9), frente al cultivo celular que ha sido catalogado como el gold standard para el diagnóstico viral. De otra parte, es utilizada la técnica de tiempo real de reacción en cadena de polimerasa para el virus Influenza A H1N1, desde la pandemia del año 2009 ocurrida en Bogotá y debido a su alta sensibilidad (85,7%) y especificidad (94,9%) se incluyó dentro del panel diagnóstico actual (10).
Sin embargo, nuevos virus respiratorios que no son detectados por las técnicas utilizadas actualmente en Bogotá, se han encontrado en otros países como agentes etiológicos de ERA, tales como rinovirus, metapneumovirus, bocavirus, coronavirus, causantes tanto de infecciones únicas como en asocio con otros virus ya identificados en la vigilancia epidemiológica. Se han observado como causantes de bronquiolitis y neumonías severas, principalmente en niños y sus síntomas son similares a los provocados por el virus sincitial respiratorio cuya prevalencia es alta en la población infantil (2,11-13). Estos virus que están circulando en la comunidad incrementan el número de hospitalizaciones e infecciones de origen nosocomial y episodios severos causados por nuevos virus respiratorios (14).
El Laboratorio de Salud Pública durante el año 2013 desarrolló una investigación con una nueva técnica de biología molecular, Clart pneumovir DNA array, que amplía la detección del perfil viral a 19 virus respiratorios, incluyendo los siete virus ya notificados por la prueba IFI, Influenza A genérico y H1N1/09, H3N2 por la prueba RT-PCR, además de los virus emergentes rinovirus, metapneumovirus genérico y sus subtipos A y B, bocavirus, virus sincitial respiratorio A y B, coronavirus, enterovirus, parainfluenza 4 e influenza C; se encuentra avalada por el instituto nacional que regula medicamentos y nuevas tecnologías en salud en el país (INVIMA). El estudio del perfil viral con esta prueba se realizó con muestras que llegaron por la vigilancia centinela al Laboratorio de Salud Pública, recolectadas en el año 2012, permitiendo aumentar y acercar a la realidad la circulación viral y compararla con los resultados de las otras técnicas aplicadas.
La morbilidad asociada a la ERA demanda costos directos generados por la utilización de recursos sanitarios y no sanitarios y su variación depende de la severidad de la infección, con ingreso a unidad de cuidados intensivos, hospitalizaciones prolongadas o secuelas que ocasionan reingresos hospitalarios frecuentes. Se estima además que en las infecciones nosocomiales muchas veces asociada a virus, los costos pueden elevarse en el 30,5%. (15)
El impacto en los costos de la nueva técnica Clart pneumovir DNA array no ha sido evaluado en un laboratorio de referencia, tal como lo es un Laboratorio de Salud Pública del nivel central (16).
Es importante determinar los costos asociados a esta enfermedad con la incursión de nuevas metodologías diagnósticas que permitan la detección de nuevos microorganismos que participan en la ERA, y en este caso específico de la IRAG; por cuanto pueden aumentar la posibilidad de mejorar el tratamiento y pronóstico en la población de Bogotá, e impactar en la reformulación de políticas en salud pública en Bogotá y en el país.
Materiales y Métodos
1. Alternativas a analizar
Las alternativas incluidas en el modelo fueron las pruebas actualmente utilizadas para la detección de siete virus respiratorios por IFI, la técnica de RT-PCR para la detección de Influenza A con sus subtipos H1N1 y H3N2 comparadas con la técnica de Clart pneumovir DNA array, a las muestras obtenidas de los hospitales de Bogotá a través de la vigilancia centinela para ERA con criterios de IRAG, en el año 2012.
2. Escenarios que se comparan
El modelo compara dos escenarios:
Escenario 1: sin Clart pneumovir DNA array, que equivale a continuar con el manejo estándar con las alternativas actualmente disponibles (IFI y RT-PCR).
Escenario 2: con Clart pneumovir DNA array con introducción en forma progresiva para estimar el impacto de la inclusión de esta prueba en la confirmación diagnóstica para ERA con criterios de IRAG.
3. Perspectiva del estudio
La perspectiva adoptada fue la del tercero pagador, en este caso la Secretaría Distrital de Salud, y el Laboratorio de Salud Pública como laboratorio de referencia.
4. Horizonte temporal
Aunque se hacen análisis año por año, se escogió el horizonte temporal de cinco años, (2013 a 2017), por considerar que este lapso suele ser el de mayor relevancia para el pagador. Además se espera que en el año 2017 alcance su pico de crecimiento en participación como parte del diagnóstico de la ERA con criterios de IRAG.
5. Población
El modelo parte de los estimados de prevalencia del 9% para ERA en Colombia durante el año 2010, con base en los datos emitidos por la Organización Panamericana de la Salud del año 2012 y sobre las proyecciones poblacionales de cinco años. Se obtuvo además la prevalencia de IRAG del boletín ERA de la Secretaría Distrital de Salud No.70 del año 2012, siendo esta de 0,53% (17), población a la que se le realizan las pruebas de detección viral.
Sobre este número de pacientes se asumió la introducción progresiva del método diagnóstico de Clart pneumovir DNA array hasta en un 75% de la población objetivo en el curso de cinco años.
6. Descuento y ajuste de precios
Por considerar el análisis de cada año por separado, los análisis de impacto presupuestario, en este caso, no requirieron tasas de descuento (18). El modelo asume que los costos, en general, se mantendrán constantes durante el horizonte temporal; para la conversión a dólares estadounidenses, se empleó la tasa de cambio oficial para el año 2002: ($2.864,79 pesos colombianos).
7. Costos
Teniendo en cuenta la perspectiva adoptada del tercero pagador, la técnica utilizada para la estimación de los costos de la ERA fue la de microcostos, usando la información para hospitalizaciones de neumonía presuntamente viral. Los pacientes analizados eran menores de dos años. Se revisó el costo de facturación de cuatro hospitales de Colombia del tercer nivel de atención entre los años 2001 y 2003 (19). Los costos directos aparecen desagregados en: estancia hospitalaria, medicamentos que incluyeron antibióticos y otros medicamentos; pruebas de laboratorio clínico, radiología y otros exámenes, y servicios especiales. El valor total de la atención en costos medios directos fue de US$411,30 (año 2002). No fueron considerados los costos indirectos ni los intangibles.
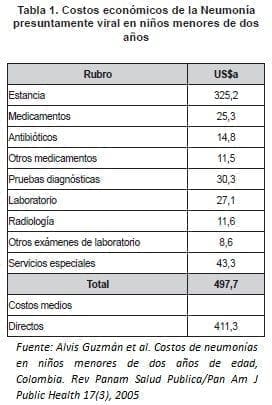
Para los costos de las pruebas a comparar se tomaron los valores determinados en el Laboratorio de Salud Pública de la Secretaría Distrital de Salud para el año 2012. Los costos directos de las técnicas incluyeron los costos de los insumos por cada prueba (kit de la casa comercial y elementos accesorios necesarios para el procesamiento) y los honorarios de los profesionales responsables y de los técnicos auxiliares, teniendo en cuenta el tiempo requerido específicamente para la realización de cada una de las pruebas (tabla 2).

1 Médico, MSc en Economía de la Salud y gestión del medicamento. Grupo Laboratorio de Salud Pública, Subsecreataría de Salud Pública, Secretaría Distrital de Salud. 2 Microbiología, MSc en Microbiología. Grupo Laboratorio de Salud Pública, Subsecreataría de Salud Pública, Secretaría Distrital de Salud. 3 Biólogo, PhD en Salud Pública.Grupo Laboratorio de Salud Pública, Subsecreataría de Salud Pública, Secretaría Distrital de Salud. 4 Nutricionista, MSc en Salud Pública. Grupo Laboratorio de Salud Pública, Subsecreataría de Salud Pública, Secretaría Distrital de Salud. 5 Candidato a PhD en Investigación de Servicios de Salud Farmacéuticos, Universidad de Maryland, Baltimore. Grupo Laboratorio de Salud Pública, Subsecreataría de Salud Pública, Secretaría Distrital de Salud.
8. Programa
Para modelar el impacto presupuestario se usó el programa Excel 2007, dado que es un programa de uso común, lo que permite a los usuarios potenciales modificar los supuestos o los valores asignados a las variables tanto clínicas como de costos. Así mismo, el programa permite visualizar y en algunos casos modificar las fórmulas empleadas en el modelo.
9. Supuestos del modelo
Se utilizó la prevalencia de pacientes con IRAG (0,53%) como población estudio a quienes se les aplica la prueba para detección viral, según lo establecido en la vigilancia epidemiológica para la ERA con criterios de IRAG. Se utilizó esta prevalencia debido a que este fue el parámetro encontrado para la población a estudio. Se asume un crecimiento progresivo del total de pacientes, desde 3.668 muestras en 2013 hasta 3.862 en 2017. Las tasas de participación que se asumen en el modelo, para pacientes nuevos y existentes, se muestran en la tabla 3.
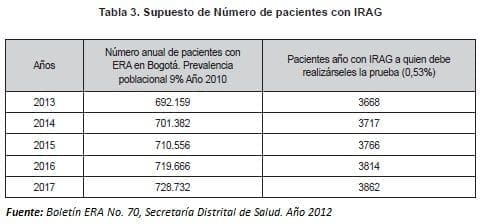
10. Definiciones empleadas en el modelo
Infección Respiratoria Aguda Grave (IRAG)
Definida como una infección que afecta el sistema respiratorio con origen viral o bacteriano cuyo manejo es exclusivamente de carácter hospitalario. Encontrando como agentes etiológicos frecuentes el virus sincitial respiratorio, parainfluenza y sus subtipos, influenza, adenovirus, Streptococcus pneumonie, Haemophilus influenza, Mycoplasma spp, Chlamydia spp y Staphylococcus aureus spp.).
Los virus generalmente se caracterizan por ser estacionales y asociados a los periodos de lluvia. La clínica está dada por cuadro menor a 14 días, asociado a fiebre mayor a 38°C, dificultad respiratoria, tos, síntomas generales como escalofríos y sudoración y cuando aumenta la severidad el compromiso sistémico puede estar dado por convulsiones y falla ventilatoria (20). El tratamiento, de acuerdo con la severidad de la infección, incluye medidas de hidratación oral, oxígeno por cánula nasal, medicamentos para el control de la fiebre y monitorización de los signos vitales. En caso de dificultad respiratoria, fiebre persistente, taquicardia, o alteraciones clínicas y paraclínicas que indiquen sepsis, se debe realizar vigilancia estricta; con sospecha de influenza A H1N1 se inicia además tratamiento con oseltamivir. En progresión rápida de la enfermedad con deterioro sistémico se debe realizar cobertura con antibióticos e intensificar la vigilancia ante cualquier respuesta negativa al tratamiento (21).
Neumonía viral
Es un tipo de infección respiratoria que compromete los pulmones, en este caso la causa con virus, siendo el más frecuente el Virus Sincitial Respiratorio en menores de edad (21%) y bacterianas en pacientes mayores. Son las muestras de secreciones las que pueden determinar su causa. Los agentes virales pueden causar bronquitis, bronquiolitis y neumonías. Generalmente presenta un cuadro previo de síntomas gripales y progresivamente tos y dificultad respiratoria. Otro virus causante de necrosis del tejido pulmonar es el Adenovirus, que causa secuelas de bronquiolitis. (22)
Resultados
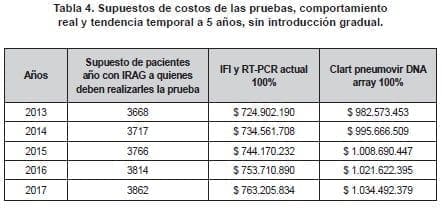
Los supuestos en los costos de las pruebas IFI y RT-PCR y de Clart pneumovir DNA array se soportan en el comportamiento real y en la tendencia temporal de cinco años.
Los costos netos anuales (2013-2017) fueron:
Escenario 1 (sin Clart pneumovir DNA array): estuvieron entre $724.902.190 y $763.205.834 para los años 2013 y 2017 respectivamente, con un incremento de $38.303.644 (5%).
Escenario 2 (con Clart pneumovir DNA array): estuvieron entre $ 982.573.453 y $1.034.492.379 para los años 2013 y 2017, respectivamente, con un incremento de $51.918.926, correspondiendo también al 5%. (tabla 4).
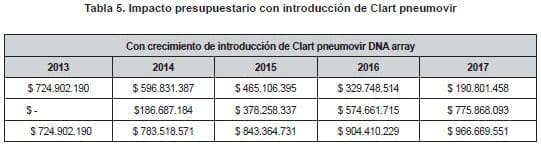
El costo anual de las pruebas de detección viral para el año 2013 con la introducción de la nueva prueba diagnóstica fue de $724.902.190 y para el año 2017 el costo neto es de $966.669.551, es decir 25 % de incremento en el horizonte temporal, cuando la introducción de la prueba fue hasta el 75% del presupuesto. (tabla 5).
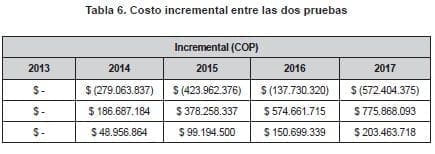
El costo incremental entre los dos escenarios fue:
- para el año 1 de $0,
- para el año 2 de $48.956.864;
- para el año 3 de $99.194.500;
- para el año 4 de $150.699.339 y
- para el año 5 de $203.463.718, cuando la introducción de la nueva prueba fue del 75%.
Los resultados del impacto presupuestario por paciente por año (2013 – 2017) fueron:
- $0 para el año 2013
- $13.171 para el año 2014
- $26.339,5 para el año 2015
- $39.512 para el año 2016 y
- $53.683,5 para el año 2017
1. Análisis de sensibilidad
El análisis de sensibilidad univariante fue realizado con el fin de ver el comportamiento de las variables y la incertidumbre sobre el análisis de impacto presupuestario. Las variables incluidas en el análisis fueron: a) el número de pacientes con IRAG a quienes se les debe aplicar las pruebas de detección viral y b) el porcentaje de variación de la introducción de la nueva prueba en forma incremental por año.
Se modificó la variable pacientes/año con IRAG, con un incremento entre 0,4 % y 1 % de prevalencia (tabla 7).
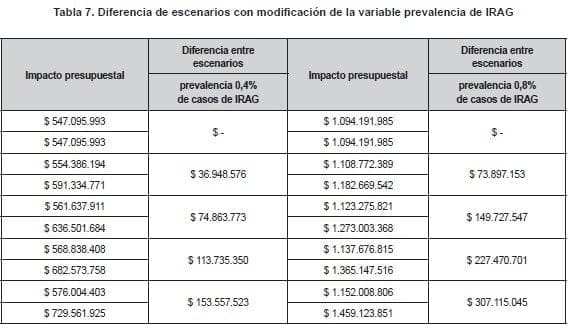
La modificación de la variable prevalencia de IRAG evidencia que con una prevalencia menor (0,4%), la diferencia entre los dos escenarios sería: $0 para el año uno, $36.948.576 para el año dos, $74.863.773 para el año tres, $113.735.350 para el año cuatro y $153.557.523 para el año cinco.
De otra parte, al incrementar la prevalencia de IRAG en el 0,8%, la diferencia entre los dos escenarios será de $0 para el año uno, $73.897.153 para el año dos; $149.727.547 para el año tres; $227.470.701 para el año cuatro y $307.115.045 para el año cinco (tabla 7).
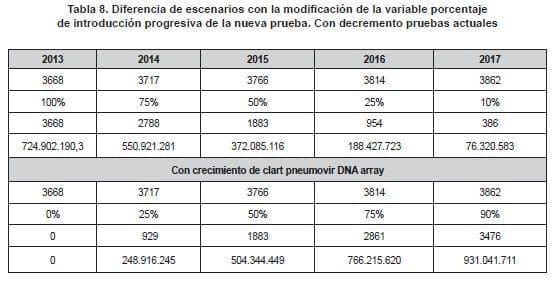
El análisis de sensibilidad, realizado con la variable porcentaje de introducción progresiva de Clart pneumovir DNA array, determinó que existe una diferencia de $282.460.104 entre el año uno utilizando solamente las pruebas actuales y el año cinco con la introducción de la nueva prueba en el 90% (tabla 8).
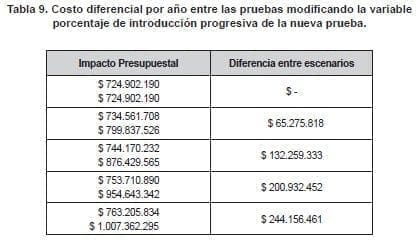
Por último, en el análisis de sensibilidad –con la modificación de la variable porcentaje de introducción de la nueva prueba con el horizonte temporal de cinco años– se observa que el costo diferencial para el primer año será de $0, para el año dos de $62.275.818; año tres $132.259.333; año cuatro $200.932.452 y año cinco $244.156.461 (tabla 9).
Discusión
La detección de un mayor perfil de circulación viral permite establecer estrategias de prevención frente a la estacionalidad de los virus, debido a que su presentación está relacionada con las temporadas de lluvias. De otra parte, la severidad de la infección puede ser atribuida a las coinfecciones virales que actualmente se desconocen por la baja sensibilidad de las pruebas actuales de diagnóstico, como también el pronóstico y reincidencia de la enfermedad respiratoria debido a las secuelas que los virus pueden dejar en el árbol respiratorio. Esto lleva a requerir la necesidad de introducir nuevas pruebas que permitan acercar a la realidad la ERA y su complicación con IRAG.
Aunque las políticas emitidas por el gobierno central han intensificado las medidas frente a la respuesta para los cuadros de ERA, con el fin de disminuir la mortalidad de esta patología de alta prevalencia en Bogotá y con carácter de notificación obligatoria, no han tenido en cuenta la presencia de nuevos virus causantes de la ERA, como son los llamados virus emergentes y que fueron determinados en el Laboratorio de Salud Pública de la Secretaría Distrital de Salud por técnicas diagnósticas de mayor complejidad, además de implicar un mayor costo.
En este estudio, la introducción de la nueva tecnología de detección viral Clart pneumovir DNA array, progresiva hasta el año 2017, con un límite del 75% de la totalidad de los pacientes con IRAG, y la realización de las pruebas actuales al 25% de los pacientes, permitió establecer que el mayor costo generado fue de $203.463.718 como diferencia entre continuar con las pruebas actuales y la introducción progresiva de la prueba.
La Secretaría Distrital de Salud, como tercero pagador, realiza presupuestos anuales para los programas en salud que impactan la población, por lo que el análisis de introducción progresiva de la nueva prueba es determinante para tomar decisiones frente al manejo de la patología de ERA, en este caso específico.
Dada la importancia de la vigilancia epidemiológica del perfil viral presente en la población con ERA, se considera necesario que el sistema de salud introduzca la prueba Clart pneumovir DNA array como parte de las estrategias de diagnóstico y de esta forma establecer las prevalencias virales reales que impactarían de forma importante el manejo de los pacientes con IRAG, previniendo las complicaciones de los cuadros hospitalarios, con disminución de costos al sistema salud.
El modelo aplicado en este estudio, con la variable de prevalencia de IRAG como la principal, permitió aproximar de manera simple el impacto en el presupuesto de una nueva prueba diagnóstica.
El análisis de sensibilidad univariado permitió establecer el comportamiento de los costos con la variación del número de pruebas y de los porcentajes de introducción progresiva de la nueva prueba.
Estudio posteriores con la introducción de nuevas variables como grupos de edad, el cual no se tuvo en cuenta en este estudio, podrían mejorar la estrategia de aplicación de la prueba, con un mayor acercamiento en el impacto.
Conclusiones
En la ciudad de Bogotá no se conocía el impacto en el costo de la utilización de nuevas pruebas diagnósticas para la identificación de nuevos virus causantes de ERA, en un laboratorio de referencia como lo es el Laboratorio de Salud Pública.
Este estudio permitió determinar que para mejorar las estrategias de diagnóstico y tratamiento de esta enfermedad de alta prevalencia para la población, es muy factible establecer la posibilidad de financiación por un tercero pagador y que se debe considerar la medición del impacto en el presupuesto de nuevas pruebas diagnósticas en todo el país.
Referencias
1. Valero N, Larrea Y, Arocha F, Gotera J, Mavarez A, Bermudez J, et al. Etiología viral de las infecciones respiratorias agudas. Invest Clin. 2009;50(3):359 – 68.
2. Ruuskanen O, Lahti E, Jennings LC, Murdoch DR. Viral pneumonia. Lancet. 2011; 377(9773):1264-75.
3. Organización Panamericana de la Salud. Análisis de la Situación en Salud. Colombia, 2013. Dispo-nible en http: //www.minsalud.gov.co/sites/rid/Lists/ BibliotecaDigital/RIDE /VS/ED/ PSP/ ASIS24022014. Consultado: 20 de junio de 2014.
4. Organización Mundial de la Salud. The global burden of disease: 2004 update 2008. Disponible en http://www.who.int/healthinfo/global_burden_disease. Consultado: 18 de junio de 2014.
5. Grisales V, Castaño J, Paredes E, Ramírez J, Sanint, Toro I, y cols. Prevalencia de enfermedades respiratorias agudas en menores de 5 años hospitalizados en las clínicas de una entidad de primer nivel, Manizales, Años 2004-2006. Archivos de Medicina (Col) 2009. Disponible en http: //www.redalyc.org/articulo. oa Consultado: 18 de Junio de 2014.
6. Ministerio de Salud y Protección Social. Plan Decenal de Salud Pública 2012-2021. Disponible en: http:// www.minsalud.gov.co/Documentos y Publicaciones/ Plan Decenal Consultado: 15 de junio de 2014.
7. Bogotá. Secretaría Distrital de Salud. Circular informativa 026, 16 Septiembre de 2011 acerca de “Acciones ante el pico de Enfermedad Respiratoria Aguda en el Distrito Capital, mediante la cual se reactiva la alerta en la comunidad, las Entidades Administradoras de Planes de Beneficios, instituciones
8.
9. de salud, otros actores y sectores”. Disponible en hptt://www.saludcapital.gov.co/Documentos. Con-sultado: 17 de junio de 2014
10. 8. Bogotá. Secretaría Distrital de Salud. Laboratorio de Salud Pública. Disponible en: hptt://www.saludcapital. gov.co/DSP/páginas/Laboratorio de Salud Pública Consultado: 16 de junio de 2014.
11. 9. Artiles-Campelo F, Pérez-González M, Caballero- Hidalgo A, Pena-López M. Diagnóstico Etiológico de las Infecciones Respiratorias Agudas de Origen Vírico en un Hospital Pediátrico de Gran Canaria. Enferm Infecc Microbiol Clin 2006;24(9):556-61.
12. 10. Pierro A, Gaibani P, Rossini G, Landini M, Sambri V. Clinical application of a molecular method based on Real Time RT-PCR for detection of influenza A(H1N1) v virus. New Microbiol 2013;36(4):405-8.
13. 11. Panda S, Mohakud N, Peña L, Kumar S. Human Metapneumovirus: Review of an Important Respiratory Pathogen. Int J Infect Dis. 25(2014)45–52. Disponible en: http://dx.doi.org. Consultado: 16 de junio de 2014
14. 12. Zhang D, et al. Epidemiology characteristics of respiratory viruses found in children and adults with respiratory tract infections in southern China. Int J Infect Dis (2014). Disponible en: http://dx.doi.org. Consultado: 16 de junio de 2014
15. 13. Gardner and MacIntyre. Unanswered questions about the Middle East respiratory syndrome coronavirus (MERS-CoV) BMC Research Notes 2014, 7:358. Disponible en: http://www.biomedcentral.com. Consultado: 17 de junio de 2014.
16. 14. De-Paris F et al. Viral epidemiology of respiratory infections among children at a tertiary hospital in Southern Brazil. Rev. Soc. Bras. Med. Trop. vol.47 No.2 Uberaba Mar./Apr. 2014. Disponible en: http:// dx.doi.org/ Consultado: 17 de Junio de 2014.
15. Jacobs P, Lier D, Gooch K, Buesch K, Lorimer M, Mitchell I. A Model of the Costs of Community and
Nosocomial Pediatric Respiratory Syncytial Virus Infections in Canadian Hospitals. Can J Infect Dis Med Microbiol. 2013 Spring;24(1):22-6.
16. Mahony J, Blackhouse G, Babwah J, Smieja M, Buracond S, Chong S, et al. Cost Analysis of Multiplex PCR Testing for Diagnosing Respiratory Virus Infections. J. Clin. Microbiol. 2009, Vol. 47, No. 9 p. 2812–2817.
17. Bogotá, Secretaría Distrital de Salud. Boletín ERA No. 70. 2012
18. Mauskopf JA, Sullivan SD, Annemans L, Caro J, Mullins CD, Nuijten M et al. Principles of Good Practice for Budget Impact Analysis. Value Health 2007; 10(5):336-347.
19. Alvis Guzmán N, de la Hoz Restrepo F, Higuera AB, Pastor D, Di Fabio JL. Costos Económicos de las Neumonías en Niños Menores de 2 Años de Edad, en Colombia. Rev Panam Salud Publi-ca.2005;17(3):178–83.
20. Ministerio de Salud y Protección Social. Protocolo de Vigilancia de Infección respiratoria aguda. Dis-ponible en hptt://minsalud.gov.co/documentos y publicaciones/PROTOCOLO ESI-IRAG. Consultado: 25 de Junio de 2014.
21. Ministerio de Protección Social. Guías de estudio y manejo de casos y sus contactos para enfermedad similar a influenza, incluyendo el diagnóstico, manejo clínico y terapéutico. 2009. Disponible en: hptt://portal. colsanitas.com. Consultado: 25 de Junio de 2014.
22. Irastorza I, Landa J, Gonzalez E. Neumonías, Etiología y Diagnóstico. An. Pediatr Contin 003:1(1):1-8
Recibido: diciembre 15, 2015
Aprobado: febrero 16, 2016
Correspondencia:
Liliana Patricia Díaz Cuevas,
lpdiaz@saludcapital.gov.co