Acciones de los andrógenos
Estas se mencionan en el capítulo sobre fisiología del testículo, pero podemos recordar que sus efectos (básicamente de la DHEA), son anabólicos y masculinizantes, aunque en un grado más débil que el producido por la testosterona. Un 17-cetosteroide suprarrenal, la etiocolanolona, no tiene efecto androgènico pero si es una causa rara de fiebre, por su efecto pirogènico.
En los últimos años, la DHEA-S ha cobrado importancia debido a su relación con la producción de óxido nítrico. Los bajos niveles de esta hormona en la vejez están relacionados con la enfermedad cardiovascular y su suplementaciòn reduce la incidencia de aterosclerosis. La DHEA al parecer regula la actividad de las sintasas constitutivas de óxido nítrico, bien directamente o como pro-hormona formadora de estrógenos, que a su vez regulan las sintasas.
De todas maneras el consumo popular de la DHEA como sustancia contra el envejecimiento, ha aumentado en forma notoria en virtud de estos descubrimientos científicos.
Patología suprarrenal
El hipercortisolismo se ha denominado Enfermedad de Cushing, cuando su causa es una hiperproducciòn de ACTH por parte de un pequeño adenoma central hipofisiario, constituido por células anteriormente denominadas basòfilas; esta enfermedad constituye el 60% de los casos y tiene un tratamiento neuroquirùrgico.
Los adenomas funcionantes suprarrenales unilaterales son otro 30% y requieren la extirpación de la glándula afectada, generalmente por lumbotomìa. Los demás casos son carcinomas suprarrenales, que requieren tratamiento quimioteràpico adicional, y que se caracterizan –cuando son en mujeres- por marcada masculinización.
Existen los casos de producción ectòpica de corticotropina, que frecuentemente se origina en cánceres pulmonares, y que cursan con marcada hipokalemia. Además de estos casos donde la aparición es espontánea, existen los más comunes que se observan en los pacientes bajo terapia crónica de corticoides.
Los casos de Cushing presentan pérdida de masa muscular, hipertensión, hiperandrogenismo en mujeres (acné, hirsutismo, amenorrea), distribución centrípeta de grasa corporal que incluye el “morro de búfalo”, poliglobulia, hipokalemia, diabetes y con el tiempo, osteoporosis.
La insuficiencia suprarrenal crónica se denomina Enfermedad de Addison, y es causada más frecuentemente por problemas autoinmunes (donde puede hacer parte de un síndrome poliglandular autoinmune) o por infecciones del tipo tuberculosis.
(Lea También:Fisiología de la Médula Suprarrenal)
Terapia Glucocorticoide
Cuando se sospecha esta última patología, la terapia glucocorticoide (y mineralocorticoide) debe acompañarse de tratamiento antituberculoso. Los síntomas consisten en marcada debilidad, letargo, diarrea, hipotensión (que puede llevar a shock o a síncopes), microcardia, hiperkalemia y pigmentación característica de la piel.
Otra patología suprarrenal que se observa particularmente en niños (en su variedad congénita) es la hiperplasia suprarrenal, la que es debida a diferentes deficiencias de las enzimas que intervienen en la esteroidogènesis.
La deficiencia más común es la deficiencia parcial de CYP 21 A2, que impide la 21 hidroxilaciòn que da lugar al cortisol y acumula su precursor 17- hidroxi-progesterona, compuesto que no suprime la secreción de ACTH, lo que lleva a estimulación crónica de la corteza y a hiperplasia suprarrenal, con marcada producción de andrógenos.
Esto causa hipertrofia clitoridiana y progresiva virilización en niñas, y a macrogenitosomìa precoz en niños. La variedad que cursa con bloqueo enzimático completo produce una deficiencia mineralocorticoide que lleva a la muerte por deshidratación, sino se detecta y corrige prontamente el problema.
Otras deficiencias cursan con virilización e hipertensión, o pueden ser incompatibles con la vida, según el caso, y lo inicial del bloqueo en la síntesis de los corticoides. Como esta enfermedad es familiar, es posible detectarla (y tratarla) “in utero”.
Mineralocorticoides
En cuanto a los mineralocorticoides, el síndrome menos raro es la Enfermedad de Conn, donde hay hipertensión con hipocalemia, y a veces, parálisis muscular. Hay una nueva serie de síndromes clínicos como el de Exceso Aparente de Mineralocorticoides (AME), causado por una mutación del gen 17-B-HSD-tipo 2; el Pseudohiperaldosteronismo (Incluye el Síndrome de Liddle y es autosòmico recesivo; la hipertensión Juvenil, que cursa con hipokalemia, hipoaldosteronismo e hiporreninemia.
El Pseudohipoaldosteronismo tipo I causado por una mutación con pérdida de función del receptor mineralocorticoide. Finalmente una clase de hipertensión gravìdica por sensibilidad a la progesterona, en la que existe una mutación del gen del receptor mineralocorticoide, con sensibilidad a la sal y se da en homocigotos con alelos A7/A7.
Terapéutica
Los corticoides pueden usarse como terapia de suplencia en la insuficiencia suprarrenal primaria y secundaria, como terapia supresiva en la hiperplasia suprarrenal congénita, por su efecto antialérgico en reacciones de este tipo, por su efecto inmunosupresor en diferentes tipos de cáncer y otras patologías como el síndrome nefrótico, y por su efecto antiinflamatorio en artritis y otras inflamaciones crónicas, de tipo sistémico o por acción local en piel y órganos de los sentidos.
También se utilizan en algunos casos de shock y para obtener la maduración pulmonar en neonatos pretérmino. Una patología muy común, hoy reconocida como inflamatoria, y que se beneficia enormemente de los corticoides –particularmente los inhalados- es el asma bronquial. El mineralocorticoide 9-alfa-fluoro- hidrocortisona se usa en la suplencia de la Enfermedad de Addison.
Nota histórica
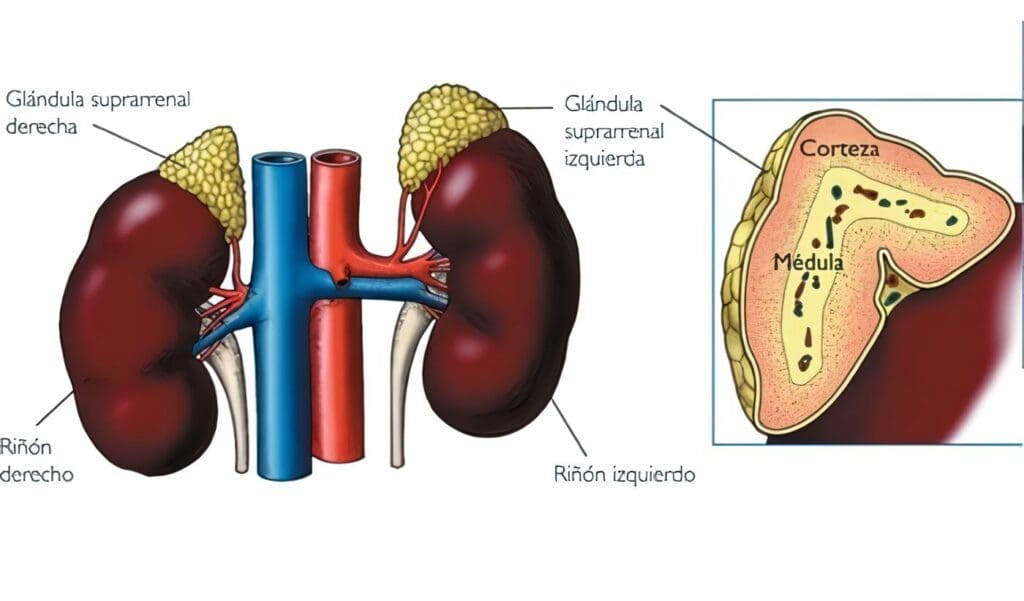
Eustaquio (1563, “Opúsculos Anatómicos”) las llamó cápsulas atrabiliarias, órganos huecos llenos de sangre oscura y más tarde Jean Riolan (1629) las denominó cápsulas suprarrenales.
La Academia de Ciencias de Burdeos intentó averiguar cuáles eran las funciones de estas glándulas por medio de un premio, pero Montesquieu tuvo que declararlo desierto en 1718.
El siglo XIX mostró alguna luz al final del túnel, ya que desde el punto de vista anatómico se describieron las zonas de la corteza: reticular y fascicular (Ecker, 1846) y glomerulosa (Arnold, 1866).
En clínica, Addison describió en1849 un caso de anemia con insuficiencia suprarrenal y en 1855 once pacientes más. Brown-Sèquard en 1856 observó que la adrenalectomìa experimental mata los animales de experimentación. Tigerstedt y Bergman en 1898 descubrieron la renina.
El siglo XX tuvo varios Nóbel relacionados con este campo.
Edward C. Kendall, descubridor de la tiroxina encontró luego la “Cortina” cristalizada en 1934 y un año después aisló la cortisona o Compuesto; Philip Hench, reumatólogo que al igual que Kendall trabajaba en la Clínica Mayo, usó el denominado compuesto E en Artritis Reumatoide en 1948.
En la década de los 30 el europeo Thadeus Reichstein realizó numerosas investigaciones que llevaron al descubrimiento del compuesto Fa/E, de la adrenosterona y del núcleo pregnano, de la síntesis de la DOCA y de 40 esteroides, 6 de los cuales resultaron activos.
Otros investigadores encontraron las células yuxta-glomerulares (Ruyter, 1935, Gourmaghtigh 1939), la aldosterona (Grundy, 1952) que inicialmente se llamó Electrocortina, la que causaba una reabsorción distal de sodio, excreción de potasio e hidrogeniones.
Se vio también que la hipofisectomìa no frenaba la producción de aldosterona pero que la nefrectomía no la dejaba actuar. En 1957, Braun-Menéndez y Schearz encontraron la angiotensina.
El siglo XX también aportó muchos conocimientos en la clìnica. El neurocirujano Harvey Cushing describió el hipercortisolismo en1932. Bartter, Bongiovani y Biglieri describieron varias deficiencias enzimàticas en los casos de hiperplasia suprarrenal congénita.
Conn publicó sus casos de hiperaldosteronismo primario) y Selye el síndrome general de adaptación o estrés, consistente en alarma, resistencia y agotamiento.
Resumen
Las cápsulas suprarrenales tienen una porción externa epitelial denominada corteza y otra interna constituída por tejido nervioso, la medula. Las zonas fasciculada y reticular –dependientes de ACTH- que se encargan de la secreción del glucocorticoide cortisol, el andrógeno DHEA-S y otros corticoides en pequeñas cantidades y la zona glomerular –dependiente del sistema renina-angiotensina- que se encarga de la producción del mineralocorticoide aldosterona.
Su regulación está dada por el feed-back que dan las propias concentraciones de la hormona segregada, más otros factores como la respuesta al estrés, a los cambios en la glicemia, o a la volemia en el caso de la aldosterona.
El cortisol y la aldosterona son esenciales para la vida y sus efectos son –en el caso del cortisol- uno hiperglicemiante y contra-regulador de la insulina, y favorecedor de la neoglucogénesis, amén de otros efectos permisivos sinergísticos con otras hormonas; y -en el de la aldosterona- retener sodio a cambio de potasio e hidrógeno, por su efecto sobre el túbulo contorneado distal.
La DHEA-S es un esteroide con la mitad de la potencia androgénica de la testosterona, pero que se constituye en uno de los andrógenos de la mujer, al igual que la androstenediona ovárica.
Referencias seleccionadas
- Aristizábal D. Fisiopatología de la hipertensión esencial. En: Cardiología (RH Rozo, A Merchàn y cols., Eds), Sociedad Colombiana de Cardiología 2000. pp.365-373.
- Biglieri EG, Arteaga E, Kater CE. Effect of ACTH on aldosterone and other mineralocorticoid hormones. In “Hypothalamic-pituitary-adrenal axis revisited. (WF Ganong, Ed.) Ann NY Acad Sci 1987. 512:426-437.
- Chiang JYL. Bile acid regulation of gene expression, role of nuclear hormone receptors. Endocr Rev 2002. 23: 443-463. Cody R. The integrated effects of angiotensin II. Am J Cardiol 1997. 79: 9-11.
- Dallman MF, Akana SF et al. Characterization of corticosterone feed-back regulation of ACTH secretion. In “The hypothalamic-pituitary-adrenal axis revisited” (WF Ganong, Ed.). Ann NY Acad Sci 1987. 512: 402-414.
- De Kloet ER, Ratka A et al. Corticosteroid receptor types in brain, regulation and putative function. In “The hypothalamic-pituitary adrenal axis revisited”(WF.Ganong,Ed.) Ann NY Acad Sci 1987. 512: 351-361.
- Goldfien A. Adrenocorticosteroids and adrenocortical antagonists. In “Basic and Clinical Pharmacology” (Katzung BG, Ed). Appleton-Lange, 1998. Pp.635-650.
- Katz A. Molecular biology of calcium channels in the cardiovascular system. Am J Cardiol 1997. 80: 171-221.
- Laragh JH, Sealy JE. The renin-aldosterone axis for blood pressure, electrolyte homeostasis, and diagnosis of high blood pressure. In: Textbook of endocrinology (RH Williams,Ed). WB Saunders, Philadelphia, 1981. Pp.1064-1079.
Bibliografías Seleccionadas
- Liddle G. The adrenals. In: Textbook of endocrinology (RH William, Ed.). WB Saunders, Philadelphia, 1981. Pp. 249-292.
- López-Jaramillo P. Bioquímica del endotelio vascular, implicaciones fisiológicas y clínicas. Horizonte Impresores, Bogotá, 5ª. Edición, 2001.Pp. 59-73.
- Miller WL. Molecular biology of steroid hormone synthesis. Endocr Rev 1988. 9: 295-318.
- Mulrow PJ,Takagi M et al. Inhibition of aldosterone secretion by atrial natriuretic peptide. In “Hypothalamic-pituitary –adrenal axis revisited” (WF Ganong, Ed.) Ann NY Acad Sci 1987. 512: 438-448.
- Sapolsky RM, Romero LM, Munck AU. How do glucocorticoids influence stress responses? Integrating permissive, suppressive, stimulatory and preparative actions. Endocr Rev 2000. 21: 55-89.
- Stein BC, Levin RI. Natriuretic peptides, physiology, therapeutic potential, and risk stratification in ischemic heart disease. Am Heart J 1998. 135. 914-923.
- Truss M, Beato M. Steroid hormone receptors, interaction with deoxyribonucleic acid and transcription factors. Endocr Rev 1993. 14:459-479.
- Varela E, Principios de biología molecular en el sistema cardiovascular. En: Cardiología (RH Rozo, A. Merchán y cols, Eds.). Soc Col Cardiol 2000. Pp.18-35.
- Williams GH, Dluhy RG. Diseases of the adrenal cortex. In “Harrison’s Principles of Internal Medicine”, 14th Ed. (Isselbacher KJ et al, Eds). McGraw-Hill 1998. Pp.2035-2056.