Dr. Germán Barón Castañeda, M.D.
El trofoblasto es la célula funcional de la placenta:
Ya que es el principal sitio de producción de hormonas y proteínas. El proceso de diferenciación celular del citotrofoblasto a sincitiotrofoblasto no es bien conocido, pero se cree que es mediado por la HCG y una variedad de factores de crecimiento. La superficie del sincitiotrofoblasto está en contacto con la circulación materna.
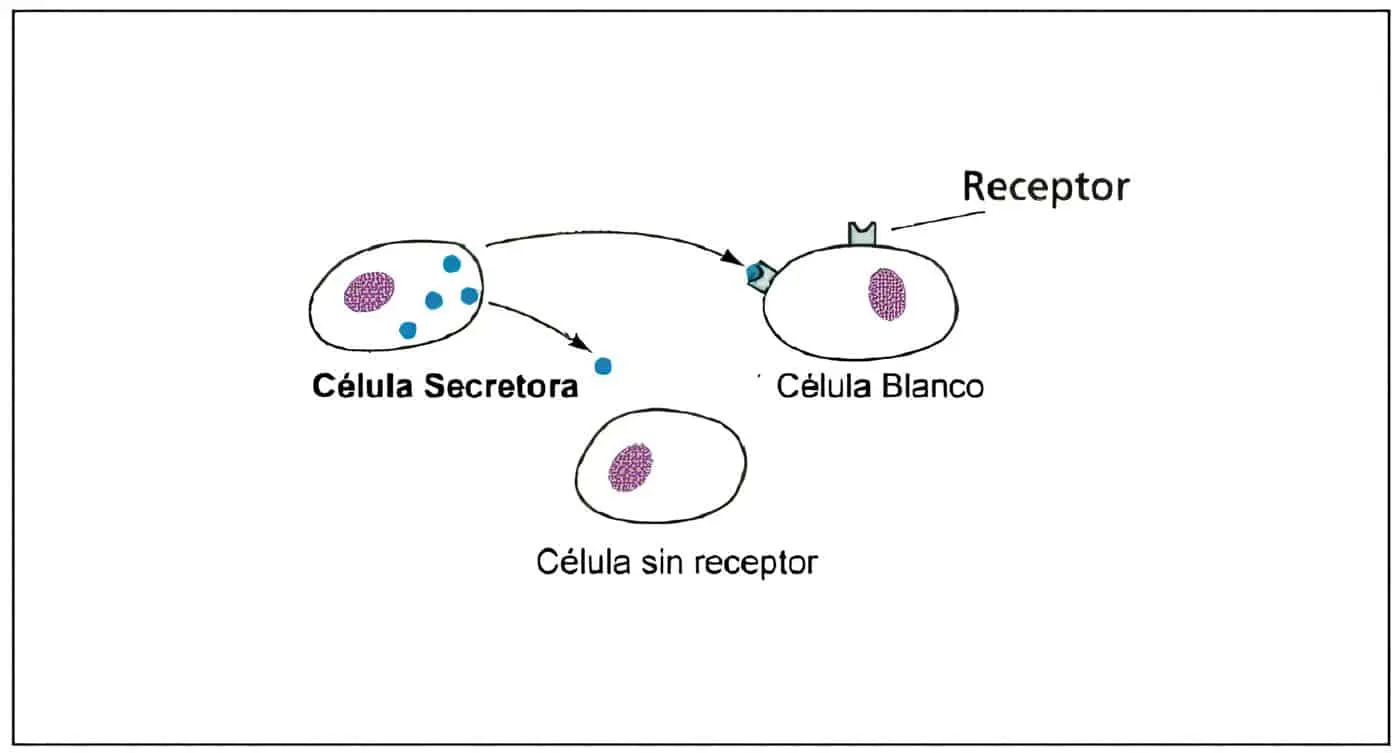
La producción placentaria de hormonas proteicas ya no se considera autónoma; los estudios in vitro han demostrado que existe una regulación endógena de sus productos hormonales, simulando una unidad hipotálamo-hipófisis-órgano blanco en miniatura. Los substratos que llegan a la placenta pueden regular la producción hormonal.
Se ha sugerido que cierto número de hormonas placentarias pueden ejercer sus efectos sobre el feto, la madre o ambos y así participan en su homeostasis durante el embarazo. La regulación hormonal en la placenta puede ser paracrina, autocrina o endocrina.
La mayoría de análogos de las hormonas hipotalámicas se producen en la capa citotrofoblástica de la placenta. Entre ellos se encuentran la GnRH y su precursor el péptido asociado a la GnRH (GAP), el factor inhibidor de la liberación de somatotropina, la CRH, la TRH y los opioides endógenos. En ratas se ha demostrado la presencia de hormona liberadora de hormona de crecimiento, hallazgo que no ha sido corroborado en humanos.
GnRH
Su presencia en la placenta humana fue reportada por primera vez en 1975 por Gibbons y cols. Este péptido similar a la GnRH aumenta la secreción de HCG, estimula la producción de las subunidades a y b. Su liberación está bajo el control de las prostaglandinas E2 y F2 y la adrenalina que la aumentan, probablemente actuando a través del AMPc. La insulina y el péptido intestinal vasoactivo también pueden estimular la GnRH placentaria en forma dependiente de la dosis. A su vez, la GnRH regula la esteroidogénesis placentaria y la liberación de prostaglandinas.
Somatostatina
En el embarazo temprano también se ha detectado una sustancia similar a la somatostatina localizada en el citotrofoblasto, pero no en el sincitio. Esta disminuye a medida que progresa la gestación. Se cree que puede tener un efecto inhibidor sobre el lactógeno placentario.
Hormona liberadora de corticotropina (CRH)
La estructura de la hormona producida en la placenta es exactamente igual a la hipotalámica. Su RNA mensajero aumenta en forma importante en las últimas cinco semanas del embarazo y es paralelo al aumento en los niveles de CRH en la circulación materna. Los glucocorticoides aumentan su síntesis en la placenta.
Se puede encontrar tanto en el citotrofoblasto como en el sincitiotrofoblasto. Su liberación puede ser estimulada por las prostaglandinas, los neurotransmisores como la acetilcolina y la noradrenalina y péptidos como la arginina, la vasopresina, la angiotensina II y la oxitocina. Se ha sugerido que el aumento de la CRH placentaria que precede al parto puede ser el resultado del incremento de los corticoides fetales que ocurre en ese momento. A través del estímulo de la ACTH fetal se produce un aumento de los corticoides fetales, lo cual completaría un asa de retroalimentación positiva que llevaría al comienzo del trabajo de parto.
TRH
También se encuentra una sustancia similar a ella en la placenta. Puede estimular la liberación de TSH hipofisiaria.
HCG
Esta fue la primera hormona proteica placentaria descrita. En 1927 Ascheim y Zondek hallaron una sustancia en la orina de mujeres embarazadas que inicialmente se creyó que era producto de la hipófisis materna. Estudios posteriores demostraron su origen placentario.
Biológica e inmunológicamente es similar a la LH hipofisiaria. Se cree que es producida por la capa del sincitiotrofoblasto más que del citotrofoblasto. Está compuesta por dos subunidades a y b; la primera, similar a todas las hormonas glicoprotéicas y la segunda que le confiere la especificidad única.
Durante el embarazo normal el trofoblasto primitivo produce HCG en un estadío muy temprano. Puede ser detectada después de 9 días del pico de LH, lo cual ocurre apenas 8 días después de la ovulación y un solo día después de la implantación. La concentración de HCG aumenta hasta los 80 o 90 días de gestación y a partir de entonces disminuye hasta una meseta que se mantiene durante el resto del embarazo. Los niveles de LH y FSH maternas son prácticamente indetectables durante todo el embarazo. La vida media de la HCG, a diferencia de la LH, es más larga, llegando a 32 o 37 horas.
Se sabe que uno de los papeles más importantes que juega esta hormona es el luteotrópico:
Mantiene el cuerpo lúteo del ciclo menstrual y luego lo convierte en el cuerpo lúteo del embarazo; esto posibilita la producción persistente de progesterona necesaria para el desarrollo decidual hasta que la placenta asume el control. Puede también regular la producción de otros esteroides en el feto, especialmente la DHEAS y la testosterona. Estudios in vitro han demostrado que la HCG puede inhibir la función de los linfocitos, por lo cual puede intervenir en la modulación de la respuesta inmune durante el embarazo.
Interviene también en la síntesis y secreción de otras hormonas peptídicas. Se sabe que gran parte del aumento de la actividad tiroidea observado durante el embarazo es el resultado de la estimulación de la HCG. Se especula sobre su papel en la autorregulación de las células del sincitiotrofoblasto para la síntesis de las otras hormonas. Otra posible acción es la de inducir la producción de andrógenos en los testículos fetales.
Lactógeno placentario
Es llamado también somatomamotrofina coriónica humana. Es una hormona proteica con similitud inmunológica y biológica con la hormona de crecimiento. Fue aislada de la placenta a comienzos de la década de los 60 por Josimovic y MacLaren. Es sintetizada al parecer por el sincitiotrofoblasto. Puede hallarse en el suero y la orina de mujeres que cursan con embarazos normales y con mola hidatiforme y desaparece rápidamente después del alumbramiento. Su concentración en la circulación materna se correlaciona en forma directa con el peso del feto y de la placenta, sin tener variación circadiana; sólo cantidades muy pequeñas de esta hormona ingresan a la circulación fetal.
Experimentalmente se ha demostrado que puede tener efectos promotores del crecimiento; sobre el metabolismo de lípidos y carbohidratos sus efectos son similares a los de la hormona del crecimiento, incluyendo la inhibición de la captación periférica de glucosa y la estimulación de la liberación de insulina. Produce un aumento de los ácidos grasos libres plasmáticos luego de su administración.
Su concentración va aumentando en forma progresiva durante la gestación, llegando a un nivel máximo en las últimas cuatro semanas. Su secreción no es alterada por los mismos factores que intervienen en la secreción de hormona de crecimiento hipofisiaria, pero se ha visto que el ayuno prolongado en el segundo trimestre de embarazo y la hipoglicemia inducida por insulina aumentan la concentración de lactógeno placentario, mientras que su nivel disminuye en forma rápida ante la presencia de prostaglandina F2a.
Se ha sugerido que el principal efecto metabólico lo ejerce sobre la madre, asegurando que los requerimientos nutricionales del feto se hallen cubiertos.
TSH coriónica
Es una glicoproteína con peso molecular aproximado de 30.000 y propiedades similares a las de la TSH hipofisiaria. Aumenta la secreción de hormonas tiroideas y estimula la incorporación de fosfato inorgánico en la glándula tiroides, aunque su potencia biológica es menor que la de la hormona hipofisiaria.
Su papel fisiológico no ha sido elucidado totalmente. Se ha sugerido que puede desempeñar un papel en la variación de los índices de la función tiroidea y en la incidencia del aumento de tamaño de la glándula tiroides durante el embarazo.
ACTH y opioides endógenos
Se ha demostrado también la presencia de un péptido similar a la ACTH cuya función no ha sido establecida. La placenta también sintetiza su precursor, la proopiomelanocortina y por ende la b-endorfina que tiene similitud con la hipotalámica. Se ha sugerido que esta endorfina es liberada en forma paralela con la ACTH y que factores como la hipoxia y la acidosis pueden llevar a un aumento en su secreción.
Otro de los opiodes endógenos que se ha detectado en la placenta es la dinorfina, la cual se une con los receptores k de los opiáceos; estos receptores son abundantes en la placenta y aumentan al final del embarazo.
También se ha localizado el neuropéptido Y, especialmente en el citotrofoblasto y el trofoblasto intermedio. Su nivel materno se encuentra por encima del presente en mujeres no embarazadas desde el comienzo de la gestación; permanece elevado hasta el término y aumenta durante el trabajo de parto, llegando a un pico máximo con la dilatación cervical y el parto. Las concentraciones en el líquido amniótico también son elevadas; puede estimular la liberación de CRH en las células placentarias.
Otro péptido hallado en la placenta es la inhibina. Su liberación es estimulada por el péptido intestinal vasoactivo y por el nueropéptido Y, en una forma relacionada con la dosis. Se plantea que puede jugar un papel inhibidor en la regulación de la liberación de HCG, además de una acción inhibitoria local sobre la GnRH placentaria. Por el contrario, la activina aumenta las concentraciones de GnRH y progesterona.
Alfafeto proteína
Es una glicoproteína única con 590 aminoácidos derivada en gran parte del hígado fetal y parcialmente del saco vitelino. Su función es desconocida, pero su tamaño es similar y su secuencia guarda homología con la albúmina, por lo cual se postula que puede actuar como una proteína transportadora de hormonas esteroideas en la sangre fetal. Puede ser un modulador de la proliferación celular, teniendo una acción sinérgica con varios factores de crecimiento.
Los niveles pico de esta proteína en sangre fetal se alcanzan al final del primer trimestre y luego disminuyen gradualmente hasta las 32 semanas cuando caen en forma rápida. Los niveles maternos son mucho más bajos que los fetales, aumentado en forma constante hasta la semana 32. Su concentración en el sistema nervioso fetal es muy elevada, y se incrementa en forma importante en los casos en los cuales hay defectos del tubo neural.
(Lea También: Papel Endocrino de la Decidua y las Membranas Fetales)
Relaxina
Es una hormona peptídica producida por el cuerpo lúteo y no es detectada en los hombres ni en mujeres fuera del estado de embarazo. Está compuesta de dos cadenas cortas de péptidos unidas por puentes disulfuro. Ha sido identificada también en la placenta, la decidua y el corion. Los niveles en suero aumentan durante el primer trimestre y disminuyen en el segundo.
Prolactina
Es producida por el endometrio decidualizado desde el día 23 del ciclo. Durante el embarazo la secreción de prolactina está limitada a la hipófisis materna, la hipófisis fetal y el útero. Ni el trofoblasto ni las membranas secretan prolactina, mientras que sí lo hacen el miometrio y el endometrio. La progesterona es necesaria para la síntesis de esta hormona en el endometrio, mientras que la inhibe en el miometrio.
Las concentraciones en el líquido amniótico son paralelas a las del suero materno hasta la décima semana de embarazo, aumentan en forma marcada hasta la semana 20 y luego disminuyen. Una de sus principales funciones parece ser la regulación hidroelectrolítica; se encuentran receptores en la hoja del corion y disminuye la permeabilidad del amnios hacia el lado materno.
Factores de crecimiento y citoquinas
La producción local de citoquinas en la placenta se cree que es indispensable para el crecimiento embrionario y para modular la respuesta inmune materna, esencial para la sobrevida del embarazo.
La interleuquina-1b es producida en el endometrio decidualizado durante el embarazo y el factor estimulador de colonias 1 es sintetizado tanto por la decidua como por la placenta. La placenta también produce interleuquina-6, sustancia que aumenta la liberación de HCG.
Los factores de crecimiento similares a la insulina juegan papel en el crecimiento pre y post-natal; no cruzan la placenta hacia la circulación fetal, pero pueden regular el crecimiento placentario. Durante el embarazo hay un incremento en los niveles maternos de la IGFBP-1 empezando en el primer trimestre y llegando a un pico al término; ahora se sabe que es la misma proteína placentaria 12 y por lo tanto, que es producida en la decidua.
El IGF-I producido en la placenta regula la transferencia de nutrientes de la placenta al feto y estimula el crecimiento fetal. La IGFBP-1 interfiere con la acción del IGF-I y por lo tanto en el crecimiento fetal. De esta manera el peso del recién nacido se correlaciona en forma directa con los niveles maternos de IGF-I e inversamente con los de IGFBP-1.
El factor de crecimiento epidérmico es sintetizado por el sincitiotrofoblasto y probablemente juega papel en la diferenciación de citotrofoblasto a sincitiotrofoblasto.
Inhibina y activina
La inhibina y la activina son producidas en el sincitiotrofoblasto y su síntesis es estimulada por las prostaglandinas E2 y F2a; son responsables en la regulación de la producción placentaria de HCG, GnRH y esteroides; la activina es estimuladora, mientras que la inhibina es inhibitoria.
Factor temprano de embarazo
Es una sustancia que puede ser detectada en la circulación materna uno o dos días después del coito que ha resultado en embarazo; desaparece antes del parto. Antes de la implantación posiblemente es producido como respuesta del ovario a una señal ovular; después de la implantación es derivado del mismo embrión. Se trata de una proteína asociada con la proliferación celular y el crecimiento; además posee propiedades inmunosupresoras y se encuentra en concentración abundante en las plaquetas.