5.4 Recomendaciones sobre tratamiento antirretroviral del fracaso terapéutico del manejo de la infección por VIH/Sida
Pregunta clínica 7
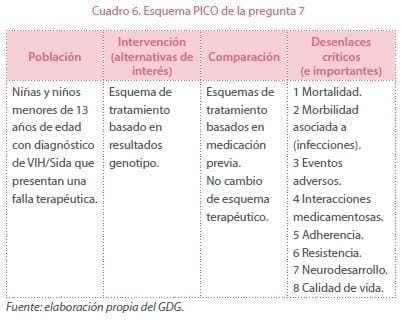
¿Cuál debe ser el esquema de tratamiento antirretroviral de segunda línea de acuerdo con la terapia previa en niñas y niños menores de 13 años de edad con diagnóstico de VIH/Sida que presentan una falla terapéutica?
Los resultados de la síntesis de estos estudios muestran que no hay información acerca de cuál es el mejor esquema antirretroviral posterior a una primera falla terapéutica. Por lo cual para diseñar una tratamiento antirretroviral óptimo para disminuir el riesgo de nuevas emergencias de resistencia deben tenerse en cuenta otros aspectos como frecuencia mediana de resistencia por clase de antirretrovirales. Con diferencias sustanciales en la ocurrencia de resistencia a diferentes medicamentos antirretrovirales puede explicarse por la diversidad en la barrera genética para generar resistencia a uno o más medicamentos.
Esta barrera genética se define como el número de mutaciones requeridas para superar esa presión selectiva específica del medicamento antirretroviral; los INNTR y la Lamivudina tiene una barrera genética de uno; por lo cual el virus del VIH fácilmente selecciona la resistencia cuando el paciente continua usando ese medicamento a pesar de falla virológica (44).
Tratamiento antirretroviral de segunda línea en caso de falla virológica
La guía OMS del año 2013 (42), aborda la pregunta sobre esquemas de tratamiento antirretroviral de segunda línea en caso de falla virológica. Pero no incluye la genotipificación como determinante del esquema, en sus recomendaciones. Esta guía recomienda los cambios basados en el régimen inicial: si el tratamiento antirretroviral inicial incluye un inhibidor de proteasa. Recomiendan, para menores de 3 años de edad, no hacer ningún cambio y para niñas y niños mayores de 3 años de edad cambiar a un régimen con Efavirenz.
Si el tratamiento antirretroviral de primera línea es basado en INNTR. Recomiendan el uso de Lopinavir/Ritonavir en todos los mayores de 3 años de edad. Para mayores de 3 años de vida la guía de la OMS sugiere las recomendaciones de adultos.
Es importante destacar que los desarrolladores de la guía describen que la evidencia para esta pregunta tanto en adultos como en niñas y niños es de muy baja calidad.
La guía de EEUU del año 2012 (18) recomienda hacer pruebas de genotipificación para evaluar resistencia y con base en estos resultados escoger la terapia apropiada. Pero no asocian evidencia que sustente esta recomendación. La cual puede ser basada en el consenso de expertos y en la proyección del supuesto de reducción de resistencia a los antirretrovirales.
Es de resaltar en este punto que no hay consenso a través de las diferentes recomendaciones acerca de los puntos de corte de conteos de LT CD4 para la definición de falla virológica.
La RSL de Sigaloff 2013 sobre resistencia al tratamiento antirretroviral. Muestra gran variabilidad a través de los estudios en el número de copias virales en los recuentos de ARN viral (45).
Recomendaciones
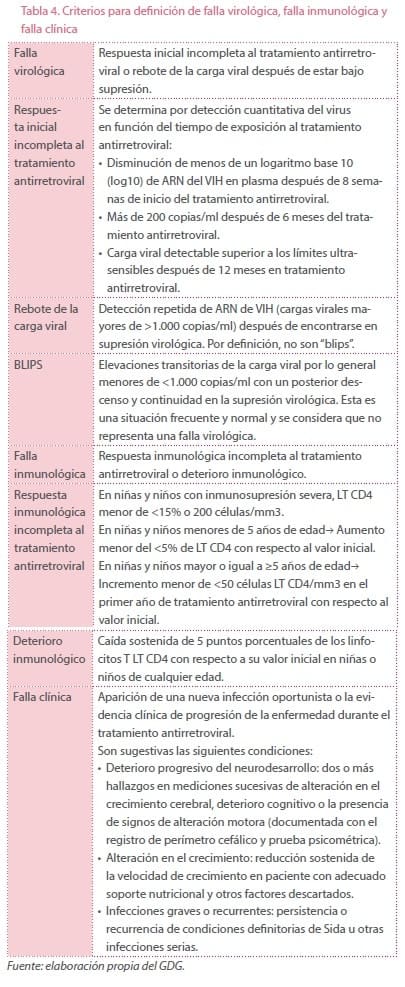
Ante una falla virológica, inmunológica o clínica (ver definiciones Tabla 4) en el tratamiento de primera línea en una niña o niño menor de 13 años de edad con infección por VIH/Sida. Se sugiere:
Recomendación 17
Hacer el cambio del tratamiento antirretroviral basado en el resultado de la genotipificación.
Fuerza y dirección de la recomendación: FUERTE A FAVOR DE LA INTERVENCIÓN. (Recomendación condicional por la falta de evidencia. Consenso del GDG).
Puntos de buena práctica clínica
- La genotipificación debe ser interpretada por un médico experto en VIH. Dada la relación directa que tiene el tratamiento de la falla virológica con las tasas de resistencia y la complejidad en la interpretación de las pruebas de genotipificación.
Se presentan las categorías de médico tratante para los pacientes con VIH/Sida en Colombia. Según consenso entre el Ministerio de Salud y Protección Social, el Fondo de Población de las Naciones Unidas. El Instituto de Evaluación Tecnológica en Salud y la Asociación Colombiana de Infectología. - Durante el tratamiento de las niñas y niños con antirretrovirales es fundamental realizar un adecuado seguimiento del paciente. contiene Plan de seguimiento sugerido por el GDG que puede ser adoptado por los profesionales de la salud a cargo de estos pacientes.
Referencias
- 1. López P, Beltrán S, Sierra A, Echeverri L, Zapata AF, Laura Valderra¬ma L. “Recomendaciones para el abordaje, diagnóstico y tratamiento del niño con VIH/Sida en Colombia 2011.ed: Casa Editorial Catorse ISBN: 978-958-8404-11-0. pags. 128
- 2. Programa Conjunto de las Naciones Unidas sobre el VIH/Sida. In¬forme de ONUSIDA sobre la epidemia mundial de Sida. [Gene¬va]: ONUSIDA, 2012. Available from: http://www.unaids.org/en/media/unaids/contentassets/documents/epidemiology/2012/gr2012/20121120_UNAIDS_Global_Report_2012_with_annexes_es.pdf
- 3. Sierra- Alarcón C. Boletín Epidemiológico de VIH/Sida 2013, situa¬ción del VIH/Sida, Colombia 2013. Ministerio de Salud y Protección Social, Colombia 2014.
- 4. Grupo de Actualización de la Guía Metodológica. Guía Metodológica para la elaboración de Guías de Práctica Clínica con Evaluación Eco¬nómica en el Sistema General de Seguridad Social en Salud colom¬biano – Tercer borrador: COLCIENCIAS; 2013.
- 5. Asociación Colombiana de Infectología. Documentos preliminares – Guías de práctica clínica para el manejo de infección por VIH de ado¬lescentes y adultos hombres y mujeres con 13 o más años de edad; y para niños y niñas menores a 13 años: ACIN; 2013. Available from: http://www.acin.org/new/.
- 6. Connor EM, Sperling RS, Gelber R, Kiselev P, Scott G, O’Sullivan MJ, et al. Reduction of maternal-infant transmission of human im¬munodeficiency virus type 1 with zidovudine treatment. Pediatric AIDS Clinical Trials Group Protocol 076 Study Group. N Engl J Med. 1994;331(18):1173-80.
- 7. Lallemant M, Jourdain G, Le Coeur S, Kim S, Koetsawang S, Comeau AM, et al. A trial of shortened zidovudine regimens to prevent mo¬ther-to-child transmission of human immunodeficiency virus type 1. Perinatal HIV Prevention Trial (Thailand) Investigators. N Engl J Med. 2000;343(14):982-91.
- 8. Lallemant M, Jourdain G, Le Coeur S, Mary JY, Ngo-Giang-Huong N, Koetsawang S, et al. Single-dose perinatal nevirapine plus standard zidovudine to prevent mother-to-child transmission of HIV-1 in Thailand. N Engl J Med. 2004;351(3):217-28.
- 9. Gray GE, Urban M, Chersich MF, Bolton C, van Niekerk R, Violari A, et al. A randomized trial of two postexposure prophylaxis regimens to reduce mother-to-child HIV-1 transmission in infants of untreated mothers. Aids. 2005;19(12):1289-97.
- 10. Nielsen-Saines K, Watts DH, Veloso VG, Bryson YJ, Joao EC, Pilotto JH, et al. Three postpartum antirretroviral regimens to prevent intra¬partum HIV infection. N Engl J Med. 2012;366(25):2368-79.
- 11. Panel on Treatment of HIV-Infected Pregnant Women and Preven¬tion of Perinatal Transmission. Recommendations for Use of Anti¬rretroviral Drugs in Pregnant HIV-1- Infected Women for Maternal Health and Interventions to Reduce Perinatal HIV Transmission in the United States. 2012 [updated 2012; cited 2013 Septiembre]. Available from: vailable at http://aidsinfo.nih.gov/contentfiles/lv-guidelines/PerinatalGL.pdf.
- 12. Capparelli EV, Mirochnick M, Dankner WM, Blanchard S, Mofenson L, McSherry GD, et al. Pharmacokinetics and tolerance of zidovudine in preterm infants. J Pediatr. 2003;142(1):47-52.
- 13. Thior I, Lockman S, Smeaton LM, Shapiro RL, Wester C, Heymann SJ, et al. Breastfeeding plus infant zidovudine prophylaxis for 6 mon¬ths vs formula feeding plus infant zidovudine for 1 month to reduce mother-to-child HIV transmission in Botswana: a randomized trial: the Mashi Study. JAMA [Internet]. 2006 Aug 16 [cited 2013 Nov 25];296(7):794–805. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16905785
- 14. Peltier CA, Ndayisaba GF, Lepage P, van Griensven J, Le¬roy V, Pharm CO, et al. Breastfeeding with maternal antirre¬troviral therapy or formula feeding to prevent HIV postna¬tal mother-to-child transmission in Rwanda. AIDS [Internet]. 2009 Nov 27 [cited 2013 Oct 18];23(18):2415–23. Availa¬ble from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3305463&tool=pmcentrez&rendertype=abstract
- 15. Nduati R, John G, Mbori-Ngacha D, Richardson B, Overbaugh J, Mwa¬tha A, et al. Effect of breastfeeding and formula feeding on trans¬mission of HIV-1: a randomized clinical trial. JAMA [Internet]. 2000 Mar 1 [cited 2013 Nov 28];283(9):1167–74. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10703779
- 16. McGrath CJ, Nduati R, Richardson BA, Kristal AR, Mbori-Nga¬cha D, Farquhar C, et al. The prevalence of stunting is high in HIV-1-exposed uninfected infants in Kenya. J. Nutr. [Inter¬net]. 2012 Apr [cited 2013 Nov 6];142(4):757–63. Availa¬ble from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3301992&tool=pmcentrez&rendertype=abstract
- 17. Binagwaho A, Pegurri E, Drobac PC, Mugwaneza P, Stulac SN, Wagner CM, et al. Prevention of mother-to-child transmission of HIV: cost-effec¬tiveness of antirretroviral regimens and feeding options in Rwan¬da. PLoS One [Internet]. 2013 Jan [cited 2013 Oct 1];8(2):e54180. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3577801&tool=pmcentrez&rendertype=abstract
- 18. Panel on Antirretroviral Therapy and Medical Management of HIV-Infected Children. Guidelines for the Use of Antirretroviral Agents in Pediatric HIV Infection [Internet]. 2012 [cited 2013 Jun 11]. p. 333. Available from: http://aidsinfo.nih.gov/guidelines on
- 19. World Health Organization, editor. Summary of findings and qua¬lity of evidence evaluation for the use of virological testing. WHO Recommendations on the Diagnosis of HIV Infection in Infants and Children. Geneve: WHO; 2010. p. 1–27. Available from: http://whq-libdoc.who.int/publications/2010/9789241599085_eng.pdf.
- 20. Lilian RR, Bhowan K, Sherman GG. Early diagnosis of human immu¬nodeficiency virus-1 infection in infants with the NucliSens EasyQ assay on dried blood spots. J Clin Virol [Internet]. Elsevier B.V.; 2010 May [cited 2013 Jun 6];48(1):40–3. Available from: http://www. ncbi.nlm.nih.gov/pubmed/20211580
- 21. Sivapalasingam S, Ahmed A, Mendillo M, Holzman R, Marshed F, Mwamzuka M, et al. Early detection of HIV infection among Ken¬yan infants using a reverse transcriptase activity assay. Pediatr Infect Dis J [Internet]. 2012 Jul [cited 2013 Jul 6];31(7):732–5. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3405543&tool=pmcentrez&rendertype=abstract
- 22. Maritz J, Preiser W, van Zyl GU. Establishing diagnostic cut-off cri¬teria for the COBAS AmpliPrep/COBAS TaqMan HIV-1 Qualitative test through validation against the Amplicor DNA test v1.5 for infant diagnosis using dried blood spots. J Clin Virol [Internet]. Elsevier B.V.; 2012 Feb [cited 2013 May 23];53(2):106–9. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22196872
- 23. Burgard M, Blanche S, Jasseron C, Descamps P, Allemon M-C, Cira¬ru-Vigneron N, et al. Performance of HIV-1 DNA or HIV-1 RNA tests for early diagnosis of perinatal HIV-1 infection during anti-retro¬viral prophylaxis. J Pediatr [Internet]. 2012 Jan [cited 2013 Jul 6];160(1):60–6.e1. Available from: http://www.ncbi.nlm.nih.gov/pubmed/21868029
- 24. Zhang Q, Wang L, Jiang Y, Fang L, Pan P, Gong S, et al. Early infant human immunodeficiency virus type 1 detection suitable for re¬source-limited settings with multiple circulating subtypes by use of nested three-monoplex DNA PCR and dried blood spots. J Clin Microbiol [Internet]. 2008 Feb [cited 2013 May 23];46(2):721–6. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=2238144&tool=pmcentrez&rendertype=abstract
- 25. Ngo-Giang-Huong N, Khamduang W, Leurent B, Collins I, Nanta¬sen I, Leechanachai P, et al. Early HIV-1 diagnosis using in-house real-time PCR amplification on dried blood spots for infants in re¬mote and resource-limited settings. J Acquir Immune Defic Syndr [Internet]. 2008 Dec 15 [cited 2013 Jul 28];49(5):465–71. Avai¬lable from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3111749&tool=pmcentrez&rendertype=abstract
- 26. Jacob SM, Anitha D, Vishwanath R, Parameshwari S, Samuel NM. The use of dried blood spots on filter paper for the diagnosis of HIV-1 in infants born to HIV seropositive women. Indian J Med Microbiol [In-ternet]. 2008 [cited 2013 Jul 28];26(1):71–4. Available from: http:// www.ncbi.nlm.nih.gov/pubmed/18227604
- 27. Owens DK, Holodniy M, McDonald TW, Scott J, Sonnad S. A me¬ta-analytic evaluation of the polymerase chain reaction for the diagnosis of HIV infection in infants. JAMA [Internet]. 1996 May 1;275(17):1342–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/8614121
- 28. Puthanakit T, Tangsathapornpong A, Ananworanich J, Wongsawat J. Thai national guidelines for the use of antirretroviral therapy in pediatric HIV infection 2010. Asian Biomed [Internet]. 2010 [cited 2014 Feb 14];4(4):505–13. Available from: http://www.aidstar-one.com/sites/default/files/Thailand_pediatric_guidelines_2010.pdf
- 29. Cornett Jk, Kim TJ. Laboratory diagnosis of HIV in adults: a review of current methods. Clin Infect Dis. 2013 Sep;27(5): 712-8.
- 30. Puthanakit T, Jourdain G, Hongsiriwon S, Suntarattiwong P, Chokephaibulkit K, Sirisanthana V, et al. HIV-1 drug resistance mu¬tations in children after failure of first-line nonnucleoside reverse transcriptase inhibitor-based antirretroviral therapy. HIV Med [In¬ternet]. 2010 Oct 1 [cited 2013 Aug 22];11(9):565–72. Available from: http://www.ncbi.nlm.nih.gov/pubmed/20345882
- 31. Sigaloff KCE, Calis JCJ, Geelen SP, van Vugt M, de Wit TFR. HIV-1-re¬sistance-associated mutations after failure of first-line antirretrovi¬ral treatment among children in resource-poor regions: a systema¬tic review. Lancet Infect Dis [Internet]. 2011 Oct [cited 2013 Aug 22];11(10):769–79. Available from: http://www.ncbi.nlm.nih.gov/pubmed/21872531
- 32. Gray L, Newell ML, Thorne C, Peckham C, Levy J. Fluctuations in symptoms in human immunodeficiency virus-infected children: the first 10 years of life. Pediatrics [Internet]. 2001 Jul [cited 2014 Feb 17];108(1):116–22. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11433063
- 33. Penazzato M, Prendergast A, Tierney J, Cotton M, Gibb D. Effecti¬veness of antirretroviral therapy in HIV-infected children under 2 years of age. Cochrane database Syst Rev [Internet]. 2012 Jan [cited 2013 Aug 9];7:CD004772. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22786492
- 34. Violari A, Cotton MF, Gibb DM, Babiker AG, Steyn J, Madhi S a, et al. Early antirretroviral therapy and mortality among HIV-infected in¬fants. N Engl J Med. 2008 Nov;359(21):2233–44.
- 35. Laughton B, Cornell M, Grove D, Kidd M, Springer PE, Dobbels E, et al. Early antirretroviral therapy improves neurodevelopmental out¬comes in infants. AIDS. 2012 Aug;26(13):1685–90.
- 36. Shiau S, Arpadi S, Strehlau R, Martens L, Patel F, Coovadia A, et al. Initiation of Antirretroviral Therapy Before 6 Months of Age is As¬sociated with Faster Growth Recovery in South African Children Perinatally Infected with Human Immunodeficiency Virus. J Pediatr. Elsevier Ltd; 2013 Jun;162(6):1138–1145.e2.
- 37. Paediatric HI V, Markers P, Study C. Predictive value of absolute CD4 cell count for disease progression in untreated HIV-1-infected chil¬dren. AIDS. 2006 Jun;20(9):1289–94.
- 38. Marin B, Thiebaut R BH et al. Non AIDS defining deaths and inmu¬nodeficiency in the era of combination antirretroviral therapy. AIDS. 2009;23(13):1743–53.
- 39. Kitahata MM, Gange SJ AA et al. Effect of early vs deferred antirretrovi¬ral therapy for HIV on survival. N Engl J Med. 2009;360(18):1815–26.
- 40. Sterne JA MM et al. Timing of initiation of antirretroviral therapy in AIDS – free HIV 1 infected patients: a colaborative analysis of 18 HIV cohort studies. Lancet. 2009;373(9672):1352–63.
- 41. Welch S, Sharland M, Lyall EGH, Tudor-Williams G, Niehues T, Win¬tergerst U, et al. PENTA 2009 guidelines for the use of antirretroviral therapy in paediatric HIV-1 infection. HIV Med [Internet]. 2009 Nov [cited 2013 Oct 27];10(10):591–613. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19878352
- 42. World Health Organization. Consolidated Guidelines on the use of antirretroviral drugs for treating and preventing HIV Infection. [In¬ternet]. Geneva; 2013. Available from: http://www.who.int/hiv/pub/guidelines/arv2013/en/
- 43. Sociedad Argentina de Infectologia. Recomendaciones para el segui¬miento y tratamiento de la infección por VIH/Sida y sus comorbili¬dades asociadas [Internet]. 2012. Available from: http://aidstar-one.com/sites/default/files/Argentina_2012_tagged.pdf
- 44. Nichols BE, Boucher C a B, van de Vijver D a MC. HIV testing and an¬tirretroviral treatment strategies for prevention of HIV infection: im¬pact on antirretroviral drug resistance. J Intern Med [Internet]. 2011 Dec [cited 2013 Nov 20];270(6):532–49. Available from: http://www.ncbi.nlm.nih.gov/pubmed/21929723
- 45. Sigaloff KCE, Calis JCJ, Geelen SP, van Vugt M, de Wit TFR. HIV-1-resis¬tance-associated mutations after failure of first-line antirretroviral treatment among children in resource-poor regions: a systematic re¬view. Lancet Infect Dis [Internet]. Elsevier Ltd; 2011 Oct [cited 2013 Aug 22];11(10):769–79. Available from: http://www.ncbi.nlm.nih.gov/pubmed/21872531
- 46. Caicedo S, Idarraga S, Villegas P, Osorio A. Estrategia para la reduc¬ción de la transmisión perinatal del VIH y de la sífilis congénita. Ma¬nual de procedimientos 4 edición. Ministerio de la Protección Social. Colombia 2009.
- 47. Sierra García A, López López P, Beltrán Higuera SJ. Recomendaciones para el Abordaje, Diagnóstico y Tratamiento del Niño con VIH/Sida. Camilo Torres Serna y Cia S.C.S; 2012
- 48. Health ND of, Africa S. Guidelines for the Management of HIV in Chil¬dren National Department of Health South Africa. 2010;87.
- 49. MMRWR. Revisión del sistema de clasificación para la infección por VIH en niñas y niños menores de 13 años de edad. Recomm Rep. 1994; 43 (RR-12):1-19.
- 50. Acip P, Rutledge TF, Boyd MF. Morbidity and Mortality Weekly Report Prevention of Rotavirus Gastroenteritis Among Infants and Children Recommendations of the Advisory Committee. 2009;58.
- 51. Acip IP. Prevention of Measles , Rubella , Congenital Rubella Syndro¬me , and Mumps , 2013 Summary Recommendations of the Advisory Committee on. 2013;62(4).
- 52. Eileen F. Dunne, MD, Lauri E. Markowitz, MD H, Chesson, PhD, Div of STD Prevention NC for H, AIDS, Viral Hepatitis S and TPCR, Curtis, MD, Immunization Svcs Div NC for, Immunizations and Respiratory Diseases; Mona Saraiya M, Div of Cancer Prevention and Control NC for, et al. Recommendations on the Use of Quadrivalent Human Pa¬pillomavirus Vaccine in Males- Advisory Committee on Immuniza¬tion Practices (ACIP), 2011. MMWR. Morb. Mortal. Wkly. Rep. 2011 Dec;60(50):1705–8
- 53. Lisa A. Grohskopf M, David K. Shay M, Tom T. Shimabukuro M, Les¬lie Z. Sokolow, MSc, MPH1 3, Wendy A. Keitel M, Joseph S. Bresee M, et al. Prevention and control of seasonal influenza with vaccines. Recommendations of the Advisory Committee on Immunization Practices–United States, 2013-2014. MMWR. Recomm. Rep. 2013 Sep;62(RR-07):1–43.
- 54. Nancy M. Bennett, MD AC on I, Practices Pneumococcal Work Group. Tamara Pilishvili M, Cynthia G. Whitney, MD, Matthew Moore, MD RG, MPH, Respiratory Diseases Br, Div of Bacterial Diseases N, M. C for I and RDA, Harris, MD, EIS Officer CC contributor:, et al. Use of 13-Va¬lent Pneumococcal Conjugate Vaccine and 23-Valent Pneumococcal Polysaccharide Vaccine Among Children Aged 6–18 Years with Im-munocompromising Conditions: Recommendations of the Advisory Committee on Immunization Practices (ACIP). Morb. Mortal. Wkly. Rep. 2013;62(25):521–4.
- 55. Acip IP. Prevention and Control of Meningococcal Disease Recom¬mendations of the Advisory Committee on. 2013;62(2).