Dr. Germán Barón Castañeda, M.D.
La evaluación paraclínica inicial del hirsutismo consiste en medir los niveles séricos de testosterona, DHEAS y 17-hidroxiprogesterona (17-OHP). Como parte de la valoración de la anovulación se debe realizar la medición de prolactina y TSH.
Siempre se debe pensar en la posibilidad de la hiperinsulinemia. Como ya se había mencionado en capítulos anteriores, las pacientes con aumento de andrógenos pueden tener amenorrea por pseudodecidualización del endometrio, caso en el cual puede estar ausente el sangrado después de una prueba progestacional. Una de las posibilidades que hay que descartar es la del síndrome de Cushing.
Síndrome de Cushing
Es la secreción persistente y elevada de cortisol, que puede aparecer por cinco vías diferentes:
- Producción exagerada de ACTH por la hipófisis (Enfermedad de Cushing).
- Producción ectópica de ACTH por tumores.
- Secreción autónoma de cortisol en la glándula suprarrenal.
- Tumores ováricos.
- Producción de CRH por un tumor.
Clínicamente se caracteriza por obesidad de tipo central, estrías e hiperpigmentación de la piel, fracturas patológicas, diabetes, hipertensión arterial y amenorrea.
Los exámenes de laboratorio básicos para confirmar el síndrome de Cushing son la excreción de cortisol libre en orina de 24 horas (normal de 10 a 90 mg) y el cortisol plasmático tomado en horas de la tarde (menor de 15 mg/dl).
Las mediciones de 17-cetoesteorides y 17-hidroxiesteroides urinarios y el cortisol basal son menos confiables, ya que hay un rango estrecho y entrecruzado entre los valores normales y los patológicos.
La prueba de supresión con dosis única de dexametasona es muy útil, ya que su tasa de falsos positivos es muy baja. Se administra 1 mg vía oral la noche anterior y se realiza una medición de cortisol basal a las 8:00 a.m.; si el nivel basal es menor de 5 mg/dl descarta el síndrome de Cushing; es poco probable con valores entre 5 y 10 mg/dl y valores superiores a 10 mg/dl confirman la hiperfunción suprarrenal.
Cuando existe duda se administra dexametasona 0.5 mg cada 6 horas por 2 días consecutivos y después de 2 días se mide cortisol y 17-hidroxiesteroides en orina de 24 horas. En pacientes con el síndrome de Cushing no hay disminución de los 17-hidroxiesteroides por debajo de 4 mg/día y del cortisol por debajo de 20 mg.
Estados de hipercortisolismo
Se pueden encontrar estados de hipercortisolismo moderado en situaciones como el alcoholismo, estrés, anorexia y bulimia nerviosa, obesidad severa y depresión. La combinación de la prueba de supresión con dosis bajas de dexametasona con la estimulación con CRH sirve para diferenciar el verdadero síndrome de este hipercortisolismo.
Después de dos días de supresión con dexametasona se mide el cortisol plasmático 15 minutos después de administrar CRH 1 mg/kg. intravenoso; el valor de cortisol superior a 1.4 mg/dl requiere mayor evaluación.
La etiología del síndrome de Cushing puede establecerse usando la supresión con dosis elevadas de dexametasona. Se administran 2 mg cada 6 horas por 2 días; al segundo día se miden 17 – hidroxiesteroides y cortisol libre en orina. Si el valor basal de ACTH está por debajo de 5 pg/ml y los esteroides urinarios no disminuyen por lo menos en un 40% lo más probable es que se trate de un tumor suprarrenal.
Cuando la ACTH está por encima de 20 pg/ml la posibilidad de un tumor ectópico productor de ACTH es poco probable si los esteroides han disminuido por lo menos en 40%. La enfermedad de Cushing está presente cuando el nivel de ACTH se encuentra dentro de rangos normales, los RX de tórax son normales y los RX de silla turca muestran alteraciones.
El nivel plasmático de ACTH por encima de 50 pg/ml sugiere una liberación ectópica de la hormona y por debajo de 5 pg/ml sugiere un tumor autónomo de la glándula suprarrenal productor de cortisol.
Hiperandrogenismo e hiperinsulinemia
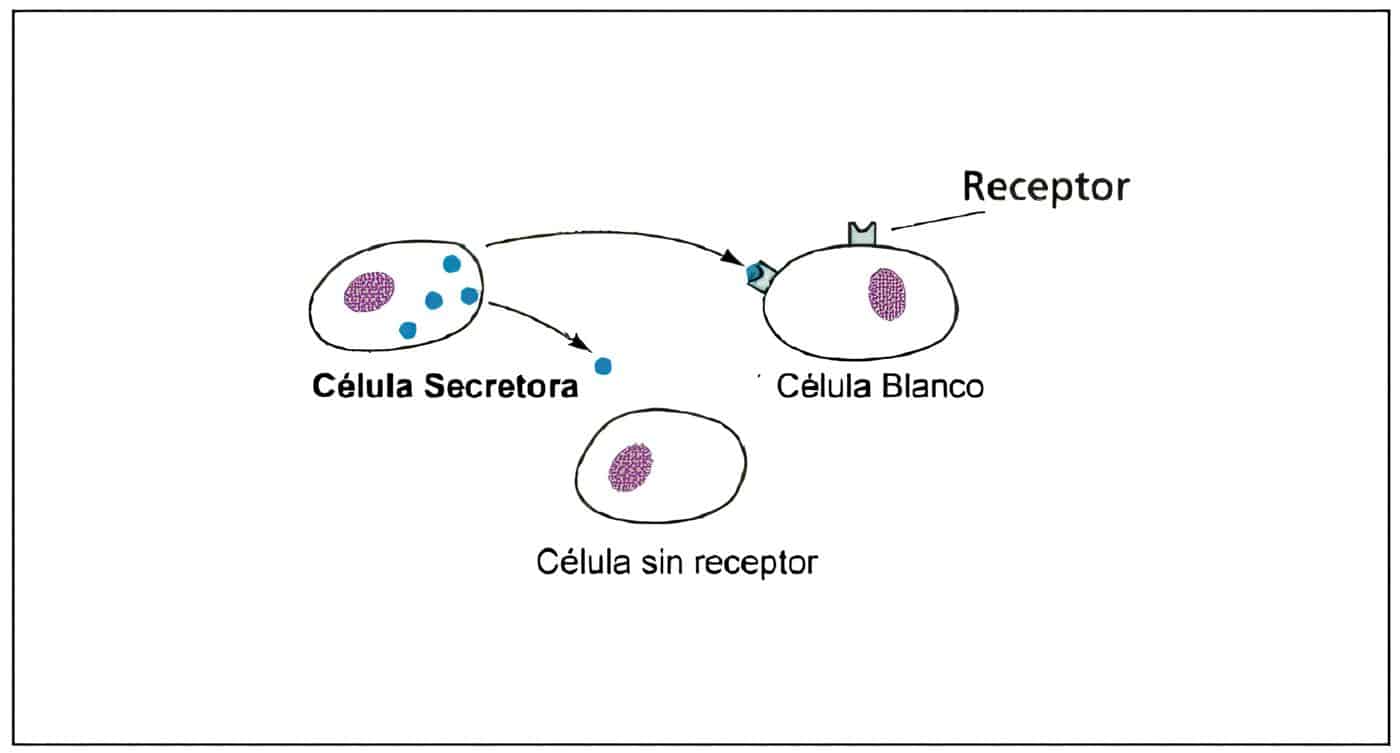
Este tema ha sido ya tratado en detalle en el capítulo de anovulación. Como existe similitud entre los receptores para insulina y para IGF-I, la hiperinsulinemia puede conducir a un aumento en la producción de andrógenos en las células de la teca.
La hiperinsulinemia contribuye al hiperandrogenismo inhibiendo la síntesis hepática de SHBG y de IGFBP-1, acciones que aumentan los niveles de testosterona libre e incrementan la estimulación del IGF-I sobre las células tecales para mayor producción de andrógenos. Además se cree que tanto la insulina como el IGF-I pueden tener un efecto estimulador sobre la actividad de la 5a-reductasa.
El único tratamiento que ha mostrado algún efecto benéfico en la hiperinsulinemia es la reducción de peso. Desafortunadamente el laboratorio hasta el momento no cuenta con unos exámenes confiables que permitan comprobar el diagnóstico de hiperinsulinemia; no existen guías precisas que permitan analizar los resultados de insulina basal y su respuesta a la estimulación con glucosa.
Se acepta que una proporción glucosa en ayunas/insulina en ayunas menor de 3 puede ser útil para identificar a las pacientes con hiperinsulinemia significativa. Como la única medida terapéutica consiste en la disminución de peso, no hay justificación para hacer este examen de laboratorio en forma rutinaria, ya que no cambiará el manejo.
Hiperplasia suprarrenal de comienzo tardío
La DHEAS es el andrógeno que se encuentra en mayor concentración en la circulación; procede en forma casi exclusiva de la secreción suprarrenal, por lo cual es útil como medida directa de la función suprarrenal; tiene correlación clínica adecuada con los 17-cetoesteroides urinarios. Se acepta como normal un valor inferior a 350 mg/dl.
El envejecimiento está asociado a una disminución en la concentración sanguínea de DHEAS, descenso observado después de la menopausia, llegando a valores indetectables después de los 70 años.
Tanto los 17-cetoesteroides urinarios como la DHEAS se encuentran elevados en pacientes con hiperprolactinemia; su valores vuelven al rango normal después de la supresión con agonistas de la dopamina. Estos cambios en los andrógenos probablemente son secundarios al estado anovulatorio persistente, aunque puede haber efectos directos de la prolactina sobre la glándula suprarrenal, el ovario o la SHBG.
Cuando la DHEAS se encuentra normal, la posibilidad de enfermedad suprarrenal es poco probable y lo más seguro es que se trate de un exceso de producción de andrógenos en el ovario. Solo hay casos raros de tumores suprarrenales con valores normales de DHEAS y la su investigación estaría indicada cuando hay una elevación importante de los valores de testosterona. Esos tumores responden a la estimulación con LH, sugiriendo que son derivados de restos de células embrionarias.
La hiperplasia suprarrenal de comienzo tardío generalmente no está asociada a un aumento importante en la DHEAS. Esta hormona se puede encontrar ligeramente elevada en pacientes anovulatorias con ovarios poliquísticos. Un valor de DHEAS superior a 700 mg/dl ha sido propuesto como el marcador para la función anormal de la suprarrenal; en la práctica clínica este valor se encuentra en muy pocas oportunidades y no cambia el manejo.
En los trastornos suprarrenales el punto final es el aumento en la concentración de testosterona:
Ya sea por producción directa o por conversión periférica de DHEA; por lo tanto, en ausencia de síndrome de Cushing se considera que la medición de testosterona es suficiente para descartar patología suprarrenal y que al parecer no justificaría medir en forma rutinaria la DHEAS.
Dentro de las alteraciones adrenales acompañadas de hirsutismo la más importante es la hiperplasia suprarrenal congénita de comienzo tardío. Se produce por un defecto enzimático que lleva a una producción excesiva de andrógenos.
Las enzimas comprometidas con mayor frecuencia son la 21 – hidroxilasa (P450c21), la 11b-hidroxilasa (P450c11) y la 3b-hidroxiesteroide deshidrogenasa. Es transmitida por un gene autosómico recesivo. En la forma de comienzo tardío no hay manifestaciones hasta la pubertad.
A medida que la suprarrenal se activa con la maduración puberal hay hirsutismo progresivo y ocasionalmente virilización. La deficiencia relativa de cortisol lleva por retroalimentación negativa al aumento de la ACTH; de esta manera se aumentan los precursores de cortisol y por ende los andrógenos adrenales.
La forma más frecuente es la deficiencia de 21-hidoxilasa. La severidad de la expresión clínica es explicada por el concepto de las variables alélicas. El diagnóstico puede ser comprobado con los niveles de 17-OHP; justifica comprobarlo ya que requiere un manejo diferente y a largo plazo.
En casos de embarazo es conveniente la consejería genética para el diagnóstico prenatal y posiblemente instaurar el tratamiento en los casos severos e impedir la masculinización de un feto femenino.
El defecto enzimático de la 3b-hidroxiesteroide deshidrogenasa está presente tanto en los ovarios como en las suprarrenales. Este defecto produce un aumento significativo en las concentraciones de andrógenos aunque la actividad de la enzima parece ser normal en los tejidos periféricos.
El hirsutismo visto en estas pacientes probablemente es secundario a la conversión periférica de precursores en los órganos blanco.
Hasta el momento no existen marcadores genéticos que nos aproximen a la enfermedad. El diagnóstico se puede comprobar con la estimulación con ACTH exógena, demostrando un aumento entre la proporción de 17-hidroxipregnenolona y 17-OHP.
La deficiencia de 11b-hidroxilasa es bastante rara. Generalmente se diagnostica en edades más tempranas. Por su baja frecuencia no justifica medir en todas las pacientes con hirsutismo la respuesta del 11-deoxicortisol a la estimulación con ACTH.
Entre el 1 y el 5% de las mujeres tienen una respuesta bioquímica consistente con una hiperplasia suprarrenal de comienzo tardío. Esto hace indispensable la medición de 17-OHP en todas las pacientes.
Cuando existe la historia familiar de aumento de andrógenos, se debe pensar en la posibilidad de un defecto congénito. El hirsutismo en estos casos es más severo y generalmente su comienzo es más temprano, típicamente en la pubertad. La baja estatura y los niveles sanguíneos muy elevados de andrógenos son indicativos de un trastorno más severo.
La 17-OHP debe medirse en las horas de la mañana para evitar las variaciones de la secreción diurna de ACTH. El nivel basal debe ser inferior a 200 ng/dl. Niveles entre 200 y 800 ng/dl requieren de la prueba de estimulación con ACTH; niveles superiores a 800 ng/dl confirman el diagnóstico de deficiencia de 21-hidroxilasa.
El nivel de DHEAS generalmente es normal. La ACTH sintética se administra en dosis de 250 mg intravenosos; se mide luego el nivel de 17-OHP una hora después; en pacientes portadores de la deficiencia, los valores pueden llegar a 1000 ng/dl; en la hiperplasia de comienzo tardío están por encima de 1200 ng/dl.
Para el diagnóstico de la deficiencia de 3b-hidroxiesteoride deshidrogenasa se realiza la estimulación con ACTH de forma similar, midiendo y haciendo la relación 17-hidroxipregnenolona/17-OHP; se sospecha la enfermedad cuando la relación es superior a 6; en estos casos puede haber una elevación marcada de la DHEAS, con niveles de testosterona normales o ligeramente aumentados.
(Lea También: Tratamiento de Hirsutismo)
La glándula suprarrenal y la anovulación
Siempre ha existido la duda del compromiso de la glándula suprarrenal en pacientes con anovulación. La primera pregunta es si la anovulación es secundaria al aumento de producción de andrógenos en la suprarrenal. Una posibilidad es que el aumento en la actividad de la suprarrenal, marcado por la mayor producción de DHEA sea debido a una insuficiencia de la 3b-hidroxiesteroide deshidrogenasa inducida por los estrógenos.
Se llegaría a un estado similar al de la suprarrenal fetal: disminución de esta enzima por el alto contenido de estrógenos. Un dato inconsistente con esta explicación es que los niveles de ACTH no se elevan; esto podría explicarse porque la actividad de esta enzima es inhibida tanto por los andrógenos como por los estrógenos en concentraciones esperadas en el interior de la suprarrenal pero difíciles de alcanzar con la administración exógena.
Por lo tanto los cambios en la secreción adrenal pueden mostrar acciones variables de los esteroides, especialmente los estrógenos, en capas diferentes de la corteza suprarrenal sin que induzcan cambios en la ACTH.
Se ha tratado de frenar la producción ovárica con análogos de la GnRH para medir la función suprarrenal en estas condiciones.
Hasta el momento los estudios reportados no han demostrado ningún impacto en la producción suprarrenal de andrógenos.
Sin que haya diferencias en peso, dieta, raza o factores ambientales, la actividad androgénica suprarrenal está aumentada hasta en las dos terceras partes de las mujeres anovulatorias y la hiperinsulinemia se puede encontrar hasta en 70% de ellas. Parece que existe alguna modulación por parte de los factores de crecimiento tanto en la suprarrenal como en las células del ovario.
Las mujeres con ovario poliquístico e hiperinsulinemia tienen una mayor respuesta esteroidogénica a la ACTH que aquellas mujeres anovulatorias con insulina normal.
Tanto los receptores para insulina como para IGF-I están presentes en las células de la glándula suprarrenal. Al parecer la infusión de insulina induce una disminución en la producción de DHEAS y la hiperinsulinemia inhibe la actividad de la 17,20-liasa (P450c17), sugiriendo que la insulina reduce la producción de este andrógeno adrenal.
Tumores productores de andrógenos
Los niveles normales de testosterona en plasma son de 20 a 80 ng/dl; se pueden encontrar elevados en la mayoría de mujeres (70%) con anovulación e hirsutismo. Los niveles de la SHBG se encuentran disminuidos ante el aumento de andrógenos e insulina.
A pesar del aumento en la testosterona libre, la testosterona total puede estar en el rango normal. Se acepta que en la mujer con hirsutismo un nivel normal de testosterona total es consistente con un aumento en la tasa de producción de andrógenos.
No es necesario medir la testosterona libre, ya que la total sirve en forma adecuada para evaluar los tumores productores de testosterona, casos en los cuales su nivel es superior a los 200 ng/dl.
Se debe sospechar la presencia de un tumor productor de andrógenos en dos situaciones. La primera es cuando ocurre masculinización de progresión rápida. La segunda es cuando se encuentra la testosterona total por encima de 200 ng/dl.
La mayoría de tumores ováricos funcionantes son palpables. Se recomienda la laparotomía con extirpación quirúrgica de la masa. Siempre se debe tener en cuenta que tumores pequeños localizados hacia el hilio pueden secretar testosterona. Ocasionalmente se puede encontrar virilización con tumores no funcionales debido a la estimulación de la secreción de andrógenos por las células del estroma que están alrededor del tumor.
El dilema diagnóstico se presenta cuando no hay una masa palpable.
Se sabe que las pruebas de estimulación y supresión no son muy confiables en estos casos. La mayoría de tumores ováricos productores de andrógenos responden a la LH, por lo cual responderán a la estimulación y supresión ovárica.
La angiografía selectiva con muestras venosas selectivas de esteroides tanto adrenales como ováricos es un procedimiento invasivo no exento de riesgos; técnicamente es difícil lograr la cateterización bilateral de los ovarios; la secreción de esteroides es episódica.
Cuando se sospecha un tumor productor de andrógenos en ausencia de una masa ovárica palpable se recomienda utilizar técnicas de imágenes diagnósticas de los ovarios y las glándulas suprarrenales, incluyendo ecografía y TAC. La imagenología de la suprarrenal es bastante sensible para pequeñas masas que producen síndrome de Cushing y adenomas virilizantes.
El tumor primario de la suprarrenal generalmente está asociado con una secreción excesiva de glucocorticoides y andrógenos. El tamaño de la lesión es significativo, ya que está directamente relacionado con la posibilidad de malignidad: cuando es de 2 cm de diámetro la probabilidad de malignidad es del 20%, mientras que si tiene 8 cm, su probabilidad es del 80%.
Lesiones bilaterales menores de 3 cm generalmente son debidas a enfermedades metastásicas. La recomendación actual es explorar las masas unilaterales mayores de 3 cm. La aspiración con aguja fina está recomendada en aquellas masas suprarrenales unilaterales.
El seguimiento se hace con imágenes diagnósticas a los 3, 9 y 18 meses. Cualquier masa que no ha sufrido cambios en este lapso puede dejarse en observación.
El hallazgo incidental de una masa suprarrenal requiere investigación bioquímica.
La presencia de hipertensión debe hacer sospechar síndrome de Cushing, hiperaldosteronismo o feocromocitoma.
La evaluación debe incluir pruebas de tamizaje para feocromocitoma como catecolaminas plasmáticas después de la administración de clonidina, electrolitos, actividad de renina, cortisol libre en orina de 24 horas y niveles de andrógenos.
TABLA 8.2
Causas neoplásicas de hiperandrogenismo
| OVÁRICAS Tumores de la granulosa-teca corresponden a 15-20% Tumores gonadales estromales (arrenoblastomas) Tumores de Sertoli-Leydig Tumores de células del hilio Tumores de restos adrenales Disgerminomas Gonadoblastomas Luteoma del embarazo No funcionales Metastásicos |
| ADRENALES Adenoma: produce DHEA-S Adenoma “puro”: secretor de testosterona Adenoma-ganglioneuroma |
| OTROS |
Hirsutismo idiopático
Hay un grupo de pacientes en las cuales hay hirsutismo pero tienen ovulación regular, no hay tumores ni alteraciones suprarrenales. Se ha llamado el hirsutismo idiopático familiar, siendo más marcado en algunas zonas geográficas. La única explicación hasta el momento es el aumento en la actividad de la 5a-reductasa.
Incluso en estos casos el hirsutismo responde a la supresión ovárica con anticonceptivos orales o al uso de espironolactona. La respuesta clínica al tratamiento se ha relacionado con los niveles de 3a-androstenediol glucorónido, la cual confirma el diagnóstico del problema a nivel del órgano blanco.