Dr. Germán Barón Castañeda, M.D.
Como principio general podemos plantear que el hirsutismo es un problema cosmético grave para la mujer. Los tratamientos cosméticos no alteran el medio ambiente hormonal, por lo cual después de practicados se observa de nuevo su crecimiento.
Por otro lado, el manejo hormonal impide el crecimiento de nuevos vellos pero no altera los que ya se han formado. Por este motivo no se recomienda el manejo cosmético coadyuvante antes de seis meses de iniciada la terapia específica; el método que mejores resultados ha dado ha sido la electrólisis. Los tratamientos médicos deben realizarse por lo menos durante seis meses, aunque es recomendable el lapso de 2 años.
La mayoría de pacientes que presentan hirsutismo tienen un aumento en la producción de andrógenos debida a un estado anovulatorio persistente. El manejo pretende romper este círculo. En aquellas pacientes con deseo de embarazo se puede hacer la inducción de la ovulación con cualquiera de los esquemas disponibles. En las mujeres que no desean embarazo se debe suprimir la esteroidogénesis ovárica usando el efecto inhibitorio de los agentes progestacionales sobre la LH.
Anticonceptivos orales y progestágenos
La producción de andrógenos en las mujeres con hirsutismo generalmente es dependiente de LH; por lo tanto la supresión de la esteroidogénesis ovárica depende de una adecuada supresión de la LH.
Para este fin es muy adecuada la porción progestacional de los anticonceptivos orales. Además, su contenido de estrógenos permite aumentar el nivel de SHBG, lo cual lleva a una mayor captación de los andrógenos con una disminución en la testosterona libre. El progestágeno inhibe la 5a-reductasa en la piel, contribuyendo así a la mejoría clínica.
Teóricamente las fórmulas que contienen desogestrel, gestodeno y norgestimato están asociadas con un mayor aumento en la concentración de SHBG y por lo tanto con una mayor disminución de los niveles de testosterona libre. Estos productos serían más efectivos en el tratamiento del acné y el hirsutismo, pero todavía faltan más estudios clínicos para comprobar el hecho.
La supresión de la testosterona continúa por 6 meses a 2 años después de haber suspendido el tratamiento. Si el estado anovulatorio regresa, se puede esperar la reaparición del hirsutismo.
Cuando existe contraindicación para el uso de anticonceptivos puede ser útil el acetato de medroxiprogesterona 150 mg intramusculares cada 3 meses o 30 mg orales diarios. Su mecanismo de acción es algo diferente. La supresión de las gonadotropinas es menos intensa, por lo cual persiste algún grado de actividad folicular.
La supresión de LH es significativa y con ella se logra la disminución en la producción de testosterona, aunque en menor grado que los anticonceptivos. Se aumenta la tasa de depuración de la testosterona por inducción de la actividad enzimática en el hígado.
El acetato de medroxiprogesterona disminuye la SHBG, pero el efecto neto es que la supresión de la producción de testosterona es mayor, por lo cual su concentración libre disminuye.
Cuando se utilizan anticonceptivos orales o agentes progestacionales se logra también una inhibición de los niveles de DHEAS. Aunque no se conoce exactamente el mecanismo, se cree que la secreción de DHEAS se ve aumentada en el estado hiperestrogénico persistente de la anovulación; al cambiar el medio ambiente endocrino de la glándula suprarrenal se restaurará la actividad normal de secreción de este andrógeno.
Se postula que estos esquemas alteran la liberación de ACTH o la respuesta de la suprarrenal. La efectividad de la supresión suprarrenal puede ser debida a una disminución de los andrógenos circulantes que lleva a una disminución en la cantidad de DHEAS disponible para la conversión a testosterona en el folículo ovárico.
En las mujeres mayores cuando no hay más deseo de fertilidad, el uso continuo de esteroides puede aumentar sus riesgos relacionados con la edad y se debe considerar la posibilidad de la ooforectomía bilateral, especialmente cuando hay hirsutismo progresivo y severo. Las pacientes con hipertecosis responden pobremente a la supresión hormonal, por lo cual también son candidatas al manejo quirúrgico.
Hay que tener presente la posibilidad de la hiperinsulinemia en estas pacientes. Se sabe que no responden en forma tan adecuada al manejo hormonal, por lo cual está recomendado el manejo dietético coadyuvante.
Espironolactona
La espironolactona es un diurético antagonista de la aldosterona; potente antiandrógeno, débil progestágeno y débil inhibidor de la síntesis de testosterona. Inhibe la biosíntesis ovárica y suprarrenal de andrógenos, compite con el receptor de andrógenos en el folículo piloso e inhibe directamente la actividad de la 5a-reductasa.
La inhibición de la esteroidogenésis se logra a través de su efecto sobre el sistema del citocromo P450 (P450c17), efecto bastante variable. Su principal acción está en el bloqueo de los receptores en el órgano blanco, ligándose a los sitios de unión específicos para la dihidrotestosterona. Esta probablemente es la explicación de por qué los niveles de cortisol, DHEA y DHEAS no cambian en forma significativa mientras que la androstendiona lo hace.
El impacto del tratamiento con espironolactona está directamente relacionado con la dosis. Se recomienda utilizar dosis de 100 mg dos veces al día; después de seis meses se puede disminuir a una dosis de mantenimiento de 25 a 50 mg diarios.
La respuesta es lenta y el efecto máximo no se ve antes de seis meses de tratamiento Sus efectos secundarios son mínimos, incluyendo el aumento de la diuresis los primeros días, ocasionalmente fatiga, hemorragia disfuncional, presencia de ciclos cortos, hipokalemia y reacciones alérgicas.
Si se utiliza solo espironolactona se debe recordar que no tiene protección anticonceptiva y que se desconocen sus efectos teratogénicos sobre el feto.
(Lea También: Hiperprolactinemia)
Acetato de ciproterona
La ciproterona es un progestágeno potente, antiandrógeno potente y glucocorticoide débil. Actúa uniéndose al receptor específico de la dihidrotestosterona y disminuyendo los niveles séricos de testosterona.
Reduce el nivel de 5a-reductasa en la piel y disminuye la secreción ovárica de andrógenos por inhibición de la liberación de gonadotropinas. Clínicamente el efecto es similar cuando se utilizan dosis altas de 100 mg o dosis bajas de 2 mg contenidas en anticonceptivos orales. Los efectos secundarios incluyen fatiga, edema, pérdida de la libido, aumento de peso y mastalgia.
Se observa una mejoría importante del hirsutismo facial en el tercer mes de tratamiento. Sus efectos sobre el metabolismo de carbohidratos y el perfil de lipoproteínas son similares a los observados con anticonceptivos orales de macrodosis. Se administra los días 5 a 25 del ciclo acompañado de anovulatorios orales.
Dexametasona
Suprime la secreción de ACTH endógena, por lo cual se utiliza en aquellas mujeres con deficiencias enzimáticas suprarrenales. Se administra en la noche en dosis de 0.5 mg. La dosis equivalente de prednisona de 5 a 7.5 mg también se puede utilizar.
El seguimiento se hace con niveles de cortisol plasmático en la mañana; si son menores a 2 mg/dl se debe reducir la dosis para evitar la imposibilidad de reacción ante el estrés.
Agonistas de la GnRH
Como la producción de andrógenos en el ovario es dependiente de la LH, la supresión de las gonadotropinas con estos agonistas mejora el hirsutismo. Hay resultados inconsistentes en la literatura, de manera que no se ha podido establecer la dosis necesaria para lograr una supresión efectiva y una respuesta clínica.
Se recomienda la dosis de acetato de leuprolide 3.75 mg intramuscular mensual. El tratamiento es costoso, por lo cual se reserva para los casos en los que hay hiperandrogenismo severo secundario a una hipertecosis con marcada hiperinsulinemia.
Flutamide
El flutamide es un antiandrógeno no esteroideo aprobado para el tratamiento de carcinoma de próstata. Se administra en dosis de 250 mg dos veces al día.
Inhibe el crecimiento del vello sin mayores efectos secundarios. Hasta el momento no hay estudios que comparen su uso con otros tratamientos para el hirsutismo. Siempre debe combinarse con un método anticonceptivo.
Otras drogas
Se ha utilizado la cimetidina 300 mg cuatro veces al día, siendo el menos potente de los bloqueadores del receptor androgénico y su respuesta clínica no es la más adecuada.
Las cremas con progesterona son efectivas pero deben aplicarse en forma frecuente. Su acción es muy concentrada en el lugar de aplicación.
El minoxidil tiene acciones estimuladoras directas sobre el folículo piloso. Ha sido utilizado en mujeres hirsutas con alopecia temporal. El ketoconazol en dosis de 400 mg diarios bloquea la síntesis de andrógenos por inhibición del sistema del citocromo P450; su efecto sobre el hirsutismo es bueno, pero tiene gran incidencia de efectos colaterales y cambios en las enzimas hepáticas.
Referencias
- Adams J., Paulson DW., Frank S. Prevalence of polycystic ovaries in women with anovulation and idiopathic hirsutism. Br Med J. 1986; 293: 355.
- Adashi EY. Potential utility of gonadotropin-releasing hormone agonists in the managemento of ovarian hyperandrogenism. Fertil Steril. 1990; 53: 765.
- Adashi EY., Levin PA. Pathophysiology and evaluation of adrenal hyperandrogenism. Semin Reprod Endocrinol. 1986; 4: 2.
- Andreyko JL., Monroe SE., Jaffe RB. Treatment of hirsutism with a gonadotropin-releasing hormone agonist. J Clin Endocrinol Metab. 1986; 63: 854.
- Avgerinos PC., Cutler GB., Tsokos GC., et al. Dissociation between cortisol and adrenal androgen secretion in patients receiving alternate day prednisone therapy. J Clin Endocrinol Metab. 1987; 65: 24.
- Azziz R., Boots LR., Parker CR., et al. 11b-hidroxilase diciency in hyperandrogenis, Fertil Steril. 1991; 55 :733.
- Azziz R., Bradley EL., Potter HD., et al. 3b-hidroxiesteroid deshydrogenase deficiency in hyperandrogenism. Am J Obstet Gynecol. 19993; 168: 889.
- Barbieri RL., Makris A., Randal RW., et al. Insulin stimulates androgen accumulation in incubations of ovarian stroma obtained from women with hyperandrogenism. J Clin Endocrinol metab. 1986; 62: 904.
- Barbieri RL., Smith S., Ryan KJ. The role of hyperinsulinemia in the pathogenesis of ovarian hyperandrogenism. Fertil Steril. 1988; 50: 197.
- Azziz R., Zacur HA. 21-hidroxilase deficiency in females hiperandogenism: screening and diagnosis. J Clin Endocrinol Metab. 1989; 69: 577.
- Barth JH, Cherry CA., Wojnarowska F., et al. Spironolactone is an effective and well tolerated systemic anti-androgen therapy for hirsute women. J Clin Endocrinol Metab. 1989; 68: 966.
- Barth JH, Cherry CA., Wojnarowska F., et al. Ciproterone acetate for severe hirsutism: results of a double-blind dose-ranging study. Clin Endocrinol. 1991; 35: 5.
- Belisle S., Love EJ. Clinical efficacy and safety of ciproterone acetate in severe hirsutism: results of a multicentric Canadian study. Fertil Steril. 1986; 46: 1015.
- Biffignandi D., Massacchetti C., Molinatti GM. Female hirsutism: pathophysiological considerations and therapeutic implications. Endocrin Rv. 1984; 5: 498.
- Carlstrom K., Gersschagen S., Rannevik G. Free testosterone and testosterone/SHBG index in hirsute women: a comparison of diagnostic accuracy. Gynecol Obstet Invest. 1987; 24: 256.
- Carmina E., Koyama T., Chang L., et al. Does ethnicity influence the prevalence of adrenal hyperandrogenism and insuline resistance in polycistic ovary syndrome? Am J Obstet Gynecol. 1992; 167: 1807.
- Carmina E., Lobo RA. Evidence for increase androsterone metabolism in some normal androgenic women with acne. J Clin Endocrinol Metab. 1993; 76: 1111.
- Cassidenti DL., Paulson RJ., Serafini P., et al. Effects of sex steroid on skin 5a-reductase activity in vitro. Obstet Gynecol. 1991; 78: 113.
- Chang RJ. Ovarian steroid secretion in polycistic ovarian disease. Seminars Reprod Endocrinol 1984; 2: 244.
- Chapman MG., Dowsett M., Dewhurst CJ., et al. Spironolactone in combination with an oral contraceptive: an alterantive treatment for hirsutism. Br J Obstet Gynecol. 1985; 92: 983.
- Chetkowski RJ., DeFazio J., Shamonki I., et al. The incidence of late-onset congenital adrenal hyperplasia due to 21-hidroxilase deficiency amng hirsute women. J Clin Endocrinol Metab. 1984; 58:595.
- Cheung AP., Chang RJ. Polycystic ovaries and other ovarian causes of hyperandrogenism. Infertil Reprod Clin North Am. 1991; 2:465-478.
- Christman GM., Hammond MG. Ovulation induction in the hypernadrogenic woman. Infertil Reprod Clin North Am. 1991; 2:547-560.
- Cumming DC., Yang JC., Rebar RW., et al. Treatment of hirsutism with spironolactone. JAMA. 1982; 247:1295.
- Cusan L., Dupont A., Tremblay R., et al. Treatment of hirsutism with the pure antiandrogen flutamide. Recent Rev Gynecol Endocrinol. 1988; 1:577.
- Deaton JL. Hyperandrogenism and uterine bleeding. Infertil Reprod Clin North Am. 1991; 2:561-584.
- Dunaif A., Green G., Sutterweit W., et al. Suppression of hyperandrogenism does not improve peripheral or hepatic insuline resistance in the polycistic ovary syndrme. J Clin Endocrinol Metab. 1990;70:679.
- Faber K., Hughes CL. Laboratory evaluation of hyperandrogenic conditions. Infertil Reprod Clin North Am. 1991; 2: 495-510.
- Ferriman D., Gallway JD. Clinical assesment of body hair in women. J Clin Endocrinol Metab. 1961; 24:1440.
- Glickman SP., Rosenfield RL., Bergenstal RM., et al. Multiple androgenic abnormalities, including elevated free testosterone, in hyperprolactinemic women. J Clin Endocrinol Metab. 1982; 55:251.
- Golditch IM., Price VH. Treatment of hirsutism with cimetidine. Obstet Gynecol. 1990; 75:911.
- Gonzalez F., Hatala DA., Speroff L. Basal and dynamic responses to gonadotropin-releasing hormone agonists treatment in women with polycystic ovary with high and low dehydroepiandrosterone sulfate levels. Am J Obstet Gynecol. 1991; 165:535.
- Greet N., Hoopes M., Horton R. Androstenedione glucoronide plasma clearence and production rates in normal and hirsute women. J Clin Endocrinol Metab. 1986; 62:22.
- Gross MD., Wortsman J., Shapiro B., et al. Scintigraphic evidence of adrenal cortical dysfunction in the polycystic ovary syndrome. J Clin Endocirnol Metab. 1986; 62:197.
- Haning RV., Flood CA., Hackett RJ., et al. Metabolic clearence rate of dehidroepiandrosterone sulfate, its metabolism to testosterone, and its intrafollicular metabolism to dehydroepiandrosterone, androstenedione, testosterone, and dyhidrotestosterone in vivo. J Clin Endocrinol Metab. 1991; 72:1088.
- Haning RV., Hackett RJ., Flood CA., et al. Plasma dehydroepiandrosterone sulphate serves as a prehormone for 48% of follicular fluid testosterone during treatment with menotropins. J Clin Endocrinol Metab. 1993; 76:1301.
- Helfer LH., Miller SL., Rose EDI. Side effects of spironolactone therapy in the hirsute women. J Clin Endocrinol Metab. 1988; 66: 208.
- Herbert CM., Hill CA., Diamond MP. The use of intravenous glucose tolerance test to evaluate non-obese hyperandrogenic women. Fertil Steril. 1990; 53: 647.
- Higuchi K., Nawata H., Maki T., et al. Prolactin has a direct effect on adrenal androgen secretion. J Clin Endocrinol Metab. 1984; 59: 714.
- Horton R. Dyhidrotestosterone is a peripheral paracrine hormone. J Androl. 1992; 13:23.
- orton R., Hawks D., Lobo R. 3a, 17b-androstanediol glucoronide in plasma: a marker of androgen action in idiopathic hirsutism. J Clin Invet. 1982; 69:1203.
- Hutchinson-Williams KA. Androgenic effects in normal and hyperandrogenic women. Infertil Reprod Clin North Am. 1991; 2: 455-464.
- Jung-Hoffman C., Cuhl H. Divergent effects of two low-dose oral contraceptive on sex hormone-binding globulin and free testosterone. Am J Obstet Gynecol. 1987; 156:199.
- Kaufman FR., Gentzschein E., Stanczyk SZ., et al. Dehydroepiandrosterone and dehydroepiandrosterone sulfate in human genital skin. Fertil Steril. 1990; 54:251.
- Killinger DW., Perel D., Daniilescu D., et al. Influence of adipose tissue distribution on the biological activity of androgens. Ann N Y Acad Sci. 1990; 595:199.
- Kirschner MA., Samojlik E., Szmal E. Clinical usefulness of plasma androstenediol glucoronide measurements in women with idiopathic hirsutism. J Clin Endocrinol Metab. 1987; 65:597.
- Kuttenn S., Couillin P., Girard F., et al. Late-onset adrenal hypperplasia in hirsutism. New Engl J Med. 1985; 313:224.
- Lanzone A., Fulghegu AM., Guido M., et al. Differential androgen response to adrenocorticotropic hormone stimulation in polycistic ovarian syndrome: relationship with insulin secretion. Fertil Steril. 1992; 58:296.
- Lissak A., Sorokin Y., Calderon I., et al. Treatment of hirsutism with cimetidine: a prospective randomized controlled trial fertil Steril. 1989; 51:247.
- Levy MJ. Hirsutism. Infertil Reprod Clin North Am. 1995; 6:215.
- Lobo RA. Hisrutism and virilism. En Carr BR., Blackwell RE. Textbook of reproductive medicine. Appleton & Lange (1a). 1993; 371-387.
- Lobo RA., The role of the adrenal in polycistic ovary syndrome. Seminars Reprod Endocrinol. 1984; 2:251.
- Lobo RA., Paul WL., Gentzschein P., et al. Production of 3a-androstanediol glucroronide in human genital skin. J Clin Endocrinol Metab. 1987; 65:711.
- Lobo RA., Paul WL., Goeblesmann U. Dehydroepiandosterone sulfate as an indicator of adrenal androgen function. Obstet Gynecol. 1981; 57:69.
- Lobo RA., Shoupe D., Serafini P., et al. The effects of two doses of spironolactone on serum androgens and anagen hair in hirsute women. Fertil Steril 1985; 43:200.
- Marcondes JAM., Minnani SL., Luthold WW., et al. Treatmenr of hirsutism in women with flutamide. fertil Steril 1992; 57: 543.
- Marcondes JAM., Wajchenberg BL., Abujamra AC., et al. Monthly cyproterone acetate in the treatment of hirsute women: clinical and laboratory effects. Fertil Steril. 1990; 53:40.
- Martikainen H., Heikkinen J., Ruokonen A., et al. Hormonal and clinical effects of ketoconazole in hirsute women. J Clin Endocrinol Metab. 1988; 66:987.
- Marynick SP., Chakmakjian ZH., McCaffree DL., et al. Androgen excess in cystic acne. New Engl J Med. 1983; 308-981.
- Matteri RK., Stanczyk FZ., Gentzschein EE., et al. Androgen sulphate and glucoronide conjugates in non-hirsute and hirsute women with polycystic ovarian syndrome. Am J Obstet Gynecol. 1989; 161:1704.
- Meikle AW. A diagnostic approach to Cushing’s syndrome. Endocrinologist. 1993; 3:311.
- Miller JA., Jacobs HS. Treatment of hirsutism and acne with ciproterone acetate. Clin Endocrinol Metab. 1986; 15:373.
- Moltz L., Schwartz U. Gonadal and adrenal androgen secretion in hirsute females. Clin Endocrinol Metab. 1986; 15: 229.
- Nestler JE., McClanahan MA., Clore JN., et al. Insulin inhibits adrenal 17,20-lyase activity in man. J Clin Endocrinol Metab. 1992; 74:362.
- New MI. Polycystic ovarian disease and congenital and late onset adrenal hyperplasia. Endocrinol Metab Clin North Am. 1988; 17:634.
- O’Brien RC., Cooper ME., Murray RML., et al. Comparison of sequential cyproterone acetate/estrogen versus spironolactone/oral contraceptive in the treatment of hirsutism. J Clin Endocrinol Metab. 1991; 72:1008.
- Pang S. Relevance of biological properties of progestagen of oral contraceptives in treatment of androgen excess symptoms. J Clin Endocrinol Metab. 1990; 71:5.
- Paulson RJ., Serafini PC., Catalino JA., et al. Measurements of 3a-, 17b-androstenendiol glucoronide in serum and urine and the correlation with skin 5a-reductase activity. Fertil Steril 1986; 46:22.
- Pittaway DE. Neoplastic causes of hyperandrogenism. Infertil Reprod Clin North Am. 1991; 2:531-546.
- Pittaway DE., Maxson WS., Wentz AC. Spironolactone in combination drug therapy for unresponsive hirsutism. Fertil Steril. 1985; 43:878.
- Reiner BJ., Donohoue PA., Migeon CJ., et al. Serum 3a-androstenediol glucoronide measurements in sexually mature women with congenital adrenal hyperplasia during therapy. j Clin Endocrinol Metab. 1989; 69:105.
- Reschef E., Wild RA. Hypernadrogenic effects on lipid metabolism. Infertil Reprod Clin North Am. 1991; 2:599-610.
- Rittmaster RS. Androgen conjugates: physiology and clinical significance. Endocr Rev. 1993; 14:121.
- Rittmaster RS. Differential suppression of testosterone and estradiol in hirsute women with the superactive gonadotropin-releasing hormone agonsit Leuprolide. J Clin Endocrinol metab. 1988; 67:651.
- Rittmaster RS. Evaluation and treatment of hirsutism. Infertil Reprod Clin North Am. 1991; 2:511-530.
- Rittmaster RS., Loriaux DL., Cutler GB. Sensitivity of cortisol and adrenal androgens to dexamethasone suppression in hirsute women. J Clin Endocrinol Metab. 1985; 61:462.
- Rittmaster RS., Thompson DL. Effect of leuprolide and dexamethasone on hair growth and hormone leveles in hirsute women: the relative importance of the ovary and the adrenal in the pathogenesis of hirsutism. j Clin Endocrinol Metab. 1990; 70:1096.
- Ross NS., Aaron DC. Hormonal evaluation of patient with an incidentally discovered adrenal mass. New Engl J Med. 1990; 323:1401.
- Scherzer WJ., Adashi EY. Adrenal hyperandrogenism. Infertil Reprod Clin North Am. 1991; 2:479-494.
- Schwartz LB., Diamond MP. The coexistence of hyperandrogenism and hyperinsulinemia: a relationship between reproductive function and carbohydrate metabolism. Infertil Reprod Clin North Am. 1991; 2:611-636.
- Serafini P., Ablan F., Lobo RA. 5a-reductase activity in the genital skin of hirsute women. J Clin Endocrinol Metab. 1985; 60:349.
- Serafini P., Lobo R. Increased 5a-reductase acivity in idiopathic hirsutism. Fertil Steril. 1985; 43:74.
- Serafini P., Lobo RA. The effects of spironolactone on adrenal steroidogenesis in hirsute women. Fertil Steril. 1985; 44: 595.
- Serafini P., Lobo RA. Prolactin modulates peripheral androgen metabolism. Fertil Steril. 1986:45:41.
- Speroff L., Glass RH., Kase NG. Hirsutism. En Speroff L., Glass RH., Kase NG. Clinical Gynecologic Endocrinology and Infertility. Ed. Williams & Wilkins (5a), 1994; 483-513.
- Spritzer P., Billaud L., Thalabarb JC., et al. Cyproterone acetate versus hydrocortisone treatment in late-onset adenal hyperplasia. J Clin Endocrinol Metab. 1990; 70:642.
- Tiitinen A., Bekonen F., Stenman UH., et al. Plasma androgens and estradiol durin oral glucose tolerance test in patients with polycystic ovaries. Hum Reprod. 1990; 5:242.
- van der Vangen N., Blankenstin MA., Kloosterboer HJ., et al. Effects of seven low-dose combined oral contraceptives on sex hormone binding globulin, corticosteroid binding globulin, total and free testosterone. Contraception. 1990; 41: 345.
- Ordas J. Androgenismos femeninos. En Vanrell JA., Calaf J., Balasch J., Viscasillas P. Fertilidad y esterilidad humanas. Salvat (1a). 1992: 149-167.
- Venturoli S., Fabbri R., Dal Prato L., et al. Ketoconazole therpapy for women with acne and/or hirsutism. J Clin Endocrinol Metab. 1990; 71:335.
- Wiebe RH., Morris CV. Effect of an oral contraceptive ona drenal and ovarian androgenic steroids. Obstet Gynecol. 1984; 63: 12.
- Wild RA., Applebaum-Bowden D., Demers LM., et al. Lipoprotein lipids in women with androgen excess: independent associations with increase insulin and androgen. Clin Sem. 1990; 36:283.
- Wild RA., Bartholomew M., Applebaum-Bowden D., et al. Evidence of heterogenous mechanism in lipoprotein lipid alterations in hyperandrogenic women. Am J Obstet Gynecol. 1990; 163:1998.
- Wild RA., Grubb B., Hartz A., et al. Clinical signs of androgen excess and risk factor for coronary artery disease. Fertil Steril. 1990; 54:255.
- Wild RA., Umstot ES., Andersen RN., et al. Adrenal function in hirsutism: II. Effects of an oral contraceptive. J Clin Endocrinol Metab. 1982; 54:676.
- White PC., New MI., Dupont B. Congenital adrenal hyperplasia. New Engl J Med. 1987; 316:1519.
- Wortsman J., Khan MS., Rosner W. Suppression of testosterone-estradiol binding globulin by medroxiprogestoerne acetate in polycistic ovary syndorme. Obstet Gynecol. 1986; 67:705.
- Yanovski JA., Cutler GB., Chrousos GP, et al. Cortictotropin-releasing hormone stimulation following low-dose dexametasone administration. JAMA 1993; 269:2232.
- Yen SCC. Anovulación crónica causada por trastornos endocrinos periféricos. En Yen SSC., Jaffe RB. Endocrinología de la reproducción. Ed. Panamericana (3a). 1993: 614-620.
- Young RL., Goldzieher JW., Elkind-Hirsch K. The endocrine effects of spironolactone used as an antiandoregen. Fertil Steril. 1987; 48:223.


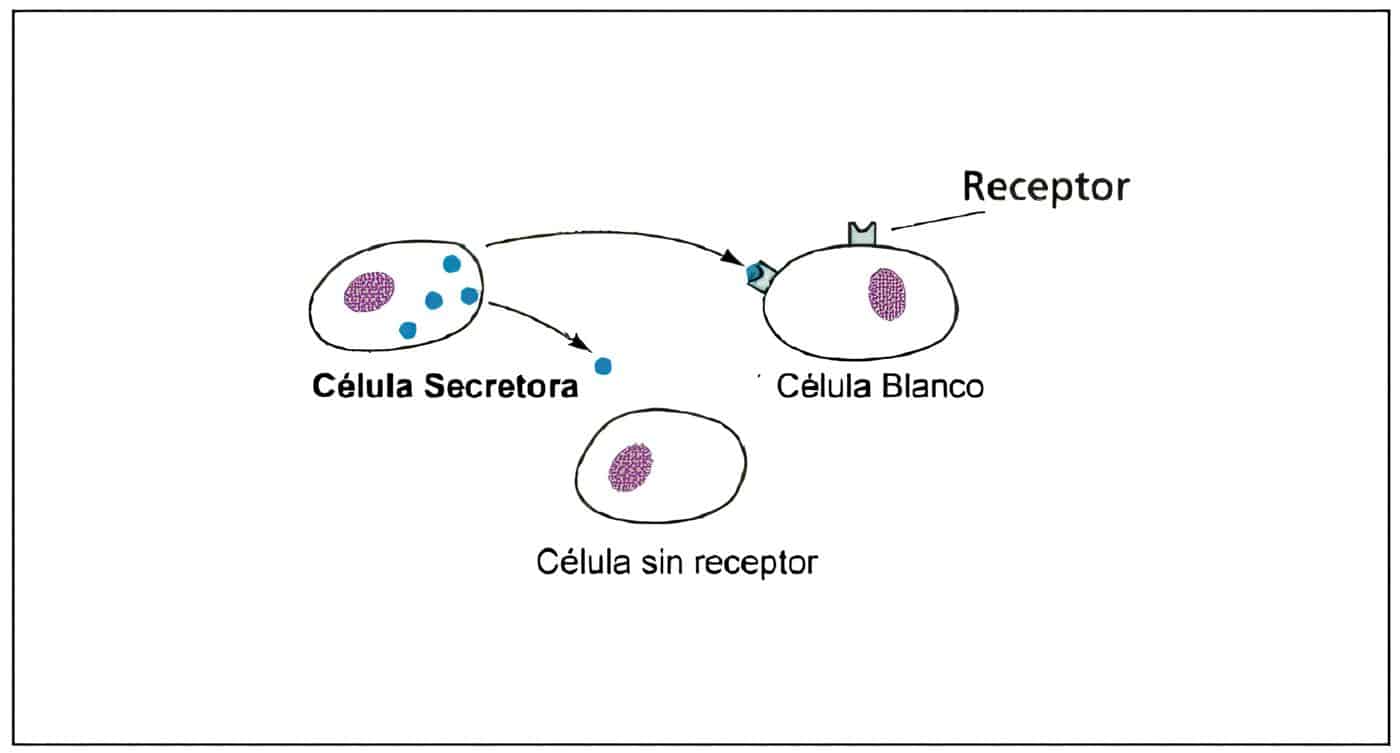


que tipo de hormonas predomina y que enfermedad pueden producir
el hirsutismo en la mujer