Capítulo II
Dr. Germán Barón Castañeda, M.D.
La relación entre el hipotálamo y la hipófisis ha atraído a los científicos desde hace muchos años. Galeno proponía que “impurezas del cerebro drenan a la nasofaringe a través de la hipófisis”. Este concepto permaneció vigente hasta el siglo XVII cuando Schneider y Lower hablan de sustancias que son destiladas de la hipófisis a la circulación.
Hace varias décadas surgió el interrogante de la posible participación del sistema nervioso central dentro del fenómeno reproductivo en la especie humana. En 1932 Hohlewg y Junkmann sugieren la posibilidad de un “centro sexual” dentro del cerebro, capaz de regular la función reproductora, pero posiblemente Stieve en 1913 es el primero en conducir una investigación científica al demostrar que las gallinas en presencia de un zorro dejan de poner huevos.
Inicialmente se creyó que la hipófisis era la “glándula maestra”, siendo luego el hipotálamo el centro de principal atracción. En forma repetitiva en las dos guerras mundiales pudo observarse cómo mujeres inducidas al estrés presentaban trastornos del ciclo e incluso amenorrea.
Se le atribuye a Ashner en 1912 ser el primero en demostrar la relación funcional:
Entre el hipotálamo y las glándulas de secreción interna al inducir la atrofia ovárica en perros luego de inyectar parafina en la región hipotalámica. Green y Harris en 1937 se convierten en pioneros en este campo, al lograr inducir la ovulación en animales a través de la estimulación eléctrica de la eminencia media del hipotálamo. En el mismo año Westman y Jacobsohn logran demostrar que la sección del tallo pituitario bloquea la ovulación.
En 1946 Markee y colaboradores observan que la estimulación eléctrica de la hipófisis no produce los mismos resultados, lo cual lleva a pensar en la existencia de sustancias producidas por el hipotálamo transportadas a través del sistema porta hipofisiario, que actúan sobre las células hipofisiarias y regulan los eventos reproductivos.
Muchos experimentos posteriores, conducidos especialmente por Schally y Guillemin, demuestran la relación directa entre hipotálamo e hipófisis; poco a poco se identifican factores estimuladores e inhibidores de la función hipofisiaria. En 1971 y 1972 los grupos de Matsuo y Burgos logran aislar y analizar la estructura de la Hormona liberadora de Gonadotropinas (GnRH).
A diferencia de la hipófisis anterior o adenohipófisis, controlada por factores producidos en el hipotálamo, la hipófisis posterior es una prolongación del hipotálamo donde residen las neuronas de los núcleos paraventricular y supraóptico que secretan oxitocina, vasopresina y neurofisinas.
Las hormonas producidas en la hipófisis son secretadas en forma episódica, algunas en relación con el ritmo circadiano, otras con la ingesta de alimentos y otras con el ciclo de luz y oscuridad.
El Sistema Hipotálamo – Hipofisiario
El hipotálamo está localizado en la base del cerebro por encima de la unión de los nervios ópticos. La eminencia media del hipotálamo es la vía final de comunicación con la hipófisis anterior. Recibe neuronas del tracto túbero-infundibular.
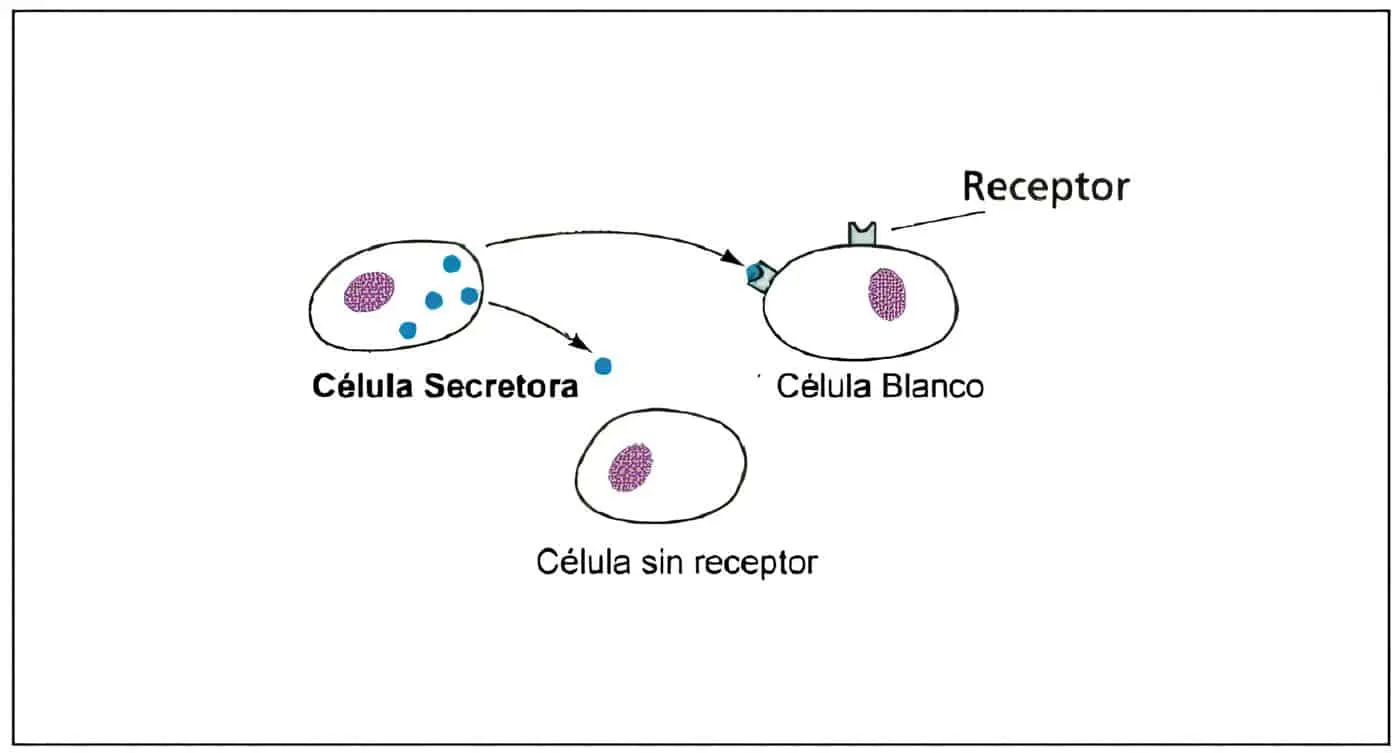
Los factores producidos en él, neurohormonas, son transportados por los capilares portales hacia la hipófisis, donde actúan a través de receptores específicos. La circulación en este sistema porta es del cerebro hacia la hipófisis, aunque existe también un flujo retrógrado que permite el transporte de hormonas hipofisiarias hacia el hipotálamo.
La influencia que ejerce el hipotálamo sobre la hipófisis es mediada por una serie de agentes neuroendocrinos que tienen efecto estimulador sobre la hormona de crecimiento, la TSH, la ACTH y las gonadotropinas; representan las neurohormonas individuales del hipotálamo. La neurohormona que controla la secreción de prolactina, llamada por algunos hormona inhibitoria de la prolactina, probablemente es la dopamina.
Además de sus acciones en la hipófisis se ha demostrado que varias neurohormonas influyen sobre el comportamiento. Por ejemplo la TRH antagoniza el efecto sedante de varias drogas y tiene un efecto antidepresivo en humanos. La GnRH induce la conducta del apareamiento.
Inicialmente las investigaciones de fisiología reproductiva trataron de encontrar dos factores hipotalámicos para el control de la secreción de FSH y LH, pero en la actualidad se acepta que es solo uno, la GnRH.
La secreción de GnRH se realiza en forma pulsátil, similar a lo que ocurre con las gonadotropinas. La liberación de FSH y LH depende de la frecuencia y amplitud de los pulsos de GnRH, siendo fisiológicos entre 60 y 90 minutos. Esos pulsos tienen características diferentes durante el ciclo ovárico, siendo de baja amplitud y alta frecuencia durante la fase folicular, mientras que en la fase lútea son de alta amplitud y baja frecuencia. Si la frecuencia es menor se produce anovulación y si es mayor o continua se frena la liberación de gonadotropinas.
Otra función primordial de la GnRH es el control de la producción de cadenas a y b de la LH, de la subunidad b de la FSH y la unión de las dos cadenas. Estudios realizados en las últimas décadas han sugerido que la GnRH no solo influye en la síntesis sino también en la bioactividad de las gonadotropinas. De acuerdo con la frecuencia y amplitud de los pulsos interviene en la síntesis de cadenas b, de manera que a mayor amplitud y frecuencia es mayor la producción de LH.
Los neurotransmisores clásicos son secretados en la terminal nerviosa. Los péptidos cerebrales requieren que dentro del cuerpo neuronal existan los fenómenos de transcripción, traducción y procesamiento post-traducción; el producto final es transportado a través del axón para su secreción. Las moléculas así producidas sirven como precursores para varios péptidos activos.
(Lea También: Secreción Hipofisiaria de Gonadotropinas)
Secreción de Prolactina
La expresión de los genes de prolactina ocurre en los lactotropos de la hipófisis, en el endometrio decidualizado y en el miometrio.
La secreción de prolactina está principalmente bajo el control de la dopamina, acción mediada por receptores que inhiben la adenilciclasa. Aumenta la actividad biológica de los lisosomas, lo cual dificulta la secreción de los gránulos que contienen prolactina. Además bloquea la síntesis de fosfoinositol, el recambio de fosfolípidos y la liberación de ácido araquidónico, acciones que frenan la secreción de prolactina.
Hay varios factores que aumentan su secreción, entre los cuales se pueden nombrar el estrés, la succión, la TRH, la vasopresina, la oxitocina y los ritmos circadianos. El efecto del estrés puede estar mediado a través del péptido intestinal vasoactivo, mientras que la TRH tiene su propio receptor en la superficie del lactotropo.
Los estrógenos aumentan en forma importante la secreción de prolactina, efecto que puede ser el reflejo de una acción hipotalámica por freno de la dopamina y otra a nivel hipofisiario, interviniendo directamente en el mecanismo lisosómico.
La prolactina, actuando a través de un sistema de retroalimentación negativa, no solo bloquea su propia producción sino la de GnRH.
Secreción de GnRH
Dentro del hipotálamo hay células nerviosas peptidérgicas que secretan las hormonas liberadoras e inhibitorias. Estas células comparten características de neuronas y de células endocrinas. Responden tanto a señales del torrente circulatorio como a neurotransmisores.
Las células productoras de GnRH se originan en el área olfatoria. Durante la embriogénesis migran hacia su principal localización en el núcleo arcuado del hipotálamo. Las neuronas aparecen en la placa olfatoria y entran al cerebro con las terminaciones de un nervio craneal que se proyecta de la nariz al núcleo septal-preóptico.
Las neuronas productoras de GnRH no están agrupadas en núcleos separados sino formando redes laxas diseminadas en el hipotálamo, especialmente en el núcleo paraventricular posterior, el hipotálamo medio basal y el área preóptica; la mayoría están localizadas en el núcleo arcuado. Sus axones se proyectan hacia muchas áreas en el cerebro, pero especialmente hacia la eminencia media, a través del tracto túbero-infundibular.
La GnRH es un decapéptido derivado de la transcripción de una molécula precursora, la pre-pro-GnRH.
El precursor consta de 92 aminoácidos; 23 iniciales que actúan como secuencia de señal y una secuencia de Gly-Lis-Arg indispensable para el procesamiento de la molécula de GnRH. El residuo de 56 aminoácidos es conocido como péptido asociado con la GnRH (GAP), molécula que posiblemente interviene en la inhibición de la prolactina. Este péptido es codificado por un solo gen localizado en el brazo corto del cromosoma 8.
La vida media de la GnRH es solo de 2 a 4 minutos y su ingreso a la circulación general es muy bajo; por lo tanto se requiere de la secreción continua para el control del ciclo reproductivo. A su vez, esta función depende de la interacción con otras sustancias por mecanismos de retroalimentación. El asa larga de retroalimentación hace referencia al efecto ejercido por las hormonas producidas en la célula blanco; ocurre tanto a nivel hipofisiario como hipotalámico. El asa corta indica la retroalimentación negativa que ejercen las hormonas hipofisiarias sobre su propia secreción, inhibiendo posiblemente la secreción de hormonas liberadoras en el hipotálamo. La retroalimentación ultracorta es la inhibición que en el hipotálamo ejerce la hormona liberadora sobre su propia síntesis.
El tracto dopaminérgico
Neuronas productoras de dopamina se encuentran en los núcleos arcuado y paraventricular. El tracto dopaminérgico túbero-infundibular se extiende desde el hipotálamo medio basal hacia la eminencia media. A diferencia de las otras neuronas dopaminérgicas, las túbero-infundibulares no tienen receptores para dopamina pero sí para prolactina.
Se cree que la dopamina puede inhibir directamente la actividad de GnRH en el núcleo arcuado y al ser transportada por la circulación portal inhibe la prolactina a nivel hipofisiario.
Aparentemente la GnRH puede tener un efecto directo de estimulación sobre la secreción de prolactina, acción que representa una interacción paracrina entre los gonadotropos y los lactotropos en la hipófisis.
El tracto noradrenérgico
Las neuronas que sintetizan norepinefrina están localizadas en el mesencéfalo y parte baja del tallo cerebral, sintetizan también serotonina. Sus axones terminan en varias estructuras incluyendo el hipotálamo.
Las catecolaminas modulan la liberación pulsátil de GnRH. Se cree que la noradrenalina tiene efecto estimulador, mientras que la serotonina y la dopamina son inhibidores.