¿Cuáles son los Gérmenes más Frecuentemente Aislados en IU?
Cerca del 95% de los gérmenes aislados, reportados en la literatura, son Gram Negativos de tipo entérico, sobresaliendo la Escherichia Coli. Los gérmenes Gram positivos se limitan al tipo del estafilococo y enterococo pero en su frecuencia no supera el 5%.
Escherichia Coli (76% -90%)65,69,74,82,88-90
Klebsiella (0.5% -8%)65,69,74,82,88,89
Proteus (0.5% – 6%)65,69,74,88,89
Stafilococo s,p. (1% – 5%)65,69,74
Pseudomona (2%)88,89
Enterobacter (0.8% – 5%)82,88
Enterococos (8%)88
Serratia (0.8%)88
Recomendación:
En primera instancia si se quiere iniciar tratamiento empírico para un episodio agudo de IU, previo a conocer el resultado del urocultivo, se deberán emplear antibióticos con un espectro específico contra gérmenes gram negativos de tipo entérico, aunque no desconociendo la probabilidad remota de gérmenes gram positivos tipo Staphilococo o Enterococos.
Nivel de Evidencia: Buena (series prospectivas, Estudios de pruebas diagnóstic
¿Cuál es el Tratamiento Antibiótico Específico?
Uno de los pilares fundamentales en el tratamiento de la IU es la administración de antibióticos. Estudios experimentales en modelos animales, han demostrado suficientemente que la administración pronta de antibióticos pueden prevenir o reducir significativamente las cicatrices renales91. El impacto inicial que se persigue es el de detener la replicación y disminuir la población crítica de bacterias para así prevenir el daño tisular; sin embargo es la reacción inflamatoria generada por las bacterias, y no su número absoluto, lo que modifica la aparición de cicatrices91.
De cualquier manera los fines últimos que se pretenden obtener son los de prevenir daños estructurales a largo plazo, a través fundamentalmente de la erradicación bacteriana del árbol urinario, muy especialmenmte del parenquima renal.
Todos los antibióticos que consuetudinariamente han sido contemplados, con un espectro terapéutico para los gérmenes prevalentes, muestran aceptables tasas de erradicación bacteriana (arriba del 80%).
Las connotaciones de todo orden son diferentes si se está en presencia de una pielonefritis o de una cistouretritis. La primera es una condición severa que potencialmente pone en peligro la vida del paciente a corto o largo plazo y que requiere de manejo hospitalario y administración antibiótica intravenosa, la segunda, guardadas las proporciones, es una entidad relativamente benigna sin las implicaciones de la primera, y que según el estado clínico puede ser sujeta de manejo ambulatorio por vía oral.
Como se ha revisado en párrafos anteriores, los elementos para diferenciar entre una u otra han fallado o son de pobre consistencia. La ausencia de lineamientos uniformes ha determinado la conducción de investigaciones, a este respecto, con definiciones operativas disímiles lo que ha impedido la generalización de los resultados a poblaciones aun clínicamente similares.
Si bien la gran heterogeneidad de resultados en los diferentes estudios conducidos, las preguntas implícitas que se pueden detectar se encuentran bajo cuatro dominios, ocasionalmente independientes:
Manejo hospitalario vs. Ambulatorio, Ruta de administración, Tipo de antibiótico, Tiempo de administración.
Aun cuando no existe evidencia directa, los autores tienen el sentimiento y la experiencia que en situaciones en donde el vómito es más intenso o es mayor la alteración del estado general, aumentan las probabilidades depielonefritis y en el mismo sentido su severidad.
Dado lo anterior y siguiendo los lineamientos de Baraff y colaboradores, en cuanto hace referencia al manejo de los niños menores de 36 meses con fiebre sin foco evidente46, es recomendable que cuando las condiciones generales sean deficientes, con un estado de urosepsis instaurado, especialmente en niños menores de 3 meses; si existe deshidratación o conflicto con la hidratación o la administración de líquidos por la vía oral, ya sea por rechazo o por vómito; o que haya dificultades para la asistencia médica oportuna, se interne al paciente y se maneje por vía intravenosa.
Aquellos en aceptable estado general, si están tolerando la vía oral, se encuentran hidratados, o son mayores de tres meses, podrán ser tratados, a discreción del médico a cargo, en forma ambulatoria.
Dado el rango de gérmenes condicionantes aislados y los reportes locales de resistencias bacterianas crecientes a la Ampicilina, los antibióticos parenterales de elección se han circunscrito a las Cefalosporinas (de primera a cuarta generación) solas o asociadas a los Aminoglucósidos ( Tabla 8,9 ) y para el caso de los antibióticos orales el Trimetoprim-Sulfametoxasol y las Cefalosporinas orales88,92-98.
Tabla No 8. Guía de práctica clínica Antibióticos de uso parenteral para el tratamiento en infección urinaria.
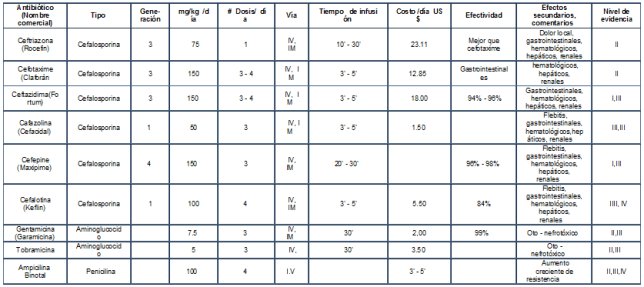
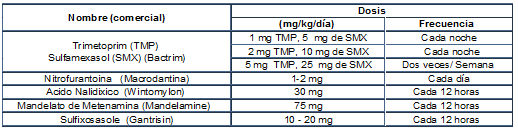
Tabla No 9 Guía práctica clínica antibióticos de Uso Oral para el Tratamiento en infección Urinaria
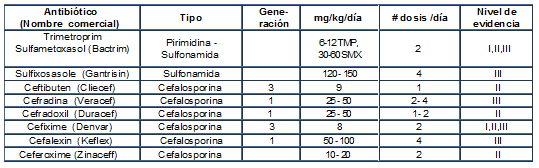
Las diferencias en los beneficios en cuanto a eficacia de los diversos antibióticos parenterales son relativamente pocos y bajo esta perspectiva, la elección antibiótica dependerá de otros factores como la seguridad, los costos, la calidad, el patrón de resistencia local, la disposición del medicamento y las facilidades logísticas y humanas para su administración, o la tasa de efectos secundarios etc.
Para estos últimos, si bien la Gentamicina tiene los mejores reportes de eficacia (virtualmente 100%), la probabilidad de efectos oto-nefrotóxicos es elevada; esta se disminuye si se dispone de su dosificación sérica, lo que encarece los costos y no excluye totalmente su ocurrencia. La Gentamicina a juicio del panel podría darse como coadyuvante en aquellos casos severos, con evolución inadecuada o con sospecha de absceso renal.
Dado que ocurre mejoría de la sintomatología y de los signos de sepsis en un plazo habitual de 72 horas (momento en que se supone controlada la infección)8, y que a continuación se consolidará el tratamiento por unos días más con un antibiótico oral de la misma línea, las cefalosporinas se ajustarían idealmente a este proceso terapéutico lógico. Sin embargo, los tratamientos de consolidación probados (Tabla 8, Tabla 8) han comparado preferentemente al Trimetoprim-Sulfametoxasol contra la Amoxacilina con ligeros beneficios del primero.
No existen reportes en los que se haya comparado, así sea como serie de casos tratados, la administración parenteral contra la oral de antibióticos. En algunas ocasiones Gentamicina (Dosis única diaria por 10 días)98 o Ceftriaxona (Dosis única)99, han demostrado ser totalmente efectivas en aquellos casos en los que la terapia oral falló.
Se han reportado terapias en IU de diferentes intensidades y duración:
Dosis Unica, Dosis única diaria por 3 días, cuatro o 10 días de tratamiento. El perfil de estos trabajos no tienen una clara definición y diferenciación entre las IU altas y bajas.
En todos ellos el Trimetoprim-Sulfametoxasol fue consistentemente mejor con un riesgo atribuible del 4% al 42%. En aquellos tratados con Amoxal, no hay diferencias en las tasas de curación inicial y recidivas en la administración de una sola dosis, 3 días, o 10 días, de tratamiento. Diversos estudios han comparado 7 ó 10 días contra dosis única diaria por tres días arrojando mejorías atribuibles de la primera en rangos del 5% al 21%92,94-,99.
En resumen, los manejos a corto plazo (menores de 3 días) no han demostrado ser mejores que los de 7 días, pero un mínimo necesario no ha sido demostrado todavía.
A juicio del panel de expertos, aquellos con un curso de enfermedad leve pueden ser susceptibles de manejo ambulatorio durante 7 (siete) días, hasta que se decidirá si continuar con profilaxis.
Aquellos con cuadros clínicos más severos, en quien es más probable e implícito la existencia de una forma más intensa de pielonefritis, serán susceptibles de manejo intravenoso inicial durante los tres primeros días, para continuar la consolidación durante 14 (catorce) días, momento en que se decidirá si se continua profilaxis (Algoritmo 1).
1. La probabilidad de IU dado este escenario es de 4 %- 8% (Evidencia IV) Cualquier alternativa puede ser empleada para solicitar el uro-análisis; Urocultivo exclusivamente mediante PSP o CTU. Evitar CTU en prepucio fimótico o sospecha de Cardiopatía Congénita. (Evidencia III, IV)
2. Se considera Uroanálisis Positivo cualquier hallazgo anormal en uno o más de los siguientes ítems:
Cualquier Leucocitarias, cualquier título de nitritos, cualquier bacteria en muestra teñida o no, cinco o más leucocitos/campo de alto poder, diez o más leucocitos/mm3. (Evidencia III,IV)
Tratamiento Parenteral (Evidencia II-IV, recomerdación B y D)
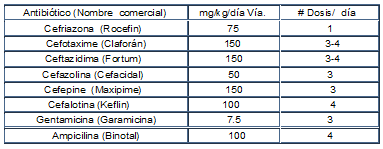
Tratamiento Oral o de Consolidación (Evidencia II-IV, recomerdación B y D)
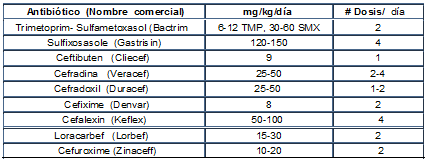
La evidencia existentes es muy pobre; Se reportan series de casos tratados con ceftriaxona I.M. ambulatoria. (Evidencia V).
Desaparición de la fiebre, adecuada hidratación, tolerancia vía oral, actividad y reactividad.
El valor predictivo positivo (VPP) inferior, corresponde a Urocultivos tomados por CTU, el superior lo es a los tomados por medio de PSP.
(Evidencia III,IV).
Lo más pronto posible significa, tan pronto exista defervescencia y desaparación de los
Anormal como asociado a signos directos o indirectos de obstrucción aguda del flujo urinario. (Evidencia III, IV)
Anormal como asociado a signos indirectos de obstrucción del flujo urinario, anomalías anatómicas, o reflujo vésicouretral. (Evidencia III, IV)
Terapia profiláctica. (Evidencia III-IV, recomendación B)
El papel que la Gamagrafía Renal DMSA ocupa en el episodio agudo de IU no es claro; su resultado no modifica práctica clínica en la terapia inicial (Evidencia VI)
Bibliografía
- 1. Browman GP, Levine MN, Mohide EA, Hayard RSA, Ptritchard KI, Gafni A, Laupacis A. The Practice Guidelines Development Cycle: A conceptual Tool for Practice Guideline Development and implementación. J. Clin Oncol 1995; 13(2):502-512.
- 2. CooK DL, Guyatt GH, Laupacis A, et al. Rules of evidence and clinical recommendations on the use of antithrombotics agents. Chest 1992;102:305S-311S.
- 3. Sackett DL. Rules of evidence and clinical recommendations on the use of antithrombotics agents. Chest 1989;95:2S-4S.
- 4. US Department of Health Services, Public Health Service. Agency for Health Care Policy and Research (1992).
- 5. Miller T, Phillips S. Pyelonephritis: The relationship between infection, renal scarring, and antimicrobial therapy. Kidney International 1981; 19:654-62.
- 6. Ginsburg CM, McCraken GH. Urinary tract Infections in Young Infants Pediatrics 1982 69(4):409-12.
- 7. Fredman AL, Vates TS, Slovis TL, Fischer H, Stewart GM. Evaluation the Child with UTI: Controversy and Consensus. Dialogues in Pediatric Urology 1998;21(2):1-8.
- 8. Winberg J. Clinical Aspects of Urinary Tract Infection. In Holliday MA, Barrat TM, Vernier RL Eds. Pediatric Nephrology. 2 Edition. William & Wilkins, Baltimore 1987: 626-46.
- 9. Stull TL, Lipuma JL. Epidemiology and Natural History of UTI in Children. Med Clin NA 1991; 75(2):287-97.
10. Francois P, Croize J, Bost C, Wollschlager K. Etude comparant le cefixime a l´association amoxixilline-acide clavulanique dans le traitement par voie orale des infections urinaires de l´enfant 1995. Arch Pediatr; 2(9):897 - 11. Craig JC, Irwig LM, Knight JF, Roy LP. Trends in the health burden due to urinary tract infection in children in Australia. J Paediatr Child Health 1997 Oct; 33(5):434-8
- 12. Kunin C. Urinary tract Infection in Clidren. Hosp Pract 1976;11:91-98.
Otras Bibliografías
- 13. Wimberg J, Andersen HJ, Bergstrom T, et al. Epidemiology of syntomatic urinary tract infection in chilhood. Acta Paediatr Scand 1974;(suppl 252) 63:1.
- 14. Wimberg J, Bergstrom, Jacobson B. Morbidity, age and sex distribution, recurrences and renal scarring in symptomatic urinary tract infection in chilhood. Kidney Intl 1975; 8:101.
- 15. T Mitchell CK, Franco SM, Vogel RL. Incidence of urinary tract infection in a n inner-city outpatient pupulation. 1995. J Perinatol; 15(2): 131 – 4.
- 16. Asscher AW, McLachlan MSF, Verrier-Jones, et al. Screening for asymtomatic urinary tract infection in schoolgirls. Lancet 1973;2:1-5.
- 17. Jodal U. The natural history of bacteriuria in childhood. Infect Dis Clin NA 1987;1:713-29.
- 18. Hoberman A, Chao HP, Keller DM, Hickey R, Davis HW, Ellis D Prevalence of urinary tract infection in febrile infants. J Pediatr. 1993; 123(1):17-23.
- 19. Hoberman A, Wald ER, Reynolds EA, Penchansky L, Charron M. Pyuria and bacteriuria in urine specimens obtained by catheter from young children with fever. J Pediatr 1994; 124:513 – 9.
- 20. Ring E, Zobel G. Urinary tract infections and malformations of the urinary tract in infancy. Arch Dis Child 1988;63:818-20.
- 21. McCraken G. Diagnosis and management of acute urinary tract infection in infants and children. Pediatr Infect Dis J 1987;6:
- 22. Wiswell TE, Smith FR, Bass JW Decreased incidence of urinary tract infections in circumcised male infants. Pediatrics. 1985; 75:901-903.
- 23. Wiswell TE, Roscelli JD Corroborative evidence for the decreased incidence of urinary tract infections in circumcised male infants. Pediatrics. 1986; 78:96-99.
- 24. Wiswell TE, Hachey WE Urinary tract infections and the uncircumcised state: an update. Clin Pediatr (Phila). 1993; 32:130-13.
Referencia
- 25. Downs SM. Technical Report: Urinary tract infection in febrile infants and young children Pediatrics 1999. 103(4) p.e. 54.
- 26. Bergstron T, Carson H, Lincoln K, et al. Studies of Urinary tract infections in infancy and chilhood. XII. Eightty consecutive patients with neonatal
- 27. Cohen M The first urinary tract infection in male children. Am J Dis Child. 1976; 130:810-813.
- 28. Shah KJ, Robins DG, White RH Renal scarring and vesicoureteric reflux. Arch Dis Child. 1978; 53:210-217.
- 29. Hellstrom M, Jacobson B, Marild S, Jodal U. Voiding cystourethrography as a predcitor of reflux nephropathy in children with urinary-tract infection. AJR Am J Roentgenol. 1989;152: 801-804.
- 30. Littlewodd JM. 66 infants with UTI in first month of life. Arch Dis Child 47:218, 1972.
- 31. Pylkkanen J, Vliska J, Koskimies O. The value of diagnosis of childhood urinary tract infection in predicting renal unjury. Acta Paediatr Scand 1981: 70: 879 – 83.
- 32. Benador D, Benador N, Slosman D, Mermillod B, Girardin E. Are younger children at higher risk of renal sequellae after oyelonephritis ¿ Lancet 349: 17 –19 1997.
- 33. Bergson SJ, Coulthard MG, Lambert HJ, et al. BMJ 199711;315(7173):905-8
- 34. McKerrow W, Davidson-Lamb N, Jones PF Urinary tract infection in children. Br Med J (Clin Res Educ). 1984; 289:299-303.
- 35. Bisset GS III, Strife JL, Dunbar JS Urography and voiding cystourethrography: findings in girls with urinary tract infection. AJR Am J Roentgenol. 1987; 148:479-482.
- 36. Gleeson FV, Gordon I Imaging in urinary tract infection. Arch Dis Child. 1991; 66:1282-1283.
- 37. Buys H, Pead L, Hallett R, Maskell R Suprapubic aspiration under ultrasound guidance in children with fever of undiagnosed cause. Br Med J. 1994; 308:690-692.
Otras Referencias
- 38. Mihindukulasuriya JC, Maskell R, Polak A A study of fifty-eight patients with renal scarring associated with urinary tract infections. Q J Med. 1980; 49:165-178.
- 39. Jacobson SH, Eklof O, Lins LE, Wikstad I, Winberg J Long-term prognosis of post-infectious renal scarring in relation to radiological findings in childhood: a 27-year follow up. Pediatr Nephrol. 1992; 6:19-24.
- 40. Wolfish NM, Delbrouck NF, Shanon A, Matzinger MA, Stenstrom R, McLaine PN Prevalence of hypertension in children with primary vesicoureteral reflux. J Pediatr. 1993; 123:559-563.
- 41. Welch TR, Forbes PA, Drummond KN, Nogrady MB Recurrent urinary tract infection in girls: group with lower tract findings and a benign course. Arch Dis Child. 1976; 51:114-119.
- 42. Sackett DL, Richardson WS, Rosemberg W, Haynes RB. Evidence Based-Medicine: How to Practice and Teach EBM. Churchill Livingstone, London. First Edition.1997.
- 43. North AF. Bacteriuria in children with acute febrile illnesses. J Pediatr 1963;63:408-11.
- 44. Bonadio WA. Urine culturing technique in febrile infants. Peditr Emerg Care 1987; 3:75-78.
- 45. Bauchner H, Philipp B, Dashefsky B, Klein JO Prevalence of bacteriuria in febrile children. Pediatr Infect Dis J. 1987; 6:239-242.
- 46. Baraff L, Bass JW, Fleisher GR, Practice guideline for the management of infants and children 0 to 36 months of age with fever without source. Pediatrics. 1993; 92:1-12.
- 47. Tappin DM, Murphy AV, Mocan H, et al. A prospective study of children with first acute symptomatic E Coli urinary tract infection: early 99 m technetium dimercaptosuccinic acis scan appearences. Acta Pediatr Scand 1989;78:923-29.
Fuente
- 48. Verboven M, Ingels M, Delree M, Piepsz A. 99 mTc-DMSA scintigraphy in acute urinary tract infectionin children. Pediatr Radiol 1990;20:540-42.
- 49. Rosenberg AR, Rossleigh MA, Brydon MP, Bass SJ, LeigthonDM, Farnsworth RH. Evaluation of acute urinary tract infection in children by dimercaptosuccinic acis scintigraphy: a prospective study. J Urol 1992;148:1746-49.

