Trabajos de investigación
*Jacinto Sánchez;*Profesor Asociado. Departamento de Obstetricia y
Ginecología. Facultad de Medicina. Universidad Nacional de Colombia.
Clínica de Climaterio. Instituto Materno Infantil. Santafé de Bogotá.
**William Onatra;**MD. Radiólogo. Colegio Mayor
Nuestra Señora del Rosario. Clínica Reina Sofía.
***Juan Guillermo Villegas;***MD. Ms, Sección de Epidemiología.
Instituto Nacional de Cancerología. +Héctor Posso;+MD.
Adscrito Sección de Epidemiología INC. Israel Díaz Jr.
Resumen
Objetivos:
Conocer si el aumento de peso modifica la densidad mineral ósea (DMO)
Material y métodos:
Se tomaron 1971 pacientes pre y postmenopáusica que fueron remitidas para practicar de rutina una densitometría ósea. Las pacientes se dividieron en dos grupos de acuerdo a su estado socioeconómico Grupo 1> de 2 salarios mínimos, grupo 2 < de 2 salarios mínimos. Se utilizó para la medición un aparato de absorciometría de rayos X de doble fotón (DEXA) con los standares de un equipo Lunar DPX.
Las pacientes se clasificaron de acuerdo al índice de masa corporal (ICM) en 4 categorías;<20 delgadas normales 20-24, sobrepeso 25-29 y obesas > de 30.
Resultados:
De acuerdo al índice de Masa Corporal, se encontró que el 10% de las mujeres eran delgadas, normales 64%, sobrepeso 20.4% y obesas 5.2%. La DMO promedio en las pacientes delgadas a nivel de columna Lumbar fue 950.52 m-m2 y de la obesas de 912.82 g-m2 sin ser significativa esta diferencia. Cuando la DMO fue comparada entre los dos grupos socioeconómicos, se encontró diferencia significativa a nivel de la columna lumbar en las mujeres con sobrepeso (p<0.03).
En la misma forma se encontraron niveles de DMO significativamente más altos en el Grupo 2 a nivel de la columna y el fémur en las pacientes normales y con sobre peso (p<0.003 y p < 0.001 respectivamente).
Conclusión:
El presente estudio demuestra como la DMO se modifica con el IMC y muestra diferencias significativas según el estudio socioeconómico a nivel y fémur.
Palabras claves: Densitometría, índice de masa corporal, pre y postmenopasia.
Summary
Objetive:
To know if the weight gain influences the bone mineral density (bmd)
Study desing:
1971 pre and postmenopausal women were assessed with a routine bone densitometry. Patients were divided into two group according to the socioeconomical status: group 1 with an income over 2 minimum salaries and group 2 with in income under two minimum salaries. The densiometry was carried out with dexa technique which used a lunar dpx equipment. The patients were classified according to the body maas index (bmi) into 4 categories: < 20, thin patient; normal 20-24; overweigh 25 -29 and obese > 30.
Results:
According to the bmi 10% were thin women, 64% normal, 20.4% overweigthed 5.2% obese. The mean bmd at the level of the spine was 950.52 gs/m2 in the thin patients and 105.15 g/m2 in the obese group, and there was significant difference (p<0.003). When the bmi was compared according to the socioeconomical status, there was only a significant difference (p<0.003). When the bmi was compared according to the socioeconomical status, there was only a significant difference in the normal group (p<0.001) (group 1: 22.8 vs group 23: 3) when the bmd was compared between group 1 and 2, it was only significantly higher in the group 2 at the level of the women with overweight (p<0.03), as well as at the level of the femur in the same group, in normal and overweighted patients (p<0.003 and p<0.0001 respectively).
Conclusion:
The present study shows some significant differences in the bmd related with the bmi when different socioeconomical populations are compared.
Key words: Densitometry, body mass index, pre and postmenopause
Introducción
La osteoporosis es una enfermedad metabólica prevenible que compromete tanto a hombres como mujeres a partir de la quinta década. Es conocido que el pico de masa ósea se alcanza entre los 30 y 35 años dependientes de factores genéticos, nutricionales, ejercicio y endocrinometabólicos. La mujer después de los 40 años pierde aproximadamente entre un 0.3% a 0.5% de hueso cortical por año, después de la menopausia la pérdida es de 3 a 4% por año. La pérdida anual de hueso trabecular medida por densitometría de energía dual (DEXA) es de 1.2%1.
El pico de masa ósea se define como la cantidad de tejido óseo presente al final de la maduración esquelética.
Se ha demostrado que existe una disminución progresiva de la masa ósea después de los 30 años para ambos sexos. En la mujer después de la menopausia el deterioro es mayor, igualando o aumentando según los diferentes estudios comparativos al hombre en el riesgo de fractura a nivel lumbar o de fémur proximal2-3.
Clásicamente se ha aceptado que son multifactoriales los determinantes en el tamaño y contextura de la masa ósea: herencia, sexo femenino, dieta (grasas, proteínas, calcio), factores endocrinos (esteroides sexuales, calcitriol, factores de crecimiento-1 similares a la insulina -IGF-1), fuerzas mecánicas (actividad física, pero corporal) y exposición a factores de riesgo como los medicamentos (corticoides)4.
El peso siendo uno de los factores determinantes de la masa ósea ha merecido el análisis de uno de sus componentes como es el tejido graso.
La mujer obesa soporta más peso y desde el punto de vista mecánico tendría mayor masa corporal que la mujer delgada y como consecuencia tendría mayor posibilidad de conservar la masa ósea. Dentro de estos componentes se ha podido demostrar que la mujer premenopáusica tiene un 56% de masa libre de gras (FFM) y después de la menopausia es de sólo 50%5.
Metabólicamente las mujeres en sobre peso absorben calcio con mayor eficiencia, al tener un aparato óseo de remodelación más sensitivo a la hormona paratiroidea utilizan el calcio disponible en forma óptima conservando por este mecanismo la masa ósea6. La mujer obesa pierde relativamente poco hueso después de la menopausia a pesar de una disminución teórica de los estrógenos.
Se conserva elevada la relación estrona-estradiol, en parte debido a la aromatización periférica de los andrógenos adrenales (androstendiona) en el tejido graso y por acción de las aromatasas (17b-OH-esteroide óxido reductasa) la Testosterona es convertida en Estrona (E1) y menor concentración estradiol (E2)7. El riesgo de fractura es menor en este grupo etario.
Alteraciones metabólicas lleva una disminución de la masa ósea
Por otra parte la reducción de peso además de las alteraciones metabólicas lleva una disminución de la masa ósea con el consiguiente riesgo de fractura.
En las mujeres jóvenes anoréxicas al contenido mineral óseo se le encuentran 2 desviaciones por debajo de la media a nivel de columna lumbar como en fémur8.
La paciente delgada contrario a la obesa maneja menores niveles de estrógenos, baja ingesta de calcio y proteínas, el contenido de grasa es menor y por lo tanto el metabolismo a nivel de hueso se encuentra disminuido.
Es conocido que el manejo nutricional, hormonal y de terapia física lograra recuperar peso y por consiguiente mejorar la calidad ósea 9.
Fue de interés de los autores conocer el comportamiento de la densidad mineral ósea frente al peso y talla utilizando el índice de masa corporal (IMC) en mujeres pre y postmenopáusicas.
Material y Métodos
Se tomaron 1971 pacientes de la ciudad de Santafé de Bogotá entre los 40 y 74 años que asistieron a control radiológico para medir el contenido mineral óseo (CMO). Las pacientes fueron remitidas de la consulta de Climaterio del Instituto Materno Infantil, Departamento de Obstetricia y Ginecología de la Universidad Nacional de Colombia y la consulta especializada de medicina prepagada (Colsanitas), entre el 1º de enero de 1993 y 31 de diciembre de 1994.
Se tabularon la edad, el peso, la talla y se calculó el índice de masa corporal (IMC) de acuerdo a los parámetros internacionalmente aceptados (IMC= peso – talla2), se hicieron las determinaciones de contenido mineral óseo a nivel de columna lumbar (L”-L4) y en fémur (Triángulo de Ward´s).
Para el IMC se consideró pacientes normales las que encontraban entre 20 y 24, sobrepeso entre 25 y 29, obesas mayores de 30 y delgadas menores de 20. Las pacientes a su vez fueron divididas en dos grupos de acuerdo con su estado socioeconómico (valorando el salario mínimo, Grupo > de dos salarios mínimos.
Instrumento:
Para la medida de densidad mineral ósea (DMO) se utilizó un aparato de absorciometría de energía dual de RX (DXA, Lunar DPX, Lunar Radiation Corporation, Madison WI). Las medidas fueron a nivel de columna lumbar 12-14 con un coeficiente de variación del 0.9-1% y a nivel de cuello femoral (Triángulo de Ward´s) de 1.5-24%. Se consideró pacientes normales las que estaban dentro del promedio para la edad, utilizando el Z-score, osteopénicas con 1 desviación estándar (DS) mayor en relación con el promedio, osteopénicas más de 2.5 DS. Para el análisis sólo se tuvo en cuenta el promedio total de DMO.
Estadística:
Los datos fueron introducidos al Dbase III plus y para el análisis se contó con la ayuda de Epi-info y SAS. Los datos de densitometría ósea se analizaron según grupos quinquenales de edad, sitios de medición, separación de grupos 1 y 2. Se compara con otros hallazgos a nivel internacional.
Para valorar las diferencias se utilizó el análisis de varianza (ANOVA) y chicuadrado de Bartles. Para las variantes no homogéneas se utilizó el test de significancia menor de 0.005 (p<0.05).
Revista de menopausia
Resultados
Se analizaron 1971 densitometrías en pacientes pre y postmenopáusicas en edades comprendidas entre 40 y 74 años. El mayor grupo correspondió a las edades entre 50 y 54 años (609), siendo el menor (6 casos) las mayores de 70 años.
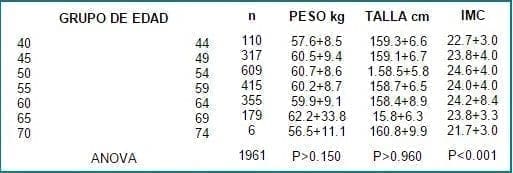
Como se muestra en la Tabla 1, se aprecia un moderado aumento de peso a partir de los 45 años con una discreta disminución de la estatura sin ser significativa. El índice de masa corporal en los diferentes grupos por quinquenios de edad se encuentra dentro de los límites de normalidad, con un discreto aumento después de los 45 años que se mantienen hasta los 64 años.
Las pruebas de chi-2 reporta 21.15 con 6 grados de libertad y una p>0.001 indicando una diferencia significativa en este grupo de mujeres.
Tabla 1. Índice de masa corporal por grupo de edad.
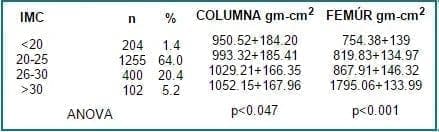
La tabla 2 muestra el comportamiento de las pacientes categorizadas por índice de masa corporal y los hallazgos de densidad mineral ósea en columna lumbar y fémur. Se observa como a medida que aumenta el peso, la densidad mineral ósea también aumenta siendo esta diferencia más significativa a nivel de fémur que en columna. Para este grupo poblacional se demuestra que las pacientes con sobrepeso y obesas son 25.6%, en límites normales 64% y delgada el 10.4%.
Tabla 2. Correlación entre el IMC y DMO en columna y fémur.
Al dividir la población de acuerdo a su clase socioeconómica Tabla 3 se observa que no hay diferencias en relación con el IMC excepto en el grupo con IMC dentro de límites normales, donde el grupo 2 (bajo ingreso) presenta una diferencia significativa.
Tabla 3. IMC según origen.
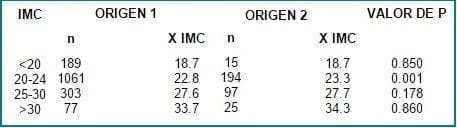
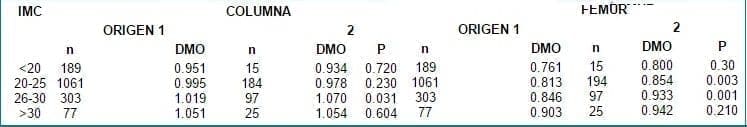
Tabla 4. Se mantiene la relación proporcional entre mayor IMC, mayor DMO. No hay diferencia significativas entre delgadas (<20) y las obesas (>30) en ambos grupos tanto en columna lumbar como en fémur. Existiendo una diferencia significativa entre el grupo 1 y grupo 2 a nivel columna en las mujeres con sobrepeso (26-30) en fémur en paciente normales (20-25) y en sobrepeso.
Estos datos muestran una tendencia sin ser significativa de una DMO en fémur en el grupo 2 (bajo recursos) frente al grupo 1.
Tabla 4. IMC según origen y DMO en columna y fémur.
Discusión
La osteoporosis se ha considerado como un problema de salud pública y la disminución en la medición de la densidad mineral ósea como un potente predictor de riesgo de fractura10. Diferentes estudios experimentales y longitudinales han mostrado la pérdida gradual de la DMO a medida que avanza la edad11-12.
Esta pérdida ocurre por un imbalance entre la resorción y formación: aumento de la resorción con normal o reducción de la formación o normal resorción con reducción de la formación.
En la postmenopausia existe una pérdida acelerada de hueso trabecular con disminución de los cuerpos vertebrales y fracturas espontáneas. Esta pérdida se desacelera unos 10 a 15 años después de la menopausia pero a nivel de fémur continua13.
Dentro de las técnicas más comúnmente utilizadas se ha impuesto la densitometría con energía dual de Rx(DEXA):
La cual ha servido para evaluar la densidad mineral ósea (masa ósea) a nivel de cuerpo total, columna lumbar, cadera y antebrazo14. Una de las ventajas de esta técnica es que su rayo de luz más potente permite un mejor rastro y una resolución e identificación más confiable de los límites vertebrales. El error de reproductibilidad in vivo es del 0.4% e in vivo del 2%.
Como método para predecir el riesgo de fractura la sensibilidad con 1 DS es del 38%, para 2.5 DS del 52% y la especialidad es del 98 y 100% respectivamente 15. En el presente estudio los datos muestran unos valores tanto para columna como para fémur dentro de límites normales para su edad y que fue motivo de una publicación16. El observa que la DMO aumenta en forma proporcional16.
El observar que la DMO aumenta en el grupo formal proporcional a medida que se incrementa el IMC siendo significativamente mayor en fémur que en columna, confirma en nuestro medio la evidencia descrita por otros autores17.
Contrario a esta evidencia e independencia del concepto de pico de masa ósea, factores genéticos y otros, las mujeres por factores ambientales o nutricionales que cursan con aumento de peso, su densidad mineral ósea también se encuentra independiente del área geográfica Holanda18, Japón19 o China20.
Merece anotar que cuando se utiliza el IMC en una población general y en este caso en mujeres pre y postmenopáusica el promedio se mantiene dentro de límites normales21, haciendo imperioso el poder clasificarla en el presente estudio se tiene un grupo del 10% de mujeres delgadas con IMC < 20, menor DMO como se ha descrito en otros estudios8, 22.
Las causas de pérdida ósea en las mujeres delgadas puede ser multifactorial:
Desde los factores genéticos, nutricionales (bajo aporte calórico, proteico, ingesta de calcio), ambientales (ejercicio, estado socioeconómico). Estado de sus función ovárica como los períodos prolongados de amenorrea, hiper-prolactinemia, exceso de ejercicio, anorexia nerviosa.
Fármacos como el uso de agonista de la GNRH, o las pacientes que reciben corticoides para su lesión artrítica23-24. El haber detectado un 10% de nuestras mujeres que llegan a la menopausia por debajo de los límites normales del IMC, sería recomendable buscar su etiología e iniciar un manejo preventivo desde la consulta ginecológica.
La obesidad es citada con frecuencia como un factor protector contra la osteoporosis. Sin embargo, la distribución de esta grasa es un factor de riesgo para diabetes mellitus, colelitiasis, hipertensión, enfermedad cardiovascular, cáncer de útero y mamá25.
Estudios de corte longitudinal con DEXA han encontrado que en mujeres postmenopáusicas existe un aumento de grasa total de cuerpo en un 20%11, 26. Estudios prospectivos no han encontrado un incremento del peso después de la privación estrogénica, aún con terapia hormonal de reemplazo27-28.
De estos estudios se deduce que durante la postmenopausia hay un aumento de masa grasa que se deposita a nivel abdominal, con una disminución en la grasa magra en un 3.78% a los 3 años después de la última regla25.
El presente estudio confirma lo expresado por otros autores donde la densidad mineral ósea aumenta con el peso26-27 y plantea la necesidad de hacer estudios prospectivos sobre el estado nutricional metabólico en el grupo.
El estado socioeconómico podría ser uno de los factores condicionantes de la osteoporosis ante la baja ingesta de calcio y proteínas.
El presente estudio no pudo demostrar estas diferencias observándose que la densidad mineral ósea a nivel lumbar se mantiene en ambos grupos excepto en la de sobrepeso25-30. A nivel de fémur en el grupo 2 (bajo recursos) muestra un aumento mayor en la DMO, con diferencias significativas entre las normales y las pacientes con sobrepeso.
Datos previos no publicados por la sección de nutrición del hospital informan que este grupo maneja una proporción mayor de hidratos de carbono frente a proteínas y grasas, dieta baja en calcio. Valdría la pena profundizar en este tópico dado los cambios metabólicos que se presenta en pacientes con sobrepeso y el riesgo de fractura a largo plazo.
En resumen podemos afirmar que la densidad mineral aumenta proporcional al índice de masa corporal con una proporción significativamente mayor a nivel lumbar en pacientes de estatus socioeconómico bajo.
Bibliografía
- 1. Burckardt P. The peak bone mass concept. Clin Rehumatol 1989; 8 S: 16-21.
- 2. Notelovitz M. Osteoporosis screening, prevention and management. Fertil Steril 1993; 59: 707 – 724.
- 3. Riggs BL, Melton LJ. Medical Progress: involutional osteoporosis. N Engl Med 1986; 314: 1676 – 1686.
- 4. Bonjour J Ph, Theiniz G, Law FD et al. Peak bone mass. Osteoporosis Int 1994; 4:
- 5. Aloia JF, Vaswani A, Flaster E. To what extent is bone mass detemined by fat-free or fat-free or fat mass? Am J Clin Nutr 1995; 61: 1110-1114.
- 6. Reid IR, Plank LD, Evans MC. Fat mass is an important determinant of whole and body bone density in premennopausal women but no in men. J Clin Endocrinol Metab 1992; 75: 779-782.
- 7. Longoope C, Baker R, Johnston Jr CC. Androgen and estrogen metabolis, relationship to obesity. Metabolism 1986; 35: 235-237.
- 8. Davies KM, Pearson PH, Hugemann CA. Reduced bone mineral in patient with eating disorders. Bone 1990; 11: 143-147.
- 9. Baschrach LK, Gido D, Katzman D et all. Recovery from osteopenia in adolescent gins with anorexia nervosa. J Clin Endocrinol Metab 1991; 72: 602-606.
- 10. Riggs BL, Walhner HW, Seeman E et al. Changes in bone mineral density of the proximal femur and spine with aging. J Clin invest 1982; 70: 716-723.
- 11. Lindsay P, Cosman F, Herrington DS et al. Bone messend body composition in normal women. J Bone Miner Res 1992; 7: 55-63.
- 12. Stevenson JC, Lees B, Devenport M et all. Determinants of bone density in normal women: risk factors for future osteoporosis? BMJ 1989; 298: 924-926.
- 13. Greespan SL, Maitland LA, Krasnow MB et all. Femoral bone progresses with age in elderly women. J Bone Miner 1993; 8S: 147.
Referencias
- 14. Diagnostic and Therapeutic Assessment (DATTA). Measurement of bone density with dual xray absorptiometry (DEXA) J Am Med Assoc 1992; 267: 286-294.
- 15. Duboeuf F, Jergas M, Schott AM et al. A comparison of bone densitometry measurements of the central skeleton in post-menopausal women with and without vertebral fracture. BJR 1995; 68: 747 -753.
- 16. Villegas JG, Onatra W, Sánchez J et al. Estudio comparativo de Densitometría en Santafé de Bogotá, en dos poblaciones diferentes. Rev Col Meno 1996; 1: 96-97.
- 17. Marcus R, Greendale G, Blunt BA et al. Correlates of bone mineral density in the postmenopausal estrogen – progestin interventions trial. J Bone Miner Res 1994; 9: 1467-1476.
- 18. Erdtsiek RJ, Pols HA, Algra D et al. Bone mineral densitry in healthy dutch women: spine and hip measurements using dual-energy Xray absorptiometry. Neth J Med 1994; 45:198-205.
- 19. Tsunenani T, Yamada S, Kawakatsu M et al. Menopause related changes in bone mineral density in Japanese women: a longitudinal study on lumbar spine and proximal femur. Calcif Tissue Int 1995; 56: 5-10.
- 20. Kao CH, Chem CC, Wang SJ. Normal data for lumbar spine bone mineral content in health elderly Chinese: influences of sex, age, obesity and ethnicity. Nucl Med Commun 1994; 15: 916-920.
- 21. Garton M, Martin J, New S et al. Bone mas and metabolism in women age 45-55.
- 22. Vetter U, Dragun K, Boehles HJ. Bone mineral density in children and adults with constitucional delay of growth and puberty. J Boner Miner Res 1983; 85: 458.
- 23. Prior JC, Vigna YM, Schecheter MT et al. Spinal bone loss ovulatory disturbances. N Engl J Med 1990; 323: 1221-1227.
Fuentes
- 24. Kroger H, Honkanen R, Saarikoski S et al. Decreased axial bone mineral density in perimenopausal women with theumatoid arthritis a population based study. Ann Rheum Dis 1994; 53: 18-23.
- 25. Aloia JF, Vaswani A, Russo L et al. The influence of menopause and hormonal replacement therapy on body cell mass and body fat mass. Am J Obsted Gynecol 1995; 172: 600-896.
- 26. Ley CJ, Lees B, Stevenson JC. Sex and menopause associated changes in body-fat distribution. Am J Clin Nutr 1992; 25: 950-954.
- 27. Tonkelaar ID, Seidell JG, van Noord PAH et al. Fat distribution in relation to age, degree of obesity, smoking habits, parity and estrogen use: a cross-seccional study in 11825 Dutch women participanting in the DOM-projet. Int J Obes 1990; 14: 753-761.
- 28. Kaye SA, Folsom AR, Solter JY et al. Association of body mass and fat distribution with sex hormone concentrations in postmenopausal women. Int J Epidemiol 1991; 20: 151-156.
- 29. Rico H, Revilla M, Hernández ER et al. The relationship of total body mineral (TBBMC) to anthropometric variables in postmenopausal women and contribution of chronological age and years since menopause to TBBMC loss. Clin Rheumatoln 1993; 12: 475-478.
- 30. Aguado F, Revilla M, Hernández ER et al. Behavior of bone mass measurements dual energy xray absorptiometry total body bone content, ultrasound bone velocity and computed metacarpal radiogrammetry, with age, gonadal status and weight in healthy women. Invest Radiol 1996; 31: 218 -222.