Monique Chalem, M.D.
Internista Reumatóloga
Departamento de Medicina Interna
Fundación Santafé de Bogotá
Asociación Médica de los Andes
Santafé de Bogotá, D.C.
En la actualidad disponemos de varios fármacos para el tratamiento de la osteoporosis. Pueden ser clasificados de manera esquemática aunque no exacta, como inhibidores de la resorción ósea o estimulantes de la formación ósea. (Ver Tabla).
Tabla. Algunos fármacos utilizados en el tratamiento de la osteoporosis
| Inhibidores de la resorción ósea Estrógenos Calcitoninas Biofosfonatos Calcio Diuréticos tiazídicos Derivados de la vitamina D Estimuladores de la formación ósea |
| Adaptado de (2). |
Este artículo revisa los mecanismos de acción, indicaciones, contraindicaciones y posología de los tratamientos más empleados actualmente en el manejo de la osteopororsis tipo I como son el calcio, los biofosfonatos, las calcitoninas, los derivados de la vitamina D y el flúor.
Calcio
La administración de suplementos constituye una de las intervenciones farmacológicas de mayor importancia en el manejo de la osteoporosis.
Se han publicado varios estudios controlados que han demostrado que la dosis farmacológicas de calcio disminuyen la pérdida ósea trabecular y cortical.
Esto se debe probablemente al incremento en el calcio sérico y a la consecuente disminución en los niveles de hormona paratoidea (PTH) y por ende de al resorción ósea.
Muchos estudios se han interesado en el efecto del calcio sobre la prevención de fracturas. Hasta el momento los trabajos efectuados no arrojan resultados concluyentes en este sentido1.
En la mayoría de los casos el calcio se administra con otro fármaco ya sea un antiresortivo o un formador de hueso.
Las mujeres postmenopáusicas requieren dosis diarias de 1000-1500 mg de calcio elemental. Es muy raro en nuestro medio, en donde la ingesta de calcio es muy pobre, complementar los requerimientos cotidianos con la dieta.
Es por ello que deben administrarse suplementos de calcio. La mayoría de las preparaciones disponibles en el comercio son de carbono de calcio con tabletas que contienen 500 ó 600 mg de calcio elemental.
Es importante reconocer que el contenido de calcio elemental varía con el producto: el carbonato de calcio contiene 40% de calcio elemental, el fosfato de calcio 31%, el lactato 13% y el gluconato de calcio 9%2.
El calcio se absorbe mejor una hora después de las comidas y por la noche. El administrar dosis mayores a 500 mg de calcio elemental no aporta ningún beneficio. Es frecuente la aparición de efectos secundarios menores de origen gastrointestinal.
Vitamina D y derivados
La fuente principal de vitamina D es la síntesis de su precursor en la piel durante la exposición a los rayos solares. Los metabolitos de la vitamina D son importantes para regulación del metabolismo del calcio. La carencia de vitamina D se manifiesta por cuadros de raquitismo en los niños y osteomalacia en los adultos.
El metabolisno activo de la vitamina D, 1,25(OH)2D3 (calcitriol) que se produce en los riñones, aumenta la absorción intestinal de calcio, estimula el osteoblasto y es importante para la mineralización del hueso3. Las poblaciones del hemisferio norte son muy susceptibles a deficiencias en vitamina D, en especial en individuos de la tercera edad.
Un estudio prospectivo realizado en ancianos institucionalizados demostró que la administración de calcio y 25 (OH)D3 (calcidiol) redujo la incidencia de fractura de cadera4. Este estudio fue realizado en una población especial y sus resultados no pueden ser extrapolados en nuestro medio.
Varias preparaciones comerciales disponibles contienen calcidiol (150 a 300 U por 500 a 600 mg de calcio elemental) y es posible que la administración de estos suplementos de vitamina D se vuelva una práctica de rutina.
La administración de 300 a 800U diarias de calcidiol no causa por lo general efectos secundarios. El calcidiol no se emplea como agente único en el tratamiento de la osteoporosis postmenopáusica.
Incremento significativo en la densidad mineral ósea
En algunos estudios controlados se demostró un incremento significativo en la densidad mineral ósea (DMO) con la administración de 0.5 mcg de calcitriol al día. La suspensión del medicamento produce una pérdida rápida de la DMO, tal como sucede con los estrógenos o con otro tipo de tratamientos.
Las dosis de 0.5 cmg de calcitriol son rara vez causa de complicaciones (hipoercalemia en 0.6% de los casos)5. La administración de dosis mayores pueden ser causa de hipercalcituria en un porcentaje importante de pacientes6.
Los análogos de la vitamina D 1µ (OH)D3 y 1µ (OH)D2 se utilizan en ciertos países como agentes terapéuticos de la osteoporosis tipo l. Los estudios controlados demuestran un incremento significativo de la DMO aunque la magnitud varía según los estudios3.
Calcitonina
La calcitonina es una hormona constituida por 32 aminoácidos que ha sido aislada de varias especies que incluyen el cerdo, el salmón, las anguilas y los humanos. Calcitonina de salmón, disponible en nuestro medio es la más potente.
La calcitonina es un potente inhibidor de la actividad osteoblástica y por consiguiente de la resorción ósea lo que justifica su utilización en la osteoporosis tipol.
La calcitonina se ha empleado como terapia alternativa a los estrógenos en la prevención de al osteoporosis postmenopáusica. Overgaard y cols demuestran en un estudio doble ciego realizado en 52 mujeres en la postmenopausia inmediata, una prevención de la pérdida ósea en columna vertebral de las mujeres que recibieron 100 UI/día de calcitonina nasal de salmón. No se previno la pérdida ósea en sitios esqueléticos con predominio de hueso cortical como antebrazo y cuerpo total7.
Un estudio más reciente utilizando dosis cotidianas más bajas (50UI) muestra resultados similares8. Sin embargo, algunos estudios sugieren que se requieren dosis más latas (hasta 400UI/día) para lograr un efecto preventivo en este grupo de mujeres que tienen un porcentaje significativo de individuos con pérdida ósea acelerada9.
Administración de calcitonina nasal o parenteral
Varios estudios han demostrado que la administración de calcitonina nasal o parenteral reduce la velocidad de pérdida ósea en pacientes con osteoporosis establecida.
Overgaard y cols encontraron, al cabo de dos años, un efecto benéfico sobre la DMO de columna con la administración de 50, 100 ó 200 UI diarias de calcitonia de salmón a mujeres de edad con osteoporosis establecida, siendo más importante el aumento en la DMO lumbar con esta última dosis10.
La pérdida ósea se revierte una vez se suspende el tratamiento por lo que algunos investigadores han utilizado un régimen intermitente (un año con tratamiento seguido de un año sin tratamiento o ciclos más cortos).
La administración intermitente ofrece la ventaja de reducir costos y aumentar la adherencia al tratamiento. Todavía no se ha encontrado el esquema óptimo de tratamiento.
Como los demás tratamientos antiresortivos la calcitonina tiene un mayor efecto en hueso trabecular y en pacientes con un alto recambio óseo11.
La calcitonina también tendría un efecto sobre la prevención de fracturas vertebrales y posiblemente de cuello femoral, según algunos de los estudios prospectivos realizados.
La calcitonina tiene otras indicaciones terapéuticas como son el tratamiento de estados hipercalcémicos, el manejo de la distrofia simpática refleja, la prevención de la osteoporosis inducida por y el manejo de una entidad rara en nuestro medio, la enfermedad de Paget del hueso.
La gran diferencia con los demás agentes antiresortivos radica en el potente efecto analgésico de la calcitonina, especialmente en los casos de fracturas osteoporóticas.
Esta hormona polipeptídica es destruida por las enzimas gástricas. Puede administrarse por diferentes vías: IM, SC, intranasal. En algunos países se encuentra disponible por vía rectal. La dosis a administrar oscila entre 50 y 200 UI al día. El esquema de tratamiento depende de la indicación.
Bifosfonatos
Los bifosfonatos son una serie de compuestos análogos de los pirofosfatos. Por su estructura química tienen una alta afinidad por los cristales de hidroxiapatia y una prolongada retención esquelética.
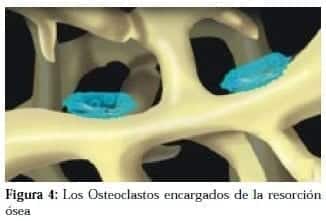
Los bifosfonatos son también potentes inhibidores de la resorción ósea. Un componente importante de su mecanismo se explica por la presencia del fármaco en las superficies de resorción ósea. También inhiben el desarrollo de los precursores de los osteoclastos.
Así como la calcitonina, la acción antiresortiva explica su utilización en una variedad de trastornos metabólicos óseos.
Aunque la estructura de todos los biofosfonatos es similar, la potencia entre los diferentes compuestos radica en la cadena lateral. El interés en los nuevos bifosfonatos ha sido el desarrollo de compuestos que no tengan efectos indeseados sobre la mineralización ósea.
Este problema que se observó con el etidronato y que se solucionó con el esquema cíclico ahora empleado, no se ha observado con los nuevos bifosfonatos.
Se evaluó el efecto del etidronato en un estudio doble ciego, placebo control que involucró a 429 mujeres postmenopáusicas con fracturas vertebrales. Al cabo de dos años se demostró con fracturas vertebrales.
Al cabo de dos años se demostró un incremento de 4 a 5% en la DMO de columna y una disminución del 50% de nuevas fracturas vertebrales en el grupo etidronato12.
El alendronato, de reciente introducción, es el único de estos agentes disponible en nuestro medio.
Un estudio multicéntrico controlado reciente estudió los efectos del alendronate sobre la DMO en diferentes sitios esqueléticos. Después de tres años de tratamiento con 10 mg diarios de esta droga se observó un incremento del 9% en la DMO de columna y de 7.8% en el trocánter.
En los sitios con mayor contenido de hueso cortical el incremento fue menor: 6% en cuello femoral y 2.5% en 48% en la proporción de mujeres con nuevas fracturas vertebrales con respecto a las pacientes del grupo placebo-carbonato de calcio.
Se observaron pocos efectos secundarios13. Garnero y colaboradores estudiaron marcadores óseos de formación y resorción ósea en un subgrupo de pacientes de este estudio y demostraron una rápida normalización de los marcadores de resorción.
Los marcadores de formación alcanzaron los valores de mujeres premenopáusicas al cabo de tres meses de tratamiento14.
En la actualidad se encuentran en estudios de fase III otros bifosfonatos de última generación como el residronato o el tiludronato. El clodronato es de amplia utilización en Europa y su principal indicación es el manejo de la osteolisis y la hipercalcemia tumoral a largo plazo. El pamidronato IV ha demostrado excelentes resultados en el manejo de la enfermedad de Paget de hueso.
Los bifosfonatos deben administrarse siempre con calcio; por lo menos 500 mg de calcio elemental al día.
La tasa de absorción intestinal de estos medicamentos es muy baja. El alendronato debe administrarse en ayunas. No se ha definido bien la duración de estos tratamientos.
El lógico suponer que se prosiga hasta la obtención de una DMO que no se asocie con riesgo elevado de fractura. No hay estudios actualmente en relación con terapia cíclica con el alendronato.
Flúor
Desde hace más de 30 años el flúor se utiliza para el manejo de la osteoporosis tipo l. Su empleo está actualmente aprobado en ocho países europeos.
Con el incremento de la exposición se observa un aumento en el número de osteoblastos, en la velocidad de formación ósea y en la actividad sérica de la fosfatasa alcalina. Los estudios de histomorfometría confirman esta acción formadora de hueso; las dosis altas inducen defectos en la mineralización del hueso.
Las técnicas de medición de la Dmo han permitido el seguimiento de un gran número de pacientes manejados con flúor. Varios estudios prospectivos demostraron un incremento significativo de la DMO vertebral, que oscila entre 4% y 10% por año, en 70% de los pacientes.
Un 25% a un 30% de los pacientes manejados con dosis adecuadas no responden al tratamiento.
El principal objetivo de un tratamiento contra la osteoporosis es la prevención de fracturas. Mamelle y Cols del grupo de Meunier y Lyon (Francia), en un estudio abierto prospectivo con 257 pacientes demostraron después de dos años de tratamiento con 50 mg diarios de fluoruro de sodio (23 mg de flúor elemento), una disminución significativa en la incidencia de fracturas no vertebrales15.
Los estudios de Riggs16 y Kleerekoper, publicados dos años después, han generado una gran controversia durante los últimos años. Estos autores no solamente no demostraron una disminución en el riesgo de nuevas fracturas vertebrales, sino que además encontraron un incremento en la aparición de fracturas periféricas. A diferencia del estudio de los franceses en estudios se administró a los pacientes un tratamiento más prolongado con dosis mayores de flúor elemento (en promedio 38 mg).
Además se administró una presentación de flúor con mayor biodisponibilidad.
El equipo de Riggs de la Clínica Mayo publicó recientemente:
Los resultados del seguimiento durante dos años adicionales de 50 pacientes que habían recibido flúor durante los cuatro años de su estudio.
Concluyen que la administración de dosis de flúor que produzcan un incremento moderado en los niveles séricos de flúor y en la DMO, puede permitir una disminución en la incidencia de fracturas vertebrales de un 30% a un 35%17. El grupo de Charles Pak obtuvo resultados similares mediante la administración de un régimen cíclico de tratamiento18.
El flúor puede inducir efectos secundarios, particularmente gastrointestinales y osteoarticulares, que dependen de la disponibilidad de la sal de flúor administrada y de la dosis.
El porcentaje es mucho menor con la administración de tabletas de fluoruro de sodio con cubierta entérica y/o de liberación prolongada. Los efectos secundarios gastrointestinales ocurren en 10 a 40% de los pacientes y consisten en náuseas, vómito y, con menor frecuencia, sangrado digestivo.
El síndrome doloroso de los miembros inferiores se ha informado en 10 a 50% de los pacientes.
La incidencia de este síndrome es mucho mayor con la administración de monofluorofosfato, otra sal de flúor, que la de fluoruro de sodio.
La dosis diaria nunca debe sobrepasar los 25 mg diarios de flúor elemento (F).
Las tabletas de 25 mg de fluoruro de sodio contienen 11.25 mg de F. La mayoría de los esquemas recomiendan la administración de dos tabletas diarias.
El paciente debe recibir calcio pero éste debe administrarse lejos del flúor ya que inhibe su absorción. El monofluorofosfato en cambio se administra concomitantemente con el calcio.
Este tipo de medicamento no está disponible en nuestro país. En nuestro medio disponemos de grageas que contienen 40 mg de fluoruro de sodio de liberación lenta y con cubierta entérica. Una gragea contiene 18 mg de F.
Es posible que la administración de una gragea al día sea suficiente para el manejo de la osteoporosis tipo l pero no se han realizado estudios con estas dosis. No existen estudios en nuestro medio.
Son múltiples los esquemas de tratamiento propuestos. El más común es el tratamiento continuo. Se han propuesto varios esquemas cíclicos.
La toxicidad se relaciona con los niveles séricos de flúor. El rango terapéutico se sitúa entre 5 y 10 uM/L. Deben monitorizarse los niveles séricos o en orina cada seis meses.
La principal indicación del fluoruro de sodio es la osteoporosis de tipo l. Como contraindicaciones a este tratamiento están el embarazo, la lactancia y la insuficiencia renal. Debe administrarse con precaución en pacientes ancianos. No debe administrarse flúor a niños y a mujeres en edad fértil.
Bibliografía
- 1. Reid IR, Ames RW, Evans MC, Gamble GD, Sharpe SJ. Effect of calcium supplementation on bone loss in postmenopausal women: see comments. N Engl J Med 1993; 328: 460-464.
- 2. Kains JA. Tratamiento de la osteoporosis generalizada con inhibidores de la resorción ósea. En: Kanis JA, de. Osteoporosis. Oxford, Londres: Blackwell Science Ltd. 191-222.
- 3. Gallagher JC. Drug Therapy. Calcium and vitamin D. In: Riggs LB, Melton JK, eds. Osteoporosis Etiology, diagnosis and management. Philadelphia-New York: Lippincot-Raven 371-389.
- 4. Chapuy MC, Arlot ME, DuBoef F et al. Vitamin D and calcium to prevent hip fractures in elderly women. N Engl J Med 1992; 327: 1637-1642.
- 5. Tilyard MW, Spears GF, Thomson J, Dovey S. Treatment of postmenopausal osteoporosis with calcitriol or calcium. N Engl J Med 1992; 326: 357-362.
- 6. Riggs BL, Nelson K. Effect of long term treatment calcitriol on calcium absorption and mineral metabolism in postmenopausal osteoporosis. J Clin Endocrinol Metab 1985; 61: 457-465.
- 7. Overgaard KY, Riis BY, Chistiansen C, Hansen MA. Effect of salmon calcitonin given intranasally on early postmenopausal bone loss. Br Med J 1989; 299: 477-479.
- 8. Reginster JY, Denis D, Devoisy R, Lecant MP et al. Long-term (3 years) prevention of trabecular postmenopausal bone loss with dose intermittent nasal salmon calcitrion. J Bone Miner Res 1994; 9: 69-73.
- 9. Overgaard K. Effect of salcatonin therapy on bone mass and bone turnover in early postmenopausal women: a dose response study. Calcif Tissue Int 1994; 55: 82-86.
- 10. Overgaard K, Hansen MA, Jensen SB, Christiansen C. Effect of salcatonin given intramusculary on bone mass and fracture rats in established osteoporosis: a dose response study. Br Med J 1992; 305: 74-79.
Referencias
- 11. Consensus Development Conference: Prophylaxis and treatment of osteoporosis. Am J Med 1991; 90: 107-110.
- 12. Watts NB, Harris ST, Genant HK et al. Intermittency cyclical etiodronate treatment of postmenopausal osteoporosis. N Engl J Med 1990; 323: 73-79.
- 13. Liberman UA, Weiss SR, Bröli J et al. Effect of oral alendronate on bone mineral density and the incidence of fractures in postmenoapusal osteoporosis. N Engl J Med 1995; 333: 1437-1443.
- 14. Garnero P, Shij WJ, Gineyts E, Karpf DB, Delmas PD. Comparision of new biochemical markers of bone turnover in late postmenopausal osteoporotic women in response to alendronate treatment. J Clin Endocrinol Metab 1994; 79: 1693-1700.
- 15. Mamelle N, Dusan, Martin JL et al. Risk-benefit ratio of sodium fluoride treatment in primary vertebral osteoporosis. Lancet 1988; 2: 361-365.
- 16. Riggs BL, Hodgsen SF, O’Fallon WM et al. Effect of fluoride treatment on the fracture rate in postmenopausal women with osteoporosis. Nwe Engl J Med 1990; 322: 802-809.
- 17. Riggs BL, O’Fallon WM, Lane A et al. Clinical trial of fluoride therapy postmenopausal osteoporotic women: extended observations and additional analysis. J Bone Miner Res 1994; 9: 265-275.
- 18. Pak CYC, Sakhae K, Piziak V et al. Slow-released sodium fluoride in the management of postmenopausal osteoporosis. Ann Intern Med 1994; 120: 625-632.