Resistencia a la insulina: Endocrinología Reproductiva
Resumen
La resistencia a la insulina es una condición patológica donde hay una respuesta disminuida a la insulina lo que lleva a que los tejidos diana no eliminen la glucosa adecuadamente, inhiban la lipolisis, estimulen la síntesis de glucógeno e inhiban la producción de glucosa hepática.
Los tres sitios principales de resistencia a la insulina son el músculo, el hígado y el tejido adiposo.
La presentación clínica de la resistencia a la insulina es variable y depende del subconjunto de resistencia a la insulina presente, la duración de la afección, el nivel de función de las células beta y la propensión del individuo a las enfermedades secundarias debido a la resistencia a la insulina.
El tratamiento está representado en las intervenciones en el estilo de vida con intervención dietética, actividad física y si bien no hay medicamentos aprobados por la FDA para el tratamiento de la resistencia a la insulina, los enfoques generales incluyen: metformina, agonistas del receptor de GLP-1, inhibidores de SGLT2, tiazolinedionas, inhibidores de la DPP-4, terapias con insulina además intervención quirúrgica para personas calificadas con obesidad.
Palabras clave: resistencia a la insulina, glucosa, lipolisis, síntesis de glucógeno, metformina, agonistas del receptor de GLP-1, intervención quirúrgica.
Abstract
Insulin resistance is a pathological condition in which the body experiences a decreased response to insulin. That, in turn, leads to the target tissues not being able to eliminate glucose adequately, inhibiting lipolysis, stimulating glycogen synthesis, and inhibiting hepatic glucose production.
The three main sites of insulin resistance are the muscle, liver, and adipose tissue.
The clinical presentation of insulin resistance is variable and depends on the subset of insulin resistance present, the duration of the condition, the level of beta cell function, and the individual’s propensity for secondary diseases due to resistance to insulin.
Treatment is represented in lifestyle interventions through dietary intervention and physical activity.
While there are no FDA-approved drugs for the treatment of insulin resistance, general treatments include: metformin, GLP receptor agonists -1, SGLT2 inhibitors, thiazolinediones, DPP-4 inhibitors, insulin therapies, as well as surgical intervention for qualified obese patients.
Key words: insulin resistance, glucose, lipolysis, glycogen synthesis, metformin, GLP-1 receptor agonists, surgery.
El páncreas se deriva de dos brotes, dorsal y ventral, que surgen del endodermo distal del intestino proximal y contiene una combinación distintiva de linajes celulares.
El tejido exocrino comprende células acinares que secretan jugo digestivo y un sistema de conductos por el cual el líquido drena al intestino.
La parte endocrina está dispuesta como pequeños islotes de Langerhans, que contienen distintos tipos de células que secretan hormonas en la circulación: células α, glucagón; células β, insulina; células δ, somatostatina; células ε, grelina, y células γ, polipéptido pancreático.1,2
La formación del páncreas humano inicia a los 26 días de gestación con la formación del brote dorsal, seguida por la aparición de dos brotes ventrales a los 30 días.
La yema ventral izquierda retrocede de manera gradual y la yema ventral derecha migra hacia atrás fusionándose con la yema dorsal en la rotación intestinal entre las 6 y 7 semanas de gestación.
El páncreas dorsal da lugar a la mayor parte del páncreas: la parte superior de la cabeza, el istmo, el cuerpo y la cola mientras que la yema ventral derecha da lugar a la parte inferior de la cabeza del páncreas (ver figura 1) .1,2
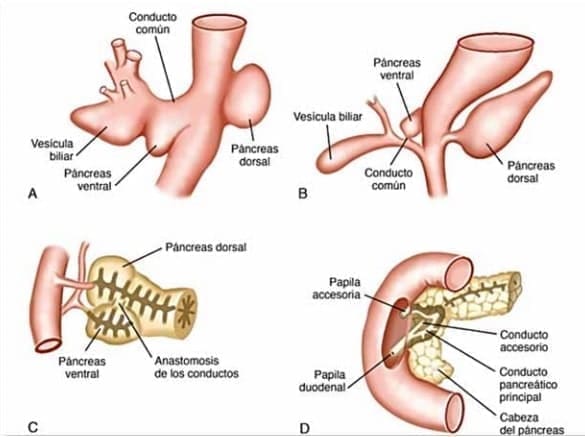
Figura 1. Etapas del desarrollo embrionario del páncreas. A. Aproximadamente a las 4 semanas de gestación se forman las yemas dorsal y ventral desde el duodeno. B. Hacia las 6 semanas, el páncreas ventral se extiende hacia el páncreas dorsal, de mayor tamaño. C. Alrededor de las 7 semanas, se produce la fusión de los páncreas dorsal y ventral y comienza la anastomosis de los conductillos. D. En el nacimiento, el páncreas es un órgano único y la anastomosis de los conductillos es completa.2
Comenzando desde el día 45 hasta el día 47 de gestación, el epitelio pancreático experimenta crecimiento activo y una morfogenia ramificada para dar lugar a células endocrinas y acinares bajo influencia de señales de acción local y activación de factores de transcripción específicos del linaje.
Durante este proceso, el epitelio pancreático se incrusta en el mesénquima suelto y está rodeado por un mesénquima peri pancreático denso. Aproximadamente en las semanas 7-8, el epitelio comienza a ramificarse y a formar un patrón lobular.1
Las primeras células endocrinas que aparecen expresan insulina en la semana 7,5, seguido por la aparición de células que expresan glucagón y somatostatina en la semana 8 y células que expresan polipéptido pancreático y grelina en la semana 9.
La proliferación y la diferenciación de células β en curso dependen de la expresión del factor de crecimiento similar a la insulina de tipo 2 (IGF2).
La formación de islotes comienza en la semana 12 y su volumen aumenta aproximadamente de un 4 a un 13% del tejido pancreático total a término.1
La cinética de la insulina neonatal y la sensibilidad de los órganos terminales a la insulina se establecen durante el tercer trimestre como preparación para el metabolismo del combustible extrauterino.
El entorno materno y el genoma fetal parecen influir en el número y/o función de las células β pancreáticas en los primeros años de vida, con implicaciones de por vida.1
El páncreas endocrino posee una gran reserva funcional.
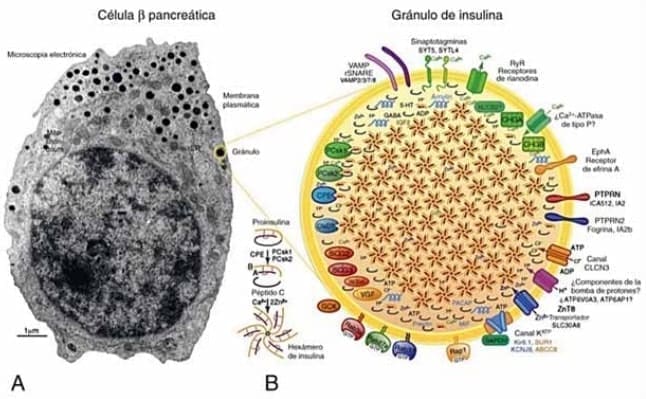
En el citoplasma de las células β, la insulina está empaquetada en 5.000 a 8.000 gránulos secretores distribuidos espacialmente en poblaciones de distintas edades y cada gránulo contiene un núcleo con alta densidad de electrones compuesto por cristales estrechamente empaquetados de hexámeros de insulina estabilizados por un ion calcio y dos iones zinc.
Los gránulos no son solo depósitos de suministro, sino estructuras dinámicas que contienen un gran número de proteínas, pequeñas moléculas y iones en la luz. Así como varías proteínas transmembrana, canales y proteínas asociadas a la membrana.
La reposición y tráfico de gránulos es un proceso altamente regulado en el que intervienen las relaciones con el citoesqueleto, la degradación de insulina intracelular, la movilidad, el empalme y la fusión con la membrana plasmática.
Funcionalmente, como respuesta a la estimulación de glucosa in vitro aguda, se secreta solo una pequeña fracción (muy inferior al 1%) de insulina en gránulos con una semivida inferior a 5 días, donde la degradación intracelular comienza ya en unos 3 días, y los gránulos más jóvenes existen en menor cantidad. Pero poseen más movilidad que los antiguos, aun cuando procedan de la profundidad del citoplasma y, por tanto, forman una reserva fácil de liberar (figura 2).3
Figura 2: A. Micrografía electrónica de una célula β humana. Los cuerpos esféricos con alta densidad electrónica del citoplasma son gránulos de insulina B. Ampliación de un gránulo de insulina para destacar esquemáticamente su compleja estructura: además de hexámeros de insulina, en la membrana de la vesícula y el gránulo se encuentran canales iónicos, transportadores y otras proteínas.13
La insulina es una hormona peptídica endocrina conformada por 51 aminoácidos con un peso molecular de 5808, compuesto por una cadena α y una β, unidas entre sí como un dímero por dos puentes disulfuro con un tercer puente dentro de la cadena α que se une a los receptores unidos a la membrana plasmática en las células diana para orquestar una respuesta anabólica integrada a la disponibilidad de nutrientes.
Esta hormona se produce en las células beta de los islotes pancreáticos como preproinsulina, luego se convierte en proinsulina mediante la escisión de su péptido N-terminal por enzimas microsomales y luego se almacena en cristales unidos a zinc en gránulos secretores después de ser empaquetada por el aparato de Golgi.
La insulina madura es generada por proteasas que residen en las mismas vesículas de almacenamiento junto con la proinsulina.
Por lo tanto, los gránulos secretores unidos a la membrana celular están preparados para la exocitosis de insulina en respuesta a un estímulo circulatorio.4,5
Liberación de insulina
La liberación de insulina es estimulada principalmente por la entrada de glucosa en las células beta hepáticas a través de la difusión facilitada por GLUT-2.
Dentro de las células beta, la glucosa se fosforila a G6P por la actividad de la glucoquinasa, que se considera el «sensor de glucosa», ya que controla la tasa de retención de glucosa en las células beta que, a su vez, controla la tasa de liberación de insulina.
La síntesis de trifosfato de adenosina (ATP) por G6P en las células beta aumenta la relación ATP / difosfato de adenosina (ADP) que, a su vez, cierra los canales de K + sensibles al ATP, despolariza las membranas de las células beta y aumenta los niveles de calcio intracelular al abrir el voltaje de los canales de Ca 2+ regulados.
Los niveles elevados de Ca 2+ intracelular inducen la exocitosis de los gránulos secretores que contienen insulina / proinsulina de las células beta.5
El hígado es el primer órgano que encuentra la insulina a lo largo de su viaje.
Por consiguiente, está expuesto de forma única a concentraciones más altas de insulina que otros tejidos que responden a la insulina, como el músculo y la grasa.
La vena porta libera insulina desde el páncreas al hígado en pulsos discretos que ocurren cada ~5 min, donde la amplitud de estos pulsos de insulina es de 0.5 a 1 nmol / litro en ayunas y se elevan a ~5 nmol / litro después de una comida.
El suministro de insulina pulsátil al hígado es una señal fisiológica importante que regula tanto la acción de la insulina hepática como el aclaramiento de insulina.6
La circulación portal entrega insulina a los capilares de los sinusoides, que no están sostenidos por una membrana basal y sus células endoteliales contienen fenestraciones, que en conjunto permiten el intercambio de contenidos entre la sangre y células hepáticas circundantes.
La estructura única de los sinusoides hepáticos permite que la insulina se difunda fácilmente fuera de la circulación y hacia el espacio perisinusoidal, donde entra en contacto con los hepatocitos.6
Durante este paso, los hepatocitos del hígado eliminan más del 50% de la insulina y la insulina restante sale del hígado a través de la vena hepática, donde sigue la circulación venosa hasta el corazón.
La insulina se distribuye al resto del cuerpo a través de la circulación arterial promoviendo la vasodilatación. Posteriormente la insulina sale de la circulación a nivel de la microvasculatura, llegando a las células musculares y adiposas, donde estimula la translocación de GLUT4 y la captación de glucosa.
La insulina circulante restante es administrada y finalmente degradada por el riñón (figura 3).6
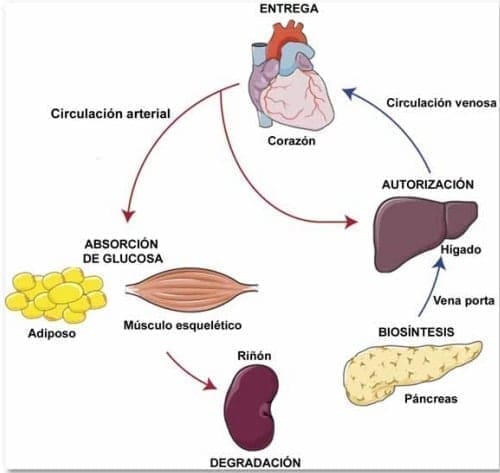
Figura 3: Viaje de la insulina en el cuerpo.6
La insulina ejerce todos sus efectos fisiológicos conocidos al unirse al receptor de insulina en la membrana plasmática de las células diana el cual es un receptor de tirosina quinasa heterotetramérico formado a partir de dos subunidades α extracelulares, que se unen a la insulina, y dos subunidades β que atraviesan la membrana, cada una de las cuales contiene un dominio de tirosina quinasa.
Existen dos isoformas de receptor de insulina, A y B el cual es más específico para la insulina. Es la isoforma primaria expresada en hígado, músculo y el tejido adipocitario blanco diferenciados. Y, por tanto, se cree que media la mayoría de los efectos metabólicos de la insulina.7
La unión de la insulina a las subunidades α de su receptor estimula la actividad tirosina de la subunidad β del receptor:
Esta tirosina quinasa fosforila varias proteínas intracelulares que conducen a la activación de diferentes vías de señalización.
Aunque la vía de la quinasa regulada por señales extracelulares (ERK) participa principalmente en el crecimiento, la activación de la fosfatidilinositol 3-quinasa (PI3K) está involucrada en las acciones metabólicas de la insulina.
Tales acciones están mediadas por la fosforilación catalizada por el receptor de insulina de los sustratos 1 y 2 del receptor de insulina (IRS1, IRS2).
Las proteínas IRS fosforiladas con tirosina luego interactúan y activan PI3K, un jugador crítico en la señalización de la insulina, particularmente con respecto a la homeostasis de la glucosa. PI3K parece facilitar la translocación a la membrana plasmática del transportador de glucosa que responde a la insulina (GLUT4), que reside principalmente en los sitios de almacenamiento intracelular.
El proceso juega un papel crucial en el transporte de glucosa mediado por insulina al músculo esquelético. Pero el vínculo entre PI3K y el transporte de glucosa no se conoce por completo.
Es probable que el mecanismo esté mediado por el reclutamiento y la activación de cinasas dependientes de 3-fosfoinosítidos (PDK) y la fosforilación posterior dependiente de PDK de una serina/treonina cinasa, proteína cinasa B (PKB/AKT).
Aunque AKT tiene varios sustratos, incluidas las isoformas atípicas de la proteína quinasa C (PKC) y la glucógeno sintasa quinasa 3 (GSK3), otro sustrato de 160 kDa (AS160), ha surgido como una molécula adicional importante en la activación del transporte de glucosa en el músculo. AS160 es una proteína que en forma activada previene la translocación de GLUT4 a la membrana.
Es fosforilada e inactivada por AKT de modo que, por inhibición de AS160, la insulina promueve la translocación de GLUT4 desde las vesículas internas, promoviendo la fusión a la membrana plasmática y consecuentemente la captación de glucosa.8
Papel de la insulina en la homeostasis de la glucosa
El papel de la insulina en la homeostasis de la glucosa se caracteriza por los efectos directos de esta sobre el músculo esquelético, el hígado y el tejido adipocitario blanco y la diversidad de las respuestas fisiológicas de la insulina en los diferentes tipos de células se debe en gran parte a distintos efectores distales 4
El músculo esquelético es un tejido que consume energía y toda la energía que almacena el miocito es principalmente para su propio uso. En el músculo esquelético, la insulina le da la indicación de que la glucosa es abundante promoviendo la utilización y el almacenamiento de esta. Aumentando su transporte y además la síntesis neta de glucógeno6.
Lo anterior descrito se debe a una exquisita serie de señales que cooperan para llevar los transportadores de glucosa (isoforma GLUT4) a la superficie celular, proceso conocido como translocación GLUT4.6
La translocación de GLUT4 tiene lugar a los pocos minutos de la unión de la insulina a sus receptores en la superficie de los miocitos y adipocitos y no implica la internalización de la hormona (figura 4).6
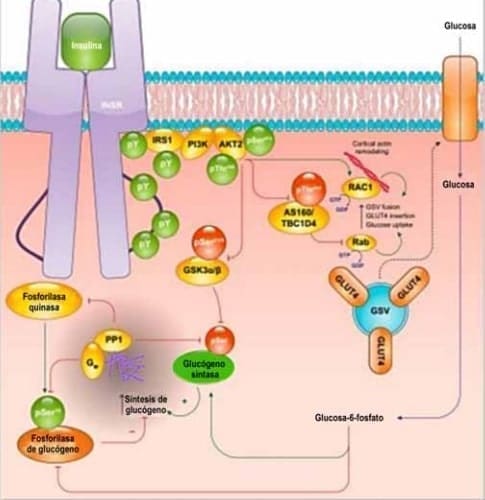
Figura 4: La cascada de señalización de insulina en el músculo esquelético. La activación del receptor de insulina tiene dos funciones metabólicas principales en el miocito esquelético: captación de glucosa y almacenamiento de glucógeno. La estimulación por insulina de la captación de glucosa se produce a través de la translocación de las vesículas de almacenamiento que contienen GLUT4 a la membrana plasmática. El aumento resultante en la producción intracelular de glucosa-6-fosfato, junto con una desfosforilación coordinada de las proteínas metabólicas del glucógeno, permite la síntesis neta de glucógeno. Los círculos y flechas verdes representan eventos de activación; los círculos rojos y las flechas representan eventos inhibitorios. GSK3, glucógeno sintasa quinasa 3; PI3K, fosfoinositido-3-quinasa; PP1, proteína fosfatasa 1.6
En el hígado, la insulina activa la síntesis de glucógeno, aumenta la expresión de genes lipogénicos y disminuye la expresión de genes gluconeogénicos. 4
En el tejido adiposo la insulina es un regulador crítico de prácticamente todos los aspectos de la biología de los adipocitos, y los adipocitos son uno de los tipos de células con mayor respuesta a la insulina.
La insulina promueve las reservas de triglicéridos en los adipocitos mediante una serie de mecanismos, que incluyen el fomento de la diferenciación de preadipocitos en adipocitos y, en los adipocitos maduros, estimulando el transporte de glucosa y la síntesis de triglicéridos (lipogénesis). Así como inhibiendo la lipólisis (figura 5).
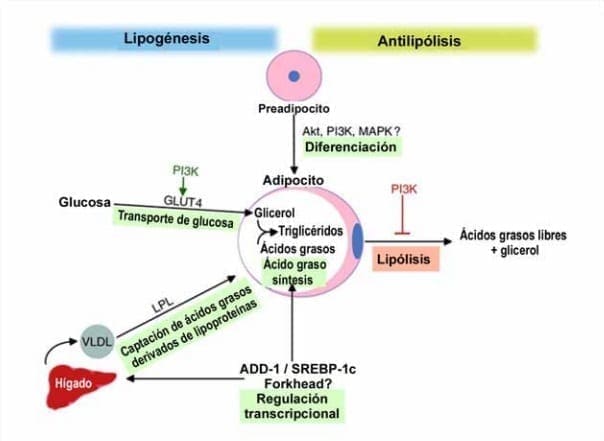
Figura 5: Efectos pleiotrópicos de la insulina para promover el almacenamiento adiposo. La insulina estimula la diferenciación de preadipocitos en adipocitos. En los adipocitos, la insulina promueve la lipogénesis estimulando la captación de glucosa y ácidos grasos derivados de lipoproteínas e induciendo ADD-1 / SREBP-1c, que regula los genes que promueven la síntesis de ácidos grasos y la lipogénesis, no solo en los adipocitos sino también en los hepatocitos. La insulina también puede regular la transcripción a través de factores de transcripción de Forkhead. La insulina disminuye la degradación de los triglicéridos al inhibir la lipólisis. Muchas de estas vías metabólicas están reguladas por la vía de señalización PI3K.9
La insulina también aumenta captación de ácidos grasos derivados de las lipoproteínas circulantes al estimular la actividad de la lipoproteína lipasa en el tejido adiposo.
Los efectos metabólicos de la insulina están mediados por una amplia gama de acciones específicas de tejido que implican cambios rápidos en la fosforilación y función de las proteínas. Así como cambios en la expresión génica.9
La insulina también activa la cascada de señalización de la proteína quinasa activada por mitógenos ras (ras-MAPK).
Esta vía parece ser importante para los efectos mitogénicos de la insulina. Pero la mayoría de los datos no implican a la vía MAPK en las acciones metabólicas bien estudiadas de la insulina.
La acción de la insulina en los adipocitos adicionalmente implica cambios en la transcripción de genes, al inducir genes implicados en la lipogénesis y reprimir a los implicados en la oxidación de ácidos grasos.
Los factores de transcripción de la familia forkhead también pueden desempeñar un papel importante en la transducción de señales de insulina al núcleo.9
El término «resistencia a la insulina» hace referencia a una situación patológica donde hay una respuesta disminuida a la estimulación de la insulina lo que hace que los tejidos diana no eliminen adecuadamente la glucosa en sangre, inhiban la lipolisis, estimulen la síntesis de glucógeno e inhiban la producción de glucosa hepática.
Tradicionalmente visto como una respuesta compensatoria, la secreción de insulina aumenta y conduce a hiperinsulinemia.10
Estos defectos pueden ser reversibles con pérdida de peso, ejercicio y dietas nutricionales adecuadas. Sin embargo, si se deja sin oposición, la resistencia a la insulina es un evento precursor que probablemente contribuya a la disfunción de las células β. 10
Existen múltiples mecanismos moleculares que pueden producir resistencia a la acción fisiológica de la insulina:
Como los defectos prerreceptor (alteración en la molécula de insulina) y la existencia de receptores anómalos para la insulina (por mutaciones genéticas).
Sin embargo, las formas frecuentes de resistencia a la insulina asociadas a la diabetes de tipo 2 suelen deberse a defectos postreceptor, es decir, alteraciones en la transmisión de señales intracelulares.
En los tejidos diana de la insulina, la transmisión de señales a través de la vía de fosfatidilinositol 3-cinasa es responsable de la translocación del transportador de glucosa GLUT4, que es necesario para que la célula capte la glucosa.
Se han descrito varios defectos en esta vía en pacientes con resistencia a la insulina, entre otras alteraciones en el sustrato 1 del receptor de insulina y la proteína cinasa B/Akt2.
Se han identificado algunas mutaciones genéticas específicas asociadas a la resistencia a la insulina. Pero esta puede ser adquirida como consecuencia de la obesidad, el aumento de las concentraciones de ácidos grasos libres circulantes, algunos fármacos (glucocorticoides, niacina) y estados inflamatorios.11
Sitios principales de resistencia a la insulina
Los tres sitios principales de resistencia a la insulina son el músculo, el hígado y el tejido adiposo y se postula que la resistencia a la insulina comienza en el tejido muscular con un cambio inflamatorio inmunomediado y un exceso de ácidos grasos libres, lo que provoca el depósito de lípidos ectópicos.
El músculo representa hasta el 70% de la eliminación de glucosa.
Con la captación muscular deficiente, el exceso de glucosa regresa al hígado aumentando la lipogénesis de novo (DNL) y los ácidos grasos libres circulantes, lo que contribuye aún más a la deposición de grasa ectópica y la resistencia a la insulina.12
La evaluación epidemiológica de la resistencia a la insulina se mide típicamente en relación con la prevalencia del síndrome metabólico o síndrome de resistencia a la insulina y desde un punto de vista demográfico, la resistencia a la insulina afecta a todas las razas con datos limitados sobre las comparaciones entre diferentes grupos raciales.12
En cuanto a los factores de riesgo para la resistencia a la insulina, junto con el sobrepeso o la obesidad o llevar un estilo de vida sedentario, numerosos componentes genéticos pueden aumentar las posibilidades de que ocurra, y existen algunas circunstancias particulares correlacionadas con la resistencia a la insulina.12,14
Factores de riesgo |
|
45 años |
Presencia de sobrepeso u obesidad
La presencia de sobrepeso u obesidad aumenta de forma importante el riesgo de diabetes tipo 2 y posiblemente explique el incremento de la prevalencia de diabetes durante las últimas décadas.
De hecho, la presencia de sobrepeso u obesidad es el predictor clínico aislado más importante de diabetes tipo 2, sobre todo en individuos jóvenes o de mediana edad.
La relación entre el IMC y la diabetes tipo 2 es lineal, y se puede observar un aumento del riesgo incluso dentro del rango de valores del IMC considerado normal (< 25 kg/m 2).
Los factores relacionados, como la vida sedentaria y la dieta (aumento del consumo de alimentos de alta carga glucémica y de grasas trans y saturadas), pueden también contribuir al riesgo de diabetes independientemente del IMC.
La distribución de la grasa corporal también juega un importante papel, y la obesidad visceral (que se mide con el perímetro de la cintura y el cociente entre cintura y cadera) es un factor de riesgo de diabetes especialmente importante en las poblaciones asiáticas, que tienden a desarrollar diabetes tipo 2 con valores de IMC inferiores a otros grupos raciales o étnicos.
La acumulación ectópica de tejido adiposo en el hígado, que se suele manifestar como esteatosis hepática no alcohólica, se asocia también de forma importante a un aumento del riesgo de diabetes.11
El aumento de la masa de tejido adiposo altera la acción de la insulina a través de una serie de mecanismos:
Entre los que se incluyen la alteración del metabolismo de los ácidos grasos, la acumulación de triglicéridos en el hígado y la inflamación sistémica de baja intensidad.
Los macrófagos del tejido adiposo producen citocinas proinflamatorias, entre las que se incluyen el factor de necrosis tumoral α y la interleucina 6, que pueden interferir en la transmisión de señales por la insulina.11
La obesidad se asocia también a una menor concentración del péptido derivado de la grasa, adiponectina, que tiene una actividad antiinflamatoria y sensibilizadora a la insulina.
El aumento de los ácidos grasos libres circulantes característico del obeso puede interferir en la acción de la insulina en el músculo esquelético y el hígado, y el incremento de los lípidos dentro de las células musculares se asocia también a resistencia a la insulina.
Además, el aumento de la acumulación de lípidos en los islotes pancreáticos también puede alterar la secreción de insulina.
Es interesante que algunos obesos muestran una sensibilidad a la insulina y un metabolismo de la glucosa aparentemente normales. Lo que se denomina a veces la paradoja de la obesidad.
Los mecanismos que protegen a algunas personas de los efectos diabetógenos del exceso de grasa se desconocen. Pero un buen estado cardiorrespiratorio puede tener influencia.11
Entre los principales factores etiológicos en la patogénesis de la resistencia a la insulina se encuentra:
El efecto de la lipotoxicidad que corresponde a un tipo de estrés celular inducido por la acumulación de intermediarios lipídicos como diacilgliceroles (DAG), ceramidas y triglicéridos que facilitan el desarrollo de resistencia a la insulina en los músculos, el hígado y el tejido adiposo.
Además, en el músculo esquelético, la sobreabundancia de ácidos grasos intermedios impide la señalización de la insulina a través de la reducción de los transportadores GLUT4 en la superficie de la membrana del miocito.
En otros tejidos como el hígado, la acumulación de triglicéridos intrahepáticos (IHTG) y el eje DAG – PKC ε se han relacionado con la patogenia de la resistencia a la insulina hepática.
En cuanto al tejido adiposo, se ha teorizado que un aumento de la lipólisis, gobernado por una cascada similar que se encuentra en el tejido esquelético y hepático, es la causa de resistencia a la insulina (figura 6).10

Figura 6. Posibles mecanismos que conducen a la resistencia a la insulina. (a) una mayor producción de especies oxidativas reactivas (ROS). Los ROS son subproductos necesarios del metabolismo energético mitocondrial; sin embargo, si su producción no está adecuadamente acoplada por antioxidantes intracelulares, puede ocurrir daño oxidativo al ADN mitocondrial (ADNmt). (b) El deterioro de la oxidación de la glucosa y la oxidación de los ácidos grasos puede deberse a la inflexibilidad metabólica. En última instancia, estos eventos pueden conducir tanto al desarrollo de ROS como a la acumulación de lípidos ectópicos, resultando en daño mitocondrial y eliminación a través de vías de mitofagia. Una mayor investigación sobre los genes implicados en la mitofagia (es decir, Bnip3, Nix, Fundc1) puede permitir el descubrimiento de vías que expliquen la correlación entre la disfunción mitocondrial y la resistencia a la insulina en el tejido muscular adiposo, hepático y esquelético. (c) El estrés del retículo endoplásmico (RE) también está involucrado en la patogénesis de la disfunción mitocondrial. La lipotoxicidad y la glucotoxicidad pueden inducir estrés en el RE, que puede desencadenar una vía de señalización adaptativa, conocida como respuesta de proteína desplegada (UPR). Si el estrés del RE no se alivia con esta UPR, entonces esto puede conducir a la provocación de vías de muerte celular tanto dependientes como independientes de las mitocondrias. Juntos, la capacidad de las mitocondrias para responder a las alteraciones metabólicas es esencial para una bioenergética celular saludable, y la interferencia con este proceso puede provocar una biogénesis mitocondrial y mitofagia no reguladas, contribuyendo así a la resistencia a la insulina. 10
La flexibilidad metabólica se describe como la capacidad de un organismo para adaptar la oxidación del combustible a la disponibilidad de combustible.
En consecuencia, la inflexibilidad metabólica se caracteriza por un cambio de combustible deficiente y una desregulación energética, conceptos que están estrechamente asociados con la resistencia a la insulina y la enfermedad cardio metabólica.
La capacidad de cambio de combustible disminuida puede resultar en la acumulación de lípidos intramiocelulares (IMCL). Así como la activación de DAG – PKC θ y el deterioro de las vías proximales de señalización de la insulina.
Este último, en última instancia, altera la señalización de la insulina a través de diferentes mecanismos, ya sea un aumento de la fosforilación de serina de IRS1 en Ser – 1101 y / o una reducción de la fosforilación de serina de PKB / Akt.10
En respuesta a un exceso de disponibilidad de ácidos grasos, los transportadores de ácidos grasos pueden limitar la absorción de ácidos grasos celulares y mitocondriales. Reduciendo así la oxidación de grasas y aumentando la acumulación de metabolitos lipotóxicos, lo que contribuye a la aparición de resistencia a la insulina.
En última instancia, los defectos en el cambio de combustible pueden intensificarse con un contenido y/o funciones mitocondriales deficientes, lo que contribuye aún más a la resistencia a la insulina y la disfunción mitocondrial (figura 6).10
Resistencia a la insulina en el músculo esquelético
Una de las primeras teorías propuestas para explicar los mecanismos de la resistencia a la insulina muscular fue postulada por Randle y colegas en la década de 1960, donde concluyeron que un aumento agudo de la oxidación de los ácidos grasos musculares conduce a acumulación de citrato, que inhibe la fosfofructoquinasa (PFK), enzima fundamental en la glucólisis, dando como resultado el deterioro de la utilización de la glucosa.
Otros estudios han elaborado más que la reducción de la síntesis de glucógeno muscular estimulada por la insulina y la oxidación de la glucosa pueden impulsar la resistencia crónica a la insulina.
Sin embargo, estudios en humanos que evalúan la función de GLUT4 han sugerido que la activación fallida de la cascada de señalización de INSR y la translocación alterada de GLUT4 es el defecto principal en la resistencia a la insulina del músculo esquelético.
Además, en pacientes con diabetes tipo 2, se informó que la fosforilación de tirosina de IRS1 estaba gravemente afectada como consecuencia de la hiperglucemia.
Por lo tanto, los defectos en el nivel proximal de la señalización de la insulina que involucran las vías INSR, IRS1, PI3K y Akt son más evidentes en la resistencia a la insulina del músculo esquelético, lo que resulta en una disminución en la captación de glucosa estimulada por insulina.10
Exposición a los lípidos del músculo esquelético
En cuanto a las teorías modernas, estas sostienen que la exposición a los lípidos del músculo esquelético es una de las principales causas de resistencia a la insulina del músculo.
Las infusiones de lípidos en humanos dieron como resultado un aumento en la señalización de DAG y PKCθ, lo que altera la fosforilación de tirosina de la activación de IRS1.
Como IRS1 es el activador principal de PKB / Akt, la inhibición de esta vía bloquea los eventos en cascada de señalización de la insulina y previenen la captación de glucosa estimulada por la insulina en el músculo esquelético.10
Otro mecanismo propuesto implica la presencia de aminoácidos de cadena ramificada (BCAA), ya que se demostró que estos están elevados en pacientes obesos con DM2.
De manera similar, estudios en animales y humanos han demostrado que la infusión de aminoácidos provocó un deterioro de la captación de glucosa del músculo esquelético.
Los mecanismos de los BCAA no están claros. Pero se ha relacionado con la lipotoxicidad que conduce a la resistencia a la insulina.10
Las teorías recientes sostienen que la acumulación excesiva de β-oxidación y de acilcarnitina en las mitocondrias está relacionada con el desarrollo de resistencia a la insulina muscular.
En este entorno desequilibrado de β-oxidación excesiva, las mitocondrias se vuelven más susceptibles a la acumulación de acil-CoAs y acilcarnitina, lo que posiblemente contribuya a la insuficiencia mitocondrial.10
Las matrices de expresión génica realizadas en biopsias de músculos humanos encontraron:
Una serie de genes involucrados en el metabolismo oxidativo estaban regulados a la baja en pacientes con diabetes tipo 2.
Esta incapacidad para cambiar la oxidación del combustible por la disponibilidad de nutrientes probablemente contribuya a la resistencia a la insulina.10
Finalmente, evidencia actual sugiere que la inflamación ocurre en el músculo esquelético en la obesidad, caracterizada por una mayor infiltración de células inmunes y activación proinflamatoria en el tejido intermiocelular.
Los niveles elevados de citocinas como TNF α e IL – 1α activan las vías PKC, JNK e IKK / NF – κB en los miocitos y pueden afectar la señalización de la insulina a través de la fosforilación de serina o treonina, que interrumpe la fosforilación de tirosina estimulada por insulina de IR o IRS.10
Resistencia a la insulina en el hígado:
Los estudios sugieren que la desregulación de FOXO1 contribuye a un aumento de la gluconeogénesis hepática en humanos con DM2. FOXO1 aumenta la producción de enzimas necesarias para la gluconeogénesis. Por lo que su regulación positiva da como resultado una mayor conversión de sustrato en glucosa hepática.10
Evidencia reciente sugirió que la PGC 1α hepática baja en pacientes con DM2 también se asocia con resistencia a la insulina hepática. PGC 1α impulsa la proporción de IRS1 e IRS2 en los hepatocitos, y los niveles bajos de la misma dieron como resultado la interrupción de la expresión de IRS1 y 2 que afecta la homeostasis normal de la glucosa.10
Como la insulina también juega un papel en el metabolismo de los lípidos a través de SREBP – 1C, las personas resistentes a la insulina pueden presentar una lipogénesis disminuida. Como se muestra en modelos animales de resistencia a la insulina hepática, hay una disminución en el DNL.10
La acumulación de lípidos ectópicos en el músculo o el hígado es consecuencia de un estado de sobrealimentación o de un metabolismo defectuoso de los ácidos grasos de los adipocitos.
Como resultado, esto conduce a la activación del eje DAG – PKCε en el hígado y la posterior inhibición de la señalización de INSR a través de la fosforilación de INSR en Thr1160).
Alternativamente, también se ha demostrado que las ceramidas activan una isoforma PKCζ (Zeta) atípica y median la resistencia a la insulina hepática.
Por lo tanto, algunas de las principales consecuencias de este estado de resistencia a la insulina inducida por lipotoxicidad son la alteración de la estimulación de la síntesis de glucógeno hepático por insulina, la alteración de la regulación positiva de los genes de transcripción de DNL y la alteración de la regulación negativa de los genes de transcripción gluconeogénica.
Es importante destacar que en el hígado, la resistencia a la insulina originada por lipotoxicidad no tiene relación con la capacidad mitocondrial deteriorada, que se ha atribuido a una adaptación mitocondrial para promover una mayor lipólisis.10
Resistencia a la insulina en el tejido adiposo
El tejido adiposo es un regulador esencial de la salud en general. Por tanto, la función deteriorada del mismo puede conducir a una serie de graves complicaciones de salud global como resistencia a la insulina, DM2, entre otras enfermedades metabólicas.9
Los mecanismos por los cuales la activación del tejido adiposo conduce a la resistencia a la insulina dependen de la activación de las citocinas.
Las citocinas inflamatorias, como el factor de necrosis tumoral (TNF) α, la interleucina – 1 beta y la 6 (IL – 1β, IL – 6), aumentan en los seres humanos y roedores diabéticos obesos y la neutralización de el TNF – α mejora la sensibilidad a la insulina en roedores obesos.
Además, se ha demostrado que el TNF-α induce la fosforilación de la serina del IRS-1, disminuyendo así su asociación con PI3K e impidiendo la señalización de la insulina.
Además, los mediadores inflamatorios, TNF o IL -1β aumentan la lipólisis e inhiben INSR. Por lo tanto, la alteración de la señalización de la insulina. Estos hallazgos sugieren que la resistencia a la insulina inducida por la obesidad puede resultar parcialmente de un desequilibrio en la secreción de adipocinas proinflamatorias y antiinflamatorias.10
La supresión de la lipólisis junto con una disminución en la captación de triglicéridos, como se observa en presencia de niveles elevados de insulina, puede aumentar aún más los efectos deletéreos de la acumulación de lípidos ectópicos.
Se cree que la hiperinsulinemia, o secreción excesiva de insulina, causa resistencia a la insulina, a través de mecanismos desconocidos. La hiperinsulinemia se asocia con un exceso de adiposidad.
Posteriormente, las manipulaciones dietéticas y farmacológicas que reducen la insulina pueden conducir a una reducción del tejido adiposo y una mayor sensibilidad a la insulina, aunque los resultados de tales intervenciones han sido mixtos (figura 7).10
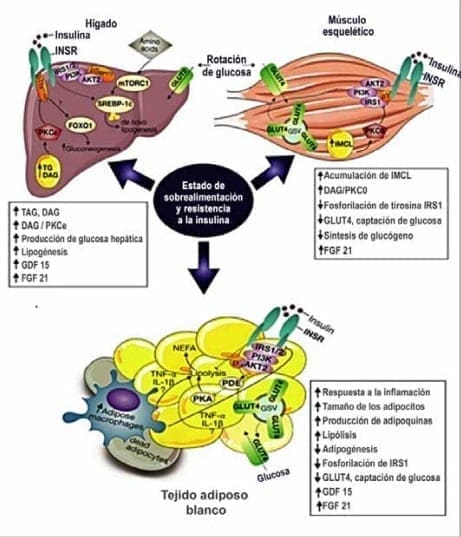
Figura 7. Mecanismos de resistencia a la insulina muscular y la intercomunicación con el hígado y el tejido adiposo.10
La presentación clínica de la resistencia a la insulina es variable y depende del subconjunto de resistencia a la insulina presente, la duración de la afección, el nivel de función de las células beta y la propensión del individuo a las enfermedades secundarias debido a la resistencia a la insulina.
Las presentaciones incluyen: pacientes asintomáticos con obesidad, hipertensión o hiperlipidemia, aquellos con síndrome metabólico, prediabetes o diabetes mellitus tipo 2, aquellos con enfermedad microvascular sintomática (retinopatía, neuropatía o nefropatía), aquellos con enfermedad macrovascular (accidente cerebrovascular, PAD y CAD), aquellos con SOA, aquellos con resistencia a la insulina tipo A o tipo B, presión sanguínea elevada, aumento de la circunferencia de la cintura en función del género y la raza, aquellos con xantelasma o xantomas, los estigmas del SOA (irregularidades menstruales, hirsutismo, acné y alopecia), acantosis nigricans, una pigmentación parda aterciopelada irregular alrededor de la axila del cuello y las regiones de la ingle, los estigmas de uno de varios síndromes genéticos que incluyen la resistencia a la insulina.14
La resistencia a la insulina y la hiperinsulinemia compensadora juegan un papel importante en la patogenia del SOA.
El SOA parece ser un estado en el que los tejidos esteroidogénicos y adiposos son paradójicamente sensibles a la insulina en un estado de resistencia general a los efectos metabólicos de la glucosa.
Se han descrito distintos defectos de unión al postreceptor en la señalización de la insulina en fibroblastos, adipocitos y células del músculo esquelético en el síndrome de ovario androgénico.
Estos defectos están específicamente asociados con la síntesis de glucógeno y la captación de glucosa deficientes y no involucran la señalización mitogénica.
En contraste con el músculo esquelético y los fibroblastos de la piel, no hay evidencia de defectos intrínsecos en la señalización de la insulina en el linaje de células adiposas del SOA, aunque no se puede excluir la posibilidad de que el entorno in vivo ejerza efectos.14
La relación entre la resistencia a la insulina y el hiperandrogenismo parece resultar principalmente del efecto de la hiperinsulinemia compensadora sobre la esteroidogénesis.
En el ovario, la insulina actúa junto con la LH para regular al alza la unión de la LH y potenciar la respuesta androgénica a la LH. La evidencia clínica indica uniformemente que la esteroidogénesis en el SOA procede como si fuera sensible a la insulina.
La insulina puede actuar a través de su propio receptor en las células de la teca, mediante una vía de señalización separada de la que media sus efectos metabólicos. Los estados resistentes a la insulina también suprimen la SHBG, lo que aumenta la biodisponibilidad de la testosterona.14
En una minoría de estudios se ha informado que el exceso de andrógenos causa resistencia a la insulina in vitro.
En uno de ellos, altas dosis de andrógenos indujeron resistencia a efectos de la insulina como la estimulación de la captación de glucosa en adipocitos cultivados de mujeres normales. El tratamiento con el antiandrógeno flutamida durante 12 meses redujo significativamente la masa grasa visceral y mejoró la sensibilidad a la insulina.14
Los andrógenos pueden contribuir indirectamente a la resistencia a la insulina. Se ha pensado que la grasa visceral, que se caracteriza por una mayor actividad lipolítica, es importante para la patogénesis de la resistencia a la insulina del SOA y subyace al aumento de los niveles de ácidos grasos libres.
Los ácidos grasos libres provocan resistencia a la insulina en el músculo esquelético.
Así, se ha especulado que la hiperandrogenemia puede afectar la sensibilidad a la insulina de los adipocitos de tal manera que favorezca la distribución de la grasa corporal visceral, lo que resulta en aumentos relativos de ácidos grasos libres, que, a su vez, inducen resistencia a la insulina del músculo esquelético (figura 8).14
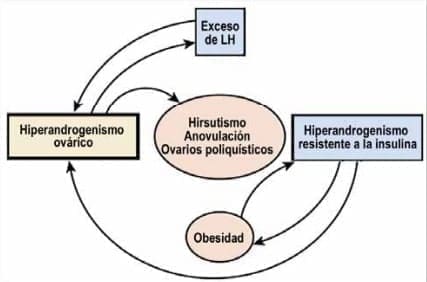
Figura 8. El hiperandrogenismo ovárico es casi universal y causa las características clínicas cardinales del síndrome. Aproximadamente la mitad de los pacientes tienen hiperinsulinismo resistente a la insulina, que agrava el hiperandrogenismo ovárico y contribuye a la adiposidad. El exceso de andrógenos también puede causar un exceso de LH, que agrava el hiperandrogenismo ovárico en presencia de hiperinsulinismo. La obesidad aumenta la resistencia a la insulina y el aumento del hiperinsulinismo resultante agrava aún más el hiperandrogenismo. 14
La acantosis nigricans es una manifestación cutánea de una afección subyacente. Suele desarrollarse en los pliegues cutáneos, como la nuca, la axila y la ingle, donde se presenta como placas aterciopeladas hiperpigmentadas con bordes poco definidos. La acantosis nigricans se asocia más comúnmente con diabetes y resistencia a la insulina.15
Hay múltiples factores involucrados en el desarrollo de la acantosis nigricans.
- Aumento de la insulina circulante que activa los receptores del factor de crecimiento similar a la insulina de los queratinocitos, en particular el IGF-1. A altas concentraciones, la insulina puede desplazar al IGF-1 de la proteína de unión a IGF. El aumento de IGF circulante puede conducir a la proliferación de queratinocitos y fibroblastos dérmicos.
- Las variantes hereditarias están asociadas con defectos del factor de crecimiento de fibroblastos.
- El aumento del factor de crecimiento transformante (TGF) parece ser el mecanismo de la acantosis nigricans asociada a malignidad. El TGF actúa sobre el tejido epidérmico a través del receptor del factor de crecimiento epidérmico.
La acantosis nigricans se diagnostica clínicamente y se confirma con una biopsia de piel. En la biopsia se puede observar hiperqueratosis, infiltración de leucocitos, plegamiento epidérmico y proliferación de melanocitos.
El diagnóstico se centra en descartar la malignidad. Dado que la gran mayoría de los casos están asociados con la resistencia a la insulina y / o la obesidad, se recomienda la detección de diabetes y la medición de la hemoglobina glicosilada.15
Valoración de la resistencia a la insulina
Se cuenta con una serie de métodos directos e indirectos que permiten realizar una medición cuantitativa del efecto biológico de la insulina endógena o exógena en relación con niveles de glucosa sanguínea.
Métodos directos:
- Clamp hiperinsulinémico-euglucémico: Es el estándar de oro para la medición de la resistencia a la insulina. Demuestra resistencia a la acción de la insulina principalmente en los tejidos periféricos (menor capacidad de estimular la captación de glucosa en el músculo y la grasa). Pero también en el hígado (menor capacidad de la insulina de suprimir la producción de glucosa hepática). Se suministra a un paciente una infusión constante de insulina para producir hiperinsulinemia. Al mismo tiempo, se suministra una segunda infusión que contiene glucosa y se ajusta para producir euglucemia. En este procedimiento la insulinemia se incrementa agudamente a un nivel de 100 uUI/ml, y el nivel de glucosa basal se mantiene constante mediante una infusión continua de glucosa. Es una prueba compleja que se reserva principalmente para fines de investigación y rara vez se realiza en entornos clínicos.12
- Modelo mínimo de Bergman: comúnmente usado para analizar resultados de tolerancia de glucosa en humanos y animales de laboratorio. El método más utilizado es proporcionar una dosis de glucosa a un paciente de manera intravenosa, durante un periodo de 60 segundos, y los niveles de glucosa e insulina se registran. 16
- Test de supresión de la insulina: infusión continua de acetato de octreotide (0.27 μg/m2/min) para bloquear la secreción endógena de insulina (en la versión original se usaba propanolol + epinefrina), insulina (32 mU/m2/min) y glucosa (267 mg/m2 /min) por 180 minutos. Se toman muestras de sangre cada 30 minutos 21 hasta los 150 minutos para monitorear la glucosa y luego cada 10 minutos hasta los 180 minutos para medir insulina adicionalmente. La medición de la glucosa los últimos 30 minutos en estado estable es una medida de la sensibilidad tisular a la insulina exógena. Los que tienen valores mayores tienen resistencia a la insulina.16
Métodos indirectos:
Estos métodos prescinden de la infusión de glucosa o insulina. Pueden estimarse de una sola muestra de glucosa o de los resultados de la prueba de sobrecarga oral a la glucosa.
Estos índices están basados en la determinación de insulina plasmática.17
- La medición de insulina plasmática es el estimador más fácil de obtener y usar. Un valor de > 20.7 uUI/ml indica resistencia a la insulina, corroborado con el clamp euglicémico con una sensibilidad y especificidad de 84.9 % y 78.7 %, respectivamente. Lamentablemente, el ensayo para la determinación de insulina no está estandarizado, sino que varía entre los diferentes laboratorios, y por radioinmunoensayo se incluye en la determinación proinsulina.18
- El logaritmo de la recíproca de la concentración de insulina tiene una correlación de 0.88 con el índice de sensibilidad a la insulina calculado por el método de Bergman.18
- El índice de Raynaud, usado en personas no diabéticas, presenta un r = 0.88 con el índice de sensibilidad a la insulina calculado con el método de Bergman.18
- La relación glucosa/insulina tiene una correlación de 0.73 con el SI del método de Bergman. Un valor < 4.5 tiene una sensibilidad de 95 % y especificidad de 84 % para el diagnóstico de resistencia a la insulina.18
- El índice Quicki desarrollado en sujetos normales y diabéticos tiene un r = 0.73 con el índice de sensibilidad calculado con el clamp euglicémico hiperinsulinémico. Se define como 1/(log insulina ayunas [μU/ ml] + log glucosa en ayunas [mg / dl]).19,20
- El índice de HOMA-IR es uno de los más usados y de mayor utilidad en no diabéticos. Tiene un r = 0.88, p < 0.0001, con respecto al IS del clamp. Se define como insulinemia (μU/ml) x glucemia (mmol/ l)/22,5.20
- Índice de Matsuda: Tiene un r = 0.77 con el clamp euglicémico hiperinsulinémico. Un valor menor de 2.5 es indicativo de resistencia a la insulina. Un valor normal es > 1.21 Teste de Speroff: insulina basal, insulina 2 horas post 75 gs glucosa oral. Valores < 20 y menor de 100 UI/l repectivamente. Sensibilidad 88% y especificidad 90% respectivamente.
- El índice de sensibilidad a la insulina (glicémico) ha tenido una limitada aplicación.19
Manejo
La piedra angular del tratamiento está representada en las intervenciones en el estilo de vida. La intervención dietética debe incluir una combinación de restricción calórica y reducción de carbohidratos de alto índice glucémico.
Adicionalmente la actividad física mejora el gasto calórico y la sensibilidad a la insulina en el tejido muscular. El Programa de Prevención de la Diabetes y su Estudio de Resultados (DPP & DPPOS) demostraron que la intervención en el estilo de vida era una intervención significativa y rentable.
Si bien no hay medicamentos aprobados por la FDA para el tratamiento de la resistencia a la insulina, los enfoques generales incluyen:
- Metformina: considerada terapia de primera línea para el tratamiento con medicamentos de la DM2 y aprobada para su uso en el SOA. El estudio DPP/DPPO mostró que la adición de metformina y las intervenciones en el estilo de vida combinadas eran médicamente útiles y rentables.
- Agonistas del receptor de GLP-1 estimulan los receptores de GLP-1 en el páncreas, aumentando así la liberación de insulina e inhibiendo la secreción de glucagón. El uso de agonistas de GLP-1 se asocia con la pérdida de peso, lo que puede reducir la resistencia a la insulina.
- Inhibidores SGLT2: aumentan la excreción de glucosa urinaria, reduciendo así los niveles de glucosa plasmática y los requerimientos de insulina exógena. El uso de inhibidores de SGLT2 también se ha asociado con la pérdida de peso, lo que puede reducir la resistencia a la insulina.
- Tiazolidinedionas: mejoran la sensibilidad a la insulina al aumentar la eliminación de glucosa dependiente de insulina en el tejido muscular y adiposo. Así como al disminuir la producción de glucosa hepática. Uso limitado por aumento de peso secundario, retención de líquidos y alteraciones cardiovasculares asociados al uso.
- Inhibidores de la DPP-4 prolongan la actividad del GLP-1 endógeno y del polipéptido inhibidor gástrico (GIP) al prevenir su degradación. Para personas en terapia con insulina:
- El uso de preparaciones de insulina concentrada cuando se requieren grandes dosis (más de 200 unidades por día) de insulina para mejorar la tolerancia y la absorción.
Cirugía
La intervención quirúrgica en forma de manga gástrica, banda y bypass está disponible para personas calificadas con obesidad. La pérdida excesiva de grasa asociada con la cirugía bariátrica mejora la sensibilidad a la insulina.22,23,24
Bibliografía – Resistencia a la Insulina
- Gleason, Christine A., and Sandra E. Juul, eds. Avery. Enfermedades del recién nacido. Elsevier Health Sciences, 2018.
- Feldman, Mark, Lawrence S. Friedman, and Lawrence J. Brandt, eds. Sleisenger y Fordtran. Enfermedades digestivas y hepáticas: fisiopatología, diagnóstico y tratamiento. Elsevier Health Sciences, 2017.
- Melmed, Shlomo, ed. Williams. Tratado de endocrinología. Elsevier Health Sciences, 2021.
- Petersen, Max C., and Gerald I. Shulman. «Mechanisms of insulin action and insulin resistance.» Physiological reviews 98.4 (2018): 2133-2223.
- Yaribeygi, Habib, et al. «Insulin resistance: Review of the underlying molecular mechanisms.» Journal of cellular physiology 234.6 (2019): 8152-8161.
- Tokarz, Victoria L., Patrick E. MacDonald, and Amira Klip. «The cell biology of systemic insulin function.» Journal of Cell Biology 217.7 (2018): 2273-2289.)
- Belfiore, Antonino, et al. «Insulin receptor isoforms in physiology and disease: an updated view.» Endocrine reviews 38.5 (2017): 379-431.
- Di Meo, Sergio, Susanna Iossa, and Paola Venditti. «Skeletal muscle insulin resistance: role of mitochondria and other ROS sources.» Journal of Endocrinology 233.1 (2017): R15-R42.
- Kahn, Barbara B., and Jeffrey S. Flier. «Obesity and insulin resistance.» The Journal of clinical investigation 106.4 (2000): 473-481
- da Silva Rosa, Simone C., et al. «Mechanisms of muscle insulin resistance and the cross?talk with liver and adipose tissue.» Physiological Reports 8.19 (2020): e14607.
- Ausiello, Dennis Arthur, and Lee Goldman. Cecil Tratado de medicina interna. Elsevier España, 2009.
- Freeman, Andrew M., and Nicholas Pennings. «Insulin resistance.» StatPearls [Internet] (2021).
- Suckale J, Solimena M. El gránulo secretor de insulina como centro de señalización. Trends Endocrinol Metab. 2010; 21 [10]: 599–609)
Referencias – Resistencia a la Insulina
- Jameson, J. Larry, and Leslie J. De Groot. Endocrinology-E-Book: Adult and Pediatric. Elsevier Health Sciences, 2010.
- Brady, Mark F., and Prashanth Rawla. «Acanthosis nigricans.» (2017).
- Zaman, Gaffar S. «Pathogenesis of insulin resistance.» Cellular metabolism and related disorders. IntechOpen, 2020.
- Steil G, Volund A, Kahn S, Bergman R. Reduced sample number for calculation of insulin sensitivity and glucose effectiveness fron the minimal model. Diabetes. 1993; 42: 250-256.)
- Borai A, Livingstone C, Kaddam I, Ferns G. Selection of the appropriate method for the assessment of insulin resistance. BMC Medical Research Methodology. 2011; 11: 158
- Yeni-Komshian H, Carantoni M, Abbasi F, Reaven G. Relationship between several surrogate estimates of insulin resistance and quantifi cation of insulin-mediated glucose disposal in 490 healthy nondiabetic. Diabetes Care. 2000; 23: 171-175
- Cuartero, B. García, et al. «Índice HOMA y QUICKI, insulina y péptido C en niños sanos. Puntos de corte de riesgo cardiovascular.» Anales de Pediatría. Vol. 66. No. 5. Elsevier Doyma, 2007.
- Henríquez, Sandra, et al. «Variability of formulas to assess insulin sensitivity and their association with the Matsuda index.» Nutrición hospitalaria 28.5 (2013): 1594-1598.
- Rácz O, Linková M, Jakubowski K, Link R, Kuzmová D. [Barriers of the initiation of insulin treatment in type 2 diabetic patients – conquering the «psychological insulin resistance»]. Orv Hetil. 2019 Jan;160(3):93-97.
- Yaribeygi H, Atkin SL, Simental-Mendía LE, Sahebkar A. Molecular mechanisms by which aerobic exercise induces insulin sensitivity. J Cell Physiol. 2019 Aug;234(8):12385-12392.
- He X, Wu D, Hu C, Xu T, Liu Y, Liu C, Xu B, Tang W. Role of Metformin in the Treatment of Patients with Thyroid Nodules and Insulin Resistance: A Systematic Review and MetaAnalysis. Thyroid. 2019 Mar;29(3):359-367.
Autores – Resistencia a la Insulina
1 YURI VANESSA CERÓN MARTÍNEZ, Division of Obstetrics and Gynecology, Department of Clinical and Experimental Medicine, University of Pisa, Pisa, Italy
2 GUSTAVO GÓMEZ TABARES, Azienda USL Toscana Nord Ovest, Pisa, Italy.