Existen dos tipos de procedimientos principales. El primero consiste en la creación de una nueva cavidad y puede ser quirúrgico o no quirúrgico; y el segundo es el reemplazo vaginal con un canal preexistente forrado con una membrana mucosa (Ej.: el intestino) o injerto de piel11; y recientemente hemos implementado el uso de material sintético15, 16.
La creación no quirúrgica de una neovagina es la primera línea de manejo en la mayoría de las pacientes1. Consiste en el uso de dilatadores vaginales por treinta minutos hasta completardos horas al día. En recientes series reportadas, el 90-95 % de pacientes lograron un éxito anatómico y funcional, con la dilatación vaginal4, 5. Pacientes que no tienen coitos frecuentes requieren continuar con la dilatación vaginal, al contrario de aquellas con vida sexual activa1.
La creación quirúrgica de la neovagina es una opción para pacientes que no tuvieron éxito con los dilatadores vaginales o para quienes aceptan este manejo como primera opción terapéutica. La creación quirúrgica de la vagina requiere dilataciones posoperatorias o coito vaginal para mantener una adecuada longitud y diámetro vaginal1.
El objetivo es la creación de un canal vaginal en el eje correcto, de un tamaño adecuado y con capacidad secretora para permitir un coito. A menudo se realiza en la adolescencia tardía o en la adultez temprana (p. e., 17-21 años). Existen varias técnicas quirúrgicas, y la realizada depende de la experiencia del cirujano. No hay consenso en la literatura acerca de la mejor opción para la corrección quirúrgica que permita un mejor resultado funcional y satisfacción sexual1.
El procedimiento quirúrgico más usado para la realización de la neovagina es el Mc Indoe- Abbe modificado. Este consiste en la disección de un espacio entre el recto y la vejiga, la colocación de un molde cubierto con injerto de piel de espesor parcial en el espacio, y el uso diligente de dilatación vaginal después de la operación. La dilatación posoperatoria es esencial para prevenir la contractura significativa del injerto de piel1.
Actualmente hemos desarrollado e implementado la técnica simplificada de neovagina (Gómez et al.), que es una modificación de latécnica Mc Indoe.
Consiste en el reemplazo del injerto cutáneo por la utilización de material sintético absorbente de bacterias, Cutimed Sorbact o Cutisorb. Este está basado en un concepto único antimicrobiano que funciona sin un agente químicamente activo. A cambio, se usa un principio físico para limpiar heridas colonizadas e infectadas: las bacterias y hongos son físicamente adheridos al apósito por una interacción hidrofóbica. Con cada cambio del apósito, los patógenos adheridos al apósito son removidos fácil y eficientemente de la herida. Este principio sorprendentemente simple ha sido exitosamente demostrado en numerosos estudios: Cutimed Sorbact es un producto confiable por su eficiencia antimicrobiana en el manejo de heridas y no está relacionado con posibles riesgos que acompañan a productos antibióticos o antisépticos de uso local.17 Esta nueva técnica para neovagina surge como una opción más práctica, más segura, con menos riesgo de morbilidad posquirúrgica y más económica, para restaurar la función sexual de mujeres con agenesia de vagina15 (caso 1).
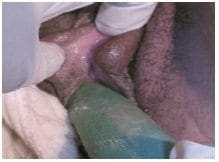 Técnica simplificada de neovagina. La imagen muestra la inserción del molde recubierto por material sintético absorbente de bacterias, en neovagina16.
Técnica simplificada de neovagina. La imagen muestra la inserción del molde recubierto por material sintético absorbente de bacterias, en neovagina16.
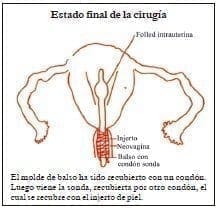
En los casos de úteros o remanentes de útero cavitados también (el mismo grupo) hemos desarrollado una técnica en dos tiempos de creación de neovagina con la técnica de membrana de Cutimed Sorbact y otro tiempo, en el mismo acto quirúrgico, en el cual por vía abdominal se permeabiliza el extremo caudal del útero, se introduce una sonda de Foley y se conecta con el fondo de saco de la reciente neovagina para crear una fístula que va a funcionar como neocuello16(caso 2).
Otros métodos para la creación de la neovagina son el procedimiento de Vecchietti y otras técnicas laparoscópicas. El procedimiento laparoscópico de Vecchietti es una modificación de la técnica abierta, donde una neovagina se crea utilizando la dilatación continua con una tracción externa de un dispositivo que se fija temporalmente a la pared abdominal. En cambio, Davydov desarrolló una operación de tres etapas, que requiere la disección del espacio rectovesical, la movilización abdominal de un segmento del peritóneo, y la posterior unión del peritóneo al introito vaginal6-8. Estudios demuestran que los resultados anatómicos y funcionales de las dos técnicas laparoscópicas (Vecchietti y Davydov) tienden a ser comparables a los 12 meses de seguimiento; la única diferencia significativa parece ser en cuanto a la mayor longitud para la neovagina obtenida por la técnica de Davydov12.
Otras técnicas, tales como injerto de intestino, el uso de la mucosa bucal, amnios y varios otros aloinjertos, se aplican con menos frecuencia a las mujeres con agenesia de los conductos de Müller6-8.
Seguimiento ginecológico
Las mujeres que tienen un historia de agenesia Mulleriana y a quienes se les ha creado una vagina funcional requieren cuidado ginecológico de rutina. Deben ser realizados exámenes médicos regulares para valorar la presencia de estenosis vaginal. Las mujeres sexualmente activas con agenesia Mulleriana deben ser conscientes de que corren el riesgo de contraer enfermedades de transmisión sexual y, por lo tanto, deben usar condones u otros métodos de barrera. Además, se debe realizar especuloscopia en búsqueda de posibles malignidades (en casos de injerto de piel o el intestino); colitis, ulceración (en los casos de vaginas intestinales) u otros problemas. La citología vaginal de rutina no se recomienda9.
La evidencia disponible es insuficiente para orientar la decisión para la vacunación contra el virus del papiloma humano en mujeres con neovagina quirúrgica, aunque el riesgo teórico de neoplasia vaginal y verrugas genitales está presente9.
A continuación se describen dos casos clínicos de mujeres con síndrome de Mayer Rokitansky Kuster Hauser, captadas en el Hospital Universitario del Valle, centro de referencia de la región Suroccidental del país.Caso clínico 1
Fecha: 12-02-2014
Paciente de 17 años, estudiante, quien consulta por cuadro de amenorrea primaria, fue valorada en periferia, donde solicitan TSH: 0,744 y ecografía pélvica transabdominal (11-12-2013) que reporta útero infantil (3,2 x 1 x 1,8 cm), endometrio lineal, ecogenicidad normal sin anormalidades pélvicas. Como antecedentes personales presenta varicela, dengue, migraña y rinitis, herniorrafia inguinal bilateral, sin inicio de relaciones sexuales. Al examen físico se evidencia paciente hemodinámicamente estable, Tanner mamario estadio III, genitales externos de configuración normal, distribución ginecoide del vello púbico Tanner III. Vagina corta, de aproximadamente 2 cm de longitud. Se considera toma de estudios de extensión cariotipo y RNM de pelvis, para valoración de órganos (anatomía pélvica y genitales internos). En la nueva valoración médica, acude con cariotipo (14-04-2014): 46 XX (normal) y RMN de pelvis (12-04-2014) que reporta ausencia de útero y vagina; ambos ovarios con folículos en su interior. Fondo de saco con líquido libre (posiblemente por ovulación reciente); vejiga, uretra, ampolla rectal y canal anal de características normales.
– Conclusión: Agenesia de útero y vagina.
– Diagnóstico: Síndrome de Mayer Rokitansky Kuster Hauser y amenorrea primaria.
– Conducta: Se programa para realización de neovagina, una vez tenga pareja sexual.
Caso clínico 2
Fecha: 5-01-2010
Paciente de 24 años, ama de casa, quien consulta por cuadro de amenorrea primaria con desarrollo de características sexuales secundarias a los 13 años. Sin antecedentes patológicos de importancia. Al examen físico, paciente hemodinámicamente estable, mamas Tanner estadio V, genitales externos de configuración normal, introito vaginal de 4 cm de largo, no se evidencia la presencia de cérvix a la especuloscopia, vello púbico Tanner V. A la paciente se le solicitan dos ecografías pélvicas, la primera del 9-09-2009: se observan dos imágenes que se consideran correspondientes a cuerpo uterino, separado por un septo o tabique. Conclusión: útero bicorne interrogado.
En una segunda ecografía, del 9-11-2009, no se visualiza útero y en el lecho pélvico se evidencia imagen de aspecto sólido, nodulada, de 7,2 x 5,1 cm.
Las anteriores se consideran ecografías no concordantes; y la paciente, con anomalía Mulleriana al examen físico y amenorrea primaria, por lo cual se solicita RMN de pelvis y cariotipo. El 1-03-2013 se realiza cariotipo que reporta 46 XX. En ecografía pélvica posterior (18-03-2013), se documenta como hallazgo incidental la presencia de imagen hiperecoica de 8,8 x 5,5 x 8,5 cm, septada, sólida en hueco pélvico, para lo cual se solicitan marcadores tumorales que son negativos, y es llevada a laparotomía exploratoria y anexectomía izquierda (20-03-203). Durante el procedimiento quirúrgico se evidencia endometrioma de 9 cm de diámetro, útero bicorne separado, con cuerno derecho rudimentario y ovario derecho de aspecto normal, trompa y ovario izquierdos dilatados con endometrioma en su interior, agenesia del cérvix y no hay comunicación de los cuernos con muñón vaginal.
Resultado de patología 20-03-2013: endometrioma e hidrosalpinx
La paciente vuelve a consulta el 14-05-2014, por cuadro de un año de evolución de dolor en fosa iliaca izquierda e hipogastrio, intenso, persistente, que mejora parcialmente con analgésicos comunes. Refiere que el dolor inició secundario al procedimiento quirúrgico del 20- 03-2013. Trae RMN de pelvis (3-05-2014): útero de 6,2 x 4,3 x 4,5 cm, endometrio de 12 mm, ovario derecho de 3,8 x 2,1 cm y ovario izquierdo de 2,1 x 1,2 cm; no se observa útero bicorne; remanente del cérvix adelgazado, elongado, sin poderse definir si existe comunicación con la cavidad endometrial, sin presencia de hematómetra. No se identifica mucosa vaginal.
Paciente al examen físico estable, orientada, con abdomen no distendido, blando, depresible, sin signos de irritación peritoneal, con dolor a la palpación profunda en hipogastrio. Paciente con disgenesia de conductos mullerianos, amenorrea primaria y endometriosis ; se programa para realización de cirugía en dos tiempos: primero la neovagina y en segundo lugar el neocérvix.
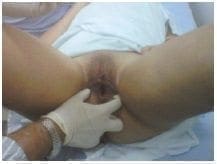 Técnica simplificada de neovagina. Resultado final.
Técnica simplificada de neovagina. Resultado final.
Conclusiones
En pacientes con síndrome de Rokitansky, los pasos más importantes en su enfoque son realizar un diagnóstico adecuado, evaluar anomalías congénitas subyacentes y realizar un adecuado asesoramiento psicosocial antes de cualquier tratamiento o intervención para hacer frente a los efectos emocionales y funcionales de las anomalías genitales.
La laparoscopia es rara vez necesaria para hacer el diagnóstico, pero puede ser apropiada en pacientes con dolor pélvico.
La creación no quirúrgica de la neovagina debe ser el manejo de primera línea. En los casos en que se requiera la intervención quirúrgica, la referencia a centros con experiencia en esta área se debe considerar porque pocos cirujanos tienen una amplia experiencia en construcción de neovaginas.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses. No tienen ninguna vinculación con los proveedores de materiales usados
Bibliografía
1. Müllerian Agenesis: Diagnosis, Management, and Treatment. Revista Ovid. 2013; 12: 1134-1137. The American College of Obstetricians and Gynecologists. Committee Opinion No. 562.
2. Pittock ST et al. Mayer-Rokitansky-kuster- Hauser anomaly and associated malformations. American Journal of Medical Genetics. 2005; 135: 314-316.
3. Courtney A. Marsh MD, MPH, and Yolanda R. et al. Mayer-Rokitansky-Kuster-Hauser Syndrome: Prevalence of Uterine Variants and Clinical Associations. Journal of Pediatric and Adolescent Gynecology. 2013; 26: 199-202.
4. Carla P. Roberts, Michael J. Haber, John A. Rock. Vaginal creation for mullein agenesis. American Journal of Obstetrics and Gynecology. 2001; 185: 1349-1353.
5. Edmonds DK, Rose GL, Lipton MG. Quack J. Mayer-Rokitansky-Kuster-Hauser syndrome: a review of 245 consecutive cases managed by a multidisciplinary approach with vaginal dilators. Fertility and Sterility. 2012; 97: 686-690.
6. Herbert de Sousa Marques, Francisca Lopes dos Santos et. al. Creation of a neovagina in patiens with Rokitansky Syndrome using peritoneum from the pouch of Douglas: An analysis of 48 Cases. Fertility and Sterility. 2008; 90: 827-832.
7. Adamyan L, Makiyan Z, Stepanian. A Differential Surgical Treatment of Female Genital Anomalies: EP8.27. An International Journal of Obstetrics and Gynaecology. 2013; 120: 393-394.
8. Lisa M. Allen, Kerith L. Lucco. Psychosexual and functional outcomes after creation of a neovagina with laparoscopic Davydov in patients with vaginal agenesis. Fertility and Sterility. 2010; 94: 2272-2276.
9. Frega A. Scirpa P. Sopracordevole F., et al. Impact of human papillomavirus infection on the neovaginal and vulval tissues of women who underwent surgical treatment for Mayer– Rokitansky–Kuster–Hauser syndrome. Fertility and Sterility. 2011; 96: 969-973.
10. Daniel Guerrier and Programme de Recherches sur les Aplasies Müllériennes (PRAM). Mayer-Rokitansky-Küster-Hauser (PRAM). Correo electronico:pram-network.coordination@univ-rennes1.
11. Edmonds, D. Keith. Congenital malformations of the genital tract and their management. Best Practice and Research in Clinical Obstetrics and Gynaecology. 2003; 17: 19-40.
12. Bianchi S., Frontino G. et al. Creation of a neovagina in Rokitansky syndrome: comparison between two laparoscopic techniques. Fertility and Sterility. 2011; 95: 1098-1100.
13. Yoo Roh-Eul, Cho Jeong Yeon et al. Magnetic Resonance Evaluation of Mullerian Remnants in Mayer Rokitansky Kuster Hauser Syndrome. Korean Journal of Radiology. 2013; 14: 233-239.
14. Karine Morcel, Laure Camborieux, Daniel Guerrier and Programme de Recherches sur les Aplasies Müllériennes (PRAM). Mayer- Rokitansky-Küster-Hauser (MRKH) syndrome. Orphanet Journal of Rare Diseases 2007; 2: 1-9.
15. Gómez G. Síndrome de Disgenesia de Conductos Mullerianos: Agenesia de Cuello, 2/3
superiores de Vagina. Revista Colombiana de Ginecología y Obstetricia. 1994; 45; 81-83.
16. Gómez G. y Nieto A. Técnica simplificada de Neovagina. Revista Colombiana de Ginecología y Obstetricia. 2010; 61169.
17. Hampton S. An evaluation of the efficacy of Cutimed – Sorbact ®, in different types of non – healing wounds . Wounds UK. 2007. Vol. 3. No. 4.
