Actualidad Inmediata
Jorge M. Tamayo, Gustavo Gómez, Rocío Barrios, Jorge Holguín, Cecilia Adrianzén*
Journal Of Clinical Psychopharmacology _ August 2004; 24 (4).
* Neuroscience Clinical Research, Eli Lilly & Co., Puerto Rico Branch, San Juan, Puerto Rico; y Department of Psychiatry, University
of Puerto Rico, San Juan, Puerto Rico; Imbanaco Medical Center, Cali, Colombia; Colsanitas Medical Center, Santa Fe de Bogotá,
Colombia; Samein Mental Health Center, Medellín, Colombia and Neuroscience Clinical Research, Eli Lilly & Co., Lima, Perú;
j.tamayo@lilly.com – gusgomez@univalle.edu.co
A los Editores
El síndrome disfórico premenstrual (SDP) es una entidad clínica bien definida y bien diferente de otros desórdenes ampliamente diagnosticados, tales como depresión mayor, desórdenes de pánico, etc.1.
El diagnóstico de SDP requiere de la presencia de al menos 5 de 11 ítems de la lista de síntomas del Diagnostic and Statistical Mental disorders, Fourth Edition, tales como modo depresivo, irritabilidad y síntomas físicos, entre otros.
Los síntomas pueden ser severos diariamente antes de la menstruación y moderados o ausentes después de ella, con una falla significativa en el funcionamiento durante el ciclo menstrual sintomático por dos o más ciclos menstruales.
El objetivo primario de este estudio fue evaluar la eficacia y seguridad del tratamiento intermitente con 20 mg/día de fluoxetina administrada durante 3 ciclos menstruales consecutivos en la fase lutea en pacientes con diagnóstico de SDP de acuerdo a los criterios del Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition. uarenta y un pacientes (promedio de edad 33 [± 8.9]) con diagnóstico de SDP y sin ningún episodio previo de depresión mayor, entraron voluntariamente al estudio después de firmar un consentimiento informado. Debían tener al menos 18 años de edad, tener ciclos regulares de alrededor de 25 a 31 días, y usar un método médico aprobado de anticoncepción diferente a contraceptivos hormonales.
Treinta pacientes concluyeron el estudio y dieron la información usada en el análisis estadístico.
Este fue un estudio prospectivo, abierto no controlado, con un período de seguimiento de cuatro ciclos menstruales (tres bajo medicación) y diez visitas.
La visita 1 fue hecha en cualquier momento del ciclo menstrual. Sin embargo, solo aquellas que tuvieron un puntaje de la escala análoga visual de >50 (para ánimo y síntomas físicos, en puntajes de 0 a 100) durante la fase lutea (visita 3) sin síntomas o con síntomas mínimos durante la fase folicular (visita 2), fueron a la visita 4.
El periodo de tratamiento incluyó tres ciclos menstruales con dos visitas en cada uno (fase folicular entre días 5 y 11 y fase lútea entre los seis días antes de comenzar la menstruación y el primer día de la siguiente menstruación).
En la visita 4, las pacientes fueron instruidas en tomarse 20 mg. de fluoxetina por día durante la fase lutea, desde 14 días antes del sangrado menstrual. La visita 10 (última visita) fue en la fase folicular después del ciclo menstrual 4.
El Calendar of Premenstrual Experiences (COPE)3 fue designado a priori como el instrumento primario de eficacia.
Los valores del COPE obtenidos por los pacientes durante el primer periodo luteo (visita 3) se usaron como puntaje de base para el análisis de los datos. Esos valores fueron comparados con los obtenidos durante los periodos luteal de tratamiento en la visita 9.
Todos los datos se evaluaron usando el análisis de intento de tratar; los datos de todos los pacientes fueron incluidos en el análisis.
Para la eficacia del análisis, se consideró como un criterio de respuesta positiva una reducción en el puntaje del COPE del 50% de la línea de base (visita 3) al final, y un puntaje de del COPE del 50% de la línea de base (visita 3) al final, y un puntaje de <40 al final.
Para simplificar la interpretación de los resultados y para expandir la eficacia del análisis, determinamos los cambios promedios por visita de los subpuntajes del COPE basados en grupos de síntomas: Bloque 1. síntomas disfóricos: depresión, irritabilidad, llanto fácil, ataques de tristeza, ansiedad, tensión y nerviosismo; Bloque 2. otros síntomas afectivos: fatiga, confusión, dificultad para concentrarse, incapacidad motora, aversión por cierta clase de alimentos, olvidadiza, aumento del apetito y cambios de humor; bloque 3. síntomas físicos: sensación de pesadez, dolor mamario, dolor abdominal, dolor de cabeza, entumecimiento (manos, rodillas y mamas); y bloque 4. síntomas relacionados: cambios en la vida sexual, y sentimientos de soledad.
Se analizaron los cambios en esos síntomas específicos y el puntaje total del COPE en comparación con la visita basal (V3) usando un análisis de varianza.
La tabla 1 muestra los resultados del análisis de los puntajes del COPE. De acuerdo a parámetros de respuesta establecidos previamente en el protocolo, el 95% de las pacientes tenían una reducción mayor del 50% en la V9 en comparación con el puntaje inicial del COPE. En la fase lutea y puntaje final de
El análisis de los resultados de los test de laboratorio (hematología, química sanguínea, y uroanálisis) no mostraron cambios estadísticamente significativos en ninguno de los pacientes. Los eventos adversos más comúnmente reportados por las pacientes fueron cefalea (10%) y mareos (6.6%).
Se conoce muy poco acerca de la etiología del síndrome premenstrual. Una de ellas es que existan receptores para esteroides hipersensibles en el sistema nervioso central como consecuencia de disturbios en la secreción de neurotransmisores tales como serotonina y de los mecanismos mediadores del ácido gamaaminobutírico (GABA)4. En las ratas, la inyección consecutiva de progesterona (P4) resulta en un aumento en la recaptación de serotonina (5 HT) en varias áreas del cerebro5.
Tabla 1. Cambios medios observados en cada visita en el Total Score y en los Bloques de Síntomas en el COPE durante la fase lútea
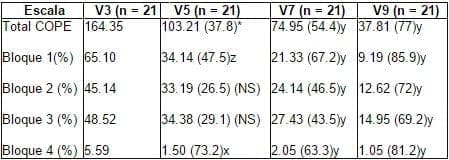
Bloque 1, síntomas disfóricos; Bloque 2, otros síntomas afectivos no disfóricos; Bloque 3, síntomas físicos; Bloque
4, síntoma relacionados.
%, porcentaje de cambio en comparación con la evaluación
en visita 3; P, valores en comparación con visita V3.
NS = no significante.
*P = 0.06.
yP < 0.006.
zP = 0.02.
xP = 0.008.
Ese efecto de la progesterona podría explicar una disminución en los niveles sinápticos de serotonina y su metabolito 5-HIAA en la orina durante la fase lutea6. Como consecuencia, se postula que los receptores de 5 HT en el hipotálamo y otras áreas del cerebro podrían experimentar variaciones cíclicas de, desensibilización después de la ovulación. Un reciente artículo investigó en ratas el tratamiento a largo plazo con fluoxetina y mostró una desensibilización hipotalámica de las señales postsinápticas del receptor de 5 HT7.
La evidencia de que los agentes antidepresivos serotoninérgicos son efectivos en el tratamiento de mujeres con irritabilidad y disforia premenstrual apoya esta hipótesis.1,8-10
En la medida que sabemos, este es el tercer estudio publicado acerca del uso intermitente de 20 mg. de fluoxetina diario durante 3 fases luteas consecutivas.
Aunque este es un estudio abierto con un número pequeño de pacientes con SDPM, corrobora la eficacia y seguridad de los hallazgos reportados en los estudios de Steiner y col. 11 y Cohen y col. 12 y ofrece los primeros datos acerca de la eficacia y seguridad de la terapia intermitente con fluoxetina en pacientes latinoamericanas latinoamericanas (colombianas). Sin embargo, es importante puntualizar que el uso del COPE como medida primaria de eficacia refleja una respuesta progresiva desde el primer ciclo de tratamiento que aumenta más a medida que los ciclos de tratamiento continúan.
El análisis de los bloques que agrupan los síntomas del COPE nos permite concluir que el efecto de tratamiento intermitente con fluoxetina es mas rápido en la reducción de síntomas disfóricos, irritabilidad y tensión.
Sin embargo, otros síntomas físicos y afectivos muestra cambios estadísticamente significativos solamente a partir del segundo ciclo de tratamiento. Esta respuesta progresiva no corresponde a un efecto antidepresivo porque en este estudio, todos los sujetos elegibles fueron tamizados por experimentados siquiatras y sicólogos para prevenir la inclusión de pacientes con desórdenes mayores depresivos o distímicos.
Sorpresivamente, los efectos antidisfóricos que comienzan en el primer ciclo de tratamiento no han sido descritos, en estudios usando una administración intermitente de un inhibidor selectivo de la recaptación de serotonina de corta vida como el citalopram y la sertralina.
En el estudio de Alpay y Turhan13 con setraline, 22 de 23 pacientes que recibieron terapia intermitente suspendieron la medicación por efectos adversos; en el estudio de Wikander y col. 14 con citalopram, solo fue evaluada la irritabilidad por medio de una escala análoga visual con mejoría estadística en el grupo intermitente en comparación con respecto al grupo placebo desde el primer ciclo de tratamiento, pero otros síntomas disfóricos estuvieron presentes solo en un subgrupo de pacientes y los cambios en los síntomas no alcanzaron significanción estadística.
Finalmente, en el estudio de Halbreich y col. 15, de bajas dosis intermitentes de sertralina, se observó una mejoría progresiva del puntaje total del Daily Record of Severity of Problems, pero en el reporte, el impacto de la sertralina en los síntomas disfóricos del primer ciclo de tratamiento no fue mencionado.
Por lo tanto nosotros especulamos que el aumento en los niveles de serotonina en las uniones sinápticas en el hipotálamo, no es suficiente para explicar la mejoría de todos los síntomas del SDPM. La rapidez del efecto antidisfórico de la fluoxetina podría deberse a ese mecanismo, y también, talvez, al aumento de los niveles de aloprenanolona, la cual es un metabolito de la progesterona con efectos antiansiolítico y antidisfóricos probablemente relacionado con la interacción de la fluoxetina con los receptores GABA16. Se debe considerar también que la larga vida de la fluoxetina y su metabolito activo puede ofrecer algunos niveles de respuesta sobre síntomas como la fatiga, dificultad de concentración, cambios secundarios del humor y síntomas físicos, los cuales requieren cambios post-sinápticos no solo en el hipotálamo sino también en las vías espinales atalámicas y en diferentes áreas del sistema límbico. Comparativamente, se necesitan más estudios entre diferentes inhibidores selectivos de recaptación de serotonina con énfasis en grupos de síntomas estratificados de SDPM, para confirmar la hipótesis establecida aquí.
Reconocimientos
Agradecemos Maria Rivas MD, (endocrinologist), y Melissa J. Joliat, PhD, por las insinuaciones de grande ayuda y la revision final del manuscrito.
Referencias
1. Endicott J, Amsterdam J, Eriksson E et al. Is premenstrual dysphoric disorder a distinct clinical entity? J Women’s Health Gend-Based Med 1999; 8: 663–679.
2. Rubinow DR, Roy-Byrne P, Hoban MC, et al. Prospective assessment of menstrual related mood disorders. Am J Psychiatry 1984; 141: 684–686.
3. Mortola JF, Girton L, Beck L et al. Diagnosis of premenstrual syndrome by a simple, prospective, and reliable instrument: the calendar of premenstrual experiences. Obstet Gynecol. 1990; 76: 302–307.
4. Halbreich U, Alt IH, Paul L. Premenstrual changes. Impaired hormonal homeostasis. Endocrinol Metab Clin North Am 1988; 17: 173–194.
5. Hackman E, Wirz-Justice A, Lichtensteiner M. Uptake of dopamine and serotonin in the rat brain due to progesterone decline. Psychopharmacologia 1973; 4: 183.
6. Leudo de Tejado A, Carrero QFB, Estrella CA. Urinary excretion of 5-hydroxyindolacetic acid during the human menstrual cycle. Gynecol Obstet (Mex). 1978; 44: 85–88.
7. VandeKar LD, Raap DK, Battaglia G et al. Treatment of cycling female rats with fluoxetine induces desensitization of hypothalamic 5-HT1A receptors with no change in 5-HT2A receptors. Neuropharmacology 2002; 43: 45–54. 8. Sundblad C, Modigh K, Andersch B, et al. Clomipramine effectively reduces premenstrual irritability and dysphoria; a placebo controlled trial. Acta Psychiatr Scand 1992; 85: 39– 47.
8. Sundblad C, Hedberg MA, Eriksson E. Clomipramine administered during the luteal phase reduces the symptoms of remenstrual syndrome: a placebocontrolled trial. Neuropsychopharmacology 1993; 9: 133–145.
9. Freeman EW, Rickels K, Yonkers KA et al. Venlafaxine in the treatment of premenstrual dysphoric disorder. Obstet Gynecol 2001; 98: 737–744.
10. Steiner M, Korzekwa M, Lamont J et al. Intermittent fluoxetine dosing in the treatment of women with premenstrual dysphoria. Psychopharmacol Bull 1997; 33: 771–774.
11. Cohen LS, Miner C, Brown E et al. Premenstrual daily fluoxetine for premenstrual dysphoric disorder: a placebo- controlled,clinical trial using computerized diaries. Obstet Gynecol 2002; 100: 435–444.
12. Alpay FB, Turhan NO. Intermittent versus continuous sertraline therapy in the treatment of premenstrual dysphoric disorders. Int J Fert Women’s Med. 2001; 46: 228–231.
13. Wikander I, Sundblad C, Andersch B et al. Citalopram in premenstrual dysphoria: is intermittent treatment during luteal phases more effective than continuous medication throughout the menstrual cycle? J Clin Psychopharmacol 1998; 18: 390– 398.
14. Halbreich U, Bergeron R, Yonkers KA et al. Efficacy of intermittent, luteal phase sertraline treatment of premenstrual dysphoric disorder. Obstet Ginecol 2002; 100: 1219–1229.
15. Uzunov DP, Cooper TB, Costa A et al. Fluoxetine-elicited changes in brain neuro steroid content measured by negative ion mass ragmentography. Proc Natl Acad Sci USA 1996; 93: 12599–12604.
