Presentación de un Caso y Revisión de la Literatura
*Janer Sepúlveda Agudelo.
**Wilma Castillo, Víctor Armando Pinto Barón, Fabricio García.
Resumen
El tumor maligno de ovario en el embarazo se encuentra en un 2 a 5% de todas las masas anexiales que ocurren en el embarazo. El embarazo no tiene un efecto adverso directo en el pronóstico de las pacientes con un tumor de ovario maligno; se requiere de una buena clasificación por estadios durante el procedimiento quirúrgico para establecer un adecuado tratamiento.
Presentamos el caso de una mujer de 35 años diagnosticado y manejado en el Hospital San Rafael de Tunja, Colombia, con 20 semanas de embarazo y un tumor de ovario gigante que fue clasificado por el estudio histopatológico como cistadenocarcinoma mucinoso; se hace una revisión detallada de la literatura de tumor de ovario y embarazo.
Palabras Claves: Embarazo, masas anexiales, cistadenocarcinoma mucinoso, ecografía, tratamiento.
Summary
2 to 5% of ovarian masses diagnosed during pregnancy are malignant. The pregnancy state does not appear to have a direct adverse effect on the prognosis of the patients with ovarian malignancy tumors. Should the surgeon find and ovarian malignancy in pregnancy, the first obligation is to stage the patient is disease properly, while providing operative intervention.
We present a case of a 35 years old woman diagnosed and treated in San Rafael Hospital Tunja, Colombia, with 20 weeks of gestation and ovarian giant tumors, witch was classified on pathological study how mucinous cystadenocarcinoma. We reviews the literature of ovarian tumors and pregnancy.
Key Words: Pregnancy, adnexal masses, mucinous cystadenocarcinoma, ultrasonography, treatment.
Introducción
La incidencia de masas anexiales en el embarazo es de aproximadamente 1:1000 embarazos1 que puede variar de 1:81 a 1:8.000 embarazos2 y de 2 a 5% de estas son tumores de ovario malignos1,3.
El cáncer de ovario es el cuarto cáncer más común que ocurre en el embarazo después del cáncer de cérvix, mama y piel4-5.
La presencia de un proceso maligno descubierto durante el embarazo plantea numerosos interrogantes: ¿Es necesaria o ventajosa la interrupción del embarazo?; ¿afectará al feto el proceso maligno o el tratamiento?; ¿debe retrasarse el tratamiento y comenzarlo al terminar el embarazo?; ¿deberá advertirse a las pacientes sobre futuros embarazos?
Caso Clínico
Paciente de 35 años de raza mestiza, procedente de Tunja (Boyacá) con amenorrea de 20 semanas, que consulta al Hospital de San Rafael de Tunja (Boyacá) por presentar aumento exagerado del abdomen con respecto a la edad gestacional; acompañado de disnea de esfuerzo progresiva en los últimos 7 días.
Antecedentes sin importancia.
Al examen físico, se encuentra una paciente en aceptables condiciones generales, con ligera dificultad respiratoria.
Cabeza y cuello normal.
Cardiopulmonar: ruidos cardiacos rítmicos sin sobreagregados, ventilación pulmonar no comprometida.
Abdomen globoso; difícil delimitar tamaño uterino y presencia de masas abdominales. Fetocardia no auscultable; ruidos intestinales positivos.
Genitales externos de aspecto normal.
Especuloscopia: Cuello de aspecto sano. Tacto vaginal: difícil delimitar tamaño uterino o presencia de masas anexiales. Cuello cerrado.
Extremidades normales.
Se decide realizar ecografía obstétrica para aclarar edad gestacional y se encuentra embarazo de 203/7 semanas y una gran masa que ocupa toda la cavidad abdominal, al parecer dependiente del ovario derecho de difícil delimitación; bordes irregulares y de contenido quístico, con una imagen en su interior de aspecto sólido de 8×6 cm; la masa rechaza útero y asas intestinales a la izquierda.
En junta médica de ginecólogos en vista de la sintomatología de la paciente se decide llevar a cirugía, en donde se encuentran los siguientes hallazgos:
- Útero aumentado de tamaño +/- 20 semanas.
- Tumor de ovario derecho de 20×30 cm con un peso de 7 kilogramos, cápsula lisa, sin excrecencias. (ver foto 1).
- No evidencia macroscópica de invasión a órganos vecinos.
- Apéndice, asas intestinales, epiplón, hígado, bazo y riñones sin evidencia macroscópica de metástasis.
- Líquido ascítico aproximadamente 100 cm.
- Ganglios sin compromiso macroscópico tumoral.
Se realiza salpingo-oforectomía derecha más apendicectomía más omentectomía más citología de líquido ascítico.
Evolución postquirúrgica satisfactoria sin presencia de actividad uterina.
Reporte de Patología
- Cistadenocarcinoma mucinoso bien diferenciado gigante de ovario derecho.
- Epiplón con compromiso microscópico por tumor mucinoso extenso.
- Apéndice cecal sin compromiso tumoral.
- Líquido ascítico: hiperplasia mesotelial reactiva severa.
- Líquido de tumor de ovario Papanicolau III.
Se realiza impresión diagnóstica de cistadenocarcinoma mucinoso de ovario derecho estadío III a. Según clasificación de carcinoma de ovario por la Federación Internacional de Ginecología y Obstetricia FIGO). (Ver tabla 1).
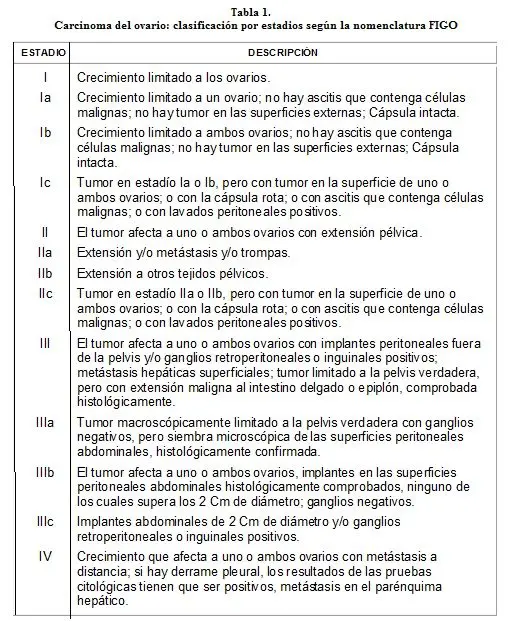
Se envía la paciente al Instituto Nacional de Cancerología (INC) donde deciden realizar manejo complementario una vez alcanzada la madurez pulmonar fetal; sin embargo la paciente no acude a los controles y consulta nuevamente al hospital para atención del parto en la semana 41 de embarazo. Obteniéndose recién nacido masculino de peso 3.250 gramos y talla 50 centímetros, con apgar normal. Se remite nuevamente al INC.
Discusión
De los tumores de los anexos que se identifican durante el embarazo, cerca de 50% tienen menos de 5 cm de diámetro, un 25% entre 5 a 10 cm y 25% mide más de 10 cm en el momento de su descubrimiento. De estas tumoraciones el 95% son unilaterales4.
Las tumoraciones unilaterales, móviles y no complejas que miden menos de 5 cm y que se identifican durante el primer trimestre se resolverán espontáneamente en el 90% de los casos4,6.
La mayor parte de los tumores ováricos que ocurren durante el principio del embarazo son benignos. Entre los no neoplásicos los tumores del cuerpo amarillo son los mas frecuentes y entre los neoplásicos el más frecuente es el teratoma quístico benigno, que ocupa entre el 24 y 40% de los casos4, 7-10.
Entre el 2 y el 5% de las tumoraciones de los anexos que persisten después del primer trimestre se confirman desde el punto de vista anatomopatológico como lesiones malignas4,11-16. El cáncer de ovario ocurre en aproximadamente 1:18.000 a 1:47.000 embarazos11,17. Una revisión reciente de la literatura realizada por Copeland y cols sobre el diagnóstico de cáncer de ovario durante el embarazo reporta que el 45% fueron de células germinales, 37% epiteliales (incluye los tumores mucinosos objeto de la presentación), 10% tumores del estroma y 7.5% otros11. (Ver clasificación de los tumores de ovario en la tabla 2).
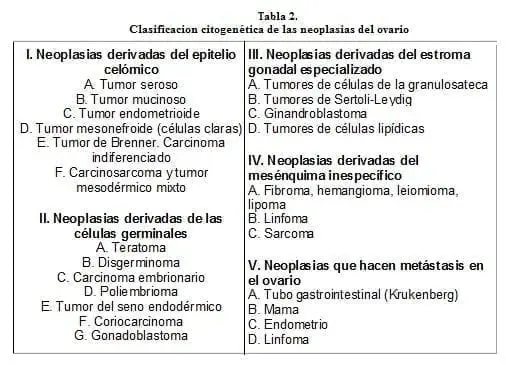
Dudley AG. afirma que el tumor maligno más común que complica el embarazo es el Disgerminoma, sin embargo los tumores malignos de origen epitelial como grupo son los más comunes con una mayor frecuencia de los tipos mucinosos y de los tumores de malignidad limítrofe10.
Generalmente estas tumoraciones en el embarazo pasan inadvertidas desde el punto de vista clínico por que la mayoría son asintomáticas y se descubre incidentalmente en una ecografía obstétrica o más frecuentemente durante la cesárea4-5. En algunos casos, los síntomas son confusos e inespecíficos; la flatulencia, la distensión abdominal y las molestias gastrointestinales referidas por estas pacientes pueden ser atribuidas al embarazo10,12.
Los síntomas que se pueden presentar son: dolor abdominal, generalmente por torsión ovárica que ocurre con mayor frecuencia entre la octava y dieciséis semana de gestación o en el puerperio y ocurre en un 10-15% de los casos5-6,15, puede ocasionar también obstrucción del trabajo de parto1,3,5 y ruptura del tumor5. Escudero y Méndez afirman que el 25 – 75% de las pacientes son asintomáticas; 35-65% pueden presentar dolor abdominal; 15% aumento del volumen abdominal en relación a la edad gestacional y de 10 a 25% un cuadro de abdomen agudo15.
La gestación no altera el pronóstico de la mayoría de los tumores malignos de ovario pero las complicaciones como torsión o ruptura pueden incrementar la incidencia de abortos espontáneos o partos pretérmino3,5,12.
Valoración de tumoraciones pélvicas. Los problemas más frecuentes asociados a los tumores ováricos en el embarazo son el diagnóstico inicial y el diagnóstico diferencial. Cuando el tumor es palpable en la pelvis, debe diferenciarse del útero grávido en retroversión, un fibroma, un carcinoma de colon, riñón pélvico o una anomalía uterina5-6.
El ultrasonido ha revolucionado la obstetricia y se ha convertido en el instrumento diagnóstico utilizado más a menudo durante el embarazo; ha sido de utilidad en la valoración de las tumoraciones de los anexos4,18.
Sassone y cols. desarrollaron un sistema de puntuación mediante ecografía transvaginal para definir las lesiones ováricas y diferenciar entre entidades malignas y benignas, logrando una especificidad del 83% y una sensibilidad del 100%; tuvieron en cuenta cuatro características: la estructura de la pared interna, el grosor de la pared, presencia de tabiques y la ecogenicidad de la masa19.
La resonancia magnética ha demostrado su seguridad en el embarazo; es otro recurso para estudio de los anexos20, pero por su alto costo no se ha estudiado con tanta amplitud para valorar las masas anexiales.
La tomografía computarizada tiene la desventaja de la utilización de la radiación ionizante por lo cual está limitado su uso en el embarazo4.
Marcadores Tumorales
El Ca 125 se utiliza rutinariamente como marcador tumoral; su uso en el embarazo está limitado, porque normalmente puede estar aumentado en el embarazo4,11, por lo cual tiene una alta tasa de falsos positivos y una baja especificidad14. Valores tan altos como de 1250U/ml (valor normal <35U/ml) han sido reportados durante finales del primer trimestre y después permanecen bajos antes del parto; sin embargo 1 hora después del parto su valor transitoriamente incrementa para bajar rápidamente21. Una vez confirmado el diagnóstico de tumor maligno puede ser usado como marcador para monitoreo del curso de la enfermedad11.
La alfa feto proteína(AFP) que ha sido usada como marcador en pacientes con tumor de células germinales es también una proteína sérica predominante durante el desarrollo fetal, inicialmente producida por el saco de yolk y posteriormente la síntesis ocurre a nivel hepático y del tracto gastrointestinal; sus niveles están incrementados en defectos del tubo neural, pero deben tenerse en cuenta en el diagnóstico diferencial con estas tumoraciones1.
La deshidrogenasa láctica (LDH), una enzima glicolítica que participa en la conversión de piruvato a lactato, ha sido usada como marcador del disgerminoma, especialmente sus isoenzimas 1 y 222-23; con excepción de la preeclampsia, los valores de la LDH cambian poco durante el embarazo.
Buller y cols describieron 2 casos de disgerminoma durante el embarazo en los que los valores de LDH se correlacionaron con la actividad de la enfermedad 23.
La gonadotropina coriónica humana beta (BHCG) está normalmente incrementada en el embarazo y tiene poco valor como marcador tumoral3.
Tratamiento
Antes de efectuar cualquier intervención quirúrgica por una tumoración pélvica durante el embarazo, será necesario explicar de manera adecuada a la paciente lo relacionado con los posibles resultados adversos, incluso los posibles riesgos planteados para el feto inmaduro. Deben verificarse los deseos de la paciente respecto a la preservación ovárica de manera informada y se le prepara para someterse a la reducción quirúrgica radical apropiada de acuerdo al tamaño, estadio, tipo y grado histológico de la tumoración.
La semana 16 a 18 de gestación es un periodo prudente para la laparotomía, tanto en cuanto a seguridad para el feto, como a la eliminación de quistes ováricos funcionales1,5,10. Si el quiste es completo y sospechoso de malignidad y aumenta de tamaño, la paciente debe ser intervenida antes de la semana 185. En cualquier edad gestacional que se lleve a cabo la exploración, la recomendación es que el útero no sea manipulado durante la cirugía5.
Si se encuentra un proceso ovárico maligno en el momento de la exploración abdominal, la primera obligación del cirujano es determinar el estadío adecuadamente; ya que el estadiaje del cáncer de ovario es quirúrgico4-5. Clasificación por estadios de la FIGO. (Ver tabla 1).
Se recomienda una incisión longitudinal en la línea media para facilitar la extirpación de la neoplasia y para lograr una buena visión de toda la cavidad abdominal1,4-5,10. El cáncer de ovario es clásicamente, una enfermedad de difusión serosa y por tanto hay que inspeccionar cuidadosamente todas las superficies peritoneales; cualquier líquido peritoneal que se encuentre al abrir la cavidad debe ser aspirado y enviado a estudio citológico4-5; en ausencia de líquido peritoneal, deberán hacerse cuatro lavados de las superficies peritoneales: la cara inferior del diafragma, por fuera del colon ascendente y descendente y las superficiales peritoneales pélvicas; las muestras se obtienen lavando estas zonas con 50 a 75 ml de solución salina normal y recuperando el líquido para el análisis del paquete de células; hay que ver y palpar todas las superficies peritoneales. Se hará biopsia de todas las lesiones sospechosas; omentectomía infracólica; resección y biopsia de cualquier adherencia; biopsia o frotis de la superficie inferior del hemidiafragma derecho; biopsia al azar del peritoneo del fondo de saco de la región vesical, goteras parietocólicas derecha e izquierda y paredes laterales de la pelvis; linfadenectomía selectiva de los ganglios pélvicos y paraaórticos5; la cual debe evitarse si el tamaño del útero limita la exposición o plantea un riesgo de manipulación excesiva10. Lo ideal es enviar el ovario afectado para biopsia por congelación durante el transoperatorio.
Los cánceres epiteliales como los cistadenocarcinomas serosos y mucinosos, cuando se detectan en el embarazo deben tratarse de acuerdo con el estadio de la enfermedad, independientes del embarazo5-6,12. La mayor parte de estas lesiones epiteliales tienen un bajo potencial maligno o se encuentran en estadío I1,5,24-25. También se han informado casos de enfermedad avanzada y diseminada básicamente porque las mujeres están retrasando la reproducción hasta una edad materna avanzada4; se considera que aproximadamente el 20% de los casos está en estadío III ó IV14. El 90% de los casos de tumor de ovario en el embarazo son unilaterales10.
Las lesiones en estadio Ia se pueden tratar en forma conservadora5-6con salpingooforectomía unilateral. Los otros estadios no pueden ser tratados conservadoramente a menos que el tumor sea de una variedad bordeline en la cual la cirugía definitiva puede ser realizada una vez se consiga la viabilidad fetal6 y en la cual no se necesita quimioterapia coadyuvante14. Si el tumor se descubre en tercer trimestre también se puede esperar alcanzar la viabilidad fetal para la realización del tratamiento14-15.
Quimioterapia en el Embarazo
Los efectos mutagénicos y teratogénicos de los agentes quimioterapeúticos han sido claramente demostrados en animales1,26.
Las drogas administradas en la primera semana después de la concepción producen probablemente el fenómeno del todo o nada con aborto espontáneo o fetos normales1. La organogénesis ocurre entre la quinta y décima semana de gestación (tercera a octava semana de desarrollo) y las malformaciones fetales ocurren si se exponen a estos agentes durante este periodo de desarrollo1.
Aproximadamente de 10 a 20% de los fetos expuestos a quimioterapia durante el primer trimestre tienen malformaciones mayores en comparación con el 3% de la población general26.
En una serie revisada por Randall T., de 210 pacientes tratados con quimioterapia en el embarazo, 29 resultaron afectados con un total de 52 anomalías. 27 de los 29 casos resultaron en la exposición a agentes citotóxicos en el primer trimestre de embarazo27.
La quimioterapia en el segundo y tercer trimestre por lo tanto no está asociada con un riesgo significativo de malformaciones pero puede haber una asociación con parto pretérmino, muerte fetal in útero o retardo de crecimiento intrauterino5. Pero en general, se considera que puede ser usada en el segundo y tercer trimestre con seguridad4-6,10,14,26.
Malfenato y Goldkrand reportaron el uso de ciclofosfamida y cisplatino para el tratamiento del carcinoma de ovario epitelial, estadio avanzado sin efectos adversos para el feto28.
Conclusión
Con el uso difundido del ultrasonido es cada vez más frecuente la identificación de una masa anexial en el embarazo; cuando ésta se encuentre, se deben definir todas las características de la misma y poder establecer la posibilidad de malignidad. Siempre que se sospeche de malignidad, el papel del cirujano es establecer el estadío de la enfermedad para establecer un adecuado tratamiento y no negarle a estas pacientes por el hecho de estar embarazadas un tratamiento que puede salvarles la vida.
Bibliografía
1. Boulay R, Podczaski E. Ovarian cancer complicating pregnancy. Obstetrics and Gynecology Clinics. Philadelphia: W. B. Saunders Company, 1998; 25: 385-399.
2. Whitecar MP, Turner S, Higby MK. Adnexal masses in pregnancy: A review of 130 cases undergoing surgical management. Am J Obstet and Gynecol, 1999; 181: 19-24.
3. Logsdon-Pokorny VK. Cirugía ginecológica durante el embarazo. En: Pitkin RM, Scott JR. Clínicas Obstétricas y Ginecológicas. México: McGraw Hill Interamericana, 1994; 2: 267-277.
4. Grendys EX, Barnes WA. Cáncer ovárico durante el embarazo. En: Delgado G. Clínicas quirúrgicas de Norte América. México: McGraw Hill Interamericana,1995; 1: 1-12.
5. Disaia PJ, Creasman WT. Oncología Ginecológica Clínica. 5a ed. Madrid: Harcourt Brace,1999; 459-64.
6. Berman ML, Disaia PJ. Pelvic malignancies, gestational trophoblastic Neoplasia and non pelvic malignancies. In: Creasy RK, Resnik R. Maternal-fetal medicine principles and practice. 3rd ed. Philadelphia: WB Saunders Company 1994; 1112-11342.
7. Caspi B, Levi R, Appelman Z, et al. Conservative management of ovarian cystic teratoma during pregnancy and labor. Am J Obstet Gynecol, 2000; 182: 503-5.
8. Parker W, Childer JM, Canis M, et al. Laparoscopic management of benign cystic teratomas during pregnancy. Am J Obstet Gynecol, 1996; 174: 1499-501.
9. Ueda M, Ueki M. Ovarian tumors associated with pregnancy. Int J Gynecol Obstet, 1996; 55: 59-65. Abstract.
10. Dudley AG. Tumores ováricos que complican el embarazo. En: Thompson JD, Rock JA. Te Linde Ginecología Quirúrgica. 8ª ed. Buenos Aires: Editorial Médica Panamericana,1998; 896-907.
11. Copeland LJ, Landon MB. Malignant disease in pregnancy. In: Gabbe SG, Niebyl JR, Simpson JL: Obstetrics, Normal and Problem Pregnancies, 3 ed. New York, Churchill Livingstone, 1996; 1155-1181.
12. Williams. Obstetricia. 20a ed. Buenos Aires: Editorial médica Panamericana,1998; 1200-1.
13. Ballard CA. Ovarian tumors associated with pregnancy termination patients. Am J Obstet Gynecol, 1984; 149: 384-7.
14. Hilgers RD. Adnexal mass and ovarian cancer in pregnacy. In: Gleicher N. Principles and practice of Medical Therapy in Pregnancy. Third edition. California: Appleton y Lange, 1998; 1322-6.
15. Escudero PM, Méndez L. Cáncer de ovario en el embarazo. En: Fiorelli S, Alfaro HJ. Complicaciones médicas en el embarazo. México: McGraw Hill Interamericana, 1996; 373-80.
16. Zúñiga JE. Cáncer ginecológico y embarazo. En. Cifuentes R. Obstetricia de alto riesgo. 4a ed. Cali, Colombia. Aspromédica, 1994; 755-64.
17. Platek DN, Henderson CE, Goldberg GL. The management of a persistent adnexal mass in pregnancy. Am J Obstet Gynecol, 1995; 173: 1236-40.
18. Hill LM, Beatty DJ, Nowak A, Tush B. The role of ultrasonography in the detection and management of adnexal masses during the second and third trimesters of pregnancy. Am J Obstet Gynecol, 1998; 179: 6703-7.
19. Sassone AM, Timor-Tritsch IE, Artner A, Westhoff C, Warren W. Transvaginal sonographic characterization of ovarian disease. Evaluation of a new scoring system to predict ovarian malignancy. Obstet Gynecol,1991; 78: 70-6.
20. Curtis M, Hopkins MP, Zarlingo T, Martino C, Graceansky-Lengyl M, Jenison EL. Magnetic resonance imagining to avoid laparotomy in pregnancy. Obstet Gynecol,1993; 82: 833.
21. Kobayashi F, Sagawa N, Nakamura K, et al. Mechanism and clinical significance of elevated CA 125 levels in the sera of pregnant women. Am J Obstet Gynecol, 1989;160: 563.
22. Schwartz PE, Morris JM. Serum lactic dehydrogenase: A tumor marker for dysgerminona. Obstet Gynecol, 1988; 72: 511.
23. Buller RE, Darrow V, Manetta A, et al. conservative surgical management of dysgerminoma concomitant with pregnancy. Obstet Gynecol, 1992; 72: 887.
24. Hahn U, Wallwiener D. Ovarian tumors and pregnancy. Zentralbl Gynakol, 1996;118: 334-5. Abstract.
25. Thornton JG, Wells M. Ovarian cysts in pregnancy: Does ultrasound make traditional management inappropriate? Obstet Gynecol, 1987; 69: 717-20.
26. Buekers TE, Lallas TA. Chemotherapy in pregnancy obstetrics and gynecology clinics. Philadelphia: W.B. Saunders Company, 1998; 323-9.
27. Randall T. National registry seeks scarce data on pregnancy outcomes during chemotherapy. JAMA, 1993; 269: 323.
28. Malfetano JH, Goldkrand JW. Cis-platinum combination chemotherapy during pregnancy for advanced epithelial ovarian carcinoma. Obstet Gynecol, 1990; 75: 545.
*Janer Sepúlveda Agudelo. MD. Especialista en Ginecología y Obstetricia. Profesor de Cátedra Universidad Industrial de Santander.
**Wilma Castillo, Víctor Armando Pinto Barón, Fabricio García. Profesores Asociados.
Departamento de Obstetricia y Ginecología. Universidad UPTC. Tunja. Hospital San Rafael de Tunja.
Recibido: Febrero 2/2001 – Revisado: Mayo 8/2001 – Aceptado: Octubre 2/2001
