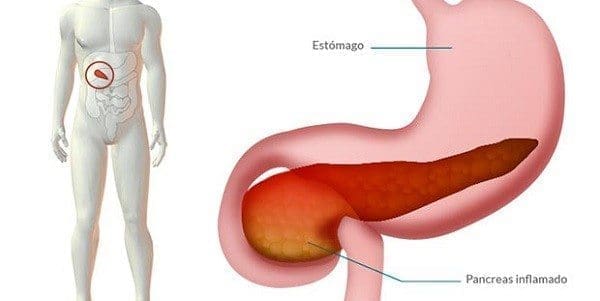
En nuestro criterio la compleja maquinaria que utiliza el páncreas para cumplir con sus funciones digestivas emplea una cadena de eventos especializados que requieren de un proceso altamente coordinado y adecuadamente controlado.
Para tal fin utiliza “Barreras de Protección” o “Semáforos de Tránsito”, que laborando ordenadamente contribuyen a que el funcionamiento se adapte y trabaje eficazmente para mantener la homeostasis.
Ciertamente para el establecimiento de la pancreatitis es indispensable que estas “Barreras de Protección” sean burladas o sobrepasadas por el insulto inicial y subsecuentemente. Por la constelación de eventos inflamatorios funestos que finalmente son los responsables del establecimiento del síndrome clínico letal.
Independientemente de la causa que precipita el establecimiento de la pancreatitis aguda finalmente el síndrome generado continúa. Siendo una enfermedad fundamentalmente homogénea que varía en severidad pero que no está relacionada con la etiología.
La unión entre la etiología y la patogénesis continúa siendo un enigma y por tal razón las bases del tratamiento desafortunadamente continúan siendo el soporte y la expectativa.
Lo más fundamental del tratamiento actual radica en que todos los cuadros de pancreatitis aguda terminan en una “vía final común” que une todas las etiologías. La observación clínica de la “vía final común” que define las principales características del curso clínico habitual de la enfermedad consiste de dos fases. Una donde se establece el daño celular inicial que se continúa con la respuesta inflamatoria sistémica.
El entendimiento de los procesos moleculares que interactúan en cada una de estas fases nos ha permitido ofrecer nuevas esperanzas terapéuticas a los pacientes que ojalá se traduzcan en mejoría de la sobrevida.
Daño Celular Inicial
Para un mejor entendimiento de los procesos moleculares que se presentan en el establecimiento de la pancreatitis aguda repasaremos brevemente algunos aspectos fisiológicos.
La célula acinar es la célula sintetizadora de proteínas más activa que posee el cuerpo de los humanos. Y más del 90% de la proteína que produce la elabora como enzimas digestivas (12).
Las enzimas digestivas junto con las hidrolazas lisosomales son sintetizadas en el retículo endoplásmico rugoso de la célula acinar.
Allí son empacadas en compartimentos rodeados de membranas y llevadas al complejo de golgi. Donde son diferenciadas por fosforilación de las proteínas destinadas a llegar a ser lisosomales (12).
Las proteínas digestivas son empacadas en vacuolas condensantes las cuales van madurando para convertirse en gránulos de zimógenos. Mientras tanto las hidrolasas lisosomales son separadas y empacadas en los lisosomas.
El sitio final dentro de la célula para los gránulos de zimógeno está en el apex. Y en la superficie luminal se presenta la fusión que permite la descarga del precursor enzimático dentro del ducto pancreático.
Secreción de las enzimas digestivas por la célula acinar
Estudios experimentales y algunas observaciones clínicas limitadas sugieren que el bloqueo en la secreción de las enzimas digestivas por la célula acinar. Puede ser el proceso fisiopatológico mas temprano que se presenta en todos los casos (independiente de la causa) de pancreatitis aguda.
Ya sea debido a alteraciones en las vías secretorias intracelulares como ocurre en la pancreatitis inducida por la ingesta de bebidas alcohólicas. O debido a un incremento en la presión intraductal como ocurre en la pancreatitis inducida por la impactación de un cálculo en la ampolla de vater (13).
Sin embargo a pesar de presentarse dicho bloqueo, al parecer los mecanismos retroalimentarios que deben existir. Dentro de la célula (como un freno de mano) y que “notifican” a la maquinaria intracelular para que la producción cese. Por razones desconocidas no funcionan (Primer semáforo desobedecido o barrera protectora desbordada).
Y así, la producción de proteínas por el retículo endoplásmico, el procesamiento y diferenciación de estas en el aparato de Golgi y la síntesis de los aminoácidos continúa normalmente.
Lo cual conduce necesariamente a que se incremente el contenido de los gránulos de los zimógenos intracelulares. Esta acumulación no puede continuar indefinidamente y eventualmente se presenta la fusión entre los gránulos de zimógenos y las enzimas lisosomales, con la consecuente descarga de los precursores de las enzimas dentro de los compartimentos lisosomales. Un proceso conocido como crinofagia (14).
Esta ubicación intracelular compartida de los dos compartimentos es un proceso fisiológico:
Que ocurre a diario y que permite que excesos de proteínas fabricadas por la célula y preparadas para ser secretadas para cumplir con sus funciones fisiológicas sean degradadas intracelularmente para mantener el equilibrio celular.
Pero este mecanismo también tiene un umbral de tolerancia (segunda barrera protectora superada) llegando al punto donde los precursores enzimáticos (principalmente el tripsinógeno) se activan intracelularmente en cantidades inapropiadas actuando dentro de la célula como uno de los asesinos más destructores sin ningún control.
Pero como lo anotamos anteriormente el páncreas sigue poseyendo mas “barreras protectoras”. E es así como fisiológicamente a diario cierta cantidad de tripsinógeno se convierte intracelularmente en su principio activo con actividad biológica, la tripsina. Pero para evitar su autoinmolación, la célula posee tres inactivadores de la tripsina que son: a) El inhibidor pancreático de la secreción de tripsina; si este es incapaz de tolerar la carga de ataque y su capacidad de bloqueo es excedida entonces entran en acción; b) la mesotripsina y c) la enzima.
Y las cuales al romper la molécula de tripsina en la arginina ubicada en la posición 117 la inactivan en forma eficaz manteniéndose el equilibrio (13). Otra vez cuando estos mecanismos protectores son desbordados se continúa en la cascada perjudicial que permite el establecimiento del síndrome de la pancreatitis (Tercera barrera protectora desbordada).
Enzimas lisosomales capaces de activar el tripsinógeno
Una de las principales enzimas lisosomales capaces de activar el tripsinógeno para convertirlo en tripsina es la Catepsina B. Esta a su vez es capaz de convertir otras pro-enzimas ubicadas dentro de los gránulos de zimógeno a su forma activa (quimotripsina, elastasa, fosfolipasa A2 etc.,).
La ruptura, liberación y derrame de estas enzimas digestivas activadas dentro del intersticio induce la autoinmolación suicida dntilde;ando la glándula y el tejido adyacente.
La lesión histología más temprana que se observa en la pancreatitis aguda experimental es la alteración estructural del ducto, del citoesqueleto de la célula acinar y de las uniones estrechas intracelulares (16). Subsecuentemente se presenta el empeoramiento de la microcirculación pancreática.
Incluyendo el estancamiento de los eritrocitos, con hamaglutinación e incremento de la permeabilidad capilar lo que facilita el acumulo de polimorfonucleares que al orquestar la secreción y producción de citoquinas, de tromboxano, y de radicales de oxígeno libre.
A su vez coordinan la expresión del óxido nítrico median el daño tisular y la pérdida de líquido dentro del espacio intersticial induciendo la aparición de edema glandular (16).
El edema, la hemorragia y la necrosis local se expanden a través del páncreas y el tejido peripancreático; el peritoneo adyacente llega a ser involucrado en el proceso inflamatorio y líquido rico en proteínas irriga la cavidad peritoneal, además también rico en enzimas y mediadores inflamatorios originados en el páncreas inflamado. Esto en efecto, es lo que más se asemeja una quemadura de tercer grado pero intra-abdominal.
Oxido Nítrico y el PAF
Es actualmente evidente (Recomendación Grado A) (17), que tanto la IL-1, TNF, IL-6, Oxido Nítrico y el PAF son producidos dentro del páncreas en todos los modelos experimentales utilizados para imitar la pancreatitis, demostrándose un incremento en sus respectivos mRNA en tan sólo 30 minutos después de inducida la pancreatitis (esto nos podría explicar por qué hasta el momento casi todos los tratamientos preventivos no han demostrado mayor utilidad).
En efecto, la producción de IL-1 y TNF es a menudo detectable antes de poder apreciar algún cambio en la histología del páncreas.
Una de las observaciones más interesantes detectadas en estos experimentos fue que la concentración de estas sustancias dentro del tejido pancreático estuvo en un orden de magnitud muchas veces mayor que las encontradas en el plasma, niveles que por lo demás son altamente tóxicos a muchos otros tipos celulares.
Mas aun, el incremento y caída en los niveles de estos mediadores se correlacionan con el desarrollo o la resolución de la enfermedad. Esencialmente todos los mediadores producidos durante el curso clínico de la pancreatitis aguda están involucrados en la producción de citoquinas pro-inflamatorias o anti-inflamatorias, o juegan un papel activo en iniciar o ampliar la cascada de las citoquinas.
Los radicales libres de oxígeno son capaces de regular un paso trascendental en la inducción intracelular del gen del TNF. Mientras que algunos de los más potentes activadores de la sintetasa inducible del óxido nítrico son las citoquinas pro-inflamatoriasTNF e IL-1.
Además, la producción del PAF, que es un potente vasodilatador y activador de los leucocitos y que ha sido implicado en el desarrollo del SDRA. Durante el curso clínico de la pancreatitis severa está estrechamente unida a la producción de TNF e IL-1 (17).
Relación a las citoquinas
Con relación a las citoquinas las cuales son las principales mediadoras de la respuesta inflamatoria en búsqueda finalmente del restablecimiento de la homeostasis la secreción de las mismas también es un proceso eficazmente coordinado en equilibrio (barrera protectora). Entre las pro-inflamatorias ( IL-1, IL-6, IL-8, TNF, PAF) y las anti-inflamatorias (IL-2, IL-10 y la antagonista al receptor de la IL-1). Para el establecimiento de la pancreatitis aguda severa es necesario que este balance se desequilibre a favor de las pro-inflamatorias (Cuarta barrera protectora desbordada).
De hecho varios estudios han demostrado (17), una correlación entre los niveles elevados de IL-6 e IL-8 y el curso clínico complicado de la pancreatitis aguda. También se ha demostrado que los niveles séricos de TNF e IL-1 se correlacionan con la severidad y la mortalidad de la pancreatitis y que como ocurre con los niveles de IL-6. Pueden ser predictivos de la falla multi-orgánica y de la duración de la estadía en el hospital.
Recomendación Grado B.
(Lea También: Diagnóstico de Pancreatitis Aguda)
Patogénesis de los Efectos Sistémicos
De las citoquinas enumeradas anteriormente una de las mejores estudiadas ha sido la interleukina 6; sus propiedades biológicas son bien caracterizadas como el factor más importante en la inducción de los reactantes de fase aguda.
Por lo anterior no es de sorprendernos, que la severidad de la respuesta sistémica asociada a la pancreatitis severa puede ser medida por el grado y duración de la elevación de IL-6.
Son precisamente las proteínas producidas como reactantes de fase aguda las que utiliza primordialmente el organismo. Para orquestar y dirigir la respuesta inflamatoria no desbordada que logre controlar el insulto inicial y permita restablecer la homeostasis.
Sin embargo, para el establecimiento de la pancreatitis severa es necesario que estos reactantes de fase aguda sean desbordados (quinta barrera desbordada). Y así la respuesta inflamatoria se descontrole y se propague a órganos distantes induciendo el síndrome de la falla multi-orgánica. Se ha demostrado que en la pancreatitis aguda se incrementa la síntesis de IL-1,TNF mRNA y de óxido nítrico en el bazo, pulmón e hígado. Pero no en músculo, riñón o tejido adiposo.
Mas interesantemente ha sido el descubrimiento que la producción de mediadores dentro del páncreas siempre precede a la síntesis de los mismos en sitios distantes por horas o incluso por días.
Efectos sistémicos de la pancreatitis aguda
Muchos de los efectos sistémicos de la pancreatitis aguda son el resultado, directa o indirectamente del derrame en la circulación de proteasas y enzimas activas con enorme potencial pro-inflamatorio. (Tabla 1). En la pancreatitis edematosa leve autolimitada, estas proteasas son capturadas eficientemte por la alfa1-antiproteasa (un reactante de fase aguda), inactivándolas.
Una vez capturadas las proteasas son transferidas a la alfa2-macroglobulina. La cual es la principal proteína inhibidora de proteasas que circula sistemáticamente, y el complejo es rápidamente consumido y fagocitado por los monocitos y macrófagos (figura 4).
En la pancreatitis severa, este sistema llega a ser saturado con el exceso de proteasas circulantes. El nivel de alfa2-macro-globulina se reduce ya que se consume y la función del sistema retículo-endotelial se deprime (Sexta barrera desbordada).
Es en esta situación cuando las proteasas libres pueden circular y causar daño sistémico generalizado por la activación de otros sistemas enzimáticos y de múltiples citoquinas inflamatorias.
Tabla 1. Enzimas involucradas en la respuesta inflamatoria sistémica
|
Calicreina: |
Induce la formación de bradiquinin incrementando la permeabilidad capilar y la vasodilatación |
|
Complemento |
Su activación induce la quimiotaxis de leucocitos que se ha visto involucrado en el daño de diferentes órganos. |
|
Trombina: |
Puede conllevar al desarrollo de coagulación intravascular diseminada. |
|
Fosfolipasa A2: |
Su activación promueve la destrucción de la membrana celular y del surfactante pulmonar. |
|
Elastasa: |
Promueve la destrucción de los vasos sanguíneos. |
|
Quimiotripsina: |
Promueve la síntesis de radicales libres derivados de oxígeno.
|
Sustancia P es un neuropéptido
La sustancia P es un neuropéptido que se encuentra en los nervios sensitivos viscerales, en la médula espinal y en el sistema nervioso central. Las funciones esenciales de la sustancia P radican en la transmisión del dolor y en mediar procesos inflamatorios.
Se ha demostrado recientemente que para el establecimiento de la pancreatitis y fundamentalmente de las complicaciones pulmonares de la misma. Es necesario y casi esencial que se libere la sustancia P y esta se una a su receptor denominado NK1(14 a).
En condiciones homeostáticas la temible y lesiva unión de estos dos elementos explosivos no se da o por lo menos se impide por mecanismos fisiológicos de control y regulación interna.
Para que las costelaciones de errores y excesos se de en forma ordenada en el establecimiento de la pancreatitis. Es indispensable e incluso un paso limitante (cuello de botella) que este mecanismo de autocontrol y freno se presente (Séptima barrera desbordada)
El tren de la pancreatitis toma la ruta
Finalmente evidencias sólidas recientes (5,15); (Recomendación Grado A), como se discutió anteriormente. Sugieren que una vez el tren de la pancreatitis toma la ruta desordenada violando inmisericordemente todas las barreras que existen naturalmente para protegernos del desarrollo de la pancreatitis. Los mediadores producidos y liberados por las células activadas de la respuesta inflamatoria. Principalmente los polimorfonucleares contribuyen considerablemente al establecimiento de las reconocidas complicaciones sistémicas que pueden ocurrir en la pancreatitis aguda severa.
En la inflamación inicial, se liberan factores quimotácticos principalmente el Complemento que activa inicialmente a los PMNS y posteriormente a los Monocitos.
En los sitios inflamados estas células activadas liberan múltiples productos biológicamente activos como los radicales de oxígeno libre, enzimas proteolíticas, sustancias vasoactivas, y citoquinas (IL-1, IL-6,IL-8 y TNF-alfa). Con las múltiples consecuencias funestas contribuyendo al establecimiento de la falla multi-orgánica.
Los PMNS también son capaces de inducir daño directo a través de la producción de elastasa y del ion super-óxido que causan considerable daño endotelial. Además, son una fuente importante del PAF al ser estimulados por el TNF. Como lo anotamos anteriormente se estima que éste es el principal responsable de mediar el desarrollo del SDRA en los pacientes con pancreatitis aguda severa (15). (Figura 2 esquema fisiopatológico como un tren con sus estaciones).