Presentación de un Caso Hospital Simón Bolívar, Santa Fe de Bogotá
Suarez Gustavo, Mendivelson Ellen, Velez Jose Roberto, Rojas Elsa, Velandia Fernando
Resumen
La histoplasmosis intestinal en pacientes con síndrome de inmunodeficiencia adquirida es una entidad rara. Se han descrito pocos casos en la literatura. La mayoría de los pacientes presenta dolor abdominal, pérdida de peso, diarrea, fiebre y hemorragia de vías digestivas.
Presentamos el caso de un paciente de sexo masculino, HIV positivo, que desarrolló histoplasmosis colónica y revisamos la literatura.
Palabras claves: SIDA, histoplasmosis intestinal.
Summary
Gastrointestinal histoplasmosis in patients with the Acquired Immune Deficiency Syndrome is a rare entity. There have been very few cases described in the literature. Most patients present with abdominal pain and weigth loss associated to diarrhea, fever and gastrointestinal bleeding. We present a case of a male patient, HIV possitive who developed colonic histoplasmosis and review all the literature available.
Key words: Gastrointestinal histoplasmosis, AIDS.
Introducción de la histoplasmosis intestinal
La Histoplasmosis Intestinal es una infección sistémica frecuente causada por un hongo dimórfico, Histoplasma capsulatum (HC), descrita por primera vez por Darling en 1906 (1) y especialmente endémica en los valles de Ohio, Missisipi y Missouri en los Estados Unidos y en el Caribe, Centro y Suramérica (2-3).
La infección se adquiere por inhalación de microconidias, las cuales llegan a los alvéolos pulmonares y son fagocitadas por los macrófagos formando granulomas que se pueden calcificar. Causa generalmente infecciones autolimitadas en pacientes inmunocompetentes, pero puede tener presentación diseminada en pacientes con alteración de la inmunidad (4).
Cuando se manifiesta como Histoplasmosis Intestinal diseminada, se considera el resultado de la reactivación de la infección latente. Se ha descrito compromiso del sistema nervioso central (5), de los ojos (6) y del sistema gastrointestinal (7), entre otros.
El diagnóstico se hace con base en el hallazgo del HC, tomando muestra de médula ósea o del tejido afectado (8-10), se realiza la tinción de Giemsa, buscando levaduras en el interior de macrófagos. También, se pueden realizar tinciones de PAS, Gomori-Grocott o de hematoxilina-eosina.
Se debe también realizar cultivo a 37°C en agar sangre-glucosa-cisteína y en agar Sabouraud. Otras ayudas diagnósticas son los estudios de tipo inmunológico como la aglutinación en látex, la fijación de complemento (4) y ELISA.
El tratamiento se hace con anfotericina B hasta llegar a una dosis acumulada de 1-2 g, aunque no parece ser curativo en pacientes con SIDA por lo cual se sugiere continuar el tratamiento con ketoconazol (400 mg/día) o con anfotericina B (1 mg/kg/semana) (11-14).
Presentación de un Caso
Se presenta el caso de un paciente de sexo masculino, de 32 años de edad, con diagnóstico de infección por VIH en agosto de 1998, en tratamiento con AZT, 3TC e indinavir, quien ingresó por un cuadro clínico de 3 meses de evolución de dolor abdominal tipo cólico, localizado en meso e hipogastrio, sin diarrea ni emesis, asociado a fiebre alta vespertina de 39°C y pérdida de peso no cuantificada de igual tiempo de evolución.
Refería ingresos hospitalarios previos por cuadros similares, asociados además a deposiciones diarreicas. En la última hospitalización, se le practicó colonoscopia total que mostró la presencia de múltiples lesiones ulceradas cuyas biopsias fueron originalmente informadas como posible infección por P. carinii por lo cual se inició tratamiento con trimetoprim-sulfametoxazol.
La última carga viral, en febrero de 1999, reportó 61.520 copias/ml y CD4 de 243/mm3.
En el examen físico de ingreso se encontró un paciente caquéctico, con TA de 100/60, FC de 88/min, FR de 18/min, palidez mucocutánea generalizada, sin alteraciones cardiopulmonares, abdomen blando y doloroso a la palpación en mesogastrio e hipogastrio sin irritación peritoneal, y atrofia muscular generalizada.
Los exámenes paraclínicos iniciales mostraron un cuadro hemático con 2.100 leucocitos, 79% neutrófilos, 16% linfocitos, hemoglobina de 7,9, hematocrito de 22% y 400.000 plaquetas.
Se realizó nueva colonoscopia en la que se observaron lesiones ulcerosas irregulares:
Múltiples, de 2 a 3 cm de diámetro, con fondo recubierto de fibrina entre áreas respetadas de mucosa normal en colon transverso, descendente y sigmoide. En el ciego, se observó una extensa lesión de iguales características que rodeaba la válvula ileocecal (figura 1), obstruyéndola parcialmente; la progresión del colonoscopio al íleon mostró compromiso similar en los últimos diez cm del íleon distal (figura 2), que adoptó una morfología tubular. Se tomaron múltiples biopsias en las que se observó un epitelio colónico ulcerado (figura 3) con áreas aisladas de necrosis (figura 4) que mostraron la presencia de gran cantidad de microconidias (figura 5) y que fueron confirmadas como correspondientes a HC.
Se inició tratamiento con anfotericina B. Ocho días después, el paciente presentó reagudización del dolor abdominal con hallazgos en el examen físico sugestivos de abdomen agudo, por lo cual fue llevado a cirugía donde se encontró peritonitis generalizada sin perforación intestinal y múltiples bridas. En el postquirúrgico, se continuó su manejo con anfotericina B; evolucionó tórpidamente y falleció.
Discusión de la histoplasmosis intestinal
Desde 1987, la histoplasmosis intestinal se reconoce como enfermedad que define SIDA (15). Se considera la segunda infección oportunista más frecuente en los pacientes con SIDA, después de P. carinii en las zonas endémicas (16) y para su diagnóstico es muy importante el antecedente epidemiológico de la procedencia.
Cuando se manifiesta como infección oportunista en el SIDA, puede presentar compromiso intestinal. La histoplasmosis intestinal (HI), descrita por primera vez en 1942 (17), es secundaria a la diseminación hematógena (18). Hay realmente pocos informes de casos de HI en la literatura mundial y puede ocurrir como manifestación única aislada. Las manifestaciones clínicas son principalmente diarrea, pérdida de peso, fiebre de aparición vespertina, sintomatología constitucional, dolor abdominal, náuseas, vómito, hemorragia de vías digestivas y perforación intestinal (19-20).
Afecta principalmente el íleon terminal y el colon aunque puede comprometer cualquier segmento del tubo digestivo (19), presentándose como lesiones múltiples, ulceradas, granulomatosas, con formas pseudopolipoides y fondo necrótico que pueden recordar enfermedades como la tuberculosis o las neoplasias, entre otras.
Se reconocen cuatro formas clinicopatológicas de HI. La primera se presenta como infiltración de macrófagos en la lámina propia con HC, generalmente es subclínica; la segunda tiene pequeños pseudopólipos causados por la agregación de los macrófagos; la tercera se asocia a necrosis tisular y ulceración, y la cuarta se presenta con inflamación localizada y estrechamiento de la luz intestinal (20).
Colonoscopia y estudio histopatológico
El diagnóstico se basa en la colonoscopia y en el estudio histopatológico (5, 21-22); el diagnóstico diferencial se debe hacer con la enfermedad de Crohn, la TBC, la colitis infecciosa, la colitis ulcerativa, el carcinoma y la amiloidosis (21, 23-24).
Por último, se plantea en la literatura médica (22) que a todo paciente con SIDA y sintomatología intestinal se le debe realizar una colonoscopia total y tomar biopsias para descarta HI, como parte del estudio gastroenterológico habitual.
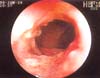
Figura 1. Compromiso del ciego y de la válvula íleocecal, observándose una extensa lesión ulcerada de bordes irregulares y fondo fibrinoide que obstruye parcialmente la luz de la válvula ileal
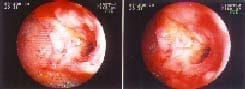
Figura 2. Compromiso de los últimos centímetros del íleon distal observándose una mucosa fibrogranular y con aspecto tubular.
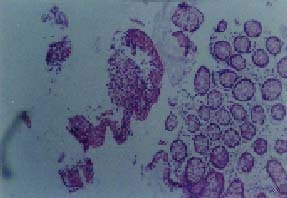
Figura 3. Epitelio colónico ulcerado. Hematoxilina-eosina, 10X.
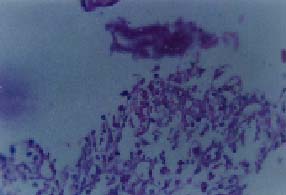
Figura 4. Area necrótica de la mucosa con sospecha de microorganismos. Hematoxilina-eosina, 40X.

Figura 5. Coloración de PAS, 100X, el mayor aumento con aceite de inmersión demuestra la presencia de microconidias de H. capsulatum (núcleo y área clara periférica por artificio).
Bibliografía
- 1. Darling ST. A protozoan general infeccion producing pseudotubercles in the lungs and focal necrosis in the liver, spleen and lymphatics. JAMA 1906; 46: 1283-5.
- 2. Wheat LJ, Slama TG, Eotzen HE, Kohler RB, French ML, Biesecker JL. A large urban outbreak of histoplasmosis. Ann Intern Med 1981; 94: 331-7.
- 3. Chretien JH, Garagusi VG. Current management of fungal enteritis. Med Clin North Am 1982; 66: 675-87.
- 4. Wheat LJ, Slama TG, Zeckel ML. Histoplasmosis in the adquired immune deficiency Syndrome. Am J Med 1985; 78: 203-10.
- 5. Sarosi GA, Johnson PC. Disseminated histoplasmosis in patients with human immunodeficiency virus. Clin Infec Dis 1992; 14(sup): 60s-67s.
- 6. Macher A, Rodríguez MM, Kaplan W, et al. Disseminated bilateral chorioretinitis due to Histoplasma capsulatum in a patient with the acquired immunodeficiency syndrome. Ofthalmology 1985; 92: 1159-64.
- 7. Haggerty CM, Britton MC, Dorman JM, et al. Gastrointestinal histoplasmosis in the adquired immune deficiency syndrome. West J Med 1985; 143: 244-66.
- 8. Bonner JR, Alexander WJ, Dismukes WE, et al. Diseminated histoplasmosis in patients with adquired immune deficiency syndrome. Arch Intern Med 1984; 144: 2178-81.
- 9. Huang CT, McGarry T, Cooper S, et al. Diseminated histoplasmosis in the adquired immunodeficiency syndrome: report of five cases from nonendemic area. Arch Intern Med 1987; 147: 1181-4.
- 10. Jagadha V, Andavolu RH, Huang CT. Granulomatous inflammation in the adquired immune deficiency syndrome. Am J Clin Pathol 1985; 84: 598-602.
- 11. Minamoto, Armstrong D. Fungal infections in AIDS, histoplasmosis and coccidioidomycosis. Infec Dis Clin North Am 1988; 2: 447-56.
- 12. Goodwin RA, Shapiro JL, Thurman GH, et al. Diseminated histoplasmosis: clinical and pathologic correlations. Medicine 1980; 59: 1-33.
Referencias
- 13. McKinsey DS, Gupta MR, Riddler SA, Driks MR, Smith DL, Kurtin PJ. Long term amphotericin B therapy for disseminated histoplasmosis in patients with AIDS. Ann Intern Med 1989; 111: 655-9.
- 14. Wheat LJ, Connolly-Stringfield PA, Baker RL, et al. Disseminated histoplasmosis in the adquired immune deficiency syndrome: clinical findings, diagnosis and treatment, and review of the literature. Medicine 1990; 69: 361-74.
- 15. Centers for Disease Control. Revision of the CDC surveillance case definition of acquire immunodeficiency syndrome. JAMA 1987; 31: 644-52.
- 16. Buechner HA, Seabury JH, Campbell CC, George LV, Kaufman L, Kaplan W. The current status of serologic, immunologic, and skin tests in the diagnosis of pulmonary mycosis. Chest 1973; 63: 259-70.
- 17. Henderson RG, Pinkerton H, Moore LT. Histoplasma capsulatum as a cause of chronic ulcerative enteritis. JAMA 1942; 118: 865-9.
- 18. Miller DP, Everett ED. Gastrointestinal histoplasmosis. J Clin Gastroenterol 1979; 1: 233-6.
- 19. Cappell MS, Mannell W, Grimes MM, Neu HC. Gastrointestinal histoplasmosis. Dig Dis Sci 1988; 33: 353-60.
- 20. Heneghan S, John Li, Edwin P, Lawrence S. Intestinal perforation from gastrointestinal histoplasmosis in acquired immunodeficiency syndrome. Arch Surg 1993; 128: 464-6.
- 21. Cimponeriu D, LoPresti P, Lavalanet M, et al. Gastrointestinal histoplasmosis in HIV infection: two cases of colonic pseudocancer and review of literature. Am J Gastroenterol 1993; 89: 129-31.
- 22. Graham B, McKinsey D, Driks M, et al. Colonic histoplasmosis in acquired immunodeficiency syndrome, report of two cases. Dis Colon Rectum 1991; 34: 185-90.
Fuentes
- 23. Balthazar E, Megibow A, Barry M, Opulencia J. Histoplasmosis of the colon in patients with AIDS: imaging findings in four cases. AJR 1993; 161: 585-7.
- 24. Raza J, Harris MT, Bauer JJ. Gastrointestinal histoplasmosis in a patient with acquired immune deficiency syndrome. Mt Sinai J Med 1996; 63: 136-40.
Autores
Gustavo Adolfo Suarez Zambrano. Residente I de Medicina Interna, Hospital Universitario San Ignacio, Pontificia Universidad Javeriana.
Ellen L. de Mendivelson. Jefe (E), Departamento de Medicina Interna, Hospital Simón Bolívar; Profesor asociado de Medicina Interna, Universidad El Bosque; Profesor de cátedra, Facultad de Medicina, Universidad de la Sabana.
Jose Roberto Velez Munera. Departamento de Medicina Interna, Hospital Simón Bolívar; Profesor asociado de Medicina Interna, Universidad El Bosque; Profesor de cátedra, Facultad de Medicina, Universidad de la Sabana.
Elsa Rojas. Unidad de Gastroenterología, Hospital Simón Bolívar; Profesora asociada de Medicina Interna, Universidad El Bosque.
Fernando Velandia Hurtado. Patólogo. Jefe, Sección de Apoyo Diagnóstico, Hospital Simón Bolívar; expresidente, Sociedad Colombiana de Patología.