Luisa Fernanda Álvarez1, Juan Carlos Mejía1, Sergio Iván Hoyos2
Palabras clave: páncreas; neoplasias pancreáticas; quiste pancreático; pancreatectomía
Resumen
Dados el incremento del uso de la imaginología en el proceso diagnóstico y los avances tecnológicos en su resolución y calidad, muchas enfermedades antes no esclarecidas, e incluso asintomáticas, están siendo descubiertas accidentalmente. Tal es el caso de las lesiones quísticas del páncreas, las cuales no eran diagnosticadas unos 30 años atrás, puesto que la mayoría cursan sin síntomas. Gran cantidad de las lesiones quísticas sintomáticas que afectan el parénquima pancreático, se deben a la presencia de seudoquistes no neoplásicos, cuyo manejo puede ser simplemente el drenaje o el seguimiento médico, mientras que las lesiones quísticas generalmente asintomáticas, son quistes neoplásicos.
Introducción
En los últimos años, es cada día más frecuente encontrarse con el diagnóstico de lesiones quísticas del páncreas, debido al mayor uso y mejores técnicas de imaginología; muchas de estas lesiones son descubiertas de manera incidental.
Anteriormente se consideraba que la mayoría de estas lesiones eran inflamatorias1, ahora se sabe que muchas pueden ser tumorales. Existen fundamentalmente cuatro tipos de lesiones identificadas y clasificadas por la Organización Mundial de la Salud (OMS), que son: la neoplasia quística serosa, la neoplasia quística mucinosa, la neoplasia papilar intraductal mucinosa y la neoplasia sólida seudopapilar (tabla 1). Es pertinente aclarar que tanto el tratamiento como el pronóstico de cada una de las lesiones, difiere según su tipo, razón por la cual es necesario lograr, en lo posible, un adecuado diagnóstico diferencial de estas neoplasias. Se propone, entonces, hacer una revisión de cada una de las neoplasias quísticas pancreáticas.
Tumor papilar intraductal mucinoso
Generalidades
El tumor papilar intraductal mucinoso fue descrito por primera vez en 1982 por Ohashi, et al. 2, como un tumor de páncreas productor de mucina. Comprende un grupo de lesiones que difieren de las neoplasias quísticas mucinosas porque están en comunicación directa con el conducto de Wirsung y no existe estroma de tipo ovárico 3. Estos tumores representan, aproximadamente, el 7 % del diagnóstico clínico de los tumores del páncreas y hasta 50 % de los quistes pancreáticos diagnosticados accidentalmente 4.

Está caracterizado por el crecimiento papilar o no del epitelio ductal, con producción de mucina y expansión quística del conducto involucrado 5,6. La historia natural de este tumor es diferente a la del adenocarcinoma ductal: en 90 a 100 % de los casos es extirpable, con una tasa de supervivencia que llega a 80-90 % para el carcinoma in situ, 50-70 % para el carcinoma invasivo y 40-50 % cuando hay metástasis ganglionar 6.
Los tumores papilares intraductales mucinosos aparecen comúnmente en hombres ancianos, con una edad media de presentación de 70 años y, aunque pueden ubicarse en cualquier parte de la glándula 7, se encuentran localizados en la cabeza del páncreas, usualmente en el proceso uncinado 5,8.
Clasificación
Se clasifican, según su localización, como del tipo del conducto pancreático principal o del conducto accesorio, definido como una comunicación entre el conducto pancreático principal normal y la lesión quística 5,6, pudiendo comprometer los dos tipos de conductos (tipo multifocal, combinado)6. Este último tipo suele ser una presentación de los tumores papilares intraductales mucinosos que comprometen el conducto principal, según la clasificación de la OMS; sin embargo, es más frecuente encontrarlo en aquellos tumores que afectan el conducto accesorio 7. El tumor que compromete los conductos accesorios tiene un curso diferente al de los otros dos tipos, ya que se encuentra más comúnmente en pacientes jóvenes y su potencial como neoplasia maligna es muy bajo 9.
El tamaño de la lesión producida por los tumores papilares intraductales mucinosos es mayor de 1 cm y varía en un rango de atipia celular que va desde la displasia leve hasta un carcinoma franco 8, por lo tanto, se consideran lesiones premalignas que pueden ser claramente malignas. Los detalles de su progresión a enfermedad invasiva no son claros, pero se estima que en un rango de 5 a 7 años 10, el tumor papilar intraductal mucinoso –que es un precursor importante del adenocarcinoma ductal pancreático– podría progresar en la secuencia hiperplasia-adenoma-carcinoma 5. Por esta razón, es importante considerarlo como un factor de riesgo, indicativo de adenocarcinoma concurrente en una etapa temprana. Se recomienda, entonces, la evaluación radiológica detallada del páncreas 5.
Histológicamente, en los tumores papilares intraductales mucinosos se encuentran células neoplásicas productoras de mucina organizadas en un patrón papilar. La producción de mucina por las células conduce a una acumulación intraductal de mucina y a una subsecuente dilatación quística. La producción de mucina puede ser tan abundante, que se puede ver saliendo por la ampolla de Vater, lo cual es un hallazgo patognomónico 8.
Manifestaciones clínicas
En general, todas las lesiones quísticas pancreáticas dan lugar a síntomas. Los pacientes frecuentemente refieren dolor en la región epigástrica que, en algunas ocasiones, se irradia a la espalda y se exacerba con la comida 3,8. El dolor se explica por el crecimiento papilar y por la obstrucción causada por el exceso de producción de mucina que bloquea el conducto pancreático 5,8. Se pueden incluir, además, otros signos y síntomas, como pérdida de peso, fiebre e ictericia 6,8. Muchos pacientes reciben un diagnóstico erróneo al considerarse que sufren una pancreatitis crónica 8.
Diagnóstico
El diagnóstico, usualmente, se basa en las imágenes radiológicas 6, en las que se observa un conducto pancreático dilatado, asociado eventualmente a masas quísticas; también es posible diferenciar entre mucina e infiltraciones papilares dentro del conducto y demostrar comunicaciones entre la lesión quística y el conducto de Wirsung normal por medio de la colangio-pancreatografía retrógrada endoscópica, la tomografía computadorizada o la resonancia magnética colangio-pancreática con estimulación de secretina 6,7 (sensibilidad de 83 % para el diagnóstico)6. La comunicación con el conducto confirmaría el diagnóstico 6,8.
En el ultrasonido de los tumores papilares intraductales mucinosos, generalmente, se encuentra un conducto pancreático dilatado en el caso de los del tipo del conducto pancreático principal, o una masa quística pleomorfa bien circunscrita en el caso de los del conducto accesorio. La ecografía no siempre demuestra comunicación con el conducto principal en las lesiones accesorias 11. Por las dificultades para la evaluación de los hallazgos, el ultrasonido no es específico para estas lesiones y, por lo tanto, requieren ser evaluadas por otro tipo de estudios imaginológicos.
En la tomografía computadorizada, el tumor del conducto accesorio aparece comúnmente como una lesión hipodensa con contornos pleomorfos cerca del conducto pancreático. Clásicamente, se encuentra en el proceso uncinado. El conducto pancreático principal no se observa dilatado. La comunicación entre la lesión y el conducto usualmente no se ve en la imagen axial. Las lesiones del conducto pancreático principal son tipificadas por su dilatación segmentaria o difusa. Una lesión discreta podría no ser visualizada. El contraste resalta las lesiones que contienen focos nodulares y permite diferenciar los glóbulos de mucina de un tumor sólido, ya que este último resalta ante el contraste, mientras que los primeros pasan desapercibidos.
La resonancia magnética colangio-pancreática permite evaluar el sistema del conducto pancreático sin ser invasiva. En ella se pueden observar lesiones del conducto pancreático principal caracterizadas por la dilatación de todo el conducto pancreático principal. Una lesión discreta podría no ser visualizada. Sin embargo, los tumores del conducto pancreático principal deben considerarse en los pacientes con un conducto pancreático dilatado sin una lesión obstructiva visible o sin estenosis y con disfunción de la ampolla. En estos casos, una resonancia magnética colangio-pancreática con inyección de secretina o una colangio-pancreatografía retrógrada endoscópica podrían ayudar a esclarecer el diagnóstico. Las lesiones del conducto accesorio tienen una apariencia pleomorfa y son hiperintensas en T2 e hipointensas en T1. La lesión se encuentra próxima o en comunicación directa con el conducto principal pancreático. Las lesiones combinadas que comprometen el conducto pancreático principal y los conductos accesorios, tienen una dilatación simultánea de los dos tipos de conductos. Luego de la infusión con gadolinio, se pueden observar las áreas de engrosamiento de la pared o los componentes nodulares de la lesión 12.
La ecografía endoscópica es una de las ayudas diagnósticas más sensibles para caracterizar las neoplasias quísticas pancreáticas. En el caso de los tumores papilares intraductales mucinosos, puede visualizar la comunicación entre el conducto pancreático principal y un conducto aledaño dilatado, y ayuda a hacer el diagnóstico diferencial entre los depósitos de moco y las lesiones polipoides intraductales; igualmente, visualiza el adelgazamiento de la pared del conducto pancreático o nodos murales. La efectividad diagnóstica de este método es de 92 %. Se sugiere una lesión maligna cuando el diámetro del conducto principal pancreático es mayor de 10 mm, se encuentran lesiones mayores de 40 mm, delgadas con tabique irregular y presencia de nódulos murales que excedan 10 mm de diámetro 13.
En el estudio de las neoplasias quísticas del páncreas también se puede utilizar técnicas de ecografía endoscópica con contraste o con Power Doppler las cuales muestran información sobre la irrigación y el flujo sanguíneo en los tejidos afectados. En los tumores pancreáticos pequeños (≤2 cm), la sensibilidad para detectar carcinoma ductal es de 83,3 % y 50 %, respectivamente. Recientemente fue desarrollada una técnica de ecoendoscopia con un transductor de banda ancha llamado harmónico; esta tecnología puede detectar señales de microtubúlos en vasos con flujo lento, permitiendo caracterizar la irrigación del tumor 13,14.
Dada la asociación que existe entre el tumor papilar intraductal mucinoso con el cáncer extrapancreático (gástrico y colorrectal, principalmente) 15, es importante descartar cualquiera de estas dos neoplasias una vez se haya hecho el diagnóstico del quiste pancreático, ya que hay series que reportan tasas de correlación que van desde 8,5 hasta 16,8 % para los occidentales 16 y de 30 a 38 % para los orientales 17. La diferencia entre los orientales y los occidentales podría ser difícil de explicar, pero puede deberse a las diferencias regionales en la incidencia individual del cáncer 18 (figuras 1a y 1b)
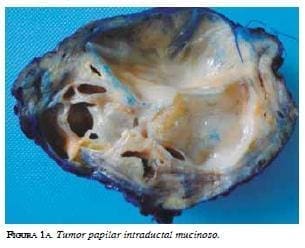 |
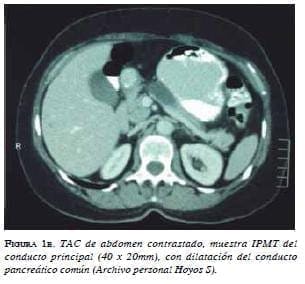 |
Manejo
Actualmente se conocen ciertas características predictoras de un proceso maligno: tumor papilar intraductal mucinoso del conducto principal, dilatación del conducto pancreático (>6 mm) 19, tamaño del tumor >30 mm, presencia de nódulos murales (>5) 20, fuga de mucina por la ampolla de Vater, niveles de CA 19-9 (>37 U/ml) 19, pancreatitis previas, presencia de ictericia y diabetes 6.
Los tumores papilares intraductales mucinosos que comprometen los conductos accesorios tienen un bajo riesgo de progresión maligna 8; por lo tanto, debe observarse si las lesiones tienen un tamaño menor de 3 cm con paredes delgadas, ausencia de nódulos murales y el paciente se encuentra asintomático 3,6,7,16. El seguimiento debe ser anual si la lesión es menor de 1 cm, cada 6 a 12 meses si mide entre 1 y 2 cm, y, por último, si el tamaño es mayor de 2 cm se debe hacer cada 3 a 6 meses 3. La cirugía se recomienda tan pronto como se evidencie progresión de la enfermedad, manifestada por crecimiento secuencial del quiste, aparición de nuevos síntomas atribuibles a la presencia del quiste, tamaño quístico mayor de 3 cm o dilatación mayor de 6 mm del conducto pancreático principal. Si durante el seguimiento no se observan cambios, el intervalo de seguimiento puede aumentar después de los primeros dos años 3, pero siempre se debe continuar con la vigilancia a largo plazo.
La diferencia de edad de los pacientes con lesiones benignas y malignas y la evidencia de “progresión clonal” o neoplasia en el conducto principal, sugieren que los pacientes con tumores papilares intraductales mucinosos del conducto principal deben ser llevados a cirugía para la resección del tumor, independientemente de la presencia o ausencia de síntomas; esto está de acuerdo con el consenso de las Guías de la Asociación de Pancreatología 3,6,16. A los cinco años, la supervivencia de los pacientes con resección del tumor con cáncer no invasivo es mayor de 70 % y de 40 % cuando hay invasión 21. Entre el 20 y el 30 % de los tumores papilares intraductales mucinosos son multifocales; se observa más comúnmente en pacientes con tumor papilar intraductal mucinoso del conducto pancreático accesorio 7 y de 5 a 10 % podrían involucrar toda la glándula 22; por esta razón, más del 15 % de los pacientes requieren pancreatectomía total. El seguimiento es importante para los restantes, ya que se ha reportado recurrencia del 7 % de los casos, aun con márgenes de resección negativos 8,21. La observación y el seguimiento de los tumores papilares intraductales mucinosos debe hacerse con resonancia magnética colangio-pancreática con estimulación de secretina o sin ella 7, ya que los niveles séricos de CA19-9 no proveen ningún valor en el seguimiento de estos pacientes 3.
Ante la controversia que generan las indicaciones quirúrgicas y la extensión de la resección pancreática, en el caso de tumores papilares intraductales mucinosos multifocales y de bajo riesgo de neoplasia maligna 6, en un estudio prospectivo 7 se propuso una clasificación de manejo basada en la localización topográfica de los quistes (tabla 2).
Se concluye, entonces, que los tumores papilares intraductales mucinosos del conducto principal requieren cirugía inmediata por el alto riesgo de un proceso maligno, mientras que los que comprometen el conducto accesorio, deben ser evaluados clínica y morfológicamente para determinar cuál es el mejor tratamiento.
1 Estudiantes, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
2 Profesor asistente, Grupo de Gastrohepatología, Facultad de Medicina, Universidad de Antioquia; Unidad de Cirugía Hepatobiliar y Pancreática, Programa de Trasplante Hepático, Universidad de Antioquia-Hospital Pablo Tobón Uribe, Medellín, Colombia.
