Los glucocorticoides promueven indirectamente la pérdida ósea mediante la inhibición de la liberación de gonadotrofinas, produciendo hipogonadismo secundario 33.
Los pacientes tratados con glucocorticoides tienen factores adicionales de riesgos independientes que con- llevan la pérdida de masa ósea y fracturas; entre ellos, está la enfermedad primaria de base, particularmente las alteraciones inflamatorias y autoinmunitarias que causan detrimento del metabolismo óseo independientemente del tratamiento con glucocorticoides.
Colestiramina
Impide la unión de los ácidos grasos y, de esta manera, reduce la absorción gastrointestinal de 25-hidroxi-vita- mina D. Además, la precipitación de las sales de calcio en el intestino, por la presencia de grasas no absorbidas, puede contribuir a la mala absorción del calcio.
Diuréticos
El uso de diuréticos es común en los pacientes con enfermedad hepática avanzada. Los diuréticos de asa promueven la pérdida renal de calcio y, en una cohorte de 8.127 mujeres mayores de 65 años seguidas por más de cuatro años, se asociaron con una pérdida pequeña de masa ósea en la cadera; en este estudio no hubo asociación con fractura 34. En una cohorte del Women’s Health Initiative (WHI) de 133.855 mujeres seguidas por más de siete años, se halló que el uso prolongado de diuréticos se asociaba con mayores riesgos de frac- tura en las posmenopáusicas, pero no se asociaba con alteraciones de la masa ósea o caídas 35. En un estudio de 3.269 hombres mayores de 65 años seguidos por más de cuatro años, se halló un incremento de la pérdida de masa ósea 36.
La espironolactona es un diurético antiandrógeno que no tiene estudios de asociación con osteoporosis y sus resultados, pero, por su efecto antiandrogénico podría contribuir al deterioro óseo.
Antivirales
Un estudio de corte transversal sugiere que la ribavi- rina puede inducir pérdida de masa ósea en pacientes con hepatitis crónica (Z score 1,5 veces disminuido, comparado con pacientes no tratados con ribavirina) 37, pero el mecanismo de este efecto no se ha determi- nado claramente y ha sido refutado por otro estudio longitudinal 38.
Consumo de alcohol
Los pacientes con cirrosis alcohólica tienen un patrón de bajo recambio óseo. En un estudio de 56 hombres alcohólicos, se demostró que 32 % tenía disminución de los niveles de 25-hidroxi-vitamina D y de la densi- dad mineral ósea 39. La ingestión excesiva de alcohol puede llevar a un desequilibrio entre la formación y la resorción ósea, que favorece el desarrollo de osteopenia. Asimismo, el consumo de alcohol es un factor de riesgo independiente para la osteoporosis y, además, incrementa el riesgo de fractura de cadera en 2,8 veces 7.
Deficiencia de vitamina D
En la literatura científica se reporta que los niveles de vitamina D están disminuidos en dos tercios de los pacientes con cirrosis y en 96 % de los que se encuentran en espera de trasplante hepático 40. En el estudio de Wiboux, et al., se reportó 88 % de prevalencia de insuficiencia y deficiencia de vitamina D 1.
El hígado tiene un papel esencial en el metabolismo de la vitamina D. Se encarga de la secreción de las sales biliares, la absorción de la vitamina D3 de la dieta y la 25-hidroxilación de la vitamina D 41. En casos de en- fermedad hepática, la colestasis y ciertos medicamentos –incluyendo los glucocorticoides–, alteran la captación y el metabolismo de la vitamina D 42.
La osteomalacia es infrecuente en los pacientes con cirrosis 10; sin embargo, la hipovitaminosis D se encuentra asociada con reducción de la densidad mineral ósea, bajo recambio óseo y aumento del riesgo de fracturas que ocurre en estos casos 41.
Inflamación Crónica
El proceso inflamatorio crónico, la alteración del flujo sanguíneo hepático, la activación de células estrelladas y la pérdida de la función sintética, son algunas de las consecuencias de la cirrosis que se encuentran relacio- nadas con las alteraciones metabólicas óseas (figura 3).
El FCI-1 juega un papel importante en la remodelación ósea y el mantenimiento de la masa ósea. Sin embargo, se encuentra disminuido en la enfermedad hepática avanzada, de manera proporcional a su gravedad. Se ha demostrado que el reemplazo de FCI-1 en ratas es efectivo para la prevención e, incluso, la reversión parcial de la osteoporosis 19.
La leptina, producida por las células adiposas, tiene acción periférica para el control de la masa ósea me- diante el aumento de la proliferación osteoblástica, la síntesis de matriz ósea y la supresión de la producción de RANK-L y, por lo tanto, disminuye la resorción ósea. Esta molécula se encuentra disminuida en algu- nas formas de enfermedad hepática, especialmente las colestásicas 19.
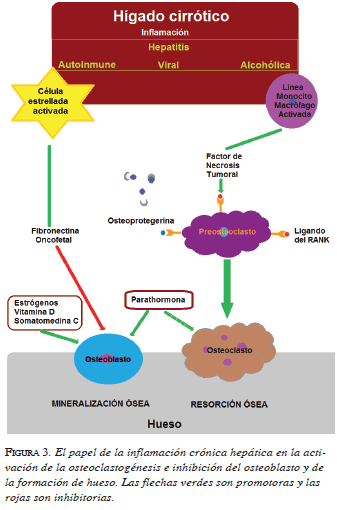
Las citocinas proinflamatorias, como el FNT y la IL-1, e incrementan la actividad de osteoclastos por activación de sus precursores. Estos se encuentran aumentados, principalmente en las hepatitis virales y en la cirrosis inducida por alcohol 19.
Conclusión
En la osteodistrofia hepática, el deterioro de la masa ósea es complejo y se debe a factores relacionados con la enfermedad en sí, complicaciones nutricionales y medicamentos. Aún no se ha evaluado la carga genética individual en esta enfermedad. Existen múltiples factores de riesgo que podemos contrarrestar con el abordaje integral en la atención médica.
Recomendaciones
Entre las medidas preventivas para detener y evitar la pérdida de la densidad mineral ósea y la aparición de osteoporosis con sus fracturas, se encuentran la tami- zación y el diagnóstico, la disminución de los factores de riesgo y el tratamiento activo.
•Al paciente con cirrosis se le debe practicar una absorciometría de rayos X de energía dual para evaluar la densidad mineral ósea.
•Se debe ordenar medición en suero de la 25-hidroxi- vitamina D, y los niveles de calcio y fósforo.
•Hay que incentivar el ejercicio y las medidas para prevenir fracturas.
•Se deben corregir los factores de riesgo modificables, como el consumo de alcohol, el bajo índice de masa corporal, el consumo de tabaco, el sedentarismo, el riesgo de caídas, etc.
•Hay que corregir los defectos de calcio y vitamina D en los pacientes que presenten alteraciones.
•Se deben tratar la osteoporosis y el deterioro de la masa ósea, según las recomendaciones actuales para el manejo de osteoporosis.
Bone loss in hepatic cirrhosis: phisiopathology of hepatic osteodystrophy
Abstract
Cirrhosis is an advanced stage of fibrosis; it is a consequence of the progression of chronic liver disease, characterized by destruction of architecture and predisposes to the development of hepatocellular carcinoma. Cirrhosis cause complex metabolic changes that led to the development of alterations in bone metabolism known as hepatic osteodystrophy (HO). In general deterioration of bone mass and quality are due to multiple factors such as nutritional deficiencies, hypogonadism, use of medications, vitamin D deficiency, chronic inflammation and severity of the disease. The incidence of osteoporosis is twice as high in patients with chronic liver disease compared with the general population. The rates of vertebral and nonvertebral fractures are increased in chronic liver disease, especially in postmenopausal women. The availability of DXA bone densitometry (BMD-DXA) has led to an increase in the diagnosis of osteoporosis and low bone mass (LBM)in patients with liver disease. Moreover, vertebral morphometry (VMP) has a high diagnostic yield of asymptomatic vertebral fractures. This an update of the literature on bone disease in patient with chronic liver disease and recommendations for the management of patients with cirrhosis, focusing on bone health.
Key words: liver cirrhosis; liver transplantation; osteodystrophy; osteoporosis; fracture.
Referencias
1. Crosbie OM, Freaney R, McKenna MJ, Curry MP, Hegarty JE. Predicting bone loss following orthotopic liver transplantation. Gut 1999;44:430-4.
2. Monegal A, Navasa M, Guañabens N, Peris P, Pons F, Mar- tínez MJ, et al. Bone disease after liver transplantation: A long-term prospective study of bone mass changes, hormonal status and histomorphometric characteristics. Osteoporosis Int. 2001;12:484-92.
3. Leidig-Bruckner G, Hosch S, Dodidou P, Ritschel D, Conradt C, Klose C, et al. Frequency and predictors of osteoporotic frac- tures after cardiac or liver transplantation: A follow-up study. Lancet. 2001;357:342-7.
4. Leslie WD, Bernstein CN, Leboff MS; American Gastroentero- logical Association Clinical Practice Commitee. AGA technical review on osteoporosis in hepatic disorders. Gastroenterol- ogy. 2003;125:941-66.
5. Millonig G, Graziadei IW, Eichler D, Pfeiffer KP, Finken- stedt G, Muehllechner P, et al. Alendronate in combination with calcium and vitamin D prevent bone loss after orthoptic liver transplantation: A prospective single-center study. Liver Transpl. 2005;11:960-6.
6. Ninkovic M, Love SA, Tom B, Alexander GJ, Compston JE. High prevalence of osteoporosis in patients with chronic liver disease prior to liver transplantation. Calcif Tissue Int. 2001;69:321-6.
7. García HD, Córdoba N, Marín JI, Restrepo JC. Osteoporosis en pacientes con hepatopatías crónicas: una complicación tar día poco conocida. Rev Colomb Gastroenterol. 2011;26:292- 302.
8. Jeanneret V, Abril D, Vera A, Romero J, González D. Osteoporosis pretransplante hepático en la FSFB. Primer Congreso Multidisciplinario sobre Manejo de Osteoporo- sis. Fundación Santa Fe de Bogotá, Bogotá, D.C., 30 de septiembre de 2011.
9. Janes CH, Dickson ER, Okazaki R, Bonde S, McDonagh AF, Riggs BL. Role of hyperbilirubinemia in the impairment of osteoblast proliferation associated with cholestatic jaundice. J Clin Invest. 1995;95:2581-6.
10. Guañabens N, Parés A. Liver and bone. Arch Biochem Biophys. 2010;503:84-94.
11. American Gastroenterological Association Medical Position Statement: Osteoporosis in hepatic disorders. Gastroenterology. 2003;125:937-40.
12. Luxon B. Bone disorders in chronic liver diseases. Curr Gastro- enterol Rep. 2011;13:40-8. 13. Mendoza-Delgado SA, Velbes-Marquetti PE, Astencio-Rodrí- guez G, Suárez-Navarro E, Santana-Porbén S. La enfermedad metabólica ósea en la cirrosis hepática: la influencia del estado nutricional. Rev Gastroenterol Méx. 2011;76:97-107.
14. Negri AL, Plantalech LC, Russo MF, Otero A, Sarli M. Osteopo- rosis postrasplante. Medicina (Buenos Aires). 1999;59:777-86.
15. Guañabens N, Parés A, Ros I, Caballería L, Pons F, Vidal S, et al. Severity of cholestasis and advanced histological stage but not menopausal status are the major risk factors for osteoporosis in primary biliary cirrhosis. J Hepatol. 2005;42:573-7.
16. Corazza GR, Trevisani F, Di Stefano M, De Notariis S, Veneto G, Cecchetti L, et al. Early increase of bone resorption in patients with liver cirrhosis secondary to viral hepatitis. Dig Dis Sci. 2000;45:1392-9.
17. Tsuneoka K, Tameda Y, Takase K, Nakano T. Osteodystrophy in patients with chronic hepatitis and liver cirrhosis. J Gastro- enterol. 1996;31:669-78.
18. Sinigaglia L, Fargion S, Fracanzani AL, Binelli L, Battafarano N, Varenna M, et al. Bone and joint involvement in genetic hemo- chromatosis: Role of cirrhosis and iron overload. J Rheumatol. 1997;24:1809-13.
19. Kaymakoğlu S, Okten A, Cakaloğlu Y, Boztaş G, Beşişik F, Taşçioğlu C, et al. Hypogonadism is not related to the etiol- ogy of liver cirrhosis. J Gastroenterol. 1995;30:745-50.
20. Diamond T, Stiel D, Posen S. Osteoporosis in hemochromatosis: Iron excess, gonadal deficiency, or other factors? Ann Intern Med. 1989;110:430-6.
21. Voskaridou E, Terpos E. New insights into the pathophysiology and management of osteoporosis in patients with beta thalassae- mia. Br J Haematol. 2004;127:127-39.
22. Cabre E, Gassull MA. Nutritional and metabolic issues in cir- rhosis and liver transplantation. Curr Opin Clin Nutr Metab Care. 2000;3:345-54.
23. Yurgaky JM, Arredondo AM. Osteoporosis asociada a glucocor- ticoides, una aproximación práctica. Rev Fac Med. 2010;18:210- 20.
24. Boling EP. Secondary osteoporosis: Underlying disease and the risk for glucocorticoid-induced osteoporosis. Clin Ther. 2004;26:1-14.
25. Lukert BP, Raisz LG. Glucocorticoid-induced osteoporosis: Pathogenesis and management. Ann Intern Med. 1990;112:352- 64.
26. Defranco DJ, Lian JB, Glowacki J. Differential effects of glu- cocorticoid on recruitment and activity of osteoclasts induced by normal and osteocalcin-deficient bone implanted in rats. Endocrinology. 1992;131:114-21.
27. van Staa TP, Leufkens HG, Abenhaim L, Zhang B, Cooper C. Oral corticosteroids and fracture risk: Relationship to daily and cumulative doses. Rheumatology (Oxford). 2000;39:1383-9.
28. van Staa TP, Leufkens HG, Abenhaim L, Zhang B, Cooper C. Use of oral corticosteroids and risk of fractures. J Bone Miner Res. 2000;15:993-1000.
29 . Ruegsegger P, Medici TC, Anliker M. Corticosteroid induced bone loss. A longitudinal study of alternate day therapy in patients with bronchial asthma using quantitative computed tomography. Eur J Clin Pharrnacol. 1983;25:615-20.
30. Baxter JD. Advances in glucocorticoid therapy. Adv Intern Med. 2000;45:317-49. 31. Cunnane G, Lane NE. Steroid-induced osteoporosis in systemic lupus erythematosus. Rheum Dis Clin North Am. 2000;26:311- 29.
32. Goldstein MF, Fallon JJ Jr, Harning R. Chronic glucocorticoid therapy-induced osteoporosis in patients with obstructive lung disease. Chest. 1999;116:1733-49.
33. Vleggaar FP, van Buuren HR, Wolfhagen FHJ, Schalm SW, Pols HA. Prevention and treatment of osteoporosis in primary biliary cirrhosis. Eur J Gastroenterol Hepatol. 1999;11:617-21.
34. Lim LS, Fink HA, Blackwell T, Taylor BC, Ensrud KE. Loop diuretic use and rates of hip bone loss, and risk of falls and fractures in older women. J Am Geriatr Soc. 2009;57:855-62.
35. Carbone LC, Johnson KC, Bush AJ, Robbins J, Larson JC, Thomas A, et al. Loop diuretic use and fracture in postmeno- pausal women. Findings from the Women’s Health Initiative. Arch Intern Med. 2009;169:132-40.
36. Lim LS, Fink HA, Kuskowski MA, Taylor BC, Schousboe JT, Ensrud KE, et al. Loop diuretic use and increased rates of hip bone loss in older men: The osteoporotic fractures in men study. Arch Intern Med. 2008;168:735-40.
37. Solis-Herruzo JA, Castellano G, Fernández I, Muñoz R, Hawkins F. Decreased bone mineral density after therapy with alpha in- terferon in combination with ribavirin for chronic hepatitis C. J Hepatol. 2000;33:812-7.
38. Trombetti A, Giostra E, Mentha G, Negro F, Rizzoli R. Lack of evidence for ribavirin-induced bone loss. Hepatology. 2002;36:255-7.
39. Mobarhan SA, Russell RM, Recker RR, Posner DB, Iber FL, Miller P. Metabolic bone disease in alcoholic cirrhosis: A com- parison of the effect of vitamin D2, 25-hydroxyvitamin D, or supportive treatment. Hepatology. 1984;4:266-73.
40. Crawford BA, Labio ED, Strasser SI, McGaughan GW. Vitamin D replacement for cirrhosis-related bone disease. Nat Clin Pract Gastroenterol Hepatol. 2006;3:689-99.
41. Arnaud SB. 25-hydroxyvitamin D3 treatment of bone disease in primary biliary cirrhosis. Gastroenterology. 1982;83:137-40.
42. Wolfhagen FH, van Buuren HR, Vleggaar FP, Schalm SW. Management of osteoporosis in primary biliary cirrhosis. Bail- lieres Best Pratt Res Clin Gastroenterol. 2000;14:629-41.
Correspondencia: Deyanira González, MD
Correo electrónico: deyaniragonzalezdevia@yahoo.com; v.jeanneret59@uniandes.edu.co
Bogotá, D.C., Colombia.
