La linfocintigrafía y en especial la detección y extracción del o los ganglios centinelas (cirugía radioinmunoguiada) mediante el rastreo de partículas radiomarcadas ha sido uno de los grandes y recientes avances de la oncología quirúrgica moderna. El desarrollo de esta tecnología ha permitido la difusión de esta técnica quirúrgica y diagnóstica; en Estados Unidos hoy en día se puede aplicar a más de 375.000 pacientes afectados por diferentes tipos de cáncer, entre los que se destacan el mamario y el melanoma (18-20).
El conocimiento del comportamiento de los radiofármacos y la consolidación de los resultados de la aplicación de la cirugía radioinmunoguiada son las bases para permitir la expansión de la aplicación de esta tecnología en el tratamiento de otras enfermedades o situaciones clínicas en las que se requiere de diagnósticos más precisos (6, 19, 20).
Para tener un mejor entendimiento de la física radiobiológica y nuclear aplicada a la medicina y en especial lo concerniente a esta investigación, describe la siguiente terminología básica.
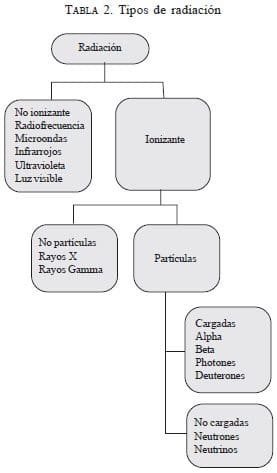
Radiación es un término que en general describe la propagación externa o superficial de energía en cualquiera de sus amplias variedades de formas.
Ionizante se refiere a la intensidad de alta energía que permite desplazar los electrones del átomo. La radiación ionizante se subdivide en sin partículas y con partículas. La radiación sin partículas o fotones son los rayos x y gamma; éstos se distinguen mediante la vía en que son formados y una vez han sido emitidos son indistinguibles. Los rayos gamma y las otras partículas formadas por radiación ionizante son creados cuando el núcleo es sometido a un estado de transición de alta a baja energía. Los rayos x de alta energía y los rayos gamma penetran el cuerpo y pueden ser detectados fuera de éste por lo que pueden ser útiles para el diagnóstico, a diferencia de la radiación con partículas cargadas (rayos alfa y beta) que a una dosis equivalente no penetran bien el cuerpo y causan mayor daño tisular biológico; son más adecuadas para el tratamiento y no así para imágenes diagnósticas (tabla 2) (6).
La cantidad de actividad de un radionucleótido se expresa en términos del número de átomos que se desintegran por unidad de tiempo (segundos).
En Estados Unidos la unidad utilizada es el Curie (3,7x 10 desintegraciones/segundo) y equivale al número de átomos desintegrados por segundo en un gramo de radium. En el sistema internacional la unidad equivalente es el Becquerel (1,0 desintegraciones/ segundo). Para estudios diagnósticos se utiliza el milicurie (1 curie = 1000 mCi) (6).
El potencial efecto deletéreo de la radiación está relacionado con la cantidad de energía que se deposita desde la fuente de radiación por gramo de tejido afectado. La unidad que expresa este fenómeno es el rad (1 erg/g de tejido), en el sistema internacional la unidad correspondiente es el gray (1 gray = 100 rad). Algunos tipos de radiación son más lesivos que otros, independiente de la misma cantidad de energía depositada. Por ejemplo, los rayos alfa son 20 veces más lesivos que los rayos gamma. La unidad que determina el efecto biológico de la radiación es el rem (1 rem = 1000 milirems), en el sistema internacional la unidad equivalente es el sievert (1 sievert = 100 rem) (6).
El promedio de exposición a radiación proveniente de fuentes naturales (aire, tierra, alimentos, etc.) para la población en general es de 300 mrem por año y el límite de exposición ocupacional es de 500 mrem por año. La dosis total calculada de depósito para el estudio fue de 1,45 mrem, garantizando la seguridad biológica del personal comprometido en el estudio.
El radionucleótido seleccionado para el estudio fue el Tecnecio 99. Esta partícula es ideal por emitir sólo rayos gamma, por tener una vida media corta de sólo 6 horas con lo que la exposición a la radiación del personal y los animales es baja y tener un pico de energía máximo constante de 140 keV. El Tecnecio 99 una vez administrado por vía oral queda confinado al tracto gastrointestinal sin presentar absorción sistémica ni eliminación renal, esta propiedad se puede incrementar al combinarlo con partículas pesadas de sulfuro coloidal > 100 nm que impiden la penetración por los microcapilares sanguíneos y linfáticos.
Una gran variedad de instrumentos se utilizan para detectar los rayos gamma: detectores de gas (cámaras de ionización, contadores Geiger-Mueller), centelleografía orgánica líquida, detectores sólidos.
Las sondas gamma intraoperatorias utilizan detectores sólidos. La energía de los rayos gamma al interactuar con los cristales es convertida en un destello de luz (excintilación) que es convertido en un pulso eléctrico por un tubo fotomultiplicador acoplado óptimamente al cristal. La intensidad de la excintilación y el subsiguiente tamaño del pulso eléctrico son proporcionales a la energía del fotón detectado.
Los dos cristales principalmente utilizados son el de Nal que a un tamaño de 9,5 mm absorbe 85% de 140 KeV de fotones de Tecnecio 99, y el de CdTe que a un tamaño de 2 mm absorbe 60%. La sonda gamma empleada en el estudio está automáticamente calibrada a 140 KeV para Tecnecio 99, utilizando un cristal de Nal con un colimador corto de 14 mm.
La lectura de los valores que emite el contador de la sonda gamma en esta técnica en particular para detectar perforación gastrointestinal, se debe interpretar de manera diferente a la realizada al efectuar estudios de ganglio centinela de tumores mamarios o melanoma o cirugía radioinmunoguiada de paratiroides, en los que se debe considerar los gradientes de valor de la radiación entre el lugar primario de inyección o aplicación y la captación del radiofármaco por el ganglio centinela, o el tumor en la paratiroides que se está buscando debido a la difusión hemática o linfática que presenta la sustancia (21-23). La detección del radiofármaco libre en el líquido peritoneal, así sea en valores mínimos pero superiores a cero, sólo se puede dar si hay disrupción del tracto gastrointestinal por donde transita el radioisótopo marcado. La interpretación del valor es más fácil al considerar valores absolutos como positivos cualquier valor superior a cero. En nuestro estudio el valor promedio fue de 467, valor que se detecta con claridad y sin lugar a dudas en el contador de la sonda gamma.
Conclusiones
Los resultados de este estudio experimental prospectivo y aleatorizado permiten concluir:
1. En el modelo animal el análisis del líquido peritoneal extraído mediante lavado, una vez se ha administrado una solución marcada con Tecnecio 99 sulfuro coloidal por vía oral es 100% sensible y específico para diagnosticar disrupción del tracto gastrointestinal (estómago), con fuga de líquido libre a la cavidad peritoneal.
2. Como las partículas marcadas con Tecnecio 99 pesado una vez instaladas en el tracto gastrointestinal, no tienen absorción hemática ni eliminación renal, el valor para considerar como positivo en el líquido peritoneal en el rastreo con la sonda gamma basta con que sea mayor a 0, sin necesidad de realizar gradientes lo que facilita su interpretación únicamente con dos opciones: negativo: 0, positivo: > 0.
Aplicabilidad
· Este experimento abre las fronteras a una nueva aplicación de la cirugía radioinmunoguiada. Queda en perspectiva una prueba diagnóstica 100% sensible y específica para detectar la disrupción o solución de continuidad del tracto gastrointestinal, con la subsiguiente fuga de los líquidos corporales en la cavidad abdominal.
· El campo de aplicación de esta técnica sería en múltiples escenarios de la patología crítica gastrointestinal tales como:
a) Postoperatorios con diagnóstico incierto de fuga de anastomosis, en los cuales solamente bastaría con tomar una pequeña muestra del líquido que sale por el drenaje testigo o análisis del líquido peritoneal mediante un lavado mínimo.
b) Trauma cerrado y penetrante de abdomen con deterioro neurológico o bajo sedación por soporte con ventilador mecánico, en el que se encuentra o no líquido libre peritoneal y en el que es necesario descartar perforación de víscera hueca.
c) Pacientes inmunosuprimidos o críticamente enfermos (sida, enteritis neutropénicas, trasplantados, dosis máximas de esteroides, toxicidad por quimioterapia, paludismo, fiebre tifoidea, etc.), en los que es necesario una prueba diagnóstica muy sensible y específica para descartar perforación gastrointestinal, dado que su condición general no permite un procedimiento quirúrgico en blanco o un diagnóstico tardío.
d) Todos los anteriores escenarios con una prueba fácil de hacer, en la que no hay que movilizar el paciente de la cama ni de la unidad de cuidados intensivos, que no requiere de preparación y no tiene contraindicaciones ni efectos secundarios.
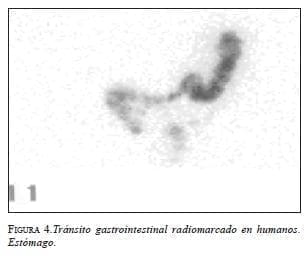
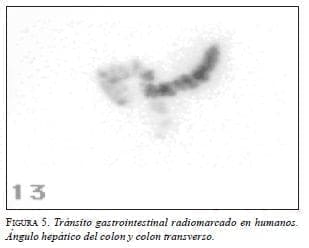
Existe suficiente evidencia que la biodisponibilidad y distribución orgánica de las partículas radiomarcadas es similar en los mamíferos; por tal motivo, en teoría este modelo diagnóstico puede ser aplicable 100% a los humanos. Esta apreciación estimuló al grupo de estudio a realizar la siguiente fase de experimentación en humanos. Inicialmente comprobamos que la administración por vía oral de la misma cantidad del radiofármaco tiene tránsito gastrointestinal exclusivo sin presentar absorción hemática o eliminación renal e inclusive con un delineamiento anatómico muy preciso de las estructuras anatómicas gastrointestinales; es posible visualizar la fuga de la sustancia radiactiva a la cavidad peritoneal (figuras 4 y 5). El análisis futuro de esta técnica para detectar disrupción del tracto gastrointestinal aplicada en humanos de ser exitosa sería un gran avance diagnóstico para unas condiciones médicas muy críticas, que en la actualidad cobran muchas vidas.
 |
 |
Abstract
This study had the purpose of evaluating the sensibility and specificity of the radiommunoguided-detection of erforations of the gastrointestinal tract utilizing Tenecium 99.
The design was a prospective, experimental triple blinded study, with an estimation of the size of the sample considering a 95% sensitivity and specificity, an alpha error of 0.05, and a precision of 0.05. There was an initial evaluation in four New Zealand rabbits in order to determine: type of anesthesia and doses, capacity of the stomach (ml), average time interval of intestinal transit, abdominal cavity capacity (ml) and the distribution of the radio material (intestinal absorption, blood dissemination and distribution, and renal excretion). Forty New Zealand rabbits were utilized for analysis in three independent work stations, randomizing 20 rabbits to each study group (perforated and nonperforated). The radio material was colloidal sulphur labeled with Tecnecium 99, >100 nm, 2.5 mCi, a 140 Kev energy prepared in 0.9% saline solution, which provided a concentration of 0.0025 mCi per ml. Scan was done with gamma 10X probe. Statistical analysis was done with the Episet V:1 and the chi square test.
All rabbits with disruption of the stomach exhibited positive radiaton activity in the peritoneal fluid, analyzing an average value of 467 and a rank of 37 to 1748. In the remaining rabbits with no perforation of the gastric wall the scan was negative.
The sensitivity of this diagnostic method was 0.98 and the specificity 0.98, with a confidence interval of 0.92- 1.0. Comparative gamma probe analysis of the peritoneal fluid in the two groups gave 37 chi square with a p<0.001.
This study concluded that the in the experimental model the diagnostic method has high sensitivity and specificity in the detection of perforations of the gastrointestinal tract.
Key words: intestinal fistula, radioimmunodetection, radiosurgery, radioisotopes
Referencias
1. WISNER DH, CHUN Y, BLAISDELL FW. Blunt intestinal injury; keys to diagnosis and management. Arch surg 1990; 125: 1319-1322.
2. KAIFE F, TOMINAGA GT, YOONG B, WAXMAN K. Factors related to outcome in blunt intestinal injuries requiring operation. Am Surg 1997; 63: 889-892.
3. GRASSI R, ROMANO S, PINTO A, ROMANO L. Gastroduodenal perforations: conventional plain film, US and CT findings in 166 consecutive patients. Eur J Radiol 2004; 50 (1): 30-36.
4. POLETTI PA, KINKEL K, VERMEULEN S, IRMAY F, UNGER PF, TERRIER F. Blunt abdominal trauma: should US be used to detect both free fluid and organ injuries? Radiology 2003; 227 (1): 95-103.
5. MIZRAHI M, MINTZ Y, RIVKIND A, KISSELGOFF D, LIBSON E, BREZIS M, GOLDIN E, et al. A prospective study assessing the efficacy of abdominal computed tomography scan without bowel preparation in diagnosing intestinal wall and luminal lesions in patients presenting to the emergency room with abdominal complaints. World J Gastroenterol 2005; 7 (11); 1981-1986.
6. HILLIER DA, ROYAL HD. Intraoperative gamma radiation detection and radiation safety. In: Whitman ED, Reintgen D. Radioguided surgery. Austin, Texas. Landes Bioscience, 1999; 2-37.
7. HARDING LK, MOSTAZA AB, RODEN L, WILLIAMS N. Dose rates from patients having nuclear medicine investigations. Nucl Med Commun 1985; 6: 191-194.
8. OLIVEROS HR. Tipos de diseño en investigación biomédica. Manual de investigación clínica. Editorial Nomos S.A. Bogotá; Colombia 2004; 2.3: 39-49.
9. CUMMINGS SR. Designing clinical research. An epidemiologic approach. 2nd ed. Lippincott Williams & Wilkins; January, 2001.
10. OLIVEROS HR. Episet v:1.0. Asociación Colombiana de Medicina Crítica y Cuidado Intensivo. Bogotá, Colombia, 2004.
11. THOMPSON WM. Diagnostic imaging and interventional techniques in reoperations in general surgery. In: McQuarrie DG, Humphrey EW. Reoperative general surgery. San Louis. Mosby Year Book 1992; 3: 21-111.
12. SKUKAS J. Anaphylactoid reactions with gastrointestinal contrast media. AJR Am J Roentgenol 1997; 168 (4): 962-964.
13. JANSEN JO, LOGIC JR. Diagnostic peritoneal lavage – an obituary. Br J Surg 2005; 92 (5): 517-518.
14. DROST TF, ROSEMURGY AS, KEARNEY RE, ROBERTS P. Diagnostic eritoneal lavage. Limited indications due to evolving concepts in trauma care. Am Surg 1991; (57): 126-128.
15. MORALES CH. Laparoscopia en el paciente crítico. En: Ordóñez CA, Ferrada R, Buitrago R. Cuidado intensivo y trauma. Distribuna Ltda. Bogotá 2002; 56: 807-812.
16. ROSIN D, ZMORA O, KHAIKIN M, BAR ZAKAI B, AYALON A, SHABTAI M. Laparoscopic management of surgical complications after a recent laparotomy. Surg Endosc 2002; 18 (6): 994-996.
17. KAISER AM, KATKHOUDA N. Laparoscopic management to the perforated viscus. Semin Laparosc surg 2002; 9 (1): 46-53.
18. HADDAD FF, SHIVERS SC, REINTGEN DS. Historical perspectives and future applications. Surg Oncol Clin N Am 1999; 8 (3): 391- 400.
19. SORENSON JA, PHELPS ME. Physics in nuclear medicine. 2nd ed. Philadelphia, WB Saunders, 1987.
20. REINTGEN DOUGLAS S. Radioguide surgery. The changing face of general surgery and surgical oncology. Surg Clin North Am 1999; 8, N° 3.
21. COX CE, WHITE L, STOWELL N, CLARK J, DICKSON D, FURMAN B, WEINBERG E, et al. Clinical considerations in breast cancer sentinel lymph node maping: a moffit review. Breast Cancer 2004; 11 (3): 225-232; discussion 264-266.
22. REINTGEN D, PENDAS S, JAKUB T, SWAR G, GIULIANO R, BAUER J, CASSALL R, et al. National trials involving lymphatic mapping for melanoma: The multicenter selective lymphadenectomy trial. The sunbelt melanoma trial, and the Florida melanoma trial. Semin Oncol 2004; 31 (3): 363-373.
23. NORMAN J. The technique of intraoperative nuclear mapping to facilitate minimally invasive parathyroidectomy. Cancer Control 1997; 4: 500-504.
Correpondencia:
WILLIAM SÁNCHEZ MALDONADO, MD
globalre@cable.net.co
Bogotá, D.C.

