SIMÓN OVALLES*, DANIK ÁLVAREZ**, JAVIER FORERO***
Resumen
La interpretación de la fisiología ácido-base ha sido revolucionada por la aproximación cuantitativa de Stewart, a veces llamada “de los iones fuertes”. Presentamos el caso clínico de una paciente con acidosis dilucional, entidad con muy pocos informes en la literatura. También discutimos los conceptos más generales de dicha aproximación.
Introducción
Tanto los cirujanos, como los anestesiólogos e intensivistas frecuentemente se enfrentan a pacientes que luego de intervenciones quirúrgicas prolongadas, generalmente de más de 4 horas de duración y que requieren soporte circulatorio con gran cantidad de cristaloides, presentan acidosis metabólica persistente que representa no sólo un reto diagnóstico sino terapéutico.
El desarrollo de acidosis metabólica intraoperatoria suele ser atribuido a hipovolemia, hipoperfusión tisular, hipoxemia celular y desarrollo de acidosis láctica; el tratamiento se fundamenta en maximizar la perfusión tisular mediante la infusión de volumen e inotrópicos1.
Una posibilidad pocas veces explorada, es la mal llamada acidosis dilucional. La diferenciación entre estas dos etiologías tiene marcadas implicaciones en la definición de la conducta a seguir. Una hipoperfusión tisular se trata con volumen infundido en forma liberal según las necesidades del paciente, mientras que la acidosis dilucional se trata moderando o restringiendo la tasa de infusión de solución salina normal (SSN) y/o modificando la composición del fluido infundido2.
La malinterpretación de una acidosis como secundaria a hipoperfusión tisular puede llevar a sobrehidratación de pacientes luego de procedimientos quirúrgicos mayores. Esto conlleva el riesgo, en este caso innecesario, de formación de edema tisular, reflejado en significativa ganancia de peso, el cual se ha asociado a deterioro en la cicatrización de heridas, prolongación de la necesidad de soporte respiratorio y estancia en unidad de cuidad intensivo (UCI)3. Este edema tisular también puede alterar el flujo sanguíneo microvascular por compresión de capilares, deteriorando la oxigenación tisular y pudiendo de esta forma contribuir al desarrollo del síndrome de disfunción orgánica múltiple (SDOM)3. Lowell et al4 reportaron que 40 % de los pacientes admitidos a una UCI quirúrgica presentaba ganancia de 10 % del peso corporal secundaria a la administración de fluidos y que esta variable se correlaciona con la estancia.
La primera descripción de la entidad fue hecha por Peters y Van Slyke en 19312. Al parecer, el trabajo publicado por Shires y Holman en 1948 en Annals of Internal Medicine popularizó el término acidosis dilucional5. Clásicamente5-8 se ha interpretado como secundaria a la expansión de volumen después de la administración de grandes cantidades de SSN, lo cual produciría dilución (de ahí su nombre) del bicarbonato plasmático (HCO-3) y pérdida renal del mismo por incremento del volumen filtrado, que se mueve a través de los túbulos proximales, sitio primario de reabsorción del HCO3; la alta carga de sodio en el filtrado interferiría con la reabsorción del HCO3, perdiéndose de esta forma y llevando a bicarbonaturia y acidosis.
Esta hipótesis fisiopatogénica fue retada por Mathes et al9 y más recientemente por Waters et al1: los primeros informaron un caso de acidosis dilucional intraoperatoria en el contexto de normovolemia, y los segundos, 12 casos en que demostraron mediante la medición del volumen plasmático, con la técnica de dilución del azul de Evans, que el incremento en el volumen plasmático no ocurrió y que no era condición sine qua non para su desarrollo, por lo cual la explicación mediante el mecanismo postulado era incompleta y la respuesta tenía que buscarse en otra parte. Esta respuesta intentaremos dilucidarla en la discusión.
Gómez y cols10 reportan una paciente con trauma craneano severo atendida en la UCI del Hospital San Juan de Dios de Bogotá, en quien se pudo documentar acidosis dilucional secundaria a infusión masiva de SSN, la cual revirtió al modificar el líquido infundido a lactato de Ringer.
muy pocos casos han sido reportados en la literatura1,9,11-13.
Describimos el caso de una paciente quirúrgica con acidosis dilucional tratada en la UCI de la Clínica San Pedro Claver del Instituto del Seguro social (ISS), Bogotá, Colombia.
Presentacion del Caso
Historia clínica número 20173358. Paciente de sexo femenino, de 88 años, quien presenta fractura intertrocantérica de cadera derecha luego de caída desde su propia altura; como antecedentes de base, osteoporosis y neumopatía por humo de leña. Manejada inicialmente con tracción cutánea, es llevada a cirugía 5 días después y se le practica hemiartroplastia tipo bipolar bajo anestesia general. En el postoperatorio inmediato presenta insuficiencia respiratoria aguda requiriendo intubación orotraqueal con radiografía sugestivas de edema pulmonar; además, desarrolla taquicardia supraventricular (TSV) que no cede a la digital ni a antagonistas de calcio requiriendo infusión de amiodarona; los electrolitos séricos muestran sodio 146 mEq/L y potasio 3,2 mEq/L.
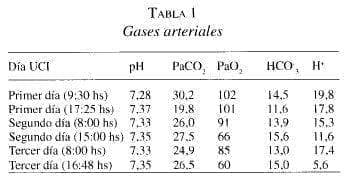
Ingresa a la UCI bajo soporte de adrenalina 0,2 mcg/Kg/min y dopamina 4 mcg/Kg/min, recibiendo transfusión de 2 unidades de GRE, con TA 139/65, FC 131, PVC 16, palidez, ingurgitación yugular, ruidos cardíacos rítmicos, roncos bibasales, abdomen blando, no distendido, peristalsis audible, herida quirúrgica en la cara lateral del muslo derecho, equimosis en periné y región inguinal derecha, cuadro neurológico sin alteraciones. Los gases arteriales de ese día mostraban pH 7,28, PaCO2 30,2, PaO2 102, HCO3 14,5, H+ 19,8. Se considera cuadro de edema pulmonar, procediéndose a restringir aporte de líquidos endovenosos (LEV), se mantiene el apoyo inotrópico y se inicia diurético. el día siguiente la paciente presenta mejoría, con resolución progresiva de los signos clínicos de edema pulmonar y adecuados parámetros de oxigenación. A las 36 horas de su ingreso a la UCI, la paciente mostraba franca mejoría clínica y se había iniciado el retiro de la ventilación mecánica, pero llamaba la atención la persistencia de acidosis metabólica: pH 7,33, PaCO2 24,9, PaO2 85, HCO3 13, H+ 17,4. Los electrolitos tomados previos a la gasimetría, reportaron cloro de 122, con sodio de 141,1 y potasio de 4,2, lo cual daba un valor de diferencia de iones fuertes (DIF) de 22,7. Al revisar los balances de líquidos administrados y eliminados previos al ingreso UCI, incluyendo el record anestésico, se obtuvo el dato de un balance positivo de 9523 ml a costa del aporte de SSN, sin contar la cantidad de SSN recibida durante su estancia en el servicio de urgencias (5 días), sobre lo cual no se encontró precisión en la historia clínica. Dado lo anterior y la DIF obtenida, se procedió a cambiar el aporte de líquidos a lactato Ringer. Los gases de control tomados 9 horas luego de esta medida, mostraron una disminución de los H+ a 5,6 y los nuevos electrolitos reportaron valores de cloro de 111,2, sodio 140,5 y potasio 4,1. La paciente siguió su curso favorable, toleró la extubación, mantuvo estabilidad hemodinámica, balances de líquidos negativos, adecuada diuresis y resolución de la acidosis metabólica. En la tarde del día siguiente fue trasladada a piso. Su último valor de cloro tomado en UCI fue 108,1.
Las tablas 1 y 2 muestran la evolución en el tiempo de los gases arteriales, electrolitos y la DIF.
 |
 |
Discusión
Existen por lo menos cuatro aproximaciones a la fisiología ácido-base: (1) la base exceso (BE), introducida por Siggaard-Andersen y Astrup, la llamada escuela de Copenhagen, a mediados de los años 5014; (2) la del bicarbonato, descrita por Schwartz, Brackett y cols, la llamada escuela de Boston15,16; (3) la brecha aniónica (aniongap) (AG), derivada de Oh y Carroll11,26 en 1978 Narins y Emmet en 198017; y (4) la cuantitativa de Stewart. Las dos primeras estaban ligadas de manera directa a la ecuación de Henderson-Hasselbalch, remontándose a Sorenson quien en 1909 introdujo el concepto de pH18. La aproximación de Stewart, publicada en 198119 y 198320 por dicho autor, teniendo como precursor el trabajo de Singer y Hastings14,21 hacia 1948 sobre la base buffer, vendría a ser la teoría heliocéntrica respecto al pasado geocéntrico en la interpretación de la fisiología ácido-base, lo cual aún motiva debate.
Stewart plantea que las variaciones en la concentración de hidrogeniones [H+] son determinadas por la disociación del agua en iones H+ y OH-; las soluciones biológicas humanas contienen todas agua, por lo cual son fuente permanente de H+; la disociación del agua está determinada por las leyes de la física-química de la electroneutralidad (en una solución acuosa la suma de todos los iones cargados positivamente debe ser igual a la suma de todos los iones cargados negativamente) y la conservación de masa (la cantidad de una sustancia permanece constante a menos que sea adicionada o generada, removida o destruida). Mientras en el agua pura la [H+] debe ser igual a la [OH-], en soluciones más complejas como la sangre se deben considerar otros determinantes de la disociación del agua; pero aun así, la fuente de H+ sigue siendo el agua. Dichos determinantes son tres: la diferencia de iones fuertes (DIF), la pCO2 y la concentración de ácidos débiles (principalmente proteínas y fosfatos). Sólo esas tres variables son importantes y son independientes; la [H+] y el [HCO3] son variables dependientes que sólo cambian si lo hacen las primeras22.
De las variables independientes, la DIF es la más importante en cuanto a las influencias metabólicas que regulan la [H+] y el pH de los fluidos corporales. Ión “fuerte” es el que está casi o totalmente disociado y no presenta reactividad química23. La DIF sería:
[Na+ + K+ + Ca2+ + Mg2+] – [Cl- + otros aniones fuertes no medidos]
Ni los H+ ni el HCO-3 son iones fuertes; por la magnitud de su contribución y propósitos prácticos, y dado que el Ca2+ y Mg2+ se ligan de forma reversible a la albúmina, la ecuación se reduciría a:
[Na+ + K+] – [Cl-] 14
La DIF simplemente es la diferencia entre los cationes fuertes y los aniones fuertes; estando su valor en las personas sanas en el rango de 40-42 mEq/L, mientras que en los pacientes críticos promedia un valor de 30 mEq/L22. Para satisfacer la ley de la electroneutralidad, cualquier diferencia en los iones fuertes debe ser balanceada por [H+] o [OH-]. Una disminución en la DIF lleva a mayor disociación del agua y una disminución en la [OH-] y acidosis, un incremento en la DIF lleva a menor disociación del agua y un incremento en la [OH-] y alcalosis1.
Una acidosis metabólica (pH < 7,35 con PaCO2 < 40) requiere en su evaluación la medición de [Na+] y [Cl-]. Si se acompaña de [Na+] bajo, la administración de bicarbonato de sodio (NaHCO3) podrá ser efectiva, recalcando que es el componente de sodio lo que se manipula y trata de influenciar y no el bicarbonato, el cual no es una variable independiente; si el [Na+] es alto, entonces no hay lugar para el NaHCO3, y en tal circunstancia debe pensarse otras opciones, como las terapias de reemplazo renal buscando remover más cloro en relación al sodio. Si la acidosis se origina en otras fuentes (p ej., cuerpos cetónicos, lactato) se debe dar tratamiento específico a la causa que la origina (p ej. insulina, reanimación)22.
Mientras la osmorregulación se mantenga, la concentración de sodio no varía marcadamente; igual sucede con el potasio, magnesio y calcio, de manera tal que los cambios en los cationes no contribuyen sustancialmente a los cambios en el pH; por el contrario, el cloro puede variar sustancialmente, al igual que otros aniones “no medidos” como el lactato, cuerpos cetónicos, fosfato, sulfato o sustancias exógenas tipo salicilatos2.
Cuando grandes cantidades de SSN son administradas, y retomando lo dicho arriba, se deduce que la carga administrada de cloro respecto al sodio aumentará su concentración en forma considerable, llevando a una disminución en la DIF, mayor disociación del agua y disminución de la [OH-] para mantener la electroneutralidad dado el aumento en el [Cl-]; todo esto trae como consecuencia la génesis de acidosis2.
Dentro de lo que disponemos, el lactato Ringer sería una alternativa de manejo; basado en su contenido (Na+ 130, K+ 4, Cl- 109), su DIF de 25 es más cercana a la DIF normal en comparación con la SSN, cuyo contenido (Na+ 154, Cl- 154) origina una DIF de 0. Con su uso, disminuiríamos el aporte de cloro llevando la DIF a la normalización progresiva y corrección de la acidosis22.
Si asumimos como válido todo el racionamiento anterior, se entendería de manera plausible y lógica el tratamiento de la alcalosis metabólica con SSN, siendo lo influenciado el incremento de la [Cl-] relativa a la de [Na+], explicación que nunca ha sido del todo satisfactoria con la aproximación clásica a la fisiología ácido-base. Este enfoque, mediante la BE, para sus cálculos asume condiciones de electrolitos, agua y proteínas dentro de rango normal24, lo cual no es lo común en los pacientes en estado crítico y mediante la brecha amónica AG para sus cálculos no asume los cambios en la pCO2 y albúmina; p ej., una disminución de la albúmina de 1 g/dl decrece la BE en 3,7 mEq/L25 y la brecha aniónica en 2,75 mEq/L26; del mismo modo, una pCO2 alta puede resultar en una brecha aniónica falsamente baja.
El modelo matemático de Stewart es mecanicista respecto a la aproximación fenomenológica del punto de vista tradicional y parece superar muchas de las deficiencias y falta de respuestas de este último. Basándose en los trabajos de Stewart, Fencl y Leith y Gilfix y cols27, se desarrollaron nuevas ecuaciones para corregir la BE según cambios en el sodio, cloro, y albúmina.
Conclusión
Se debe entender que todas las acidosis no son de origen hipovolémico e hipoperfusión, lo cual conlleva un uso más racional del apoyo con líquidos parenterales; la medición del cloro ayuda a definir dicha conducta y a evitar la iatrogenia, si se identifica la hipercloremia como la causa de la acidosis.
Abstract
The interpretation of acid-base physiology has been revolutionized by the quantitative Stewart approach, also know as the “strong ion” theory. We report the case of a patient with dilutional acidosis, an entity that rarely appears in the literature; we also discuss the more general concepts regarding the Stewart approach.
Referencias
1. Waters J, Miller L, Clack S, et al. Cause of metabolic acidosis in prolonged surgery. Crit Care Med 1999; 27: 2142-2146
2. Hamill-Ruth Robin. Dilutional acidosis: A matter of perspective. Crit Care Med 1999; 27: 2296-2297
3. Haljamäe H, Lindgren S. Fluid Therapy: Present controversies. En: Vincent JL, ed. Yearbook of Intensive Care and Emergency Medicine. Berlín, Springer; 2000: 429-442
4. Lowell JA, Schifferdecker C, Driscoll DF, et al. Postoperative fluid overload: Not a benign problem. Crit Care Med 1990;18: 728-733
5. Shires GT, Holman J. Dilutional acidosis. Ann Intern Med 1948; 28: 557-559
6. Hebert CS, Martinez-Maldonado M, Eknoyan G, et al. Relation of bicarbonate to sodium reabsortion in dog kidney. Am J Physiol 1972; 222: 1014-1020
7. Garella S, Chang BS, Kahn SI. Dilutional acidosis and contraction alkalosis: Review of a concept. Kidney Int 1975; 8: 279-283
8. Emmett M, Alpern RJ, Seldin DW. Metabolic acidosis. En: The Kidney, Vol 80.Seldin DW, Giebisch G (Eds). New York, Raven Press; 1992: 2820-2821
9. Mathes DD, Morell RC, Rohr MS. Dilutional acidosis: Is it a real clinical entity? Anesthesiology 1997; 86: 501-503
10. Gómez A, Fernández G, Gutiérrez A y col. Acidosis dilucional, a propósito de una paciente tratada en el Hospital San Juan de Dios de Santa Fe de Bogotá. Rev Fac Med UN Col 1999; 47: 146-150
11. Oh MS, Carroll HJ, Goldstein DA, et al. Hyperchloremic acidosis during the recovery phase of diabetic ketosis. Ann Intern Med 1978; 89: 925-927
12. Goodkin DA, Raja RM, Saven A. Dilutional acidosis. South Med J 1990; 83: 354-355
13. Jaber BL, Madias NE. Marked dilutional acidosis complicating management of right ventricular myocardial infarction. Am J Kidney Dis 1997; 30: 561-567
14. Schlichtig R, Grogono A, Severinghaus J. Current status of acid-base quantitation in physiology and medicine. Anesthesiol Clin North Am 1998; 16: 211-233
15. Schwartz WB, Relman AS. A critique of the parameters used in evaluation of acid-base disorders. N Engl J Med 1963; 268: 1382-1388
16. Brackett NC, Cohen JJ, Schwartz WB. Carbon dioxide titration curve in normal man. Effect of increasing degrees of acute hypercapnia on acid-base equilibrium. N Engl J Med 1965; 272: 6-12
17. Narins RG, Emmett M. Simple and mixed acid-base disorders: A practical approach. Medicine 1980; 59: 161-187
18. Kirby R, Bernards W. Acid-base chemistry and physiology. En: Civetta J, Taylor R, Kirby R (eds). Critical Care. Philadelphia, Lippincott-Raven; Third ed 3; 1997: 255-264
19. Stewart PA. How to understand acid-base. En: Stewart PA (ed). A quantitative acid-base primer for biology and medicine. Elsevier, New York; 1981: 1-286
20. Stewart PA. Modern quantitative acid-base chemistry. Can J Physiol Pharmacol 1983; 61: 1444-1461
21. Singer RB, Hastings AB. An improved clinical method for the estimation of disturbances of the acid-base balance of human blood. Medicine 1948; 27: 223-242
22. Kellum JA. Recent advances in acid-base physiology applied to critical care. En: Vincent JL, ed. Yearbook of Intensive Care and Emergency Medicine. Berlín, Springer; 1998: 577-587
23. Fencl V, Jabor A, Kazda A, et al. Diagnosis of metabolic acid-base disturbances in critically ill patients. Am J Respir Crit Care Med 2000; 162: 2246-2251
24. Zaritsky A. Unmeasured anions, deja vu all over again? Crit Care Med 1999; 27: 1672-1673
25. McAuliffe JJ, Lind LJ, Leith DE, et al. Hypoproteinemic alkalosis. Am J Med 1986; 81: 86-90
26. Oh MS, Carroll HJ. The anion gap. N Engl J Med 1977; 297: 814-817
27. Balasubramanyan N, Havens P, Hoffman G. Unmeasured anions identified by the Fencl-Stewart method predict mortality better than base excess, anion gap, and lactate in patients in the pediatric intensive care unit. Crit Care Med 1999; 27: 1577-1581
Correspondencia:
Simón Ovalles
Calle 86 103C-49 int. 3, apto. 202
Tel.: 228 47 66
recabarre@hotmail.com
* SIM(lNOVALU,S:Unidad de Cuidado Intensivo. Clínica San Pedro Clavero Instituto del Seguro Social (ISS). Docente Adscrito, Universidad Nacional de Colomhia.
** OANIKÁLVARHZ:Residente 11I año, Anestesiología, Fundación Universitaria San Martín.
*** JAVIHRFORI’Ro: Residente I año, Cirugía General, Fundación Universitaria San Martín.
