Sujetos
Se estudiaron dos poblaciones provenientes de la Ciudad de México, constituidas por 138 individuos adultos y 87 cordones umbilicales provenientes de madres atendidas en hospitales de asistencia pública del gobierno federal.
Todos los individuos estudiados son descendientes de Mexicanos al igual que sus padres y abuelos quienes negaron tener ancestros en Europa, África o países Asiáticos. La sangre se coleccionó en tubos con EDTA al 2% y el DNA genómico se extrajo mediante la técnica de expulsión salina (Miller, 1998).
Tipificación de alelos de genes HLA.
Amplificación de ADN genómico
Las regiones HLA-DQA1 y HLA–DQB1 se amplificaron mediante la técnica de reacción de polimerasa en cadena (PCR), los productos se hibridaron con sondas de oligonucléotidos específicos de secuencia. Los iniciadores utilizados para el locus HLA-DQ se sintetizaron en un equipo automático DNA-SM (Beckman, Palo Alto, CA, USA). Los protocolos utilizados siguen lineamientos aprobados durante el Décimo Segundo Taller Internacional de Histocompatibilidad.
Hibridación mediante la técnica de Dot blot
Cinco por ciento del amplificado de DNA se desnaturalizó en hidróxido de sodio 0.4 mol/L durante 10 min, se neutralizó en acetato de amonio 1 mol/L y se transfirió a membranas de nylon tipo Hybond-N (Amersham, Bucks, UK). Los filtros se prehibridaron a 42°C durante 30 min en una solución que contiene 6× SSPE (30× SSPE: 4.5 mol/L NaCl, 0.3 mol/L NaH2PO4, 30 mmol/L EDTA, pH = 7.4), 5× solución Denhard (albúmina sérica bovina 2%, polyvinylpyrrolidone al 2% Ficoll 400 al 2%), Lauryl-sarcosine al 0.1%, y SDS al 0.02%. Posteriormente, las sondas de oligonucleótidos se marcaron con uridintrifosfato de digoxigenina (Dig-11-ddUTP), la reacción se efectuó a 42°C durante 3 h.
Las membranas se lavaron dos veces con 2× SSPE, y SDS al 0.1% a temperatura ambiente durante 10 min, otro lavado con solución TMAC [50 mmol/L Tris-HCl (pH = 8.0), 3 mol/L de cloruro de tetrametilamonio, EDTA 2 mmol/L SDS al 0.1%] a temperatura ambiente durante 10 minutos y dos lavados a 60°C durante 10 min. Los puntos de reacción positiva se revelaron con el Kit de detección de ácidos nucleicos (Boehringer Mannheim Biochemical, Mannheim, Alemania) (11).
Asignación de bloques y haplotipos
Usando las frecuencias alélicas que se muestran en la Tabla 1, y basados en publicaciones anteriores, se dedujeron los haplotipos conservados Cw, B y DRB1 y DQB1 en Caucásicos, Afroamericanos y Asiáticos Americanos (Yunis, 2003; Yunis 2005a). También se dedujo que si un individuo tiene un bloque Caucásico, Africano o Asiático los alelos restantes se clasificaron como Mejicanos cuando 5 (0.01) o un mayor número de los haplotipos se pudieron identificar. Hay que anotar que en este reporte no determinamos el grado estadístico de las asociaciones al azar, Desequilibrio de Unión (LD), de los bloques de Cw, B y DRB1, DQ o de los haplotipos conservados y por lo tanto son hipotéticos.
Análisis estadístico
La diferencia de frecuencias de alelos, bloques y haplotipos entre las dos poblaciones fue calculada con de contingencia de 2×2 y la prueba exacta de Fisher. El grado de significancia fue establecido como p < 0.05.
Resultados
Frecuencia de alelos del CMH
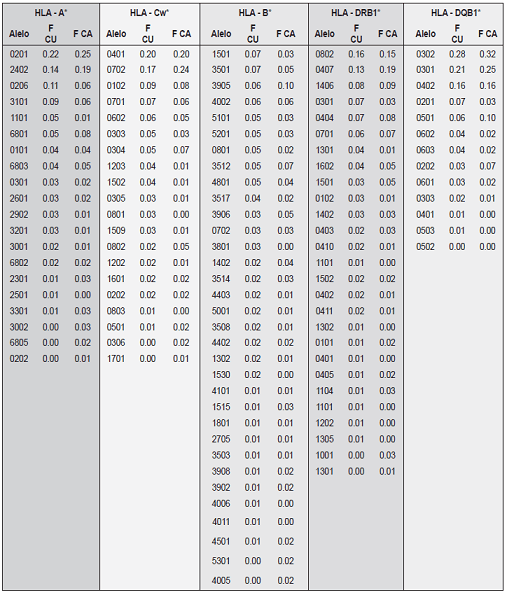
La Tabla 1 lista los alelos del CMH (HLA-A, HLA-B, HLACw, HLA-BRB1, HLA-DQB1) y sus frecuencias en ambos grupos. Como se evidencia en la Tabla, no se encontraron diferencias significativas en la frecuencia o número de alelos entre las muestras de cordones umbilicales (CU) y muestras de adultos (AC).
Tabla 1. Frecuencia de los alelos de HLA en las sangres de cordón (CU) y Mejicanos Adultos (CA)
Frecuencia de los bloques de ADN Cw*B*
Para el análisis, los bloques caucásicos fueron subdivididos en dos grupos: 1) Caucásico específicos y 2) Caucásicos compartidos por los otros dos grupos étnicos. La Tabla 2 muestra que las frecuencias de estos bloques en los dos grupos (CU y CA) son similares, aproximadamente de 0.2 en ambos. Tampoco se encontraron diferencias entre los dos grupos, en la frecuencia de los bloques atribuidos a mexicanos, con 0.4 de frecuencia en ambos grupos (Tabla 2).
Tabla 2. Frecuencia de bloques de ADN Cw B

Frecuencia de los bloque ADN HLA-DRB1, HLA-DQ
Al igual que en el análisis anterior, los bloques Caucásicos fueron subdivididos. En la Tabla 3 se muestran las frecuencias de los bloques (FAB) en los dos grupos. Encontramos que la frecuencia de bloques Caucásico específicos fue significativamente mayor en las muestras de CU 0.188 comparado con 0.073 en las muestras de AC p=0.0003. En contraste, los bloques mexicanos se encontraron aumentados en los AC, 0.58 comparado con 0.49 en los CU, p=0.01.
Más relevante aún, fue el aumento en los bloque Caucásicos cuando se consideraron solamente aquellos bloques asociados con enfermedades autoinmunes: DRB1*0301,DQB1*0201; DRB1*1501,DQB1*0602; DRB1*0402,DQB1*0302; DRB1*0401,DQB1*0302; DRB1*0701,DQB1*0201; DRB1*0401,DQB1*0301 y DRB1*0302, DQB1*0402; frecuencia de 0.144 en CU y 0.050 en CA (p<0.001).
