Circulating Tumor Cells in Oncologic Practice: Role in Epithelial Solid Tumors
Luz Fernanda Sua Villegas1, Nhora María Silva Pérez2,
Marta Vidaurreta Lázaro3, Sara Rafael Fernández3,
Virginia de la Orden3, Silvia Veganzones de Castro3
y María Luisa Maestro de las Casas3
Resumen
Las metástasis de los tumores sólidos se producen cuando las células de un carcinoma primario o metastásico migran en el sistema circulatorio y proliferan en lugares distantes. Los carcinomas son de origen epitelial y no es habitual que estas células se encuentren en el torrente circulatorio. En los últimos 20 a 30 años se han utilizado diferentes métodos y tecnologías para la determinación de células tumorales circulantes (CTC) en sangre periférica y médula ósea. Pero estos sistemas de recolección (Cyto-spins, magnetic beads, latex beads, cell-sorting (flow cytometry), density-gradient media, column separation) o de análisis (Immuno-staining, flow cytometry, Imnunohistochemistry, Fluorescence in situ hybridization, nucleic acid probes) presentan inconvenientes en cuanto a que son técnicas manuales y no estandarizadas de interpretación subjetiva, algunas sin validadación, con ausencia de un sistema de análisis específicamente diseñado para laboratorios clínicos RUO “components” y ausencia de evidencia clínica constatada que soporte la adopción del estudio de las CTC por los clínicos.
El sistema de detección CellSearch representa la primera tecnología automatizada y estandarizada que fue aprobada por la FDA para predecir la progresión y la supervivencia libre de enfermedad en el cáncer de mama metastásico. La presencia de células tumorales circulantes (CTC) en sangre periférica detectadas con CellSearch® circulating Tumor Cell System, está asociada a menor supervivencia libre de enfermedad (SLE) y menor supervivencia global (SG) en pacientes de cáncer de mama, colorrectal y de próstata metastatizante.
Palabras clave: Células tumorales circulantes (CTC), tumores sólidos y metástasis.
Abstract
Metastasis of solid tumors occurs when cells in a primary or metastatic carcinoma migrate through the circulation and proliferate at distant sites. Carcinomas are of epithelial origin and their cells are seldom seen in the bloodstream. In last decades, different methods and technologies for the identification of circulating tumor cells (CTC) in peripheral blood and bone marrow have been used. But collection systems (Cyto-spins, magnetic beads, latex beads, cell-sorting -flow cytometry- density-gradient media, column separation) or testing (Immunestaining, flow cytometry, Immunohistochemistry, Fluorescence in situ hybridization, nucleic acid probes) have drawbacks; they have no standardized manual and subjective interpretation, some are not validated, no analysis system have been specifically designed for clinical laboratory RUO “components” and no proven clinical evidence supports routine CTC determination in clinical practice. CellSearch detection system represents the first automated and standardized technology that was approved by the FDA for predicting progression and disease-free survival in metastatic breast cancer. The presence of circulating tumor cells (CTC) in peripheral blood detected circulating Tumor Cell CellSearch ® System, is associated with lower disease-free survival (DFS) and shorter overall survival (OS) in patients with metastatic breast, colorectal and prostate cancer.
Key words: Circulating tumor cells (CTC), solid tumor, metastasis.
Introducción
Los tumores epiteliales agrupan aproximadamente el 80% de la patología oncológica. Las metástasis son la principal causa de morbilidad y mortalidad en pacientes con tumores sólidos especialmente localizados en mama, colon, estósmago, próstata y pulmón. El concepto de metástasis engloba un complejo proceso de acontecimientos: las células neoplásicas del tumor primario atraviesan la membrana basal, penetran por las vías linfáticas y los vasos sanguíneos y se dispersan a tejidos distantes. (1,2,3) Esta capacidad de metástasis de los tumores sólidos a un sitio distante ha llevado a los investigadores a proponer que estos tienen fases “leucémicas”, similares a las que se conocen en los linfomas. (4)
La determinación de células tumorales circulantes (CTC) no es un concepto nuevo, en 1869 Ashworh publicó un caso donde las células malignas similares a las del tumor primario circulaban en sangreperiférica. (5) Estas observaciones permitieron que durante mucho tiempo, se supusiera que su presencia significaba una progresión de la enfermedad neoplásica maligna y que se podía relacionar directamente con las metástasis tumorales. Pero su verdadero significado biológico no había podido ser establecido, debido a su escaso número y por no contar con técnicas que permitieran su aislamiento e identificación eficaz (6-7).
La detección de las CTC puede demostrar no sólo la agresividad del cáncer originario con capacidad de lanzar células tumorales a la sangre periférica y la consiguiente potencialidad de desarrollar las metástasis, sino también su presencia per se y su facultad hipotética de iniciar la diseminación de una generación de CTC diferente desde las nuevas localizaciones metastáticas. Las CTC dependientes de los clones del tumor primario pueden ser detectadas incluso antes que el tumor donde se originan e incluso se identifican, y a menudo persisten, después de que el tumor se ha extirpado. Por tanto, la determinación de CTC ayudaría extraordinariamente a estudiar aspectos fundamentales de la Oncología, tanto en lo referente al diagnóstico como a la estadificación y al pronóstico. Más aún, abre nuevas expectativas en la evaluación de la respuesta de los cánceres ante las diferentes terapias —quirúrgicas, farmacológicas o radioterápicas— de forma individual, rápida y precisa, así como en su posterior modulación terapéutica si fuera necesario (8,9).
La determinación de las CTC en los laboratorios clínicos es un anhelo insatisfecho durante muchísimo tiempo y la complejidad es su detección se debe a su escasa presencia en el torrente sanguíneo. En los últimos años se ha avanzado en la determinación de las CTC en los tumores sólidos tanto en sangre periférica como en médula ósea, debido al desarrollo de nuevas técnicas de inmunohistoquímica, biología molecular y citometría de flujo; pero estas no han logrado ser automatizadas-estandarizadas y reproducibles hasta ahora, lo que si se ha logrado con el sistema CellSearch® circulating Tumor Cell System, el cual permite el uso de protocolos estándares para la preparación de las muestras y la interpretación de los resultados y es capaz de detectar en sangre periférica, 1 CTC por 1×105-7 células mononucleares mediante inmunomagnetismo (10, 11,12).
El sistema semiautomático CellSearch Epithelial Cell Kit (Veridex®) es el único aprobado actualmente por la FDA (US Food and Drug Administration) para la determinación de CTC en pacientes con cáncer de mama, colorrectal y próstata (13,14,15).
La determinación de CTC en sangre periférica con CellSearch® se puede realizar en cualquier momento de la enfermedad permitiendo valorar el pronóstico del paciente y predecir la sobrevida libre de enfermedad y una sobrevida global. Además, nos permite la monitorización de estos pacientes junto con los métodos clínicos actuales (Ver tabla 1).
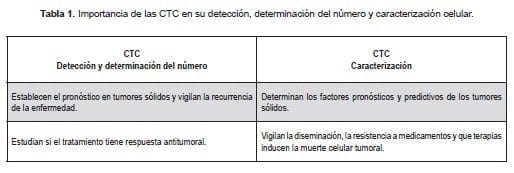
Actualmente se trabaja en otros sistemas de detección a través de RT-PCR (transcriptasa reversa y reacción en cadena de polimerasa), CTC-chip (microchips), microfiltro, citometría de flujo, FAST (método citométrico) y FISH (hibridación in situ fluorescente). Estas técnicas se encuentran en investigación o requieren ensayos clínicos para poder ser validadas. (16) (Ver tabla 2.)
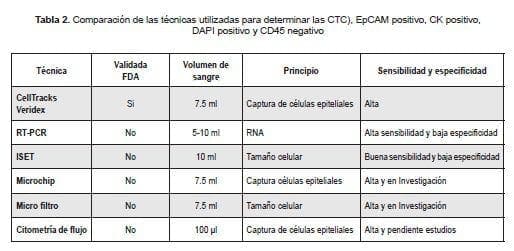
Por tanto, las biopsias del tumor no invasivas son una realidad y el seguimiento de los tratamientos podría realizarse tan frecuentemente como fuera necesario y además nos permitirían monitorizar el genotipo del tumor durante el tratamiento. Las CTC aisladas con estas tecnologías pueden asemejarse a una -Biopsia Liquida- con capacidad de estudio molecular individualizado (mutaciones, genes de resistencia conocidos a fármacos, nuevos marcadores tumorales, etc.) y especifico de cada paciente.
1 MD. Departamento de Anatomía Patológica y Patología Clínica. Universidad del Valle. <Clínica de Occidente. Unidad Oncológica. Cali. Colombia.
2 MD. Laboratorio Clínico y de Patología. Fundación Valle del Lili. Cali. Colombia.
3 Ph.D. (Dra.Maestro), Quím. (Lic. Vidaurreta), Biol. (Lic. Rafael, de la Orden y Veganzones). Laboratorio de Análisis Clínicos: Sección de Genómica. Hospital Clínico San Carlos de Madrid. España
