EL GEN Y LA ENZIMA GALNS
El gen humano GALNS se encuentra localizado en el cromosoma 16q24.3 y posee una longitud de 50 kb con 14 exones y 13 intrones (18). Un ARNm de 2,3 kb es sintetizado a partir del gen GALNS, con un marco abierto de lectura de 1,5 kb que codifican para una proteína de 522 aminoácidos (19). El contenido GC en la región reguladora 5’, sumadoa la ausencia de una caja TATA y la presencia de un alto número de sitios de unión para el factor de trascripción Sp1, sugieren que este es un gen de expresión constitutiva (15, 18).
Cerca de 150 mutaciones han sido identificadas en el gen GALNS, incluyendo mutaciones de sentido errado (69%), sin sentido (5%), alteraciones de corte y empalme (7%), deleciones pequeñas (13%) y grandes (2%), e inserciones (4%). El 46% de estas mutaciones ocurren menos de tres veces en el total de la población sugiriendo una elevada heterogeneidad molecular en las mutaciones sobre el gen GALNS (20, 21). Para la población colombiana se identificaron las mutaciones p.G301C, p.S162F y p.F69V en pacientes del viejo Caldas, de las cuales la última no ha sido reportada en otras poblaciones (6, 20). Posteriormente, las mutaciones p.A75G y pR386C fueron identificadas en pacientes del departamento de Boyacá (Saboya y Chiquinquirá), de las cuales la primera no se ha identificado aún en otros pacientes latinoamericanos (22).
A pesar de la elevada heterogeneidad molecular de las mutaciones, se han observado algunas asociaciones genotipo-fenotipo. Así, la mayoría de las mutaciones puntuales están asociadas con fenotipos atenuados, mientras que mutaciones sin sentido, deleciones grandes y alteraciones del sitio de corte y empalme se encuentran asociadas con fenotipos severos (20).
La enzima GALNS es un homodímero de 120 kDa, con monómeros de 60 kDa que son procesados a polipéptidos con un peso molecular de 40 kDa y 15 kDa unidos por un enlace disulfuro (23). Al igual que otras enzimas y proteínas lisosomales, GALNS posee un péptido señal de 26 residuos que dirige la proteína naciente al retículo endoplasmático (RE), en donde es inicialmente modificada por glicosilación cotranslacional en dos asparaginas (24). Esta glicosilación involucra la transferencia en bloque de un oligosacárido formado por tres glucosas, nueve manosas y 2 residuos de N-acetilglucosamina. Antes de salir del RE tres residuos de glucosa y uno de manosa son removidos del oligosacárido (25) (Figura 1).
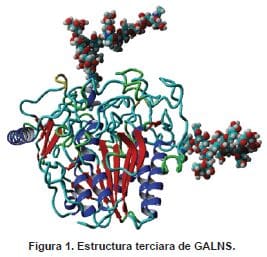
La predicción de la estructura terciara se realizóempleando el servidor I-tasser (https://zhanglab.ccmb.med.umich.edu/I-TASSER/). La predicción de los dosposibles sitios de glicosilación, así como la generación delmodelo glicosilado fueron realizados con la herramientaGlyProt (https://www.glycosciences.de/modeling/).
Antes de ser plegada en el RE, GALNS es activada por la enzima generadora de formilglicina (FGE). FGE es una enzima del RE responsable de la conversión de cisteína a formilglicina en el sitio activo de las sulfatasas, representado por la secuencia consenso CXPSRXXX[L/M]TG[R/K/L] y ubicado en el extremo N-terminal de la proteína (26). Para el caso específico de GALNS humana el sitio activo se encuentra en la posición C79 (24). FGE es codificada por el gen SUMF1 (Sulfatase Modifying Factor 1). Este gen es un factor limitante y esencial en la actividad de las sulfatasas por las siguientes razones: (i) mutaciones en SUMF1producen la deficiencia múltiple de sulfatasas, en donde la actividad de todas las sulfatasas se encuentra afectada, (ii) la sobrexpresión de una sulfatasa produce activación parcial de la enzima y disminución en la actividad de otras sulfatasas por saturación del sistema, y (iii) la coexpresión de una sulfatasa con SUMF1 lleva a un marcado incremento en la actividad de la respectiva sulfatasa (27, 28).
A diferencia de las proteínas de membrana o de la ruta secretora, en las que las cadenas de oligosacáridos son procesadas a unidades que contienen ácido siálico, las enzimas lisosomales son modificadas por la adición de residuos de fosfomanosil, el cual funciona como un componente esencial en el reconocimiento del receptor de manosa-6-fosfato en Golgi (29). Una vez llevadas a cabo estas modificaciones sobre la cadena de oligosacáridos, la enzima se une al receptor de manosa-6-fosfato y abandona Golgi en vesículas recubiertas de clatrina, que la dirigen al sistema endosomal/lisosomal. Cerca del 2 al 20% de la enzima es secretada antes de llegar al lisosoma, la cual puede ser recapturada de manera autocrina o paracrina por unión con receptores de manosa-6-fosfato ubicados en la membrana celular. Esta capacidad de captura celular y direccionamiento al lisosoma constituyen la base para el desarrollo de terapias de reemplazo enzimático, génica ycelular (25, 29, 30).





