Introducción
Carlos García-Lozano MD1, Álvaro Sanabria2
Resumen
Desde tiempos remotos el cáncer ha acompañado a nuestra especie, y los procedimientos de resección quirúrgica fueron los primeros propuestos para su control.
La comprensión de la historia del cáncer permite entender el papel de la cirugía como herramienta de tratamiento.
Los principales avances quirúrgicos ocurrieron durante el siglo XIX con el advenimiento de la anestesia y la antisepsia, lo que permitió realizar cirugías más complejas y radicales hasta llevar la cirugía al límite de la anatomía con la super-radicalidad del siglo XX.
Actualmente, con la medicina basada en la evidencia y la integración con otras especialidades como la radioterapia y la oncología clínica, se ha logrado un sinergismo que ofrece al paciente una mayor supervivencia con menor morbilidad y mejor calidad de vida. Destacamos la vida de cuatro cirujanos y sus aportes a la cirugía del cáncer en diferentes épocas.
Palabras clave: Historia de la medicina; cirugía general; oncología quirúrgica; personajes.
Historical Personalities in Surgical Oncology
Abstract
Since ancient times cancer has accompanied our species, and surgical resection procedures were the fi rst proposed for its control. Understanding the history of cancer allows us to understand the role of surgery as a treatment tool.
The main surgical advances occurred during the nineteenth century with the advent of anesthesia and antisepsis, which allowed more complex and radical surgeries to be performed until surgery was taken to the limit of anatomy with the super-radicality of the twentieth century.
Currently, with evidence-based medicine and integration with other specialties such as radiotherapy and clinical oncology, a synergism has been achieved that off ers the patient greater survival with less morbidity and better quality of life.
We highlight the lives of four surgeons and their contributions to cancer surgery at diff erent times.
Keywords: History of medicine; general surgery; surgical oncology; famous persons.
Introducción
La cirugía ha sido una opción de tratamiento para las enfermedades tumorales desde tiempos remotos. Se tienen registros del tratamiento quirúrgico de los tumores malignos en el papiro de Smith y el papiro de Evans en Egipto (1). No obstante, en el periodo clásico, los griegos hicieron muy pocos avances e incluso recomendaron no intervenir las enfermedades neoplásicas malignas, las cuales consideraban incurables. (1,2)
Durante el renacimiento y con los avances anatómicos de Andrea Vesalio, se mejoró el entendimiento de la anatomía humana y se llevaron a cabo intervenciones quirúrgicas para extirpar lesiones adquiridas, pero básicamente estas se limitaban a tumores pequeños y superficiales. Ambroise Paré, destacado cirujano del siglo XVI sostenía que sólo se debía intentar la resección quirúrgica del tumor si este se podía resecar completamente (3).
Las cavidades internas como el peritoneo y la cavidad torácica eran santuarios inviolables para los cirujanos, y salvo contadas excepciones, quien incurría en su intervención quirúrgica era considerado un asesino.
Debido a la dificultad para acceder a los órganos internos, sus afecciones eran tratadas con sustancias ingeridas o sangrías, lo que dio origen al nombre de medicina “interna” para referirse al estudio y tratamiento de las enfermedades de estos órganos (4-6).
Para el siglo XVIII, con la invención del microscopio, se abrió camino a una nueva rama en la que se podía visualizar la estructura celular de los tumores y la evaluación de los tejidos resecados (7). También se comprobaron asociaciones ocupacionales con el cáncer, al notar la alta frecuencia de cáncer de escroto en los niños deshollinadores en Inglaterra (8).
Cambios fundamentales en el campo de la cirugía
Los cambios fundamentales en el campo de la cirugía se presentaron en la mitad del siglo XIX con el desarrollo de la anestesia (1846) y posteriormente con la introducción de la antisepsia (1867), lo que abrió la posibilidad de realizar intervenciones de lesiones neoplásicas en localizaciones antes impenetrables (1,9,10).
Además, con la comprensión de los patrones de diseminación linfática nació la cirugía radical, el concepto de la cirugía en bloque y los vaciamientos linfáticos con William Halsted como principal exponente (6,9-13).
Ya en el siglo XX, el perfeccionamiento de los hospitales, el descubrimiento de los antibióticos y el uso amplio de las transfusiones sanguíneas permitió una mayor tolerabilidad del paciente a los grandes procedimientos y se idearon cirugías súper-radicales con la promesa de la cura definitiva del cáncer.
Con estas grandes resecciones, en muchos casos la única opción o al menos la más confiable conocida hasta el momento, aumentó también la morbilidad sin una disminución significativa en la mortalidad (1).
Descubrimiento de los Rayos X desde 1895 y su uso en medicina
A pesar del descubrimiento de los Rayos X desde 1895 y su uso en medicina al ver que favorecía la disminución de algunos tumores, no fue sino hasta mediados del siglo XX que su perfeccionamiento (radioterapia) permitió mayor confiabilidad en el manejo del cáncer (14).
Desde la década de los 50 se inició la carrera para descubrir formas alternativas al tratamiento quirúrgico con Farber como pionero en el tratamiento de las leucemias y linfomas.
Con la comprensión de los aspectos celulares y genéticos del cáncer, las estrategias de tratamiento con fármacos (quimioterapia) han venido en constante crecimiento.
Muchos de estos nuevos fármacos se descubrieron por casualidad probando químicos y sus combinaciones en el laboratorio y luego en los pacientes.
Sin embargo, muchas de estas estas sustancias no solo representaban un tóxico para las células tumorales sino también para las células sanas afectando su división celular.
El desarrollo de la metodología de los ensayos clínicos controlados aleatorios, facilitó una forma racional y científica de sustentar una conducta terapéutica, poniendo en una balanza el riesgo contra el beneficio (15-17).
Debido a que los cirujanos habían dominado el tratamiento del cáncer durante siglos, se mantuvo una férrea resistencia a estas nuevas alternativas farmacológicas.
Aparición de la cirugía reconstructiva
La aparición de la cirugía reconstructiva, desarrollada para tratar las mutilaciones de las guerras, fue adaptada a la cirugía oncológica, lo que permitió practicar resecciones tumorales mayores.
La cirugía radical multiorgánica acompañada de reconstrucciones complejas se convirtió en el orgullo de la cirugía.
Desde entonces, la batalla contra el cáncer se dividió en dos bandos: los tumores sólidos que eran exclusividad de los cirujanos y los tumores no sólidos que eran potestad de los quimioterapeutas (aún no se llamaban oncólogos).
Finalmente, en la segunda mitad del siglo XX, un cirujano (Bernard Fisher) se reveló contra la super-radicalidad de la mastectomía, introdujo los ensayos clínicos a la cirugía y combinó los dos tipos de tratamiento, lo que reconcilió los caminos que se habían ido separando (18).
Esto dio lugar al manejo multidisciplinario e interdisciplinario del cáncer y permitió avanzar en estrategias de tratamiento quirúrgico que guardan un mejor equilibrio entre la morbimortalidad y la mejora de la calidad de vida, tales como la conservación de órgano, las cirugías funcionales y los abordajes de mínima invasión.
Actualmente comprendemos que el trabajo en equipo entre la cirugía oncológica, la radioterapia como tratamiento locorregional y la oncología clínica como tratamiento sistémico, ha tenido un impacto positivo en la supervivencia de la mayoría de los tumores malignos (19).
Con este somero contexto histórico, queremos resaltar cuatro personajes que influyeron en los avances de la cirugía del cáncer que tenemos hoy en día y que contribuyeron en diferentes épocas: Billroth, Halsted, Martin y Fisher.
Christian Albert Theodor Billroth (1829-1896)
Billroth nació en la isla de Rügen, Prusia. Su padre, un ministro luterano, falleció cuando Theodor tenía 5 años, lo que produjo que se mudara con su abuelo materno a Greifswald, Alemania.
Considerado mal estudiante por sus dificultades del habla, en matemáticas y ciencias, requirió de un tutor para graduarse de la secundaria. Sin embargo, era un amante de la música y un gran pianista. Su madre lo alentó a estudiar medicina, básicamente por razones económicas y para alejarlo de la vida bohemia (20,21).
Inició sus estudios en la universidad de Greisfwald:
De la mano de Whilhem Baum, y posteriormente estableció amistad con George Meissner y el fisiólogo Rudolph Wagner.
Pasó un tiempo en Trieste (Italia) estudiando las terminaciones nerviosas de la anguila y regresó para terminar sus estudios en la Universidad de Berlín donde se graduó en 1852, siendo algunos de sus profesores el cirujano Von Lagenbeck, el neurólogo Romberg y el patólogo Rokitansky (20).
Intentó practicar la medicina privada sin éxito y en 1853 fue nombrado asistente de Von Lagenbeck en la universidad de Berlín. Allí amplió sus estudios de anatomía patológica y se postuló como jefe de patología, pero perdió el concurso con Rudolf Virchow (21).
En 1860 fue nombrado profesor de cirugía en Zúrich y allí introdujo las auditorías y la necesidad de publicar los resultados tanto buenos como malos, aplicó la estadística a la cirugía y diseñó los informes de morbimortalidad, pues recalcaba que “los cirujanos que no pueden informar sus resultados con honestidad son como charlatanes” (20,22).
Durante su estancia en Suiza, también estudió las infecciones de la herida quirúrgica, combinó la anatomía patológica con la microbiología (nombró el género de los Streptococcus y estudió el efecto antimicrobiano del hongo penicillium) (21,23).
Adicionalmente, escribió artículos de crítica musical e hizo una amistad de por vida con el músico Johannes Brahms (20,22).
En 1867 fue nombrado jefe de cirugía y director de la clínica quirúrgica de Viena.
Allí desarrolló sus logros más importantes, como la primera laringectomía en 1873 (24,25) y junto con su alumno y asistente Von Czerny, avanzaron en la técnica de la esofagectomía que Czerny realizaría por primera vez en humanos seis años después (22).
En 1870 se enlistó como voluntario en la guerra franco-prusiana para ampliar su experiencia en la cirugía de guerra y evaluó y mejoró los cuidados de enfermería.
Pasó a la historia al realizar con éxito la primera antrectomía con anastomosis del estómago al duodeno (Billroth I), disminuyendo la diferencia de calibres al cerrar parcialmente el estómago con puntos de seda (no de catgut, como se hacía hasta ese momento).
Posteriormente planteó una cirugía en dos etapas para un paciente muy débil, la primera con una gastroentero anastomosis para nutrirlo y posteriormente, la resección definitiva del tumor.
Posteriormente, acortó el procedimiento a un solo tiempo quirúrgico, cerrando los bordes duodenal y gástrico, lo que constituyó la cirugía Billroth II (22). También introdujo mejoras en la educación quirúrgica con periodos de estudio más largos (21). Entre sus alumnos se destacan Czerny, Kocher, Bassini, Mickulickz, Halsted, Guusenbauer, entre otros.
En 1887 sufrió una neumonía con daño pulmonar permanente que sumado a insuficiencia cardíaca fue mermando su salud y murió en 1864 a la edad de 65 años. Sus restos permanecen en Viena (22).
William S. Halsted (1852-1922)
Halsted constituye uno de los personajes más famosos y destacados dentro de la historia de la cirugía con su contribución al diseño de las residencias quirúrgicas y en especial por el desarrollo de la cirugía del cáncer de mama con la mastectomía radical.
Muchas de estas ideas no fueron de su autoría, pero sí las perfeccionó y las aplicó en el desarrollo de su técnica quirúrgica.
Nacido en Nueva York como hijo de un empresario textil, su llegada a la cirugía fue casi accidental, más por evadir su futura vida como empresario textil que por amor a la medicina.
Se interesó precozmente por la anatomía y luego por la cirugía y asumió con pasión y determinación sus estudios, lo que le permitió aprobar su examen para un internado en el Hospital Bellevue en Nueva York.
Complementó sus estudios en Europa con grandes exponentes de todas las ramas de la medicina, pasando por Berlín, Halle, Zúrich y Londres, lo que le facilitó la introducción de las técnicas quirúrgicas de Billroth para cáncer abdominal, entre otras (26).
En la década de 1880, a su regreso a Nueva York, inició una carrera destacada como profesor y cirujano audaz, inventivo y osado.
Adoptó las técnicas europeas de antisepsia con ácido carbólico de Lister.
Durante este periodo labró su fama de intrépido, de donde vienen anécdotas famosas como cuando fue llamado para atender a su hermana quien sufría hemorragias posparto y realizó una transfusión de su propia sangre (en esa época no se conocían aún los grupos sanguíneos) o como cuando fue llamado a valorar a su madre que padecía dolores abdominales y fiebre, y a quien le practicó la primera colecistostomía realizada en Estados Unidos, en la mesa de la cocina de su casa (26).
Después de haber conocido en 1884 sobre la primera cirugía ocular sin dolor:
Utilizando gotas de un nuevo anestésico local, la cocaína, Halsted probó este nuevo compuesto junto con un grupo de sus estudiantes, inyectándose para evaluar la posibilidad de anestesia regional.
Pronto descubrió los efectos de infatigabilidad y estimulación que potenciaban su personalidad hipomaníaca, eliminando el cansancio o la necesidad de dormir.
Con su uso crónico, sucumbió ante los efectos secundarios de este fármaco y cayó en la adicción, lo que lo obligó a internarse voluntariamente en el sanatorio Butler de Providence, donde se trataba la adicción con morfina.
Al año siguiente, su amigo y reconocido patólogo William Welch, lo convocó para ir a trabajar a Baltimore en el nuevo hospital Johns Hopkins, donde inicialmente fue propuesto como jefe de cirugía ambulatoria.
En 1890 Welch y William Osler lo propuesieron como jefe de cirugía. Para cuando se abrió la escuela de medicina de Johns Hopkins en 1893, Halsted fue el primer maestro de cirugía y fue aquí donde desarrolló sus conceptos sobre el uso de la cirugía en el cáncer de mama (26).
Desde su estancia en Alemania, pudo observar a Volkmann realizar cirugías más cuidadosas y extensas para el cáncer de mama, aunque era frecuente la recurrencia meses o años después.
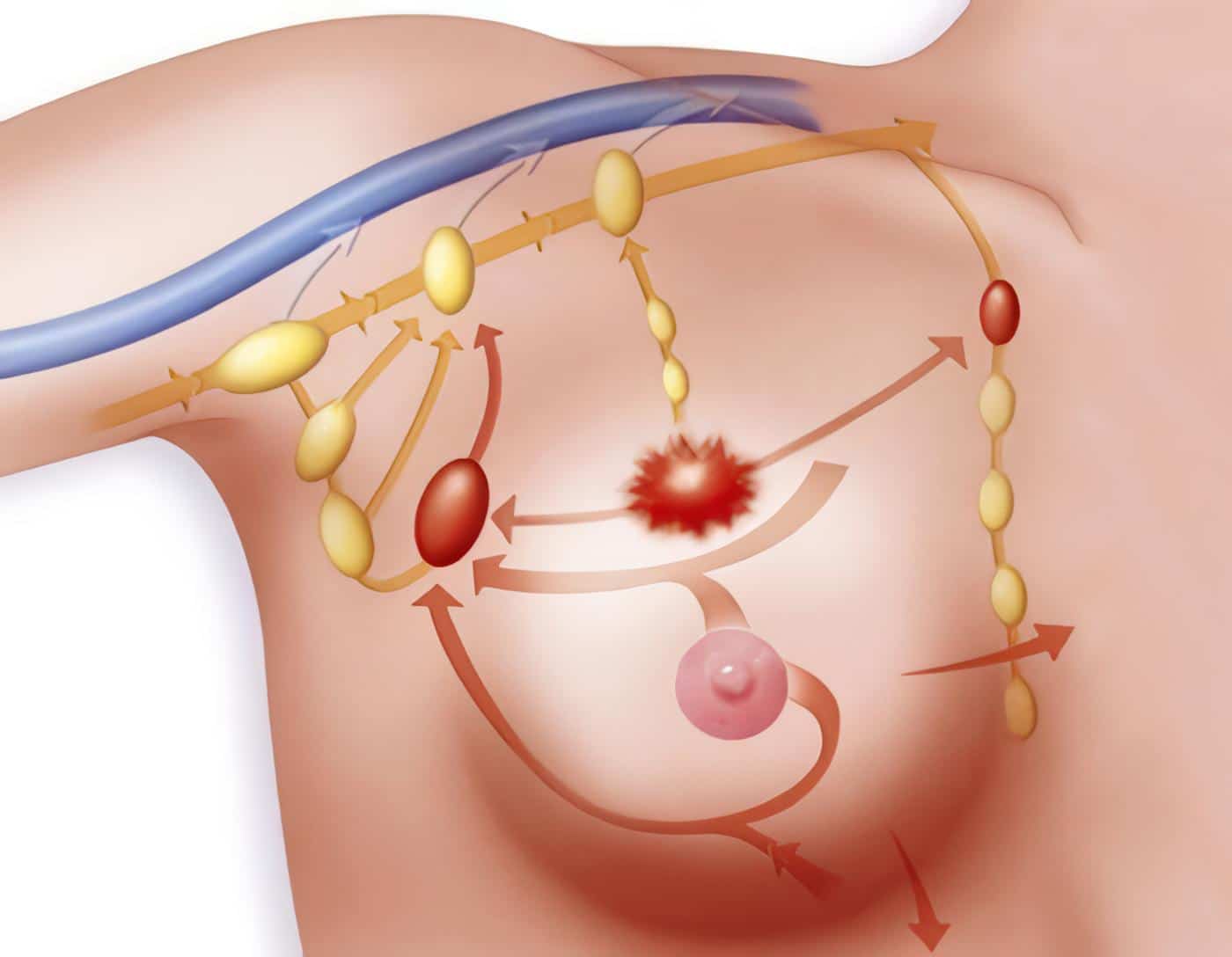
Charles Moore de Londres, frustrado por estos mismos hallazgos, comenzó a documentar las resecciones y los sitios de recurrencia, y encontró un patrón en el cual el tumor reaparecía en relación con los márgenes de resección originales y propuso ampliar y resecar más tejido. Concluyó que se requería extirpar toda la mama y que los cirujanos conservadores incurrían en una “bondad errónea” a fin de evitar una cirugía más amplia y desfigurante (27). Halsted conocía estos trabajos que evidenciaban un patrón de diseminación progresivo y centrífugo que comenzaba en el órgano afectado y se extendía a los músculos pectorales, los ganglios axilares y desde allí hacia el hígado, los pulmones y los huesos.
Así, concretó la idea que el cirujano debe interrumpir esa extensión centrífuga y cortar ampliamente todos los tejidos que se interpongan en esta propagación, una cirugía amplia que permitiera extraer el cáncer de “raíz” de donde nace el término cirugía radical.
Entre más cortaba el cirujano, más curaba. Halsted perfeccionó una técnica de mastectomía radical en bloque que resecaba la mama, los músculos pectorales y los ganglios axilares, con modificaciones técnicas como la minuciosidad en el tratamiento de los tejidos, la hemostasia exhaustiva, la reaproximación por planos y el cambio de suturas de catgut por seda.
Con esto logró aumentar la supervivencia por cáncer de mama de 13 a 40%, todo un logro para su época (13,26,28,29).
Estos mismos aspectos meticulosos y perfeccionistas propios de su personalidad dieron forma a la naciente cirugía americana y cambiaron para siempre la filosofía de las residencias quirúrgicas, en las que la infatigabilidad, la abnegación y la dedicación sobrehumana se constituían en los nuevos valores de un cirujano (26,27).
Discípulos de Halsted como Harvey Cushing, John Finney, George Heuer y Joseph Bloodgood continuaron su legado en muchas escuelas de cirugía en Estados Unidos, llevando los principios de Halsted a otras ramas nacientes de la cirugía, donde la radicalidad se convertía en el dogma y el criterio de operabilidad dependía de si la lesión era resecable independiente de las posibilidades de curación a largo plazo (26,30).
Otra famosa contribución fueron los guantes de goma. Para aliviar la dermatitis de las manos que sufría Caroline Hampton (su instrumentadora principal y posteriormente su esposa) debido a la excesiva limpieza para sus cirugías, Halsted encargó a la compañía Goodyear unos guantes de goma a su medida.
Estos eran usados únicamente por los instrumentadores, pues los cirujanos argumentaban que ellos disminuían la sensibilidad del tacto. Su uso fue popularizado por McBurney y Bloodgood cuando demostraron la disminución de las infecciones en cirugías de hernia (31). Halsted murió en 1922 luego de padecer coledocolitiasis y colangitis, fallece a causa de neumonía postoperatoria a los 69 años.
(Lea También: Herencia de la II Guerra Mundial al Estudio del Cáncer)
Hayes Martin (1892-1977)
Hijo de inmigrantes suecos, nació en Dayton (Iowa). Su padre murió de cáncer de estómago cuando tenía 10 años y su madre murió 5 meses después, quedando huérfano a cargo de su tía.
Estudió medicina en la Universidad de Iowa, bajo la tutela del Dr. Campbell Palmer Howard, discípulo de Sir William Osler en Johns Hopkins (32). Cuando estaba en su último año de medicina, estalló la Primera Guerra Mundial y se enlistó en la armada. Fue enviado a una base naval aérea en Francia y fue nombrado comandante por un breve periodo.
Regresó a Estados Unidos en 1919 e ingresó a la residencia en el Hospital Bellevue en Nueva York. Estuvo en el Memorial Hospital hasta 1923 para aprender de cáncer y volvió al Bellevue donde terminó su formación en cirugía dos años después (32-34). Aquí gestó su principal contribución al cáncer.
En un paciente que había sido operado previamente por un tumor de escroto y quien acudió con una masa en el pulmón, Martin argumentó:
En contra de la opinión generalizada, que se trataba de un segundo primario puesto que la lesión era única. Tiempo después fue llamado para declarar la muerte de un paciente en el servicio de urgencias, que resultó ser el mismo de la discusión.
Con el ánimo de confirmar su opinión, puso cortinas alrededor, tomó una aguja y una jeringa grande y dirigió la aguja donde creía que estaba la masa pulmonar hasta sentir algo firme, recolectó la muestra y la envió a patología. Diez días después, Simmers, el jefe de patología, le confirmó el diagnóstico post mortem de carcinoma escamoso.
Martin le explicó su técnica, a la cual Simmers respondió con incredulidad. De esta forma, Simmers pasó a ser el primer patólogo en leer con éxito una biopsia por aspiración de un tumor sólido, pero se opuso a ella durante toda su vida. (32).
Martin volvió al Memorial, liderado por el Dr. James Ewing, patólogo:
Quien participaba en muchas decisiones clínicas y promocionaba el tratamiento de varios tumores con radioterapia. En esta época la radioterapia externa estaba en su etapa primitiva y se usaban principalmente semillas de radio y radón en los cánceres de cabeza y cuello.
Allí convenció a Ewing sobre la utilidad de la biopsia por aspiración luego de demostrar el diagnóstico de tumor epidermoide en un paciente con una masa en el cuello. La primera publicación sobre la biopsia aspirativa se hizo en Annals of Surgery en 1930 (35-37).
En 1934 fue nombrado jefe del servicio de cabeza y cuello. Después de la Segunda Guerra Mundial, con los avances en anestesia, transfusiones sanguíneas y antibióticos, y desilusionado por los resultados con el radio, Martin enfocó su tratamiento hacia la cirugía agresiva del cáncer de cabeza y cuello y creó el concepto de Cirujano de Cabeza y Cuello.
Retomó el vaciamiento radical de cuello, descrito por George Crile en 1906 con resección en bloque de los ganglios del cuello junto con el músculo esternocleidomastoideo, la vena yugular interna y el nervio espinal, en similitud con lo realizado por Halsted en la mama (34,38).
Para 1950, se habían realizado 190 vaciamientos en el Memorial, iniciando una nueva era en el tratamiento del cáncer de cabeza y cuello con cirugías radicales.
Sus principales publicaciones incluyen “Cancer of the head and neck” en JAMA 1948 (39), “Neck Dissection” en Cancer 1951 (40) y “Radical Neck Dissection” en Clinical Symposia en 1961 (41), artículos que se reimprimieron hasta 20 años después de su fecha de publicación original. En 1957 publicó su libro “Cirugía de los tumores de cabeza y cuello”, que se convierte en el estándar para los interesados en cirugía de esta área (32,42).
Martin estableció la máxima que un crecimiento asimétrico de uno varios ganglios del cuello en un adulto, casi siempre es maligna y secundaria a una lesión en la cavidad oral o la faringe. También señaló el peligro de la extirpación imprudente de un ganglio linfático para el diagnóstico, (43) pues invariablemente disminuye la posibilidad de cura (32).
Entre sus contribuciones se encuentran la pinza de disección de Martin, una pinza con finos dientes para tracción de los tejidos, la fundación de la Sociedad de Cirujanos de Cabeza y Cuello y de la sociedad James Ewing, actualmente conocida como la Sociedad de Cirugía Oncológica (32).
Permaneció como jefe del servicio de cabeza y cuello en el Memorial hasta su retiro en 1957 y murió en 1977 por complicaciones respiratorias luego de varios accidentes cerebrovasculares.
Bernard Fisher (1918-2019)
La teoría Halstediana de diseminación centrífuga en la que es prioridad del cirujano cortarle el camino al tumor con cirugías cada vez más agresivas, mantuvo vigente el concepto de radicalidad a super-radicalidad y ultra-radicalidad (resección de músculo pectoral, ganglios axilares y supraclaviculares, mediastinales y hasta la pared torácica en cáncer de mama) durante más de la mitad del siglo XX.
El cáncer, aun en su fase inicial, era un enemigo tan fuerte que se requería una cirugía tan radical como la anatomía lo permitiera y se popularizaron frases como “entre más se corta, más se cura” o “si lo puedes cortar, lo puedes curar”.
Fisher nació en Pittsburgh en 1918.
Se formó como médico y como cirujano en la universidad de Pittsburgh, donde inició sus investigaciones en trasplantes y regeneración hepática.
Fisher comenzó a notar, al igual que otros investigadores como Geoffrey Keynes de Londres y George Barney Crile (hijo de George Crile, quien describió inicialmente el vaciamiento radical de cuello), que, a pesar de estas cirugías radicales, los tumores recurrían a distancia y dejaban pacientes con una gran mutilación y con cáncer (44).
Hasta este momento Keynes había descrito la posibilidad de una cirugía menos agresiva combinada con radiación posterior y con resultados similares a la mastectomía radical, lo cual fue repudiado por la mayoría de cirujanos en Estados Unidos y a la que llamaban despectivamente “lumpectomía”. Crile Jr., contradijo la lógica Halstediana argumentando que, si el tumor estaba confinado a un solo sitio, era posible su curación con cirugía y radiación local, pero que la resección de otras estructuras u órganos no aportaría beneficios.
Además, si el cáncer ya se había propagado más allá del seno, la cirugía entonces era inútil y una cirugía más agresiva solo era más agresivamente inútil. Crile Jr. propuso una cirugía más localizada que llamó “mastectomía simple” y pronto observó que sus resultados eran similares a la lumpectomía más radiación y sin diferencias con la mastectomía radical.
Fisher había descrito en modelos animales la presencia de células tumorales en sangre y cúmulos de micrometástasis en sitios tan distantes como el hígado o los huesos, aún en fases tumorales muy localizadas y sin invasión previa de los ganglios.
Así, el cáncer no se movía de manera centrífuga en espirales ordenadas y su propagación era más errática e impredecible.
Fisher se convenció tempranamente que la mastectomía radical carecía de racionalidad biológica, pero la ortodoxia de los cirujanos de la época y la resistencia a cambiar, impidieron realizar un ensayo clínico que permitiera una cirugía menos radical (45).
Hasta ese momento nunca se había retado la “cirugía radical”. En 1967, Fisher llegó a la presidencia del Proyecto Nacional de Cirugía Adyuvante de Mama e Intestino (NSABP), un grupo de hospitales académicos encargado de realizar ensayos sobre el cáncer de mama, e inició el estudio NSABP-04 con tres brazos aleatorios (mastectomía radical, mastectomía simple y cirugía seguida de radiación). Dadas las barreras para el reclutamiento por parte de los cirujanos americanos, hubo necesidad de incluir también pacientes en Canadá.
Los resultados de este estudio, no demostraron diferencias significativas en relación a supervivencia, recidiva o metástasis a distancia, lo que inició el derrumbe de la cirugía radical y la teoría centrífuga, y dio paso al concepto de cáncer como enfermedad sistémica con manifestaciones locales (29,46-48).
Los avances en quimioterapia para el tratamiento del cáncer avanzado y el descubrimiento del efecto de los receptores estrogénicos llevaron al desarrollo de la adyuvancia posterior a la cirugía.
De nuevo la resistencia entre los cirujanos estadounidenses obligó a desarrollar un estudio en Milán, Italia, con Bonnadona y Veronesi (un oncólogo y un cirujano), que demostró que la adyuvancia había impedido recidivas en aproximadamente una de cada seis mujeres (44,45).
En 1977, Fisher realizó en un ensayo con tamoxifeno adyuvante en pacientes con receptores estrógenos positivos y enfermedad limitada a los ganglios, que demostró la disminución de la recurrencia en cerca del 50% (47,48). Fisher se convirtió así en un revolucionario de la cirugía oncológica en el cáncer de mama, y reformuló el concepto de orientar las decisiones terapéuticas quirúrgicas con base en la experimentación científica y en la evidencia.
Rompió la tradición quirúrgica con frases como “el médico por venerable que sea, debe aceptar que el hecho de que la experiencia, aunque sea voluminosa, no puede utilizarse como un indicador de validez científica” y acuñó la célebre frase basada en el billete de un dólar “In God we trust” dijo: “En Dios confiamos, todos los demás deben traer referencias” (evidencia) (44,45). Fisher murió en Pittsburgh en 2019 a la edad de 101 años.
Desde la década de los ochenta, se cambió entonces el paradigma de la exclusividad del cirujano para el manejo del cáncer local o locorregional, comenzó la era de la multidisciplinariedad y, luego de modular las disputas, de la transdisciplinariedad en el tratamiento más humanizado e hipocrático del cáncer. A medida que aprendemos sobre él, y de la mano de la evidencia, se avanza hacia el mejor tratamiento posible de nuestros pacientes.
Referencias
-
1. Lawrence W. History of surgical oncology. En: Norton J, Barie P, Bollinger R, Chang A, Lowry S, Mulvihill S et al.,editors. Surgery: Basic Science and Clinical Evidence. 2a ed. Springer; 2008. p.1889-900.
-
2. Hajdu SI. A note from history: Landmarks in history of cancer, part 1. Cancer. 2011;117(5):1097–102.
-
3. Hajdu SI. A note from history: Landmarks in history of cancer, part 2. Cancer. 2011;117(12):2811–20.
-
4. Reyes H. ¿Qué es Medicina Interna? What is Internal Medicine? Rev Méd Chile. 2006;134:1338–44.
-
5. de la Blanchardière A, Le Dinh T. Histoire de la médecine interne. La Rev Med interne.1994;15(10):690–3.
-
6. García MG, Ortega AB, Lucero B, Sánchez S. Cirugía oncológica : evolución histórica y estado actual. Gac Med Mex. 2011;147:551–60.
-
7. Fechner RE. A brief history of head and neck pathology. Mod Pathol. 2002;15(3):221–8.
-
8. Herr HW. Percivall pott, the environment and cancer. BJU Int. 2011;108(4):479–81.
-
9. Lawrence W, Lopez MJ. Radical surgery for cancer: A historical perspective. Surg Oncol Clin N Am. 2005;14(3 SPEC. ISS.):441–6.
-
10. Lopez MJ. The evolution of radical cancer surgery. Surg Oncol Clin N Am. 2005;14(3):xiii-xv.
-
11. Inchingolo F, Santacroce L, Ballini A, Topi S, Dipalma G, Haxhirexha K et al. Oral cancer: A historical review. Int J Environ Res Public Health. 2020;17(9):3168.
-
12. Natarajan S, Taneja C, Cady B. Evolution of lymphadenectomy in surgical oncology. Surg Oncol Clin N Am. 2005;14(3):447–59.
-
13. Hajdu SI. A note from history: Landmarks in history of cancer, part 4. Cancer. 2012;118(20):4914–28.
-
14. Lederman M. The early history of radiotherapy: 1895- 1939. Int J Radiat Oncol Biol Phys. 1981;7(5):639–48.
-
15. Galmarini D, Galmarini CM, Galmarini FC. Cancer chemotherapy: A critical analysis of its 60 years of history. Crit Rev Oncol Hematol. 2012;84(2):181–99.
-
16. Keating P, Cambrosio A. Cancer clinical trials: The emergence and development of a new style of practice. Bull Hist Med. 2007;81(1):197–223.
-
17. DeVita VT, Chu E. A history of cancer chemotherapy. Cancer Res. 2008;68(21):8643–53.
-
18. Ekmektzoglou KA, Xanthos T, German V, Zografos GC. Breast cancer: From the earliest times through to the end of the 20th century. Eur J Obstet Gynecol Reprod Biol. 2009;145(1):3–8.
-
19. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019. CA Cancer J Clin. 2019;69(1):7–34.
-
20. López-Valdés J, Méndez PJ, Albert C, Billroth T. Theodor Billroth: más de un siglo de su grandeza artística. Gac Med Mex 2014;150(2):189–94.
-
21. Favara DM. Theodor Billroth: A surgeon for the 21st century. Am Surg. 2014;80(12):1192–5.
-
22. Busman DC. Theodor Billroth 1829 -1894. Acta Chir Belg. 2006;106(6):743–52.
-
23. Majno G, Joris I. Billroth and Penicillium. Clin Infect Dis. 1979;1(5):880–4.
-
24. Stell PM. The first laryngectomy. J Laryngol Otol. 1975;89(4):353–8.
-
25. Stell PM. The First Laryngectomy for Carcinoma. Arch Otolaryngol. 1973;98(5):293.
-
26. Osborne MP. William Stewart Halsted: his life and contributions to surgery. Lancet Oncol. 2007;8(3):256–65.
-
27. Mukherjee S. El emperador de todos los males. Una biografía del cáncer. 2ª ed.. Barcelona: Debate; 2014.
-
28. Jones C, Lancaster R. Evolution of Operative Technique for Mastectomy. Surg Clin North Am. 2018;98(4):835– 44.
-
29. Cotlar AM, Dubose JJ, Rose DM. History of surgery for breast cancer: Radical to the sublime. Curr Surg. 2003;60(3):329–37.
-
30. Wright JR. The radicalization of breast cancer surgery: Joseph Colt Bloodgood’s role in William Stewart Halsted’s legacy. Bull Hist Med. 2018;92(1):141–71.
-
31. Lee KP. Caroline Hampton Halsted and the origin of surgical gloves. J Med Biogr. 2020;28(1):64–6.
-
32. Helsper JT. Dr. Hayes Martin: surgeon, leader, teacher, and founder of our society. Am J Surg. 1989;158(4):278– 82.
-
33. Shah JP. The making of a specialty. Am J Surg. 1998;176(5):398–403.
-
34. MacComb WS. Introduction to the Hayes Martin Memorial Lecture. A biographical treatise of Dr.Hayes E. Martin. Am J Surg. 1978;136(4):414.
-
35. Martin HE, Ellis EB. Biopsy by Needle Puncture and Aspiration. Ann Surg. 1930;92:169–81.
-
36. Frable WJ. Fine-needle aspiration biopsy: a review. Hum Pathol. 1983;14(1):9–28.
-
37. Diamantis A, Magiorkinis E, Koutselini H. Fine-needle aspiration (FNA) biopsy: Historical aspects. Folia Histochem Cytobiol. 2009;47(2):191–7.
-
38. Patel KN, Shah JP. Neck dissection: Past, present, future. Surg Oncol Clin N Am. 2005;14(3 ):461–77.
-
39. MARTIN H. Cancer of the head and neck. J Am Med Assoc. 1948;137(16):1366-1376.
-
40. Martin H, Del Valle B, Ehrlich H, Cahan WG. Neck dissection. Cancer. 1951 May;4(3):441–99.
-
41. Martin H. Radical neck dissection. Clin Symp. 1961;13:103–20.
-
42. Myers EN, Gastman BR. Neck Dissection: An Operation in Evolution: Hayes Martin Lecture. Arch Otolaryngol Neck Surg . 2003;129(1):14–25.
-
43. Baker HW. Needle aspiration biopsy (Hayes E. Martin). CA Cancer J Clin. 1986;36(2):69–70.
-
44. Mukherjee S. El Emperador de Todos los Males. Una Biografía del Cáncer. 2ª ed.. Barcelona: Debate; 2014.45.
-
45. Travis K. Bernard Fisher reflects on a half-century’s worth of breast cancer research.J Natl Cancer Inst. 2005;97:1636–7.
-
46. Sahli ZT, Smith PW, Umbricht CB, Zeiger MA. Preoperative molecular markers in thyroid nodules. Front Endocrinol (Lausanne). 2018;9:179.
-
47. Wolmark N. Bernard Fisher, 1918-2019. J Clin Oncol. 2020 Apr 14;38(16):1751–6.
-
48. Fisher B, Redmond CK, Fisher ER. Evolution of knowledge related to breast cancer heterogeneity: a 25-year retrospective. J Clin Oncol. 2008 May;26(13):2068–71.
Recibido: Noviembre 08, 2020
Aceptado: Noviembre 09, 2020
Correspondencia:
Álvaro Sanabria
alvarosanabria@gmail.com
Autores
1. Carlos García-Lozano. MD, Cirujano de Cabeza y Cuello. IPS Universitaria Clínica León XIII. Medellín, Colombia. Centro de Excelencia en Enfermedades de Cabeza y Cuello CEXCA, Medellín, Colombia.
2. Álvaro Sanabria. MD, MSc, PhD, FACS. Cirujano de Cabeza y Cuello. IPS Universitaria Clínica León XIII. Medellín, Colombia. Centro de Excelencia en Enfermedades de Cabeza y Cuello CEXCA, Medellín, Colombia. Profesor titular. Departamento de Cirugía. Universidad de Antioquia. Medellín, Colombia. Cirujano de Cabeza y Cuello. Hospital Universitario San Vicente Fundación. Medellín, Colombia.