La revolución (2010 – 2020)
En la última década se han identificado cerca de 20 blancos moleculares potencialmente modulables en cáncer de pulmón de células no pequeñas. Después del EGFR, el primer protagonista fue ALK, y la evolución del conocimiento permitió confirmar el desempeño de los inhibidores específicos de múltiples conductores, todos con mayor impacto vs. el uso de la quimioterapia (Figura 9).
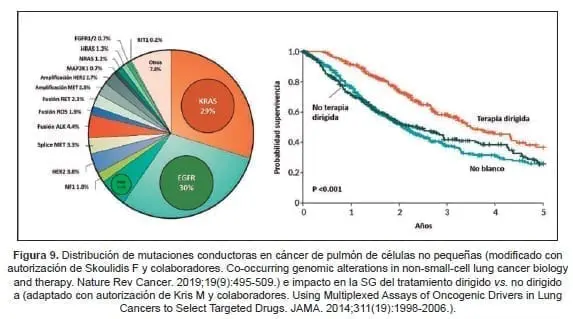
ALK en cáncer de pulmón como ejemplo de la oncología de precisión
El ALK (Anaplastic Lymphoma Kinase, CD246, NBLCT3) es un gen que codifica un receptor de tirosin quinasa que pertenece a la superfamilia de los receptores de insulina, parece estar implicado en el desarrollo primitivo del sistema nervioso central y genera una proteína transmembrana de 1620 (180 kDa) aminoácidos formada por un dominio extracelular que incluye un péptido señal amino terminal y un segmento intracelular con un espacio yuxtamembranoso que acoge el lugar de unión para el sustrato 1 del receptor y un dominio carboxiterminal.
El receptor se identificó por primera vez en 1994 como parte de la traslocación T (2;5) asociada a la mayoría de los linfomas anaplásicos de células grandes (4,5); su identidad se reveló gracias a la creación de una proteína quimérica vía traslocación entre cromosomas (2;5) (p23:q35) que generó un elemento de fusión NPM (Nucleofosmina)-ALK.
Las características globales del receptor no se conocieron hasta 1997 cuando se determinó que la región extracelular contiene una combinación única de dominios conocidos como MAM (meprin, A5 protein and receptor protein tyrosine phosphatase mu) y LDLa (low-density lipoprotein class A) (77).
Desde entonces, se han generado multiples referencias que resaltan la importancia de las alteraciones en este gen, asociado con el desarrollo de patologías como el cáncer de pulmón (≈5%), el tumor miofibrolástico inflamatorio (50%), los linfomas cutáneos (2%-30%), neuroblastoma (6%-8%), cáncer de tiroides (6%), cáncer de mama (2%-4%) y carcinoma de esófago (≈1%) (77).
En paralelo, se han diseñado y evaluado inhibidores del ALK de origen natural:
Como las estauroporinas o los inhibidores de la HSP90 (Hit Shock Protein 90), que no son específicos ni potentes; posteriormente, se incluyeron 9 subtipos diferentes de moléculas sintéticas pequeñas, incluyendo las aminopirimidinas (crizotinib), diaminopirimidinas, las piridoisoquinolinas, pirrolopiraosles, los indolocarbasoles, una pirrolopirimidina, una dianilinopirimidina, y dos moléculas sin estructura claramente definidas (78).
Después de una década contamos con tres compuestos de segunda generación en uso (ceritinib, alectinib y brigatinib), y uno de tercera generación (lorlatinib). Los resultados prometedores del estudio fase I de crizotinib (79) condujeron rápidamente al estudio PROFILE 1007 que comparó crizotinib con pemetrexed o docetaxel como segunda línea en pacientes con cáncer de pulmón de células no pequeñas localmente avanzado o metastásico con el reordenamiento de ALK después de progresar a un tratamiento previo con base en platino (80).
El desenlace primario fue la mediana para la SLP que resultó en 7,7 y 3,0 meses para el inhibidor de tirosin-quinasa y la quimioterapia (HR 0,49, P <0,001), respectivamente (justo antes, el crizotinib había recibido la aprobación acelerada por la FDA el 26 de Agosto de 2011).
En secuencia, el estudio PROFILE 1014 valoró la eficacia del crizotinib en comparación con la combinación de platino/pemetrexed como primera línea de intervención (81). La SLP en el grupo expuesto al inhibidor de tirosin-quinasa fue 10,9 meses en comparación con 7,0 meses para quienes recibieron quimioterapia estándar (HR 0,45, P <0,001), y la TRG fue del 74 y 45% para el crizotinib y la combinación con base en platino, respectivamente.
De igual forma, la administración del crizotinib se asoció con una reducción significativa de los síntomas derivados de la enfermedad, más impacto en la calidad de vida. Como resultado, y después del cambio en la historia para la población EGFR positiva, el crizotinib se convirtió en el medicamento estándar para el tratamiento de primera línea entre los pacientes con rearreglos de ALK (82).
A pesar de que el PROFILE 1014 no incluyó el mantenimiento con pemetrexed, intervención que impactó positivamente el control de la enfermedad en el estudio PARAMOUNT (83), el análisis final de la SG no alcanzó la mediana para los pacientes tratados con crizotinib, y fue de 45,8 meses para quienes iniciaron con la quimioterapia (HR 0,76, P=0,0978).
En concordancia, la SG a 4 años fue 56,6 y 49,1% para los pacientes tratados con crizotinib y quimioterapia, respectivamente. Después del ajuste del modelo de riesgos proporcionales el grupo de intervención demostró una reducción en el riesgo de muerte del 66% (84).
El uso rutinario del crizotinib desató el desarrollo del alectinib y brigatinib, y recientemente del lorlatinib.
El alectinib es un un inhibidor de segunda generación con actividad sobre ALK y RET desarrollado en Japón.
El estudio fase I/II (N=24) seleccionó como dosis óptima 300 mg c/12h, intervención que demostró en 46 pacientes una TRG del 93,5%, y una tasa de SLP y SG a 3 años del 63 y 78%, respectivamente (85).
La eficacia de la dosis de 600 mg c/12 h se evaluó en dos estudios fase II que incluyeron pacientes con resistencia adquirida o intrínseca al crizotinib. El primero (NP28673), reclutó 138 pacientes y mostró una TRG del 50% más una SLP de 8,9 meses (86).
El segundo (NP28761), evidenció resultados similares a partir del análisis de 87 pacientes que demostraron una TRG del 48% una SLP de 8,1 meses (87). Los hallazgos prometedores permitieron la aprobación acelerada del alectinib y la transición al diseño y ejecución de los estudios J-ALEX y ALEX, el primero en población japonesa, y el segundo, global. El J-ALEX incluyó 207 pacientes, la mediana para la SLP fue 34,1 meses y 10,2 para el crizotinib en primera línea (P <0,0001) (88).
El estudio ALEX comparó alectinib con crizotinib reclutó 303 pacientes (incluidos aquellos con enfermedad asintomática del SNC) que fueron asignados de forma aleatoria a recibir alectinib 600 mg c/12 h o crizotinib 250 mg c/12 h. La SLP en el grupo de alectinib fue superior al de crizotinib (34,8 meses frente a 10,9 meses, HR 0,50; P <0,001) (89).
A pesar de la disparidad de dosis del alectinib, ambos estudios ALEX mostraron una superioridad evidente del inhibidor de segunda generación sobre el crizotinib (90).
Conjuntamente, el alectinib demostró una elevada tasa de respuesta cerebral (64% y 22% respuesta completa) con una mediana de control basal en el sistema nervioso central del 36% a los 12 meses (91). En secuencia, se identificó que el alectinib tenía actividad contra la mutación gatekeeper L1196M.
La Figura 10 ilustra la rápida respuesta reflejo del uso del alectinib en un paciente con extenso compromiso visceral y ganglionar por un adenocarcinoma de pulmón ALK positivo.
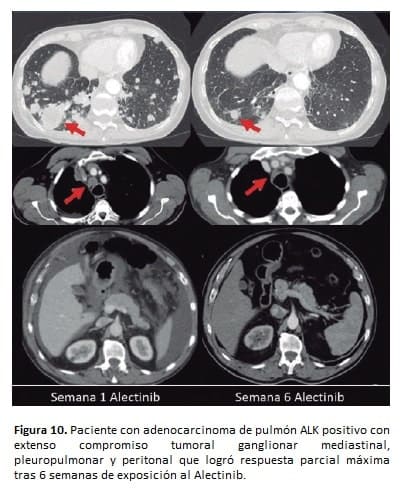
Brigatinib, otro inhibidor de ALK de segunda generación, se diferencia de otros en su amplia gama de propiedades inhibidoras contra varias mutaciones asociadas a resistencia.
El brigatinib inhibe eficazmente ALK y ROS1, y también puede revertir la resistencia a EGFR mediada por la presencia de las comutaciones C797S-T790M.
Diversos estudios sobre líneas celulares han permitido demostrar que la potencia del brigatinib in vitro e in vivo es 12 veces mayor que la del crizotinib. También se demostró que el brigatinib tiene capacidad inhibitoria sobre las 17 mutaciones secundarias de ALK, incluyendo la G1202R (92).
Después de superar la fase I/II, el estudio fase IIB ALTA incluyó 222 pacientes resistentes a crizotinib, entre los cuales el 74% también había recibido quimioterapia. La TRG fue 54% y la SLP fue 12,9 meses, superior a la descrita para el ceritinib y el alectinib en segunda línea (93).
Con base en los resultados del estudio ALTA-1L que incluyó 275 pacientes, se consideró la transición del brigatinib a primera línea, en particular, después de conocer el análisis interino preplaneado que encontró que los pacientes expuestos al inhibidor de segunda generación alcanzan una reducción en el riesgo de progresión del 51% respecto del crizotinib.
Entre aquellos con metástasis cerebrales de novo, la reducción en el riesgo de progresión o muerte fue del 80%.
Después de un año de tratamiento, el 67% de los pacientes expuestos al brigatinib permaneció libre de progresión, en comparación con el 43% de aquellos tratados con crizotinib y la mediana de SLP aún no había sido alcanzada por el brigatinib mientras fue de 9.8 meses para el de crizotinib. La TRG para el inhibidor de segunda generación fue del 71%, en comparación con el 60% alcanzado con el crizotinib.
A pesar de la diferencia negativa para los efectos adversos grado 3 (8%) y por la neumonitis en una mínima proporción de pacientes (3%), el beneficio con el brigatinib fue consistente entre las poblaciones, con especial énfasis en aquellos que debutan con alta carga de enfermedad y extensión al sistema nervioso central (94).
Lorlatinib, es un inhibidor ALK de tercera generación, fue diseñado específicamente para controlar las mutaciones que impulsan la resistencia y penetrar la barrera hematoencefálica.
Este inhibidor de tirosinquinasa macrocíclico de ALK y ROS1 revierte incluso la mutación G1202R (95,96). Las fases iniciales de demostraron una alta eficacia del lorlatinib en pacientes ALK positivos previamente tratados y con extensión al sistema nervioso central (97); en este segmento, la TRG fue 46% y la mediana de duración de la respuesta (DoR) fue 12,4 meses.
Además, el análisis de muestras pareadas de líquido cefalorraquídeo (LCR) y plasma mostró una alta penetración del fármaco a nivel cerebral donde la relación media de la concentración plasmática de lorlatinib fue 0,75 (75%), superior a la relación notificada del crizotinib (0,03). Sobre la base de la fase I y los datos de la II, se otorgó al lorlatinib una aprobación acelerada en la FDA el 2 de noviembre de 2018.
En un reciente ensayo global fase II, lorlatinib demostró una alta actividad intracraneal en pacientes con diagnóstico de novo, que habían recibido crizotinib u otros inhibidores de segunda generación (CC). En el estudio se incluyeron 276 pacientes que fueron asignados a seis cohortes (EXP1–6) sobre la base de la terapia previa utilizada, siendo el criterio principal de evaluación la TRG y la respuesta órgano específica a nivel cerebral.
Entre los pacientes sin tratamiento previo (EXP1), la respuesta objetiva se logró en 27 de 30.
Tres pacientes de esta cohorte tenían lesiones cerebrales basales logrando una respuesta intracraneal del 66,7%. La TRG en el subgrupo de pacientes pretratados con crizotinib fue 33% y 39% para aquellos expuestos a 2 o 3 inhibidores previos.
Recientemente, Shaw y colaboradores presentaron los resultados finales del estudio CROWN que comparó al lorlatinib con el crizotinib en 296 pacientes ALK positivos (98). Los resultados demostraron que el 78 y 39% de los pacientes no presentaban progresión de la enfermedad al año con el lorlatinib y el crizotinib, respectivamente (HR 0,28, P <0,001).
En adición, la TRG para la población general fue 76% con el inhibidor de tercera generación y 58% con el crizotinib, y del 82% entre aquellos con metástasis cerebrales expuestos al lorlatinib (71% de respuesta completa). Los eventos adversos más comunes con el lorlatinib fueron hiperlipidemia, edema, aumento de peso, neuropatía periférica y efectos cognitivos.
Los hallazgos de esta secuencia de experimentos clínicos son el mejor reflejo de los notables cambios que ha sufrido el cáncer de pulmón de células no pequeñas en la última década. La selección de las intervenciones y su mejor secuencia siguen ahora un patrón basado en los perfiles de resistencia valorado por secuenciación de siguiente generación (NGS) (Tabla 4).
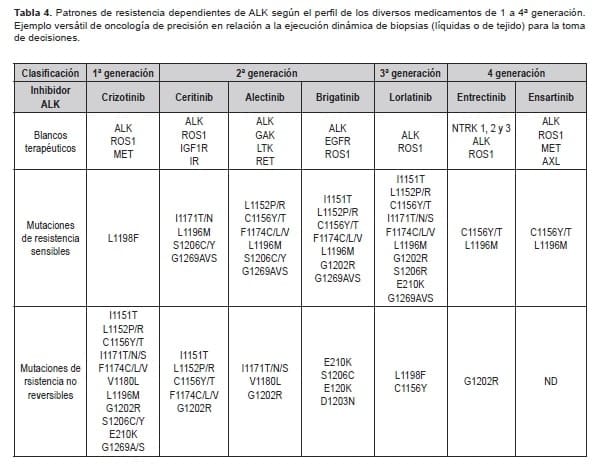
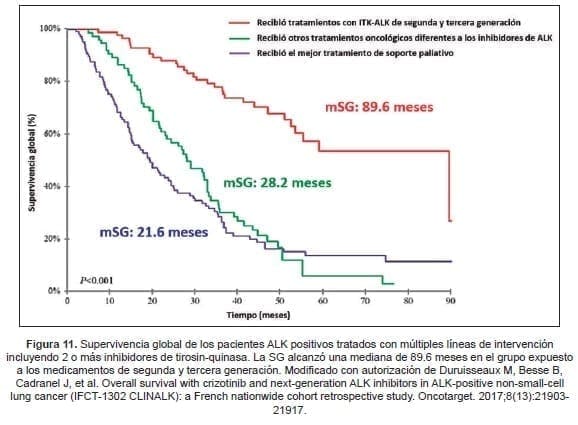
La confirmación en vida real viene de estudios como el IFCT-1302 CLINALK (N=209) que demostró que la exposición a los inhibidores del ALK de segunda y tercera generación impactó positivamente la SLP posterior al crizotinib (mediana 25 meses), y la SG a partir del diagnóstico de la enfermedad metastásica que alcanzó los 89,6 meses (7,4 años).
Este periodo temporal sigue el comportamiento de una enfermedad crónica, diferenciando la biología de los pacientes ALK del resto de los adenocarcinomas de pulmón, incluso en presencia de metástasis cerebrales o en el caso de presentar más de 3 órganos comprometidos por metástasis al momento del diagnóstico (99). La Figura 11 demuestra el impacto en la SG madura reproducida por ese estudio.
(Lea También: Cáncer de Cabeza Y Cuello: Una Perspectiva Histórica)
Todo cambia, nada es (evolución del tratamiento del cáncer de pulmón de células pequeñas)
El cáncer de pulmón de células pequeñas (SCLC, por sus siglas en inglés) representa entre el 12 y 15% de todos los casos de cáncer de pulmón, y se distingue del cáncer de pulmón de células no pequeñas por su agresividad biológica, alta tasa mitótica, y desarrollo temprano de metástasis, con especial énfasis en el sistema nervioso central (40%) (100).
Durante las últimas dos décadas, el patrón de presentación del SCLC ha seguido una tendencia constante, teniendo enfermedad limitada y extendida el 43 y 57%, respectivamente (101).
En 1973, el 1,5% de todos los pacientes con enfermedad extendida por SCLC alcanzaron 2 años de supervivencia. Este número aumentó a 4,6% en 2000 y fue 4,9% en 2015, lo que implicó una variación positiva del 3,4% en 47 años (102).
Oze y colaboradores analizaron los desenlaces de 10.262 pacientes con enfermedad extendida por SCLC incluidos en 52 estudios clínicos y 110 brazos de quimioterapia, intervenciones que posicionaron la combinación de cisplatino o carboplatino más etopósido como el estándar de tratamiento en primera línea desde 1985.
La integración de los datos también encontró que las combinaciones con base en platino modificaron la supervivencia libre de progresión (SLP) sin afectar la supervivencia global (SG).
A partir de 1990, la ganancia temporal estimada con la introducción de la quimioterapia clásica fue de 0,63 días/año, resultado que también se vio influenciado por el estado funcional de los pacientes y el uso de la radioterapia holocraneal profiláctica (103). La Figura 12 ilustra el mínimo impacto de la investigación en la historia de SCLC hasta 2019.
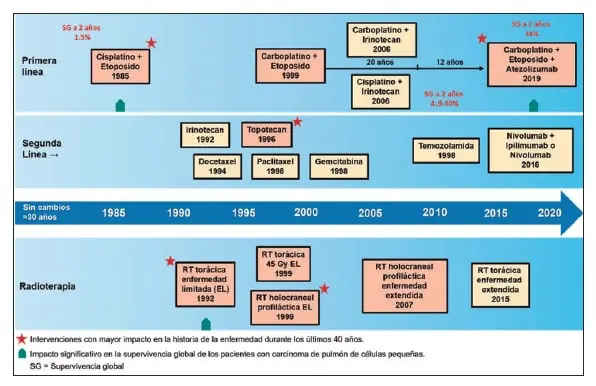
Figura 12. Cronología de los avances terapéuticos para el cáncer de pulmón de células pequeñas (SCLC, por su sigla en inglés). Esta línea de tiempo ilustra la escasez de nuevas opciones de tratamiento para los pacientes con SCLC durante las últimas tres décadas. Los recuadros sombreados en rojo representan las terapias estándar de atención que han sido aprobadas por la FDA y la EMA; los cuadros sombreados en amarillo representan terapias que han sido recomendadas por la National Comprenhensive Cancer Network (NCCN, Estados Unidos), pero que no cuentan con suficiente evidencia para considerarlas como estándar. Desde 1985 y hasta 2019, el régimen de quimioterapia con cisplatino y etopósido se mantuvo como el tratamiento sistémico de primera línea estándar para el manejo de los pacientes con SCLC y enfermedad extendida. Los regímenes posteriores, en los que el carboplatino o el irinotecan sustituyen al cisplatino o al etopósido, respectivamente, tienen una eficacia comparable, pero diferentes perfiles de toxicidad y han sido probados especialmente en población asiática. En 2019, y después de 35 años sin impactos notables en el curso de la enfermedad, se aprobó un nuevo modelo terapéutico que incluyó la combinación de carboplatino, etoposido y atezolizumab. Este nuevo régimen de tratamiento modificó notablemente la perspectiva de supervivencia a largo plazo. Las terapias de segunda línea que se recomiendan en las guías de la NCCN incluyen los inhibidores de la topoisomerasa, taxanos, agentes alquilantes y, desde 2016, la inmunoterapia. Sin embargo, la única intervención que agregó un beneficio real en este escenario ha sido la inmunoterapia. Para el SCLC que se presenta con enfermedad limitada (EL), se recomienda el uso temprano de la radioterapia en conjunto con quimioterapia, clásicamente a una dosis de 45 Gy administrada en 30 fracciones de 1,5 Gy dos veces al día (durante el curso de 3 semanas). De igual forma, y a pesar de la controversia, sigue en uso la irradiación craneal profiláctica (PCI). Recientemente, también se demostró que la radioterapia torácica proporciona algún beneficio en pacientes con enfermedad extendida que han respondido satisfactoriamente al tratamiento sistémico (Figura modificada con autorización de Gill J, Cetnar JP, Prasad V. A Timeline of Immune Checkpoint Inhibitor Approvals in Small Cell Lung Cancer. Trends Cancer. 2020 Sep;6(9):736-738. doi: 10.1016/j.trecan.2020.05.014. Epub 2020 Jun 29. y Sabari JK, Lok BH, Laird JH, et al. Unravelling the biology of SCLC: implications for therapy. Nat Rev Clin Oncol. 2017 Sep;14(9):549-561. doi: 10.1038/nrclinonc.2017.71. Epub 2017 May 23.).
La evaluación integrada de diversos estudios usando inmunoterapia como parte del tratamiento de primera línea para la enfermedad extendida por SCLC demostró a partir de 5 estudios fase III (IMpower-133, CASPIAN, KEYNOTE-604, CheckMate-451 y Reck 2016)) y uno fase IIB (ECOG-ACRIN 5161) que incluyeron en conjunto 3.609 pacientes, un impacto significativo en la SG, con una reducción del riesgo de muerte a 3 años del 16% (HR para la SG 0,84, IC 95% 0,78-0,90). La gran mayoría de los pacientes que participaron fueron hombres (2.382 sujetos), usualmente fumadores (95%) con una mediana de edad para el diagnóstico de la enfermedad de 64 años.
El mayor beneficio sobre la SG se encontró para los inhibidores de PD-L1 (especialmente, atezolizumab p<0,0001), hallazgo que también se mantuvo en el análisis meta-analítico de la SLP (SLP, p<0,00001). Adicionalmente, la ganancia global en SG osciló alrededor de los 3 meses, sin diferencia en la tasa de respuesta global (TRG) reflejando la quimiosensibilidad del SCLC, y consecuentemente la elevada respuesta en el grupo control (104).
El impacto descrito para la inmunoterapia en el estudio IMPower-133 demostró después de una mediana de seguimiento de 13,9 meses, que la SG fue mayor en el grupo que recibió carboplatino, etopósido y atezolizumab (CE+Atezolizumab) (mediana 12,3 meses; IC 95% 10,8-15,9) vs. el control expuesto a placebo (mediana 10,3 meses; IC 95% 9,3-11,3).
El análisis estratificado para la mortalidad demostró una reducción del riesgo del 30% (IC 95% 0,54-0,91; P=0,007) siendo la tasa de supervivencia global a un año del 51,7% en el grupo de atezolizumab y del 38,2% en el grupo de placebo (105).
La información actualizada en 2019 demostró que la adición del atezolizumab al régimen clásico de quimioterapia con base en platino aumentó la supervivencia a 18 meses hasta 34%, 1,6 veces más que el control. Este hallazgo permitió identificar que cerca de la tercera parte de los pacientes expuestos al atezolizumab serían largos supervivientes (106).
Para el cierre de información del 24 de Enero de 2019 y con una mediana de seguimiento de 22,9 meses en la población analizada con intención de tratamiento (373 pacientes) se encontró un número mayor de largos supervivientes en el grupo de CE+Atezolizumab (n=61, 33,5%; IC 95% 26,7-40,9) vs. el de CE+Placebo (n=39, 20,4%; IC 95% 14,9-26,8).
Cabe anotar que en el grupo expuesto al atezolizumab el IC para esta distribución fue el doble que para el placebo. Algunas de las características que se asociaron con una mejor supervivencia fueron la edad, el sexo, el estado funcional basal (ECOG), los niveles de LDH y la ausencia de enfermedad cerebral (107).
Estos datos fueron confirmados por el análisis para la población de pacientes que iniciaron el mantenimiento con atezolizumab y placebo, ya que los pacientes expuestos al anti-PD-L1 tuvieron una mediana de SG de 15,7 meses vs. 11,3 meses del placebo, diferencia a favor de una ganancia en SG de 4,4 meses.
En concordancia con los resultados del estudio IMPower- 133 se encuentran los hallazgos de Durvalumab, en particular porque confirman el papel de la inmunoterapia como estándar de tratamiento en conjunto con la combinación CE en SCLC.
En el estudio NCT01693562 (estudio fase I/II) los pacientes con enfermedad extendida recibieron Durvalumab 10 mg/kg cada 2 semanas después de una mediana de 2 líneas de tratamiento previo. La mayoría de los efectos adversos fueron 1 o 2 y la ORR fue del 9,5%.
Tras la demostración de seguridad, el Durvalumab demostró eficacia en el entorno de primera línea. El estudio CASPIAN fue un experimento clínico fase III, aleatorizado y abierto que demostró una ventaja en la SG para la combinación de Durvalumab más CE en comparación con la quimioterapia estándar (108).
El estudio tenía tres brazos de tratamiento, los dos mencionados previamente, y la combinación de Durvalumab más Tremelimumab, un inhibidor de CTLA-4. En 2019, se informaron los datos de la SG para el brazo CE+Durvalumab en comparación con el régimen CE (108).
El CASPIAN demostró una mejora significativa en la SG con una mediana de 13 meses en comparación con 10.3 meses para la quimioterapia sola, lo que representó una reducción del riesgo de muerte del 27% de muerte de 0,73 (HR 0,73, IC 95% 0,50-0,91; P=0,0047) (109). La razón de riesgo para la PFS fue de 0,78 (IC 95% 0,65-0,94), y la mediana para el grupo de tratamiento fue 5,1 meses frente a 5,4 meses del control. Esta información es análoga a la descrita extensamente para el IMpower-133.
Referencias
-
1. Wong MCS, Lao XQ, Ho KF, Goggins WB, Tse SLA. Incidence and mortality of lung cancer: global trends and association with socioeconomic status. Sci Rep. 2017 30;7(1):14300.
-
2. Howlader N, Forjaz G, Mooradian MJ, et al. The Effect of Advances in Lung-Cancer Treatment on Population Mortality. N Engl J Med. 2020;383(7):640-649.
-
3. Nwagbara UI, Ginindza TG, Hlongwana KW. Lung cancer awareness and palliative care interventions implemented in low-and middle-income countries: a scoping review. BMC Public Health. 2020;20(1):1466.
-
4. Adler I. Primary Malignant Growths of the Lungs and Bronchi. London: Longmans, 1912:22.
-
5. Ochsner A. My first recognition of the relationship of smoking and lung cancer. Prev Med 1973;2:611–14.
-
6. Wilks S, Bettany GT. A biographical history of Guy’s Hospital. London: Ward, Lock, Bowden. 1892.
-
7. Timmermann C. A History of Lung Cancer The Recalcitrant Disease . Palgrave Macmillan, London. 2015
-
8. Müller FH. Tabakmissbrauch und Lungencarcinom. Zeitschrift für Krebsforschung 1939;49:57–85.
-
9. Schairer E, Schöniger E. Lungenkrebs und Tabakverbrauch. Zeitschrift für Krebsforschung 1943;54:261–9.
-
10. Wynder EL, Graham EA. Tobacco smoking as a possible etiologic factor in bronchiogenic carcinoma; a study of 684 proved cases. J Am Med Assoc. 1950;143(4):329-36.
-
11. Doll R, Hill AB. The mortality of doctors in relation to their smoking habits. BMJ 1954;1:1451–5.
-
12. Hammond EC, Horn D. The relationship between human smoking habits and death rates: a follow-up study of 187,766 men. JAMA 1954;155:1316–28.
-
13. Brosch A. Theoretische und experimentelle Untersuchungen zur Pathogenesis und Histogenesis der malignen Geschwülste. Virchows Arch B Cell Pathol 1900;162:32–84.
-
14. Roffo AH. Durch Tabak beim Kaninchen entwickeltes Carcinom. Zeitschrift für Krebsforschung 1931;33:321.
-
15. Proctor RN. The Nazi War on Cancer. Princeton: Princeton University Press, 1999.
-
16. Wynder E, Graham EA, Croninger AB. Experimental production of carcinoma with cigarette tar. Cancer Res 1953;13:855–66.
-
17. Beyond Any Doubt. Time 1953:60–3.
-
18. Lewton LC. Substances present in tobacco smoke which are irritating to the nose and their removal by a new process. 1932.
-
19. Hilding AC. On cigarette smoking, bronchial carcinoma and ciliary action. New Engl J Med 1956;254:1155–60.
-
20. Auerbach O, Forman JB, Gere JB, Kassouny DY, Muehsam GE, Petrick HJ et al. Changes in the bronchial epithelium in relation to smoking and cancer of the lung. New Engl J Med 1957;256:97–104.
-
21. Roffo AH. Krebserzeugendes Benzpyren gewonnen aus Tabakteer. Zeitschrift für Krebsforschung 1939;49:588–97.
-
22. Fishel JB. Study of Cigarette Smoke [internet]. Legancy. library.ucsf.edu.1947 [consultado 14 noviembre 2020].Disponible en: http://legacy.library.ucsf.edu/tid/esa20e00
-
23. Proctor RN. Golden Holocaust: Origins of the Cigarette Catastrophe and the Case for Abolition. Berkeley: University of California Press, 2011.
-
24. Proctor RN. Tobacco and the global lung cancer epidemic. Nat Rev Cancer 2001;1:82–6.
-
25. Proctor RN. The history of the discovery of the cigarette- lung cancer link: evidentiary traditions, corporate denial, global toll. Tob Control. 2012 Mar;21(2):87-91..
-
26. Bates, Michael, ed. Bronchial Carcinoma: An Integrated Approach to Diagnosis and Management. Berlin: Springer, 1984.
-
27. Bleehen NM. Lung cancer–still a long road ahead. Br J Cancer. 1990 Apr;61(4):493–494.
-
28. Mountain CF. A new international staging system for lung cancer. Chest. 1986;89(4 Suppl):225S-233S. .
-
29. Cartei G, Cartei F, Cantone A, et al. Cisplatin-Cyclophosphamide- Mitomycin combination chemotherapy with supportive care vs. supportive care alone for treatment of metatstatic non-small cell lung cancer. J Natl Cancer Inst. 1993;85:794–800.
-
30. Rapp E, Pater JL, Willan A, Cormier Y, Murray N, Evans WK et al. Chemotherapy can prolong survival in patients with advanced non-small cell lung cancer—report of a Canadian multicenter randomized trial. J Clin Oncol. 1988;6:633–641.
-
31. Bonomi PD, Finkelstein DM, Ruckdeschel JC, Blum RH, Green MD, Mason B et al. Combination chemotherapy vs. single agents followed by combination chemotherapy in stage IV non-small-cell lung cancer: a study of the Eastern Cooperative Oncology Group. J Clin Oncol. 1989;7(11):1602–1613.
-
32. Crawford J, O’Rourke M, Schiller JH, Spiridonidis CH, Yanovich S, Ozer H et al. Randomized trial of vinorelbine compared with fluorouracil plus leucovorin in patients with stage IV non-small cell lung cancer. J Clin Oncol. 1996;14:2774–2784.
-
33. Sandler AB, Nemunaitis J, Denham C, et al. Phase III trial of gemcitabine plus cisplatin vs. cisplatin alone in patients with locally advanced or metastatic non-smallcell lung cancer. J Clin Oncol. 2000;18:122–130.
-
34. Wozniak AJ, Crowley JJ, Balcerzak SP, von Pawel J, Cormier Y, Gatzemeier U et al. Randomized trial comparing cisplatin with cisplatin plus vinorelbine in the treatment of advanced non-small-cell lung cancer: a Southwest Oncology Group study. J Clin Oncol. 16:2459–2465.
-
35. Kelly K, Crowley J, Bunn PA Jr, Presant CA, Grevstad PK, Moinpour CM et al. Randomized phase III trial of paclitaxel plus carboplatin vs. vinorelbine plus cisplatin in the treatment of patients with advanced non–smallcell lung cancer: a Southwest Oncology Group trial. J Clin Oncol. 2001 Jul 1; 19(13):3210-8.
-
36. Schiller JH, Harrington D, Belani CP. Eastern Cooperative Oncology Group. Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer. N Engl J Med. 2002;346(2):92-8.
-
37. Gridelli C, Gallo C, Shepherd FA, et al. Gemcitabine plus vinorelbine compared with cisplatin plus vinorelbine or cisplatin plus gemcitabine for advanced nonsmall- cell lung cancer: a phase III trial of the Italian GEMVIN Investigators and the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 2003;21(16):3025-34.
-
38. Fossella FV, DeVore R, Kerr RN, Crawford J, Natale RR, Dunphy F et al. Randomized phase III trial of docetaxel vs. vinorelbine or ifosfamide in patients with advanced non-small-cell lung cancer previously treated with platinum-containing chemotherapy regimens. The TAX 320 Non-Small Cell Lung Cancer Study Group. J Clin Oncol. 2000;18(12):2354-62.
-
39. Shepherd FA, Dancey J, Ramlau R, et al. Prospective randomized trial of docetaxel vs. best supportive care in patients with non-small-cell lung cancer previously treated with platinum-based chemotherapy. J Clin Oncol. 2000;18(10):2095-103.
-
40. Hanna N, Shepherd FA, Fossella FV, et al. Randomized phase III trial of pemetrexed vs. docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy. J Clin Oncol. 2004; 22(9):1589-97.
-
41. Shepherd FA, Rodrigues-Pereira J, Ciuleanu T, et al. Erlotinib in Previously Treated Non–Small-Cell Lung Cancer. N Engl J Med 2005;353:123-132.
-
42. Johnson DH, Fehrenbacher L, Novotny WF, et al. Randomized phase II trial comparing bevacizumab plus carboplatin and paclitaxel with carboplatin and paclitaxel alone in previously untreated locally advanced or metastatic non-small-cell lung cancer. J Clin Oncol. 2004; 22(11):2184-91.
-
43. Sandler A, Gray R, Perry MC, et al. Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer. N Engl J Med. 2006;355(24):2542-50.
-
44. Reck M, von Pawel J, Zatloukal P, et al. Overall survival with cisplatin-gemcitabine and bevacizumab or placebo as first-line therapy for nonsquamous non-small-cell lung cancer: results from a randomised phase III trial (AVAiL). Ann Oncol. 2010;21(9):1804-1809.
-
45. Scagliotti GV, Parikh P, von Pawel J, et al. Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced-stage non-small-cell lung cancer. J Clin Oncol. 2008;26(21):3543-51.
-
46. Monica V, Scagliotti GV, Ceppi P, Righi L, Cambieri A, Saviozzi S et al. Differential thymidylate synthase expression in different variants of large-cell carcinoma of the lung. Clin Cancer Res. 2009;15:7547-7552.
-
47. Cohen S. Isolation of a mouse submaxillary gland protein accelerating incisor eruption and eyelid opening the new-born animal. J Biol Chem 1962; 237: 1555-62.
-
48. Cohen S, Carpenter G, King L. Epidermal growth factor receptor protein kinase interactions. Copurification of receptor and epidermal growth factor-enhanced phosphorylation activity. J Biol Chem 1980; 255: 4834-42.
-
49. De Larco JE, Todaro GJ. Epithelioid and fibroblastic rat kidney cell clones: epidermal growth factor (EGF) receptors and the effect of mouse sarcoma virus transformation. J Cell Physiol 1978; 94: 335-42.
-
50. Ushiro H, Cohen S. Identification of phosphotyrosine as a product of epidermal growth factoractivated proteinkinase in A-431 cell membranes. J Biol Chem 1980; 255: 8363-5.
-
51. Burgess AW, Cho HS, Eigenbrot C, Ferguson KM, Garrett TP, Leahy DJ et al. An open-and-shut case? Recent insigths into the activation of EGF/Erb receptors. Mol Cell. 2003; 12: 541-52.
-
52. Grunwald V, Hidalgo M. Developing inhibitors of the epidermal growth factor receptor for cancer treatment. J Natl Cancer Inst. 2003;95:851-67.
-
53. Yarden Y, Sliwkowski MX. Untangling the ErbB signalling network. Nat Rev Mol Cell Biol. 2001;2:127-37.
-
54. Downward J,Yarden Y, Mayes E, et al. Close similarity of epidermal growth factor receptor and verb-B oncogene protein sequences. Nature 1984;307:521-7.
-
55. Riely GJ, Politi KA, Miller VA, Pao W. Update on epidermal growth factor receptor mutations in non-small cell lung cancer. Clin Cancer Res. 2006;12:7232-41.
-
56. Giaccone G, González-Larriba JL, van Oosterom AT, Alfonso R, Smit EF, Martens M et al. Combination therapy with gefitinib, an epidermal growth factor receptor tyrosine kinase inhibitor, gemcitabine and cisplatin in patients with advanced solid tumors. Ann Oncol. 2004;15:831-8.
-
57. Giaccone G, Herbst RS, Manegold C, Scagliotti G, Rosell R, Miller V et al. Gefitinib in combination with gemcitabine and cisplatin in advanced non-small cell lung cancer:A phase III trial-INTACT 1. J Clin Oncol. 2004;22(5):777-84.
-
58. Herbst RS, Giaccone G, Schiller JH, et al. Gefitinib in combination with paclitaxel and carboplatin in advanced non-small cell lung cancer:A phase III trial-INTACT 2. J Clin Oncol. 2004;22:785-94.
-
59. Giaccone G. The role of gefitinib in lung cancer treatment. Clin Cancer Res .2004;10(12 Pt 2):4233s-4237s.
-
60. Thatcher N, Chang A, Parikh P, Rodrigues J, Ciuleanu T, von Pawel J et al. Gefitinib plus best supportive care in previously treated patients with refractory advanced non-small-cell lung cancer: results from a randomised, placebo-controlled, multicentre study (Iressa Survival Evaluation in Lung Cancer). Lancet. 2005;366(9496):1527-37.
-
61. Gatzemeier U, Pluzanska A, Szczesna A, Kaukel E, Roubec J, Brennscheidt U et al. Results of a phase III trial or erlotinib (OSI-774) combined with cisplatin and gemcitabine (GC) chemotherapy in advanced non-small cell lung cancer (NSCLC). J Clin Oncol. 2007;25(12):1545-52.
-
62. Herbst RS, Prager D, Hermann R, Fehrenbacher L, Johnson BE, Sandler A et al. TRIBUTE-A phase III trial of erlotinib HCI (OSI-774) combined with carboplatin and paclitaxel (CP) chemotherapy in advanced non-small cell lung cancer. J Clin Oncol. 2005;23(25): 5892-9.
-
63. Miller V, Herbst RS, Hermann R. Long survival of never smoking non-small cell lung cancer (NSCLC) patients (pts) treated with erlotinib HCI (OSI-774) and chemotherapy: sub-group analysis of TRIBUTE. J Clin Oncol. 2004;22(14 suppl):7061.
-
64. Paez JG, Jänne PA, Lee JC, Tracy S, Greulich H, Gabriel S et al. EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science. 2004;304(5676):1497-1500.
-
65. Lynch TJ, Bell DW, Sordella R, Gurubhagavatula S, Okimoto R, Brannigan BW et al. Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib. N Engl J Med. 2004;350(21):2129-39.
-
66. Pao W, Miller V, Zakowski M, Doherty J, Politi K, Sarkaria I et al. EGF receptor gene mutations are common in lung cancers from ‘never smokers’ and are associated with sensitivity of tumors to gefitinib and erlotinib. Proc Natl Acad Sci USA 2004;101(36):13306-11.
-
67. Jänne PA. Challenges of detecting EGFR T790M in gefitinib/erlotinib-resistant tumours. Lung Cancer. 2008;60:3-9.
-
68. Sirera R, Catot S, González-Larriba JL, Masutti T, Moran T, Camps C et al. Customizing erlotinib in metastatic non-small cell lung cancer patients harboring EGFR mutations. ESMO 2008.
-
69. Mok T, Wu YL, Thongprasert S, Yang CH, Chu D , Saijo N, et al. Phase III, randomised, open-label, first-line study of gefitinib vs. carboplatin / paclitaxel in clinically selected patients with advanced nonsmall-cell lung cancer (IPASS). ESMO, 2008.
-
70. Arrieta O, Cardona AF, Martín C, et al. Updated Frequency of EGFR and KRAS Mutations in NonSmall- Cell Lung Cancer in Latin America: The Latin-American Consortium for the Investigation of Lung Cancer (CLICaP). J Thorac Oncol. 2015;10(5):838-843.
-
71. Costa DB, Kobayashi S, Tenen DG, Huberman MS. Pooled analysis of the prospective trials of gefitinib monotherapy for EGFR-mutant non-small cell lung cancers. Lung Cancer 2007; 58: 95-103.
-
72. Kobayashi K, Inoue A, Maemondo M, et al. First-line gefitinib vs. first-line chemotherapy by carboplatin (CBDCA) plus paclitaxel (TXL) in non-small cell lung cancer (NSCLC) patients (pts) with EGFR mutations: A phase III study (002) by North East Japan Gefitinib Study Group. J Clin Oncol. 2009;27:8016.
-
73. Rosell R, Moran T, Queralt C, et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J Med. 2009;361(10):958-67.
-
74. Mok TS, Wu YL, Thongprasert S, et al. Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma. N Engl J Med. 2009;361(10):947-57.
-
75. Scodes S, Cappuzzo F. Determining the appropriate treatment for different EGFR mutations in non-small cell lung cancer patients. Expert Rev Respir Med. 2020;14(6):565-576.
-
76. Bo Cheng, Shan Xiong, Caichen Li, et al. An annual review of the remarkable advances in lung cancer clinical research in 2019. J Thorac Dis. 2020;12(3): 1056– 1069.
-
77. Barreca A, Lasorsa E, Riera L, Machiorlatti R, Piva R, Ponzoni M et al. Anaplastic lymphoma kinase in human cancer. J Molec Endocrinol. 2011;47(1):R11-23.
-
78. Sasaki T, Rodig SJ, Chirieac LR, et al. The biology and treatment of EML4-ALK non-small cell lung cancer. Eur J Cancer. 2010;46(10):1773-80.
-
79. Solomon B, Varella-Garcia M, Camidge DR. ALK gene rearrangements: a new therapeutic target in a molecularly defined subset of non-small cell lung cancer. J Thorac Oncol. 2009;4(12):1450-4Kwak EL, Bang YJ, Camidge DR, et al. Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer. N Engl J Med. 2010 ;363(18):1693-703.
-
80. Saw AT, Kim DW, Nakagawa K, et al. Crizotinib vs. chemotherapy in advanced ALK-positive lung cancer. N Engl J Med. 2013; 368(25):2385-94.
-
81. Solomon BJ, Mok T, Kim DW, et al. PROFILE 1014 Investigators. First-line crizotinib vs. chemotherapy in ALK-positive lung cancer. N Engl J Med. 2014;371(23):2167-77.
-
82. Chuang JC, Neal JW. Crizotinib as first line therapy for advanced ALK-positive non-small cell lung cancers. Transl Lung Cancer Res. 2015;4(5):639-41.
-
83. Paz-Ares LG, de Marinis F, Dediu M, et al. PARAMOUNT: Final overall survival results of the phase III study of maintenance pemetrexed vs. placebo immediately after induction treatment with pemetrexed plus cisplatin for advanced nonsquamous non-small-cell lung cancer. J Clin Oncol. 2013;31(23):2895-902.
-
84. Solomon BJ, Kim DW, Wu YL, et al. Final Overall Survival Analysis From a Study Comparing First- Line Crizotinib Vs. Chemotherapy in ALK-Mutation- Positive Non-Small-Cell Lung Cancer. J Clin Oncol. 2018;36(22):2251-2258.
-
85. Seto T, Kiura K, Nishio M, et al. CH5424802 (RO5424802) for patients with ALK-rearranged advanced non-small-cell lung cancer (AF-001JP study): a single-arm, open-label, phase 1-2 study. Lancet Oncol. 2013;14(7):590-8.
-
86. Ou SH, Ahn JS, De Petris L, et al. Alectinib in crizotinibrefractory ALK-rearranged non-small-cell lung cancer: A phase II global study. J Clin Oncol. 2016;34(7):661–668.
-
87. Shaw AT, Gandhi L, Gadgeel S, et al. Alectinib in ALKpositive, crizotinib-resistant, non-small-cell lung cancer: a single-group, multicentre, phase 2 trial. Lancet Oncol. 2016;17(2):234-242.
-
88. Hida T, Nokihara H, Kondo M, et al. Alectinib vs. crizotinib in patients with ALK-positive non-small-cell lung cancer (J-ALEX): an open-label, randomised phase 3 trial. Lancet. 2017 ;390(10089):29-39.
-
89. Peters S, Camidge DR, Shaw AT, ALEX Trial Investigators. Alectinib vs. Crizotinib in Untreated ALKPositive Non-Small-Cell Lung Cancer. N Engl J Med. 2017;377(9):829-838.
-
90. Camidge DR, Dziadziuszko R, Peters S, et al. Updated Efficacy and Safety Data and Impact of the EML4-ALK Fusion Variant on the Efficacy of Alectinib in Untreated ALK-Positive Advanced Non-Small Cell Lung Cancer in the Global Phase III ALEX Study. J Thorac Oncol. 2019;14(7):1233-1243.
-
91. Mok TSK, Shaw AT, Camidge RD, et al. The updated OS and safety data from the randomised, phase III ALEX study of alectinib (alc) vs. crizotinib (crz) in untreated advanced ALK+ NSCLC. Ann Oncol. 2019;30(Supplement_5):v607.
-
92. Zhang S, Anjum R, Squillace R, et al. The Potent ALK Inhibitor Brigatinib (AP26113) Overcomes Mechanisms of Resistance to First- and Second-Generation ALK Inhibitors in Preclinical Models. Clin Cancer Res. 2016;22(22):5527-5538.
-
93. Gettinger SN, Bazhenova LA, Langer CJ, et al. Activity and safety of brigatinib in ALK-rearranged non-smallcell lung cancer and other malignancies: a singlearm, open-label, phase 1/2 trial. Lancet Oncol. 2016 ;17(12):1683-1696.
-
94. Camidge DR, Kim HR, Ahn MJ, et al. Brigatinib vs. Crizotinib in ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2018;379(21):2027-2039.
-
95. Solomon BJ, Besse B, Bauer TM, et al. Lorlatinib in patients with ALK-positive non-small-cell lung cancer: results from a global phase 2 study. Lancet Oncol. 2018;19(12):1654–1667.
-
96. Shaw AT, Felip E, Bauer TM, et al. Lorlatinib in nonsmall- cell lung cancer with ALK or ROS1 rearrangement: an international, multicentre, open-label, single-arm first-in-man phase 1 trial. Lancet Oncol. 2017;18(12):1590-1599.
-
97. Shaw AT, Bauer TM, de Marinis F, et al. First-Line Lorlatinib or Crizotinib in Advanced ALK-Positive Lung Cancer. N Engl J Med 2020;383:2018-2029
-
98. Duruisseaux M, Besse B, Cadranel J, et al. Overall survival with crizotinib and next-generation ALK inhibitors in ALK-positive non-small-cell lung cancer (IFCT-1302 CLINALK): a French nationwide cohort retrospective study. Oncotarget. 2017;8(13):21903-21917.
-
99. Saltos A, Shafique M, Chiappori A. Update on the Biology, Management, and Treatment of Small Cell Lung Cancer (SCLC). Front Oncol. 2020;10:1074.
-
100. Albain KS, Crowley JJ, Le Blanc M, Livingston RB. Determinants of improved outcome in small-cell lung cancer: An analysis of the 2,580-patient Southwest Oncology Group data base. J Clin Oncol.1990;8(9):1563-1574.
-
101. Govindan R, Page N, Morgensztern D, et al. Changing epidemiology of small-cell lung cancer in the United States over the last 30 years: analysis of the surveillance, epidemiologic, and end results database. J Clin Oncol. 2006;24(28):4539-44.
-
102. Oze I, Hotta K, Kiura K, et al. Twenty-seven years of phase III trials for patients with extensive disease smallcell lung cancer: disappointing results. PLoS One. 200913;4(11):e7835.
-
103. Landre T, Chouahnia K, Guetz GD, et al. Immune Checkpoint Inhibitor plus Chemotherapy vs. Chemotherapy alone as first line for Extensive-Stage-Small-Cell-Lung- Cancer: a meta-analysis. ESMO 2020 (Poster 1799)
-
104. Horn L, Mansfield AS, Szczęsna A, et al; IMpower133 Study Group. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. N Engl J Med. 2018;379(23):2220-2229.
-
105. Reck M, Liu SV, Mansfield AS, et al. IMpower133: Updated overall survival (OS) analysis of first-line (1L) atezolizumab (atezo) + carboplatin + etoposide in extensive- stage SCLC (ES-SCLC). Ann Oncol. 2019;30(Suppl 5):v710-v711.
-
106. Liu SV, Horn L, Mok T, et al. IMpower133: Characterisation of long-term survivors treated first-line with chemotherapy ± atezolizumab in extensive-stage small cell lung cancer. Ann Oncol. 2020;31(suppl_4):S974-S987.
-
107. Huang C, Gan GN, Zhang J. IMpower, CASPIAN, and more: exploring the optimal first-line immunotherapy for extensive-stage small cell lung cancer. J Hematol Oncol. 2020 Jun 5;13(1):69.
-
108. Paz-Ares L, Dvorkin M, Chen Y, et al; CASPIAN investigators. Durvalumab plus platinum-etoposide vs. platinum-etoposide in first-line treatment of extensivestage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet. 2019;394(10212):1929-1939.
Recibido: Diciembre 01, 2020
Aceptado: Diciembre 15, 2020
Correspondencia:
Oscar Arrieta
oscararrietaincan@gmail