
Respecto a las manifestaciones clínicas de la epilepsia rolándica, se encontró que la proporción de pacientes que presentó crisis solo en sueño (43%) fue similar a la proporción de pacientes que presentó crisis solo en vigilia (46%) y una proporción muy baja presentó crisis tanto en sueño como en vigilia (11%). El 76% de los pacientes había presentado un máximo de 4 crisis en total. Se describen las principales manifestaciones clínicas (Tabla 2). (Leer también: Caracterización de la epilepsia benigna de la infancia con puntas centrotemporales*)
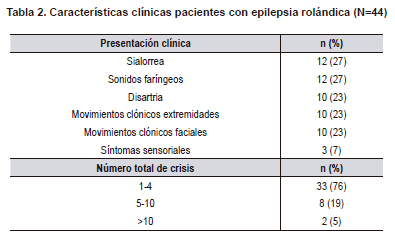
Solo en 10 pacientes se obtuvo el dato de la lateralidad de la crisis, siendo derecha en el 90% de los casos. En el 64% hubo generalización de la crisis y en el 36% se reportaron crisis con duración mayor a 5 minutos. Solo 1 paciente (2%) avisó el inicio de la crisis.
En la revisión de los electroencefalogramas se encontró que la actividad irritativa se presentaba en proporciones similares en el lado izquierdo y el lado derecho. La actividad irritativa encontrada estuvo representada principalmente por complejos punta-onda lenta (61%) y onda aguda-onda lenta (39%) focales. No se encontró actividad generalizada en ninguno de los pacientes (Tabla 3).
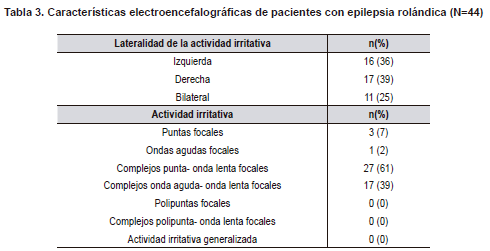
Se realizó la medición de los complejos punta-onda lenta y onda aguda-onda lenta (Tabla 4). En el 93% de los pacientes se encontró dipolo rolándico típico.

Al evaluar la actividad irritativa en sueño se encontró que esta era máxima en sueño NREM y no se encontró en REM. Las fases del NREM en las que se presentó la actividad irritativa fueron N1 (23%) y N2 (84%). El índice de actividad interictal en sueño fue bajo en el 59% de los pacientes (Figura 1).
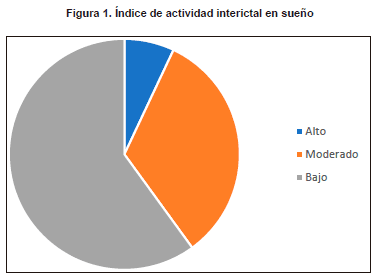
La actividad irritativa se presentó aislada en el 43% de los casos y en salvas en el 57%. Cuando se presentó en salvas, éstas estaban compuestas por máximo 5 complejos de punta-onda lenta u onda aguda-onda lenta en el 75% de los casos y solo en el 8% de los casos presentaban más de 10 complejos por salva.
Adicionalmente, se encontró que el 40% no presentaba actividad irritativa en vigilia, y el 60% que si la presentaba podía tener un índice de actividad en vigilia desde 1 hasta 29 por minuto, aunque en el 84% de los pacientes el índice era de 1-2/min.
Se presentó actividad extra centro-temporal en 9 pacientes (20%), siendo parietal en 5, occipital en 3 y frontal en 1.El 32% de los pacientes tenía antecedente familiar de epilepsia, siendo en el 79% de los casos un familiar de segundo grado quien presentaba este antecedente.
Solo en el 2% se encontró antecedente familiar de epilepsia rolándica. Otros antecedentes familiares documentados fueron TDAH (5%), trastorno del lenguaje (14%) y sonambulismo (16%). En los pacientes con epilepsia rolándica se encontraron como comorbilidades más frecuentes el bajo rendimiento escolar en 34%, trastorno del lenguaje en 25% y TDAH en 23% (Figura 2).
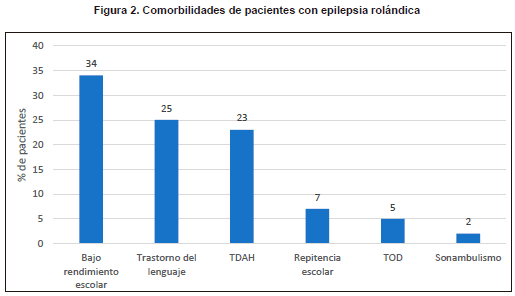
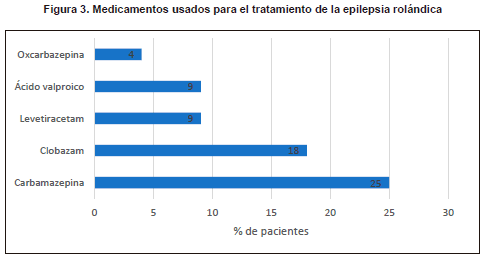
El 61% de los pacientes estaba recibiendo tratamiento farmacológico para la epilepsia, siendo la carbamazepina y el clobazam los medicamentos más usados, seguidos por levetiracetam, ácido valproico y oxcarbazepina (Figura 3). No se reportaron otros medicamentos. Todos los pacientes tenían control de la epilepsia y en ningún caso se reportó empeoramiento de la epilepsia con el tratamiento.
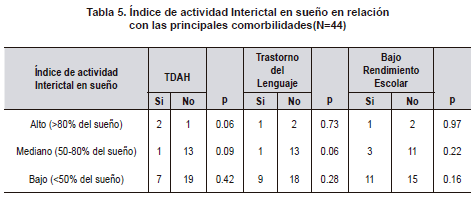
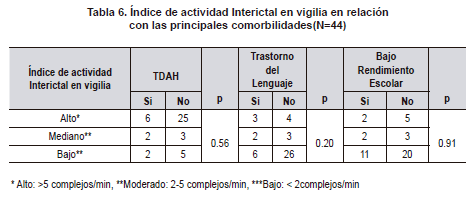
Se realizó un análisis exploratorio intentando determinar si algunas variables clínicas, eléctricas y/o familiares podían influir en la presentación de la epilepsia rolándica. Al evaluar si el índice de actividad interictal en sueño y vigilia se relacionaba con las comorbilidades TDAH, trastorno del lenguaje y bajo rendimiento escolar, no se encontraron diferencias significativas (Tablas 5 y 6).
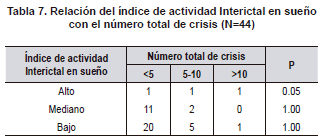
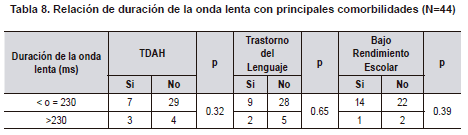
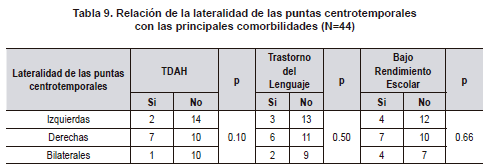
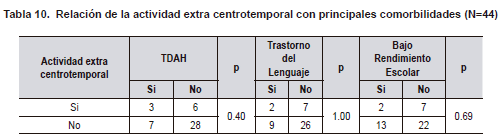
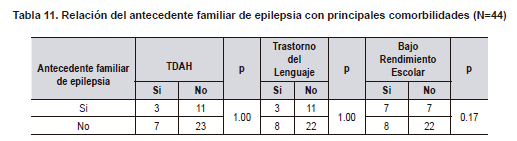
Al evaluar si el índice de actividad interictal en sueño se relacionaba con el número total de crisis, no encontramos diferencias significativas (Tabla 7). Al comparar la duración de la onda lenta, la lateralidad de las puntas centrotemporales, la actividad extra centrotemporal y el antecedente familiar de epilepsia con comorbilidades tampoco hubo diferencias (Tablas 8, 9, 10, 11). El voltaje de la punta u onda aguda no mostró ninguna relación con las principales comorbilidades.
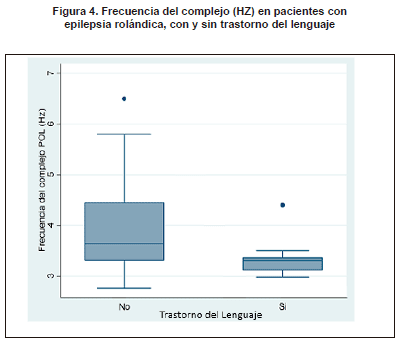
Cuando se revisó la relación entre la frecuencia de los complejos en Hz con las comorbilidades, no hubo diferencias para TDAH y bajo rendimiento escolar. Sin embargo en el caso del trastorno del lenguaje se encontró que la mediana de las frecuencias de los complejos en los pacientes con trastornos del lenguaje era más baja: 3.3 Hz, que en los pacientes sin trastorno del lenguaje: 3.6 Hz (p=0.02) (Figura 4). No hubo diferencias significativas al comparar el antecedente familiar de epilepsia según género (p=1.00).
Discusión
Como se ha mencionado previamente, la epilepsia benigna de la infancia con puntas centrotemporales es el síndrome epiléptico más frecuente de la infancia. Se ha descrito una predominancia masculina de 3: 1 (19), pero en nuestro estudio no encontramos diferencias significativas según el género.
Se sabe que este tipo de epilepsia inicia generalmente antes de los 13 años, con un pico de presentación a los 7-9 años (20); sin embargo, si bien en nuestro estudio el inicio de la epilepsia se dio antes de los 13 años, el promedio de edad de presentación fue a los 6,6 años, lo que está ligeramente por debajo de lo reportado.
Característicamente las crisis de la epilepsia rolándica se presentan durante el sueño en más del 50% de los casos y solo en vigilia en el 5-25% (21). En nuestra serie la proporción de crisis en sueño fue similar a la proporción en vigilia.
En general el número de crisis en este síndrome es bajo, siendo menor a 5 crisis en el 50% (22). En nuestra serie este porcentaje asciende a 76%.
En la revisión de Park et al (2015), se describe la frecuencia de los síntomas: Sonidos faríngeos 53%, disartria 40%, manifestaciones sensoriomotoras faciales 30%, sialorrea 30%. Estas últimas 2 manifestaciones se presentaron con una frecuencia muy similar en nuestro grupo de pacientes, pero la frecuencia de disartria y sonidos faríngeos estuvo casi un 50% por debajo de lo reportado en la literatura. Respecto a la generalización de las crisis que usualmente es cercana al 50%, se presentó en el 64% de nuestro grupo.
Al comparar las alteraciones electroencefalográficas reportadas en la revisión de Guerrini y Pellacani (2012), con nuestro estudio, podemos ver que en ambos se presenta activación de la actividad en sueño, esta actividad se presenta con frecuencia en salvas, sin formar polipuntas y la actividad irritativa es bilateral en cerca de un tercio de los pacientes.
Además, al evaluar las características electroencefalográficas clásicas de la epilepsia rolándica descritas por Kellaway en el 2000, encontramos que la duración promedio de la punta es de 74 ms, por lo que se considera que en realidad en este síndrome se presentan tanto puntas como ondas agudas, así el nombre del síndrome mencione solo puntas; las cuales son seguidas de onda lenta. En nuestros pacientes las puntas tuvieron duración promedio de 70.4 ms.
La amplitud de la punta es en promedio de 169 uV, llegando incluso hasta 300 uV. En nuestra serie el promedio de la amplitud fue un poco más baja: 122,1 uV.
Al igual que Kellaway, encontramos que la actividad rolándica se presenta principalmente en sueño NREM y es menos frecuente en vigilia. Por otro lado, Blume et al (1984) describió que la frecuencia en Hz de los complejos POL u onda aguda-onda lenta en pacientes con epilepsia rolándica era de 1,5-3 Hz (22) lo que difiere de nuestra serie en la que encontramos frecuencias promedio de 3,87 Hz.
Respecto a los antecedentes familiares de pacientes con epilepsia rolándica se ha reportado que hasta el 10% de los pacientes tienen antecedente familiar de epilepsia (23), lo que contrasta con el 32% en nuestros pacientes. Así también antecedente familiar de trastorno del lenguaje en 17% (24), similar a lo encontrado en nuestro estudio: 14 %. No hay datos respecto al antecedente familiar de TDAH, ni sonambulismo.
Los estudios que han evaluado comorbilidades en niños con epilepsia rolándica han reportado TDAH en 19-68%, bajo rendimiento escolar en el 30% y trastorno del lenguaje en el 29% (24-25). En nuestros pacientes encontramos estas comorbilidades en el 23%, 34% y 25% respectivamente, lo cual es similar a lo reportado en la literatura.
El estudio realizado por Liu et al en 2017, con 1817 pacientes, evaluó el uso de tratamiento anticonvulsivo en este síndrome epiléptico, encontrando que el 75% recibía tratamiento, siendo los medicamentos más frecuentemente utilizados: Oxcarbazepina 37%, ácido valproico 25% y levetiracetam 19% (26).
Dichos hallazgos difieren de lo encontrado en nuestros pacientes, quienes se encontraban en tratamiento farmacológico principalmente con carbamazepina y clobazam, siendo el uso de ácido valproico, levetiracetam y oxcarbazepina menos frecuente.
Sin embargo, todos los pacientes se encontraban controlados, lo que podría sugerir una eficacia similar de los medicamentos utilizados.Cuando se han evaluado las características electroencefalográficas y clínicas de la epilepsia rolándica no se han encontrado muchos factores que se correlacionen con la forma de presentación, evolución, ni comorbilidades (27).
Se plantea en un estudio (28) que la demora en el inicio del tratamiento puede ser un factor que favorece la evolución inadecuada y otro estudio reciente (29) propone que los ripples (80-250 Hz) superimpuestos a las puntas rolándicas en el EEG de superficie son útiles para predecir evolución en epilepsia rolándica. Estos aspectos no fueron valorados en nuestros pacientes.
Dado que existen pocos factores reportados como indicadores de mal pronóstico en epilepsia rolándica, decidimos realizar un análisis exploratorio para evaluar la relación de algunas variables electroencefalográficas con la presencia de comorbilidades y con la frecuencia de las crisis, sin que encontráramos diferencias estadísticamente significativas, excepto cuando evaluamos la frecuencia de los complejos (Hz) con la presencia de trastorno del lenguaje como comorbilidad.
La mediana de la frecuencia de los complejos fue menor en los pacientes con trastorno del lenguaje (3,3 Hz) respecto a los pacientes sin trastorno del lenguaje (3,6 Hz) con p= 0,02. Esto no ha sido descrito previamente por lo que sería interesante evaluar esta relación en series más grandes.
Este estudio puede valorarse como un continuo de alteraciones que parten desde un paciente con crisis aisladas hasta otros con crisis frecuentes y alteraciones cognitivas severas que afectan el lenguaje y el aprendizaje. La caracterización del cuadro clínico de la enfermedad se realizó hace más de tres décadas y se encuentran numerosos artículos en este sentido en la literatura. En el momento actual se están investigando los factores de riesgo que pudieran explicar el pronóstico del niño y se está profundizando en los aspectos genéticos.
Debido al hecho de que se trata de un estudio retrospectivo en pacientes atendidos en dos centros, el tamaño de la muestra resulta inadecuado para sacar conclusiones en los hallazgos descriptivos y en la asociación de las variables, aunque hemos revisado estudios similares en otras partes del mundo, aparecidos en el último lustro.
Encontramos sin embargo unos datos interesantes que deben profundizarse: por ejemplo, los complejos punta onda lenta con frecuencias más bajas (Hz) estuvieron más relacionados con trastornos del lenguaje; y la frecuente comorbilidad de la epilepsia rolándica con bajo rendimiento escolar, TDAH y trastorno del lenguaje.
Es posible continuar el análisis con pacientes estudiados en otras instituciones a nivel local y nacional, para poder realizar un estudio analítico en el que se evalúen varios factores de riesgo que generen información que ayude en el proceso de toma de decisiones cuando haya preguntas para tratar de explicar mejor este cuadro.
Aunque este es un tema frecuente en neurología pediátrica, esta es la primera descripción al respecto en nuestro medio. Para respaldar lo observado en esta muestra de pacientes, se requieren estudios con tamaños de muestra mayores e idealmente con diseño prospectivo para determinar las implicaciones de estos hallazgos.
Referencias
1. Lundberg S. Rolandic epilepsy: A Neuroradiological, neuropsychological and oromotor study. Compre-hensive Summaries of Uppsala Dissertations from the Faculty of Medicine. Acta Univ Upsal: Uppsala University; 2004.
2. Commision on classification and terminology of the International League against Epilepsy. Proposal for revised classification of epilepsies and epileptic syndromes. Epilepsia. 1989; 30: 389-99.
3. Chahine L, Mikati M. Benign pediatric localization-related epilepsies: Part II: Syndromes in childhood. Epileptic Disorders. 2006; 8(4):243-58.
4. Engel J. Report of the ILAE classification core group. Epilepsia. 2006; 47(9):1558-68.
5. Panayiotopoulos CP. Benign childhood focal seizures and related epileptic syndromes. In: Panayiotopoulos CP, editor. The Epilepsies: Seizures, Syndromes and Management. 1 ed. Oxford: Bladon Medical Publishing; 2005. p. 223-34.
6. Astradsson A, Olafsson E, Ludvigsson P, Björgvinsson H, Hauser WA. Rolandic epilepsy: An incidence study in Iceland. Epilepsia. 1998; 39(8):8846.
7. Perkins FF, Breier J, McManis MH, Castillo E, Whe¬less J, McGregor AL, et al. Benign rolandic epilepsy-perhaps not so benign: use of magnetic source imaging as a predictor of outcome. J Child Neurol. 2008; 23(4): 389-93.
8. Bulgheroni S, Franceschetti S, Vago C, Usilla A, Pan¬taleoni C, D’Arrigo S, et al. Verbal dichotic listening performance and its relationship with EEG features in benign childhood epilepsy with centrotemporal spikes. Epilep Res. 2008; 21 (79): 31-8.
9. Fonseca L, Tedrus G, Campregher AA, Capatto M. Benign childhood epilepsy with centrotempo¬ral spikes: A longitudinal neuropsychological and electroencephalographic study. Clin Neurophysiol. 2008; 119:S84.
10. Legarda S, Jayakar P. Electroclinical significance of rolandic spikes and dipoles in neurodevelopmentally normal children. Electro-encephalogr Clin Neurophy¬siol. 1995; 95:257-9.
11. Tsai M, Hung K. Topographic mapping and clinical analysis of benign childhood epilepsy with centro¬temporal spikes. Brain & Dev. 1998; 27–32.
12. Tavares S, Almeida RM, Figueroa SM, Temudo T. Epilepsia rolándica. Análisis de las características clínicas, electrofisiológicas, tratamiento y pronóstico en 87 pacientes. Rev Neurol. 2005; 41:327-30.
13. Dos Santos Riesgo R, Jayakar P, Tellechea Rotta N. Benign rolandic epilepsy: clinical and electroen¬cephalographic correlates. Arq Neuropsiq. 2000; 58(3-B):852-61.
14. Kellaway P. The electroencephalographic features of benign centrotemporal (rolandic) epilepsy of chil¬dhood. Epilepsia. 2000; 41(8):1053-6.
15. Drury I. EEG in benign and malignant epileptic syn¬dromes of childhood. Epilepsia. 2002; 43(S3):17-26.
16. Neubauer BA. The genetics of rolandic epilepsy. Epilepsia. 2000; 41(8):10612.
17. Willmore LJ, Ueda Y. Genetics of epilepsy. J Child Neurol. 2002; 17:S18-S27.
18. Mellish L, Dunkley C, Ferrie C, Pal D. Antiepileptic drug treatment of rolandic epilepsy and Panayiotopoulos syndrome: clinical practice survey and clinical trial feasibility. Arch Dis Child. 2015; 100:62–67.
19. Saeed M, Azam M, Shabbir N, Qamar ShA. Is Benign Childhood epilepsy with centrotemporal spikes always Benign? Iran J Child Neurol. 2014 ; 8(3): 38-43.
20. Park J, Shahid A, Jammoul A. Common Pediatric Epilepsy Syndromes. Pediat Ann 2015 ;44(2):e30-5.
21. Guerrini R, Pellacani S. Benign childhood focal epi¬lepsies. Epilepsia. 2012; 53(Suppl. 4): 9–18.
22. Blume WT, Young GB, Lemieux JF. EEG morphology of partial epileptic seizures. Electroencephalogr Clin Neurophysiol. 1984; 57(4):295-302.
23. Ma C, Chan K. Benign childhood epilepsy with cen¬trotemporal spikes: a study of 50 Chinese children. Brain & Develop. 2003; p. 390–395.
24. Vega Y, Smith A, Cockerill H, Tang S, Agirre Z, Goyal S. Risk factors for reading disability in rolandic epi¬lepsy families. Epilepsy Behav. 2015; 53: 174–179.
25. Pérez A, López L, García J, Calleja M, Lastaño C, Losada R, Fournier C. Epilepsias benignas de la infancia: dificultades académicas y alteraciones comportamentales. Rev Neurol. 2012; 54 (1): 17-23.
26. Liu M, Su X, Shi X, Wu G, Zhang Y, Gao L, et al. Clinical features of benign epilepsy of childhood with centrotemporal spikes in chinese children. Medicine. 2017; 96:4.
27. Fonseca L, Tedrus G, De Camargo E, Berretta M, Campregher A, Costa D. Benign childhood epilepsy with centro-temporal spikes: correlation between clinical, cognitive and EEG aspects. Arq Neuropsi-quiatr. 2007; 65(3-A):569575.
28. Fenglai X, Dongmei A, Sihan C, Jiechuan R, Dong Z. Clinical and Electroencephalographic (EEG) Features Associated With Refractoriness in Benign Childhood Epilepsy With Centrotemporal Spikes. Journal of Child Neurology. 2015; 1-7.
29. Van Klink N, Van ‘t Klooster M, Leijten F, Jacobs J, Braun K, Zijlmans M. Ripples on rolandic spikes: A marker of epilepsy severity. Epilepsia. 2016; 1–11.
Recibido: 29 de agosto de 2017.
Aceptado: 11 de septiembre de 2017.
Correspondencia:
Yuly Mildred Bayona Ovalles
yulybayonao@gmail.com

