Aunque por décadas se tuvo como paradigma que neurona que moría era reemplazada por tejido glial (de sostén) que actuaba como cicatriz y era considerado inactivo, en años recientes se ha observado que el cerebro tiene una capacidad para renovar o reconectar sus circuitos neuronales para así realizar nuevas tareas –en caso de lesión, por ejemplo después de un accidente cerebro-vascular- lo que se conoce como plasticidad neuronal.
Por supuesto que en lesiones agudas de este tipo, en las que ocupan espacio o en las traumáticas, ocurre mucha disfunción por edema o por sangrado, cuya desaparición contribuye a la recuperación funcional. Es también asunto aparte la neuroprotección que pueda lograrse con anticoagulantes o antiplaquetarios, generalmente en etapas muy iniciales del proceso trombótico (en el caso del ACV), en el que se puede evitar o reducir el tamaño del infarto cerebral, tal como se puede lograr en los infartos del miocardio de muy reciente iniciación. Esta plasticidad sin embargo es más notoria en cerebros infantiles que en los de adultos.
Otra cosa es la neurogénesis. Ya no se trata de la mejoría en la eficacia de la función neuronal, o el uso de otras vías nerviosas que los procesos rutinarios mantienen sin uso.
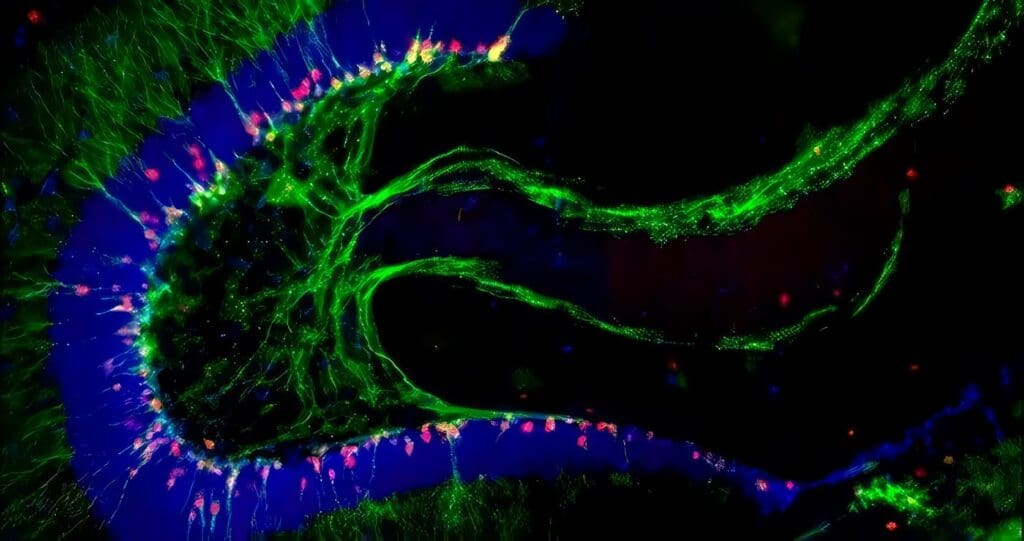
Es la aparición de nuevas neuronas (no sabemos si con idéntica función a las muertas), que se ha demostrado en el giro dentado del hipocampo y en el bulbo olfatorio de mamíferos adultos. Los precursores primarios se han identificado en nichos neurogénicos donde la célula que da origen a las nuevas neuronas expresa marcadores de glia, cuyo linaje celular es lejano al de las neuronas.
La glía radial no sólo origina astrocitos, sino también neuronas, oligodendrocitos y células ependimales. La neurogénesis en niños, organismos animales más sencillos o en el hipocampo y bulbo olfatorio se ha comprobado pero la neurogénesis en el neocórtex de primates adultos permanece cuestionado. Sin embargo, el grupo de Elizabeth Gould –de la Universidad de Princeton- encontró en 1999 que los macacos adultos tienen la capacidad de producir neuronas inmaduras en un área del cerebro llamada zona subventricular.
La aparición de estas nuevas neuronas se detectó en los márgenes cerebrales de los ventrículos cerebrales. Posteriormente, las células recién creadas emigran a varias zonas de la corteza. Unos meses después, el grupo de biología celular de la Universidad de Valencia encontró que en humanos se producía neurogénesis a partir de astrositos, en el hipocampo y en los ventrículos laterales del estriado-septum.
Esto implica la presencia allí de células madre pluripotenciales, y genera optimismo en la investigación sobre el manejo de enfermedades degenerativas del sistema nervioso y de las cada vez más frecuentes demencias asociadas con el envejecimiento. El cerebro de los mamíferos se desarrolla como un tubo que contiene un compartimiento ventricular lleno de líquido. Las células “madre” residen en la capa de células luminales en la zona ventricular, dónde se dividen rápidamente, inicialmente formando neuronas.
La profesora Gould insiste en que hay neurogénesis del adulto en la neocorteza, el estriado, la amígdala y la sustancia negra, aunque esto ha sido difícil de reproducir consistentemente excepto en cerebros dañados. Dice que las discrepancias entre varios estudios puede deberse a variaciones en la sensibilidad de los métodos usados para detectar nuevas neuronas.
Estas neuronas generadas de novo se integran funcionalmente y podrían estar implicadas en procesos de memoria y aprendizaje, así como en el mantenimiento del estado de ánimo. De hecho, se ha descrito que una disminución de la neurogénesis en el adulto induce trastornos depresivos, y que la eficacia del tratamiento con antidepresivos depende de la generación de nuevas neuronas en el hipocampo. En este proceso participan hormonas (factores de crecimiento, hormonas tiroideas), al tiempo que se observa que un porcentaje de pacientes hipo e hipertiroideos, pueden desarrollar depresión en asocio con su enfermedad hormonal.
 Como una de las hipótesis sobre los mecanismos moleculares de los antidepresivos sugiere que haya una estimulación de la señalización por factores de crecimiento y una neurogénesis en el hipocampo, Warner-Schmidt y Duman investigaron los efectos de diferentes clases de antidepresivos en la expresión en el hipocampo del factor de crecimiento endotelial vascular (VEGF), neurotrófico y proangiogénico.
Como una de las hipótesis sobre los mecanismos moleculares de los antidepresivos sugiere que haya una estimulación de la señalización por factores de crecimiento y una neurogénesis en el hipocampo, Warner-Schmidt y Duman investigaron los efectos de diferentes clases de antidepresivos en la expresión en el hipocampo del factor de crecimiento endotelial vascular (VEGF), neurotrófico y proangiogénico.
Su acción se potencia con los tratamientos electro convulsivos o electrochoques. En ratas tratadas por dos semanas con el antidepresivo fluoxetina (inhibidor de la recaptación de la serotonina) y con desipramina (inhibidor de la recaptación de la norepinefrina), aumentó la cantidad de VEGF mRNA en la capa granular del hipocampo y también la abundancia del VEGF en los homogenados de hipocampo.
El bloqueo farmacológico del receptor Flk-1 del VEGF inhibió el aumento de la proliferación celular en la zona subgranular del hipocampo producida por electrochoques por el tratamiento crónico con estos antidepresivos, mientras que el suministro intracerebroventricular de una isoforma de VEGF aumentó la proliferación de esa zona subgranular.
El bloqueo del receptor Flk-1 inhibió los efectos de la desipramina en las respuestas de la conducta de las ratas en modelos de depresión crónica y subcrónica, mientras que el VEGF tuvo un efecto antidepresivo. Como los antidepresivos promovieron la proliferación de las células endoteliales y la neurogénesis del hipocampo, los autores sugirieron que este mecanismo puede jugar un papel en el tratamiento de ciertas formas de depresión asociadas con anormalidades vasculares.
Gould E. How widespread is adult neurogenesis in mammals? Nat Rev Neurosci. 2007 ; 8(6):481-8
Warner-Schmidt JL, Duman RS. VEGF is an essential mediator of the neurogenic and behavioral actions of antidepressants. Proc Natl Acad Sci U S A. 2007 Mar 13;104 (11):4647-52
Warner-Schmidt JL, Duman RS. Hippocampal neurogenesis: opposing effects of stress and antidepressant treatment. Hippocampus. 2006;16(3):239-49
Kornack, D. and Rakic, P. “Cell Proliferation Without Neurogenesis in Adult Primate Neocortex,” Science, Vol. 294, December 7, 2001, pages 2127-2130.
Montero A, Fernández Y y col. Acciones de las hormonas tiroideas en el cerebro de mamíferos adultos.