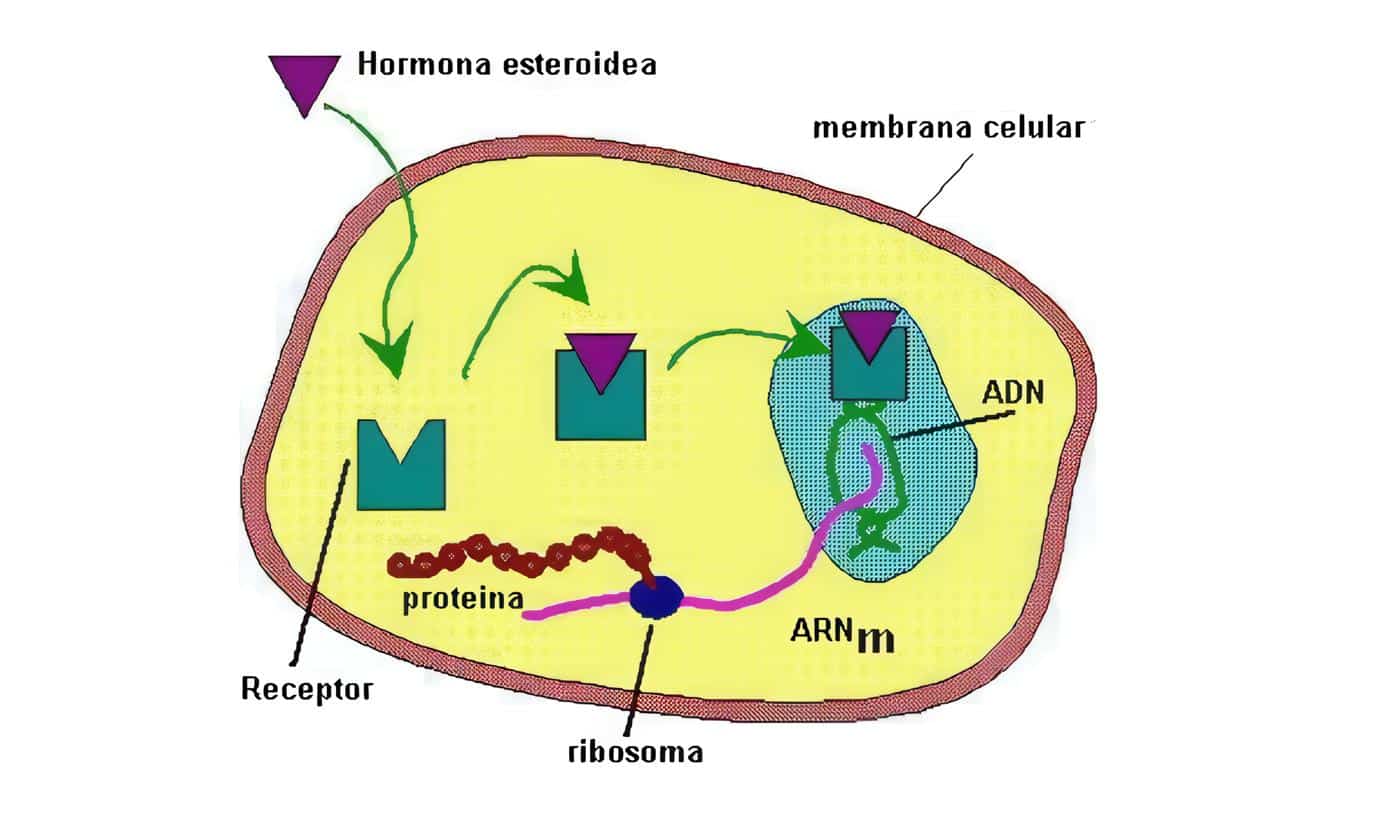
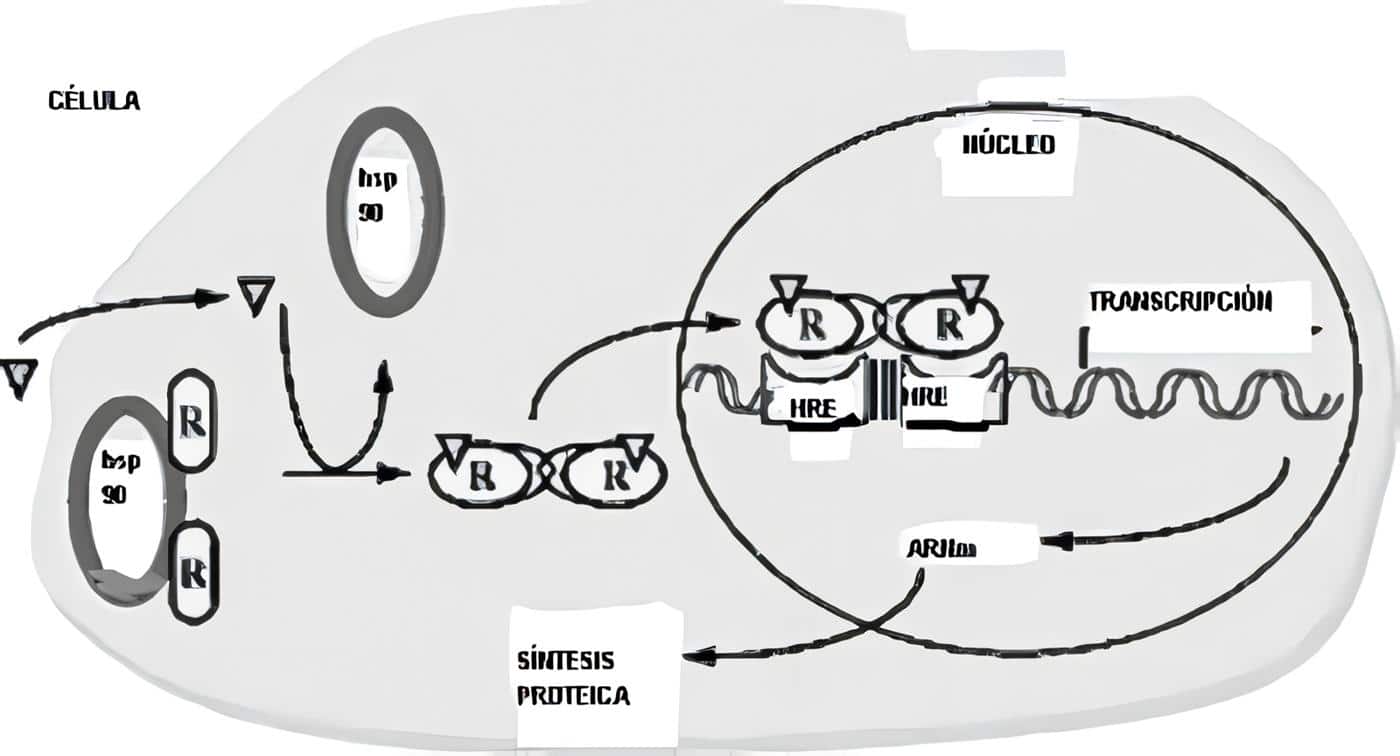
Glicoproteínas
 Hormonas hipofisarias luteinizante (LH), la folículo-estimulante (FSH) y la gonadotropina coriónica (HCG), son las hormonas gonadotrópicas. Estas – y la TSH- son glicoproteínas. En hombres y mujeres, la síntesis y secreción de FSH y LH es realizada por el gonadotropo.
Hormonas hipofisarias luteinizante (LH), la folículo-estimulante (FSH) y la gonadotropina coriónica (HCG), son las hormonas gonadotrópicas. Estas – y la TSH- son glicoproteínas. En hombres y mujeres, la síntesis y secreción de FSH y LH es realizada por el gonadotropo.
Como informábamos anteriormente, la sub-unidad alfa es idéntica en estas hormonas y tiene 89 aminoácidos, y la que cambia es la sub-unidad beta. Ambas gonadotropinas tienen el mismo número de aminoácidos –ciento quince- y su secreción es regulada por la gonado-relina hipotalámica.
En las mujeres, la progesterona y los estrógenos inhiben la liberación de LH y FSH, mientras que en los hombres son la testosterona y el estradiol las que inhiben la secreción de gonadotropina. Ambas glicoproteínas actúan en las fases finales de maduración del folículo ovárico, estimulando la descarga estrogénica.
El feedback es negativo sobre la LH cuando los niveles estrogénicos están bajos o constantes, pero si son niveles altos –cuando el folículo está maduro- el feedback es positivo y se produce el pico de LH que genera la ovulación unas nueve horas después. La LH continúa luego promoviendo la formación del cuerpo lúteo, que produce progesterona.
Otra regulación de la secreción gonadrópica es realizada por la inhibina, un péptido producido por ovarios y testículos en respuesta a la FSH. La inhibina suprime selectivamente la síntesis de FSH y su secreción, sin efectos en la síntesis y secreción de LH .
En los hombres la liberación de LH y FSH es parecida:
Aunque los impulsos de LH son mayores que la de los de FSH (Figura 5) y este patrón paralelo de secreción persiste durante toda la vida masculina. Durante la vida fértil de la mujer ocurre un patrón más complejo de secreción de LH y FSH, como resultado del ciclo menstrual.
En la menopausia cesa la función de los ovarios. Al no haber hormonas femeninas ni inhibina para suprimir la secreción de LH y FSH, se produce un gran aumento de FSH, con niveles más altos que los de LH. 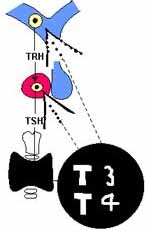
Resumiendo -en mujeres sexualmente maduras- la FSH (con la ayuda de la LH) actúa sobre el folículo para producir la liberación de estradiol (E2) y –en los hombres con maduración sexual- actúa sobre las espermatogonias para –con la ayuda de la testosterona- producir el semen.
La LH –en el sexo femenino- estimula al folículo que segrega estrógenos, y merced a su pulso en la mitad del ciclo, completa la meiosis del óvulo y lo libera, estimulando luego al folículo ya vacío para que se convierta en cuerpo lúteo, que segrega la progesterona.
En los hombres la LH (llamada también estimulante de las células intersticiales o ICSH) estimula dichas células de Leydig para que se produzca la testosterona.
La tirotropina:
TSH u hormona estimulante de la tiroides estimula esta glándula para la producción de hormonas tiroideas, tiroxina o T4 y triyodo-tironina o T3 y es a su vez regulada por la TRH del hipotálamo y por medio de la retro-alimentación, por la fracción libre de la tiroxina; La TSH tiene cierta independencia de la TRH, pues en ausencia de la última se puede mantener un grado mínimo de función tiroidea.
La somtostatina hipotalámica también inhibe su secreción. Su cadena beta –que le da sus propiedades tiro-estimulantes- tiene ciento doce aminoácidos y la alfa- al igual que la de las gonadotropinas- ochenta y nueve (Figura 6. Eje hipotálamo-hipófisis-tiroides)
(Lea También: Neurohormonas Fisiología del Hipotálamo, Pineal y Neurohipófisis)
Hormonas derivadas de la pro-opio-melano-cortina
De la POMC (péptido que llaman la mamá grande) se derivan el ACTH, un fragmento amino-terminal que da origen a la gama-MSH y la beta-lipotropina; esta última se rompe en varios fragmentos, hormona estimulante de los melanocitos (beta-MSH), encefalina y endorfinas alfa, beta y gama.
De estas, la que se encuentra en mayor cantidad en el hipotálamo es la beta-endorfina. Estos clivajes proteolíticos mencionados no ocurren en todas especies, y algunos –particularmente en animales inferiores como el camaleón- ocurren en la pars intermedia.
La beta lipotropina tiene un efecto lipolítico débil, pero su principal función es generar endorfina. La beta-endorfina influye en varias funciones hipotalámicas como la reproducción, la temperatura, funciones cardiovascular y respiratoria, percepción del dolor y estado de ánimo. La expresión del gen de la POMC a nivel pituitario es controlada por la CRH y controlada por feed-back negativo de glucocorticoides.
En el hipotálamo es regulada por esteroides sexuales. Estos opioides endógenos se encuentran en nivel inverso a la de la Gn-RH y de las gonado-trofinas. La acción de la encefalina está relacionada con la modulación de la vía de las catecolaminas, especialmente de norepinefrina. No intervienen receptores para dopamina, acetilcolina o a-adrenérgicos. Posiblemente la endorfina puede afectar directamente la liberación de GnRH.
La liberación de CRH y por tanto de ACTH, está regulada por el cortisol plasmático a través de un feed-back negativo. Este eje hace parte muy importante de las situaciones de estrés. donde con la epinefrina, el glucagón y la hormona del crecimiento conforman el grupo de las hormonas del estrés.
La corticotropina o ACTH
La corticotropina o ACTH es un polipéptido de 39 aminoácidos con un N-terminal (efectos secretores) y C-terminal (efectos antigénicos y protectores parciales de la proteólisis).
El análogo que contiene los primeros 24 aminoácidos tiene –al igual que el natural de 39- un ciento por ciento de potencia cuando se administra por vía parenteral.
Como sus primeros 19 aminoácidos tienen una estructura que es igual a la de la alfa-MSH, esto explica las propiedades pigmentarias del ACTH. Esta hormona estimula la producción de glucocorticoides y andrógenos tipo DHEA-S en las suprarrenales, e influencia algo la generación de aldosterona, aunque este mineralocorticoide responde principalmente al eje renina-angiotensina.
La suprarrenal responde al máximo durante veinticuatro horas –en forma de todo o nada- a una unidad diaria de ACTH.
Historia
– Aunque el nombre de hipófisis (que quiere decir protuberancia inferior del cerebro) fue dado por Sömmering en 1778, ya Galeno proponía que impurezas del cerebro drenan a la nasofaringe a través de ella. En 1543, Vesalio la llamó pituitaria (secretora de moco) y en el siglo XVII Schneider y Lower hablaron de sustancias que la hipófisis destilaba a la circulación.
Ashner en 1912 fue el primero en demostrar la relación funcional entre el hipotálamo y las glándulas endocrinas al inducir atrofia ovárica en perros luego de inyectar parafina en la región hipotalámica y en 1913, Stieve es el primero en demostrar que las gallinas en presencia de un zorro dejan de poner huevos.
Westman y Jacobsohn logran demuestran que la sección del tallo bloquea la ovulación. En 1940 Rioch sugirió la nueva nomenclatura anatómica y en 1946, Markee observa que la estimulación eléctrica de la hipófisis no induce la ovulación, lo cual hace pensar en la existencia de sustancias producidas por el hipotálamo -transportadas a través del sistema porta- que actúan sobre las células hipofisiarias y regulan los eventos reproductivos.
Experimentos posteriores de Schally y Guillemin demuestran la relación directa entre hipotálamo e hipófisis y se empiezan a identificar factores estimuladores e inhibidores; en 1971 Matsuo -y luego Burgos- logra aislar y analizar la estructura de la hormona liberadora de gonadotropinas (GnRH).
Patología
La deficiencia de hormonas hipofisiotropas se llama hipopituitarismo hipotalámico. Existen numerosas causas, aunque poco frecuentes; entre ellas están: la compresión o destrucción del hipotálamo por tumores (Craniofaringioma, Pinealoma ectópico, Glioma, Quiste dermoide y teratoma en línea media, tumor del seno endodérmico, metástasis), la enfermedad de Hans-Schuller-Christian, Tuberculosis y sarcoidosis, Trauma cráneo-encefálico e Irradiación.
El hipopituitarismo primario puede ser el resultado de la ablación quirúrgica o radiológica, por la presencia de tumores y lesiones infiltrativas, o por el infarto de la hipófisis (Síndrome de Sheehan).
Entre las primeras manifestaciones de esta necrosis hipofisiaria post-parto están la amenorrea, agalactia, caída del vello axilar y púbico, astenia, palidez, hipotensión, hipoglicemia, y más adelante, un cuadro clínico de hipotiroidismo.
Existen también las deficiencias selectivas de hormonas hipofisiarias, como la de la somatotropina, que conduce al enanismo hipofisiario. Otro síndrome que en ocasiones se observa es el de la silla turca vacía -que puede recordar un tumor a la imagenología- y que generalmente representa una alteración congénita con ausencia parcial del diafragma selar, que permite la extensión del espacio subaracnoideo hacia la fosa selar, aplanando la hipófisis contra el piso de la silla turca, que puede demineralizarse.
Los síndromes de excesos hormonales se ven más frecuentemente con la prolactina y la hormona del crecimiento. Los microprolactinomas son frecuentes, se asocian con el síndrome de galactorrea-amenorrea y con infertilidad.
Su manejo lleva a la corrección de las molestias, prevención de la osteoporosis y búsqueda de un embarazo, pero desde el punto de vista tumoral tienen un comportamiento benigno, pues en la enorme mayoría de los casos el tumor no aumenta de tamaño. Si es un macroprolactinoma es necesario el tratamiento quirúrgico, especialmente si hay síntomas como cefalea o trastornos visuales.
Los adenomas hipofisiarios más frecuentes son los productores de prolactina:
Corresponden al 50% de los tumores encontrados en autopsias. Hay muchas causas de hiperprolactinemia además de las tumorales, entre ellas una serie de medicamentos.
En cuanto a la hormona del crecimiento, su exceso produce gigantismo en los niños y acromegalia en los adultos. La incidencia de este último síndrome es de seiscientos casos anuales en los Estados Unidos y se caracteriza por crecimiento acral, prognatismo y separación de las piezas dentales, hiperdiaforesis, artrosis, cardiomegalia y en general organomegalia, diabetes, hipertensión, cefalea y muchas otras manifestaciones serias que requieren tratamiento.
Terapéutica
Para lo casos de hipopituitarismo, el tratamiento se base en la terapia hormonal de suplencia que se administra según los ejes comprometidos; generalmente se administran hormonas tiroideas, corticoides tipo hidrocortisona siguiendo el ritmo circadiano y hormonas estro-progestágenas.
La deficiencia de hormona del crecimiento –enanismo hipofisiario- se administra la hormona fabricada por el método de DNA recombinante, aunque algunas indicaciones adicionales –como su administración en maduradores lentos o para combatir el envejecimiento- continúan siendo debatidas.
Fertilidad, en criptorquidia o en hipogonadismos centrales se utilizan las gonadotropinas, al igual que Gn-RH de larga duración para el cáncer de próstata y otras patologías.
La acromegalia y macro-adenomas hipofisiarios, el tratamiento es usualmente quirúrgico, aunque pueden usarse drogas tipo ocreótido –en el primer caso- o tipo bromocriptina –en el segundo- que frecuentemente son de utilidad independientemente de su costo o efectos secundarios.
Resumen
La adenohipófisis o pituitaria anterior es la parte más voluminosa de este órgano, que está íntimamente relacionado con el hipotálamo pues sus hormonas liberadoras e inhibidoras regulan la función hipofisiaria. Produce, almacena y libera tres tipos de hormonas, las somatomamotróficas (hormona del crecimiento y prolactina), las glicoproteínas (TSH y gonadotropinas LH y FSH) y las derivadas de la proopiomelanocortina o POMC (ACTH, MSH y beta-endorfinas).
La hormona del crecimiento es un polipéptido de cadena única que se encarga del crecimiento post-natal, con acciones estimulantes sobre la síntesis de proteínas y sobre el crecimiento somático y visceral (efecto anabólico), sobre la glicemia (elevándola, como hormona contra-reguladora de la insulina) y es además lipolítica.
Se libera cuando caen los niveles plasmáticos de glucosa o ácidos grasos libres, o en respuesta a dietas o infusiones ricas en proteínas, en situaciones de estrés, o un par de horas después de iniciado un sueño profundo, cuando se produce regularmente un pico nocturno.
Otra hormona somatomamotrófica (al igual que el lactógeno placentario) es la prolactina, hormona básicamente inhibida por el PIF o dopamina hipotalámica, que participa en el desarrolla mamario, es responsable de la lactancia –favoreciendo la síntesis de caseína y lactosa- e influye en las funciones reproductoras, inhibiendo el pico de LH y la liberación de la correspondiente hormona hipotalámica.
Entre las glicoproteínas está la hormona estimulante de la glándula tiroides (tirotrofina o TSH), que induce la formación de las dos hormonas tiroideas. Es estimulada por la TRH e inhibida por servo-regulación por la T3 y T4. Se libera TSH en circunstancias externas como el frío y el jejum.
Otras glicoproteínas son las gonadotrofinas FSH y LH, reguladas por la gonado-relina hipotalámica y frenadas por niveles dados de estrógenos, andrógenos, prolactina y progesterona.
Estas gonadotrofinas :
Que participan en la regulación del crecimiento, la pubertad, los procesos reproductivos y la secreción de los esteroides sexuales en ambos sexos- estimulan las células testiculares de Sertoli y la ováricas de la granulosa (para la FSH) y las células productoras de testosterona de Leydig o la inducción de la ovulación (para la LH).
El más importante derivado de la POMC es el ACTH, que regula el crecimiento y secreción de la corteza suprarrenal (y a través de esta acción, la liberación del cortisol y de la DHEA-S). Responde al estrés y tiene un ritmo circadiano, con un pico pocas horas antes de despertar. De la molécula de POMC se puede también obtener por clivaje una de alfa-MSH y otra de beta-endorfina.
Referencias seleccionadas
- Barón-Castañeda G. Fundamentos de endocrinología ginecológica. Contacto Gráfico, Bogotá, 1998.
- Raff H. Secretos de la Fisiología. Editorial McGraw-Hill Interamericana. México, 2000.
- Augsten AL, Bowen RA, Rouge M. Pathophysiology of the endocrine system. Colorado State University, Fort Collins, CO, 1999. www.arbl.cvmbs.colostate.edu/hbooks/pathphys/endocrine/indexl
- Banks D. Endocrinology and nutrition. 1996. United Medical and Dental Schools, Guy’s and St. Thomas hospitals, London. www.umcls.ac.uk/physiology/banks/endonut#start
- Koeslag J. Companion to endocrinology studies. Department of Medical Physiology, University of Tigersberg, South Africa. www.sun.ac.za/med_physbio/med_physiology/dept/ENDO
Bibliografías Seleccionadas
- Christine Bole-Feysot, Vincent Goffin, Marc Edery, Nadine Binart, Paul A. Kelly
- Prolactin (PRL) and Its Receptor: Actions, Signal Transduction Pathways and Phenotypes Observed in PRL Receptor Knockout Mice Endocr Rev Jun 01, 1998 19: 225-268.
- Anne-Simone Parent, Grete Teilmann, Anders Juul, Niels E. Skakkebaek, Jorma Toppari, Jean-Pierre Bourguignon The Timing of Normal Puberty and the Age Limits of Sexual Precocity: Variations around the World, Secular Trends, and Changes after Migration Endocr Rev Oct 01, 2003 24: 668-693.
- Andrea Giustina, Johannes D. Veldhuis Pathophysiology of the Neuroregulation of Growth Hormone Secretion in Experimental Animals and the Human Endocr Rev Dec 01, 1998 19: 717-797.
- Nira Ben-Jonathan, Robert Hnasko Dopamine as a Prolactin (PRL) Inhibitor Endocr Rev Dec 01, 2001 22: 724-763.