Capítulo 2
Dr. Alfredo Jácome Roca.
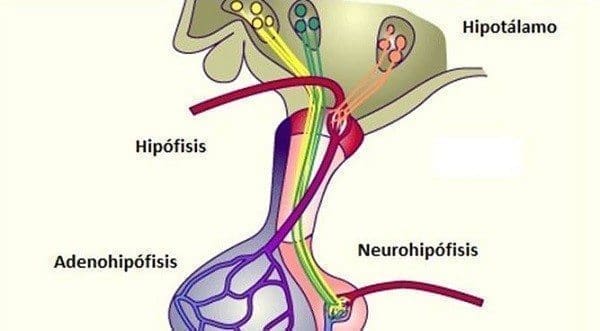
La parte anterior y más voluminosa de la pituitaria se llama adeno-hipófisis y está constituida por células epiteliales que segregan siete hormonas de naturaleza proteica, la mayoría de las cuales son hormonas trópicas, pues se encargan de estimular la función de una serie de órganos endocrinos periféricos.
Embriología, anatomía e histología
 Embriológicamente la adeno-hipófisis se desarrolla a partir de una invaginación – durante la cuarta semana – del ectodermo superficial (el techo de la región oral primitiva) denominada Bolsa de Rathke.
Embriológicamente la adeno-hipófisis se desarrolla a partir de una invaginación – durante la cuarta semana – del ectodermo superficial (el techo de la región oral primitiva) denominada Bolsa de Rathke.
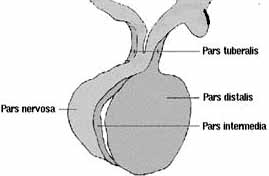
Crece esta hacia el infundíbulo y luego se separa de la cavidad oral, convirtiéndose en un islote epitelial hueco que en su parte más alta se une a una prolongación del piso del encéfalo, dando lugar más adelante a la parte tuberal de la pituitaria; en cuanto al islote, las células de su parte anterior se tornan gruesas y forman la parte anterior de la hipófisis (Fig. 1).
La hipófisis es una estructura ovoide que pesa unos 500 mg, cuya porción principal descansa en una depresión del esfenoides conocido como la silla turca.
El 75% de la glándula lo constituye la adeno-hipófisis, que consta de la pars distalis (la más importante), la tuberalis (que hace parte del tallo hipofisiario junto con el infundíbulo) y la pars intermedia, casi inexistente en el humano. Una deflexión de la duramadre en forma de diafragma –a través de la cual pasa el tallo hipofisiario- divide la glándula en sus porciones infla y supraselares.
Quiasma óptico
El quiasma óptico se encuentra arriba y adelante, abajo está el seno esfenoidal y lateralmente están los senos cavernosos, mientras que hacia atrás están los cuerpos mamilares. El sistema portal hipotálamo-hipofisiario –del que hablamos en el capítulo sobre neurohormonas- es parte importante de la estructura anatómica.
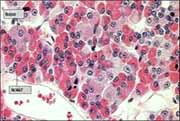
Histológicamente se ha hablado de que la hipófisis tiene – en cantidades por mitad- unas células cromófilas (que se tiñen con hematoxilina-eosina) y otras cromófobas o C (más pequeñas, que apenas se tiñen o no lo hacen).
Hoy se considera que ambos tipos de células hacen parte de un ciclo de actividad e inactividad secretora. Aunque no es muy notable la diferenciación de las células cromofilas entre basófilas o b y las acidófilas o a, esta terminología aún se menciona; las hormonas glicoproteicas (PAS positivas) y las derivadas de la pro-opio-melano-cortina (POMC) pertenecen a las primeras, y las somato-mamotróficas a las segundas.
La adeno-hipófisis contiene dos tipos de células acidófilas y tres de células basófilas. Cada una tiene una distribución característica, siendo las somatotropas la mitad (se localizan en las alas laterales), corticotropas (en la región anteromedial entre las alas mencionadas) y tirotropas (que abundan en el borde anteromedial); las mamotropas y gonadotropas tienen una distribución más irregular (Fig.2).
Hormonas de la adeno-hipófisis
Decíamos que hay allí seis tipos de células secretoras, todas –con excepción de una- especializadas en la producción de una sola hormona. Se trata del somatotropo (somatotropina), lactotropo (prolactina), tirotropo (TSH), gonadotropo (que segrega tanto FSH como LH), corticotropo (ACTH) y melanotropo (alfa-MSH).
Hay tres clases de hormonas en la adeno-hipófisis:

- las somato-mamotróficas (hormona del crecimiento, prolactina), cadenas largas de un solo péptido, con puentes di-sulfídicos.
- las glicoproteicas (tirotropina y gonadotropinas), que tienen idéntica la sub-unidad alfa de 89 aminoácidos y diferente la beta, que les da sus propiedades específicas (Fig.3. TSH, FSH y LH)
- Y las derivadas de la pro-opio-melano-cortina o POMC (ACTH, beta-MSH y lipotropina) -llamada la gran mamá- precursora de péptidos más pequeños que son producidos por un procedimiento post-translacional.
Las hormonas de naturaleza peptídica tienen sus correspondientes genes, los cuales han sido localizados. Los genes codifican la proteína inicial (formada en el retículo endoplásmico rugoso) que casi nunca es la hormona verdadera, se suele tratar de proteínas de mayor peso molecular llamadas pre-pro-hormonas.
A continuación, esta gran proteína se fragmenta aún en el retículo endoplásmico formándose una proteína de menor tamaño llamada pro-hormona. Más tarde, se realiza la última fragmentación que da lugar a la verdadera hormona en el aparato de Golgi.
Las estructuras, organización y regulación de expresión de los genes que codifican las diferentes hormonas polipeptídicas han venido definiéndose desde finales del siglo pasado –bien en humanos o en animales- y el conocimiento se ha ampliado con el proyecto del genoma humano, conocido como HUGO.
Los estudios han progresado a través de varias etapas como la clonación de genes y dilucidación de sus estructuras, determinación de secuencias de promotores y supresores responsables de la regulación de expresión transcripcional de los genes, aislamiento y caracterización de proteínas fijadoras de DNA comprometidas en la regulación de la expresión.
Regiones promotoras de los genes
En las regiones promotoras de los genes se han identificado secuencias promotoras –que determinan en qué fenotipos celulares se expresan los genes y cómo la transcripción genética responde a sustancias activadoras como el AMPc. La especificad de fijación y la actividad de transactivación de estas proteínas está regulada por su fosforilación.
En cuanto a la ingeniería genética, gracias a la tecnología del ADN recombinante se clonan los genes de ciertas proteinas humanas en microorganismos adecuados para su fabricación comercial.
Un ejemplo típico es la producción de insulina que se obtiene a partir de la levadura Sacharomyces cerevisae, en la cual se clona el gen de la insulina humana; igual puede lograrse con la hormona del crecimiento, factores de coagulación, etc. Se denomina ADN recombinante al que se ha formado cuando se intercala un segmento de ADN extraño un un ADN receptor.
La terapia génica es el proceso por el cual se inserta material genético en una célula, con el fin de hacer que ésta produzca una proteína normal. Las utilidades van desde curar enfermedades unigénicas hasta modificar el equilibrio del sistema inmune, permitiendo la modulación de la respuesta contra cualquier antígeno.
En esencia es cambiar la secuencia del genotipo de un organismo para que tenga implicaciones fenotípicas. Se realiza a través de las enzimas de restricción que son capaces de cortar el ADN en puntos concretos y luego –por medio de un vector generalmente viral- se introduce a las células en donde hay un gen alterado o deficiente que quiere modificarse.
Tabla 1.
Algunos genes que codifican hormonas, precursores hormonales y hormonas liberadoras en el homo sapiens
Genes |
Símbolo |
Localización |
Nombre |
|
|---|---|---|---|---|
Factor auricular natriurético |
NPPA NPPB |
1p36.2 1p36.2 |
Precursor A del ANP Precursor B del ANP |
|
Gonadotropina coriónica |
CGB | 19q13.3 | Betalipopéptido HCG | |
Hormona liberadora de ACTH |
CRH | 8q13 | ||
Hormona luteinizante |
LHB | 19q13.3 | Betalipopéptido LH | |
Insulina |
INS | 11p15.5 | ||
Hormona del crecimiento |
GH@ | 17q23 | Gen de un grupo de cinco | |
Hormona liberadora de TSH |
TRH | 3q13.3-q21 | ||
Prolactina |
PRL | 6p22.2-p22.1 | ||
Parathormona |
PTH | 11p15.2-p15.1 | ||
Calcitonina |
CALCA | 11p15.2-p15.1 | ||
Hormona liberadora de GH |
GHRH | 20q11.21 | ||
Eritropoyetina |
EPO | 7q21.3-q22.1 | ||
GH relina (precursor) |
Ghrh | 3p26-p25 | ||
H. liberadora de gonadotrifinas |
GnRH 1 | 8p21-p12 |
(Lea También: Glicoproteínas y Hormonas derivadas de la pro-opio-melano-cortina)
Hormonas somato-mamotróficas
La hormona del crecimiento, también llamada somatotropina, es codificada por un gen de un grupo de cinco -localizado en el brazo largo del cromosoma 17- es una mezcla heterogénea de péptidos que se diferencian por su tamaño o su carga.
Como decíamos, la mitad de las células hipofisiarias son somatotropos y la producción de la hormona del crecimiento –grande en niños- alcanza las cifras más altas en la adolescencia, bajando a niveles mínimos en la edad adulta; su secreción de hormona ocurre en pulsos separados e irregulares –con picos y valles- de manera que hay momentos en que sus niveles séricos pueden llegar a ser indetectables.
En la noche –después de comenzar el sueño profundo- los pulsos son más amplios y constantes. Debido a estas variaciones, en el diagnóstico clínico es necesario – o bien tomar varias muestras y hacer un pool, o hacer pruebas dinámicas, particularmente para detectar una deficiencia.
La gonado-relina y la somatostatina
Fisiológicamente hay dos hormonas – la gonado-relina y la somatostatina- que regulan su liberación, pero también hay varios estímulos (neuro-transmisores, fármacos o metabolitos) que influyen en la secreción de la hormona.
La glucosa plasmática también es un potente regulador y la hipoglicemia por insulina y otras causas produce un rápido aumento en su secreción, al igual que el ejercicio, el estrés, la excitación emocional y el consumo de alimentos ricos en proteínas.
 Como veíamos en el capítulo sobre generalidades, las similitudes entre la hormona del crecimiento y la prolactina son los receptores, homólogos en cuanto a secuencia de aminoácidos y organización estructural general.
Como veíamos en el capítulo sobre generalidades, las similitudes entre la hormona del crecimiento y la prolactina son los receptores, homólogos en cuanto a secuencia de aminoácidos y organización estructural general.
Numerosos tejidos reciben el efecto de la somato-tropina, entre ellos el hígado, los diferentes tejidos musculares (estriado, liso, cardiaco), fibroblastos, tejido linfoide, gonadas y el hipotálamo.
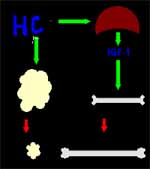
Sus efectos son anabólicos en unos tejidos o catabólicos en otros; los primeros son inhibidos por los gluco-corticoides y los segundos potenciados por ellos, pero contrarrestados por la insulina (Figura 4)
Son acciones directas de la hormona del crecimiento
- Producir el factor insulina-símil 1 (IGF-1 o somatomedina)
- Lipólisis
- Estímulo de la gluconeogénesis.
Son efectos mediados por el IGF-1:
- Producir hiperplasia –más que hipertrofia- en casi todos los tejidos
- Estimular la condrogénesis, el crecimiento del esqueleto y de tejidos blandos
La prolactina
La prolactina es otra hormona somato-mamotrófica, que contiene 199 aminoácidos y aunque pertenece a la superfamilia del gen prolactina-GH, puede ser codificada en mamíferos en estos además por más de un gen y además existe una amplia gama de variantes estructurales. Generalmente se origina en el lactotropo, pero también en el somatotropo, en el cerebro, tejido mamario, folículos ovárico y glándulas accesorias sexuales masculinas.
Su síntesis y secreción en el feto comienza en las primeras semanas de embarazo y sus concentraciones disminuyen después de nacer, en los hombres permanecen bajas durante la vida y son un poco mayores en mujeres con ciclos normales. Y en el embarazo los niveles aumentan y llegan al máximo al final de la gestación, disminuyendo en caso de que no haya lactancia materna.
En las que dan pecho a su bebé, la succión o la manipulación de las mamas estimula la secreción de prolactina, y las concentraciones circulantes de esta última pueden aumentar de diez a cien veces en la media hora siguiente a la estimulación.
Su secreción es básicamente inhibida por la dopamina o PIF y también por los estrógenos; la administración de TRH produce liberación de prolactina. Aparte de la succión y manipulación, los factores que afectan su secreción son similares a los que intervienen en la secreción de hormona del crecimiento.
La prolactina actúa sobre la glándula mamaria, que también –durante el embarazo- es influida por otras hormonas (estrógenos, progesterona, lactógeno placentario, hormona del crecimiento, insulina, cortisol y hormona tiroidea), que preparan a las mamas para la lactancia.
Durante la gestación la secreción láctea se inhibe merced a los altos niveles de estrógenos y progesterona. En el puerperio, la prolactina diferencia las células pre-secretorias en secretorias y aumenta la síntesis de la caseína, lactalbúmina y beta-lactoglobulina (proteínas de la leche), la de los ácidos grasos y fosfolípidos.
Las enzimas que intervienen en la generación de lactosa también son estimuladas por esta hormona. Durante la lactancia, la succión estimula la producción de prolactina y la hormona eyecto-láctea –la oxitocina- favorece la salida del alimento materno.