Dr. Germán Barón Castañeda, M.D.
Problemas de la terapia Estrogénica
Cuando se empezaron a utilizar los anticonceptivos orales con concentraciones elevadas de estrógenos en la década de los sesenta se observó el aumento en la incidencia de enfermedad tromboembólica, hipertensión arterial y alteración en el metabolismo de los carbohidratos. Con las dosis que se utilizan en la hormonoterapia del climaterio estos efectos metabólicos no se observan.
Se ha postulado que la terapia estrogénica puede aumentar entre una y dos veces el riesgo de litiasis biliar; hay algunos estudios de casos y controles que concluyen que este efecto no se observa en la mujer postmenopáusica.
Las contraindicaciones metabólicas para la terapia estrogénica incluyen: la alteración crónica de la función hepática, trombosis vascular aguda y enfermedad vascular neuro-oftalmológica. Los estrógenos pueden tener efecto adverso en algunas pacientes con trastornos convulsivos, hiperlipidemias familiares o migraña.
Neoplasia endometrial
La progresión anormal del endometrio a través de la hiperplasia simple, hiperplasia compleja con atipia y carcinoma temprano han sido asociadas con la actividad de los estrógenos no opuestos, administrados en forma cíclica o continua. Un año de terapia estrogénica sin oposición producirá una incidencia de hiperplasia de 20%.
Cuando hay atipia presente, 20 a 25% de los casos progresarán a un carcinoma en un lapso de un año. Los estudios retrospectivos han calculado que una mujer que ha recibido terapia no opuesta con progestágenos tiene un incremento entre dos y diez veces en el riesgo de sufrir carcinoma de endometrio y dicho aumento está directamente relacionado con la dosis de los estrógenos y la duración de la exposición.
A pesar del aumento en la incidencia de cáncer de endometrio en mujeres que han sido usuarias de estrógenos sin contraposición de progestágenos, se ha observado que el estado del tumor es menor y la sobrevida a 5 años mejor (92 vs 68%); es posible que este resultado sea debido a un diagnóstico más precoz y un mejor seguimiento.
Algunos estudios han demostrado que al adicionar progestágenos la incidencia de neoplasia endometrial puede ser menor que en la población general.
En el momento se sabe que el riesgo de carcinoma de endometrio se puede reducir con la adición de un agente progestacional a la suplencia estrogénica.
Mientras que el estrógeno promueve el crecimiento del endometrio, los progestágenos lo inhiben.
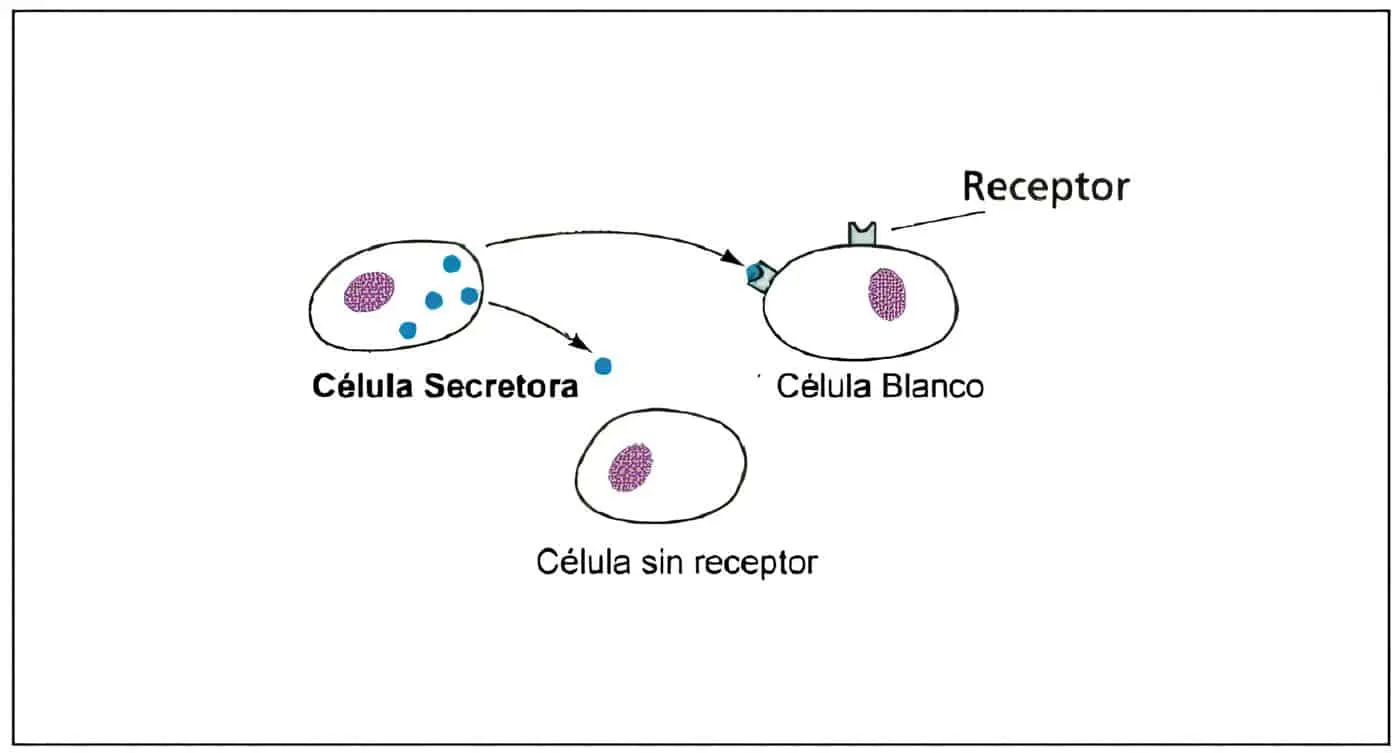
Se sabe que los progestágenos disminuyen los receptores intracelulares para estrógenos e inducen las enzimas que convierten el estradiol a metabolitos inactivos como el sulfato de estrona; además los productos progestacionales suprimen la transcripción de oncogenes mediada por estrógenos.
La acción protectora de los progestágenos actúa a través de un mecanismo que requiere tiempo, de manera que el progestágeno se debe adicionar por lo menos durante diez días, aunque hay argumentos que están a favor de que sea un mínimo de doce días.
La dosis también es importante; cuando se utilizan esquemas cíclicos se recomiendan 5 a 10 mg de acetato de medroxiprogesterona y en los esquemas continuos de 2.5 a 5 mg.
Cáncer de seno
La incidencia de cáncer en mujeres en Colombia ha ido en constante aumento en las últimas décadas. En 1995 se reportaron 4.325 casos nuevos de cáncer de seno y en 1990 murieron 1.165 mujeres por esta causa.
Los estrógenos inducen un cambio proliferativo sobre el sistema ductal, mientras que los progestágenos parecen estimular el desarrollo de lóbulos y alvéolos. Los estrógenos inducen una serie de factores de crecimiento y se podría pensar que facilitan la reproducción celular y por ende las mutaciones y aparición de cáncer.
Hasta el momento los estudios epidemiológicos respecto a la terapia de suplencia estrogénica y el riesgo de cáncer de seno no han mostrado conclusiones definitivas.
El estudio realizado en Uppsala, Suecia, concluye que hay un ligero aumento, relacionado con tiempo de exposición, alcanzando un riesgo relativo de 1.7 después de 9 años; este aumento se observa únicamente con el uso de estradiol y no con los estrógenos conjugados.
Uno de los reportes más recientes es el “Estudio de las enfermeras” donde el análisis revela que las mujeres que han utilizado estrógenos por más de diez años no tienen aumento en la incidencia de cáncer de seno; el riesgo relativo se incrementa en forma ligera a 1.33 (Intervalo de confianza de 1.12 a 1.57).
Otro de los estudios grandes es el de Dupont, en el cual hace seguimiento con biopsias en 3.303 mujeres durante 17 años. Su conclusión es que la terapia estrogénica disminuye la incidencia de cáncer de seno, incluso en aquellas pacientes con hiperplasia atípica. Datos similares se encuentran en dos estudios de Estados Unidos y Canadá.
En cuanto a metanálisis vale la pena mencionar el de Dupont y Page realizado en Nashville:
Quienes concluyen que la dosis de 0.625 mg diarios de estrógenos conjugados por varios años no aumenta en forma apreciable el riesgo de cáncer de seno. Por el contrario hay otras observaciones que sugieren que puede existir un aumento ligero en el riesgo después de cinco años de uso de la terapia.
La experiencia nacional es escasa, pero en un reporte del Hospital Infantil con 92 pacientes y cinco años de seguimiento no hay alteraciones mamarias. La experiencia personal arroja resultados similares con diez años de terapia.
Todos los estudios han llegado a la misma conclusión: a pesar de que puede existir un aumento ligero en la incidencia de cáncer de seno, en las mujeres que estaban tomando estrógenos en el momento de hacer el diagnóstico del carcinoma la mortalidad es menor.
Esto probablemente no es más que el reflejo de un diagnóstico más precoz, ya que estas pacientes tienen seguimiento más estrecho. En todo caso los riesgos relativos en todos los trabajos han estado cercanos a 1. A diferencia del endometrio, los progestágenos no parecen tener ningún efecto protector sobre el seno.
La historia de enfermedad mamaria benigna sin atipias no aumenta el riesgo por lo cual no contraindica el tratamiento. De forma paradójica, en casos de enfermedad con atipia se ha observado disminución del riesgo.
Formas de administrar la suplencia
Desde hace muchos años se comprobó que los estrógenos disminuyen los síntomas vasomotores de la menopausia. En este momento todos los estudios llegan a la misma conclusión: los beneficios de la terapia estrogénica sobre reducción de enfermedades cardiovasculares e incidencia de fracturas sobrepasan los riesgos potenciales de carcinoma de seno y endometrio.
Los metanálisis recientes sugieren que en mujeres usuarias de estrógenos hay una disminución de por lo menos 50% en enfermedad coronaria y de 70 a 90% en la mortalidad cardiovascular, además de su efecto benéfico sobre la incidencia de fracturas.
Las formas orales han sido las más utilizadas, especialmente las conjugadas o esterificadas; se hicieron pruebas con el 17-b-estradiol, pero su absorción intestinal es muy pobre incluso en forma micronizada. Al utilizar estrógenos solos se vio un aumento en la incidencia de carcinoma de endometrio, efecto que se evita al adicionar progestágeno.
El producto más utilizado en nuestro medio para la suplencia es estrógenos conjugados que consiste de una mezcla de sulfato de estrona 65% y estrógenos equinos. Al ser absorbido del tracto gastrointestinal sufre el primer paso hepático, donde 35 a 60% es transformado a estrona-3-glucorónido.
Se ha postulado que puede activar el sistema renina-angiotensina-aldosterona:
Por lo cual induciría hipertensión arterial en individuos susceptibles; este efecto es mucho menor que el observado con los compuestos sintéticos de los anticonceptivos orales. Gracias a este primer paso hepático induce una serie de globulinas hepáticas como la SHBG, TBG, CBG y factores fibrinolíticos y de la coagulación.
Los progestágenos regulan hacia abajo los receptores de estrógenos, protegiendo el endometrio. Además favorecen la protección sobre osteoporosis, son sedantes del sistema nervioso y tienen efectos anti-aldosterona y anti-andrógenos.
Al utilizar dosis de 10 mg de acetato de medroxiprogesterona se obtienen cambios secretores del endometrio, mientras que con 5 mg se revierte el efecto mitogénico de los estrógenos sin lograr cambios secretores; los esquemas continuos llevan a cambios atróficos del endometrio por lo cual conducen a la amenorrea.
La vía de administración de los estrógenos que se escoja depende mucho de la paciente. Hasta el momento los estudios parecen indicar que la vía transdérmica no tiene ningún efecto sobre el perfil lipídico. Como los estrógenos pueden aumentar los triglicéridos en aquellas mujeres que tienen niveles séricos superiores a 250 mg/dl, se recomienda adicionar un progestágeno que ayuda a reducirlos.
Los esquemas con los cuales tenemos experiencia y que se recomiendan son los siguientes.
1. Pacientes con útero
- Primero, Suplencia combinada continua: estrógenos conjugados 0.625 mg y acetato de medroxiprogesterona 2.5 mg diarios.
- Segundo, Suplencia combinada cíclica: estrógenos conjugados 0.625 mg del 1 al 21 de cada mes y acetato de medroxiprogesterona 10 mg del día 10 al 21 del mes.
- Tercero, Suplencia transdérmica: estradiol parches de 50 mg dos veces a la semana durante 3 semanas. Asociar 10 mg de acetato de medroxiprogesterona por 12 días al mes.
2. Pacientes histerectomizadas
-
Estrógenos conjugados 0.625 mg diarios.
En todos los tipos de esquemas se asocia fosfato de calcio una tableta diaria.
La terapia cíclica tiene algunas desventajas, en especial síntomas adversos relacionados con la dosis de progestágenos, tales como sensibilidad de los senos, retención de líquidos y depresión. El sangrado por supresión ocurre en 80 a 90% de las mujeres con este esquema.
Los esquemas continuos con dosis bajas de progestágenos (2.5 mg de acetato de medroxiprogesterona) mantienen su efecto benéfico sobre las lipoproteínas y no tienen efecto sobre la presión sanguínea. Con este tipo de terapia se puede presentar sangrado por disrupción hasta en el 40 a 60% de los casos durante los primeros seis meses de tratamiento; después de un año sólo se observa en el 20% de las mujeres.
Se ha discutido la utilidad de la biopsia de endometrio antes de iniciar la suplencia; no es necesario realizarla en forma rutinaria. El grosor endometrial medido por ultrasonido transvaginal se correlaciona en forma adecuada con la presencia o no de patología; si es superior a 5 mm en la paciente postmenopáusica se recomienda la biopsia.
En algunas mujeres histerectomizadas se recomienda el uso de esquemas combinados con progestágenos; ejemplo de ello son las pacientes a las cuales se les ha resecado un tumor endometrioide del ovario. Algunos reportes de la literatura sugieren que pacientes con endometriosis pélvica pueden sufrir degeneración a adenocarcinoma cuando son tratadas sólo con estrógenos.
Como se ha mencionado, es posible que los progestágenos jueguen papel importante en el metabolismo óseo, por lo cual en pacientes con osteoporosis también se recomienda el esquema combinado. De la misma forma también se recomienda en mujeres con hipertrigliceridemia por las razones expuestas.
Los efectos benéficos de los estrógenos han sido demostrados por encima de los 65 años, disminuyendo la incidencia de fracturas de cadera. De esto surge el interrogante si a las mujeres mayores que no han recibido suplencia se les debe iniciar sin tener en cuenta su edad. Se cree que las mujeres con osteoporosis o alteración del perfil de lipoproteínas sí se benefician de este régimen.
Los estrógenos también tienen efecto sobre la fisiología tiroidea, siendo el principal de ellos el aumento en la producción hepática de TBG; no inducen ningún cambio sobre la producción de TSH. Es importante tener en cuenta que las mujeres hipertiroideas tienen mayor riesgo de desarrollar osteoporosis.
Aunque se sabe que los estrógenos pueden aumentar la secreción de prolactina, la suplencia no se encuentra contraindicada en mujeres con hiperprolactinemia.
Contraindicaciones de la terapia de suplencia
La principal contraindicación para la suplencia es el cáncer estrógeno-dependiente. Se ha demostrado que pacientes a quienes se les ha tratado un carcinoma de endometrio estado I pueden recibir la suplencia sin que haya riesgo de recurrencia. Otra contraindicación es el melanoma maligno.
En las mujeres con antecedente de cáncer mamario se ha recomendado el uso de tamoxifeno, que puede tener efecto protector sobre la osteoporosis y la enfermedad cardiovascular. Es discutido si tiene efecto deletéreo sobre el endometrio cuando se utiliza por tiempo superior a dos años.
Existen varios agentes esteroideos y no esteroideos para tratar los síntomas vasomotores en aquellas mujeres en las cuales se encuentra contraindicada la suplencia. El principal parece ser el acetato de medroxiprogesterona; tanto las formas orales como las de depósito tienen la misma efectividad.
Otros agentes que han sido utilizados incluyen la clonidina, la metildopa, el danazol, el citrato de clomifeno y la naloxona. La clonidina mejora las oleadas de calor disminuyendo la respuesta vascular periférica a los estímulos vasodilatadores y vasoconstrictores; no tiene ningún efecto sobre el perfil de lipoproteínas ni sobre la prevención de osteoporosis.
En Europa se ha utilizado la tibolona, compuesto derivado de la C-19 nor-testosterona, que es débilmente estrogénico, androgénico y progestacional. Ha demostrado ser mejor que el placebo en mejorar los síntomas de la menopausia y ofrece alguna protección contra la osteoporosis.
Referencias
- Adami S., Rossini M., Zamberlan N., et al. Long-term effects of transdermal and oral estrogens on serum lipids and lipoproteins in postmenopausal women. Maturitas. 1993 ; 17 :191.
- Andrews WC. Menopause and hormone replacement: introduction. Obstet Gynecol. 1996; 87 (suppl):1.
- American College of Physicians. Guidelines for counseling postmenopausal women about preventive hormone therapy. Ann Intern Med. 1992; 117:1038.
- Bagdade JD., Wolter J., Subbaiah PV., et al. Effects of tamoxifen treatment on plasma lipids and lipoprotein composition. J Clin Endocrinol Metab. 1990; 70:1132.
- Ballinger CB. Psychiatric aspects of the menopause. Br J Psychiatr. 1990; 156:773.
- Bar J., Tepper R., Fuchs J., et al. The effect of estrogen replacement therapy on platelet aggregation and adenosine triphosphate release in postmenopausal women. Obstet Gynecol. 1993; 81:261.
- Barlow, H., Abdalla, J. Long term implant therapy: Hormonal and Clinical effects. Obstet and Gynecol, 1986:67: 321 – 325
- Barón G., Posada E., Ramírez JC. Suplencia hormonal durante el climaterio en el Hospital Infantil Universitario “Lorencita Villegas de Santos”. Rev Col Obstet Ginecol. 1994 ; 45 (supl):29.
- Barret, A., Wingard, H. Postmenopausal estrogen use and heart disease. Risk factors in the ’80s. JAMA, 1989:261: 2095 – 2100.
- Barret-Connor E. The menopause, hormone replacement, and cardiovascular disease: the epidemiologic evidence. Maturitas. 1996; 23:227.
- arrett-Connor E., Kritz-Silverstein D. Estrogen replacement therapy and cognitive function in older women. JAMA. 1993; 269: 2637.
- Barrett-Connor E., Wingard DL., Criqui MH. Postmenopausal estrogen use and heart disease risk factors in the 1980s. JAMA. 1989; 261 :2095.
- Bergkvist L., Adami HO., Persson I., et al. The risk of breast cancer after estrogen and estrogen-progestin replacement. N Engl J Med. 1989; 321: 393.
- Bhatia NN., Bergman A., Karram MM. Effects of estrogen on uretral function in women with urinary incontinence. Obstet Gynecol. 1989; 160:176.
- Body J.J., Struelens M., Borkowsky, E. Effects of estrogens and calcium on calcitonin secretion in postmenopausal women. J Clin Endocrinol Metobol, 1989; 68: 223-226.
- Bone H. The future of osteoporosis therapy. N. A. Clin Gynecol Obstet, 1984; 1:64-66
- Bourne T., Hillard T.C., Whitehead M.I. Estrogens, arterial status and postmenopausal women. Lancet, 1990; 335: 1470.
- Brian M., Henderson, J.F. Estrogen use and cardiovascular disease. Am J Obstet Gynecol, 1986; 154:1181-1186.
- Burger HG. The endocrinology of the menopause. Maturitas. 1996; 23:129.
- Cagnacci A., Soldani R., Carriero PL., et al. Effects of low doses of 17 beta-estradiol on carbohydrate metabolism in postmenopausal women. J Clin Endocrinol Metab. 1992; 74:1396.
- Campbell S., Whitehead M. Estrogen therapy and the post-menopausal syndrome. Clin Obstet Gynecol, 1987; 4: 31 – 35.
- Campos H., McNamara JR., Wilson PW., et al. Differences in low density lipoprotein subfractions and apolipoproteins in premenopausal and postmenopausal women. J Clin Endocrinol Metab. 1988; 67:30.
- Cano A., Fernandes H., Serrano S., et al. Effect of continuous oestradiol-medroxyprogesterone administration on plasma lipids and lipoproteins. Maturitas. 1991; 13:35.
- Carter BA., Fink PJ. Psychiatric myths of the menopause. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:70-91.
- Castelli WP. Menopause and cardiovascular disease. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:117-136.
- Castelo-Branco C., Durán M., González-Merlo J. Skin collagen changes related to age and hormone replacement therapy. Maturitas. 1992; 15:113.
- Christiansen C., Riis BJ. Five years with continuos combined oestrogen/progestogen therapy. Effects on calcium metabolism, lipoproteins and bleeding pattern. Br J Obstet Gynecol. 1990; 97:1087.
- Colditz GA., Egan KM., Stampfer MJ. Hormone replacement therapy and risk of breast cancer: resultas from epidemiologic studies. Am J Obstet Gynecol. 1993: 168:1473.
- Colditz GA., Stampfer MJ., Willet WC., et al. Type of postmenopausal hormone use and risk of breast cancer: 12-year follow-up from the Nurses’ Health Study. Cancer Causes Control. 1992; 3:433.
- Colditz GA., Willet WC., Stampfer MJ., et al. Menopause and the risk of coronary heart disease in women. New Engl J Med. 1987; 316:1105.
- Collins P. Vascular aspects of oestrogen. Maturitas. 1996; 23:217.
- Coope J. Hormonal and non-hormonal interventions for menopausal symptoms. Maturitas. 1996; 23:159.
- Creasman WT. Estrogen replacement therapy: Is previously treated cancer a contraindication ? Obstet Gynecol. 1991; 77: 308.
- Criqui N., Barret B. Post-menopausal estrogen use and mortality: results from a prospective study in a defined homogenous community. Am J Epidemiol, 1988; 128:606-614.
- Crook D., Cust MP., Gangar KF., et al. Comparison of transdermal and oral estrogen-progestin replacement therapy: effects on serum lipids and lipoproteins. Am J Obstet Gynecol. 1992; 166:950.
- Cullinan JA. The role of ultrasound in the evaluation of the perimenopausal and postmenopausal woman. Infertil Reprod Clin North Am. 1995; 6:757.
- Cummings SR., Black DM., Nevitt MC., et al. Bone density at various sites for prediction of hip fractures. Lancet. 1993; 341: 72.
- Daly E., Vessey MP., Barlow D., et al. Hormone replacement therapy in a risk-benefit perspective. Maturitas. 1996; 23: 247.
- DANE. Información censo 93.
- D’Amiico JF., Greendale GA., Lu JK., et al. Induction of hypothalamic opioid activity with transdermal estradiol administration in postmenopausal women. Fertil Steril. 1991; 55:754.
- Dempster DW., Lindsay R. Pathogenesis of osteoporosis. Lancet. 1993; 341:797.
- Dennerstein L. Well-being, symptoms and the menopausal transition. Maturitas. 1996; 23:147.
- Devor M., Barret-Connor E., Renvall M., et al. Estrogen replacement therapy and the risk of venous thrombosis. Am J Med. 1992; 92:275.
- De Ziegler D., Bessis R., Frydman R. Vascular resistance of uterine arteries : physiological effects of estradio and progesterone. Fertil Steril. 1991; 55:775.
- Diamond MP., Davis B. Menopause, ovarian and adrenal steroids, and carbohydrate metabolism. Infertil Reprod Clin North Am. 1995; 6:711.
- Ditkoff EC., Crary WG., Cristo M., et al. Estrogen improves psychological function in asymptomatic postmenopausal women. Obstet Gynecol. 1991; 78:991.
- Dupont A., Dupont P., Cusan L., et al. Comparative endocrinological and clinical effects of percutaneous estradiol and oral conjugated estrogens as replacement therapy in menopausal women. Maturitas. 1991; 13:297.
- Dupont WD., Page DL. Menopausal estrogen replacement therapy and breast cancer. Arch Intern Med. 1991; 151:67.
- Dupont WD., Page DL., Rogers LW., et al. Influence of exogenous estrogens, proliferative breast disease, and other variables on breast cancer risk. Cancer. 1989; 63:948.
- Duursma SA., Raymakers JA., Boereboom FTJ., et al. Estrogen and bone metabolism. Obstet Gynecol Surv. 1991; 47: 38.
- Edgren RA. Pharmacology of hormonal therapeutic agents. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:289-305.
- Ellerington MC., Hillard TC., Whitehead MI., et al. Routes of administration for oestrogen and progestogen replacement therapy. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 345 – 364.
- Eriksen EF., Colvard DS., Berg NJ., et al. Evidence of estrogen receptors in normal human osteoblast-like cells. Science. 1988; 241:84.
- Eskin BA. The breast in the menopause. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:211-228.
- Eskin BA. The menopause and aging. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 1-26.
- Ettinger B. Prevention of osteoporosis: treatment of estradiol deficiency. Obstet Gynecol. 1988; 72 :25
- Ettinger B., Gerrant HK., Steiger P., et al. Low-dosage micronized 17b-estradiol prevents bone loss in postmenopausal women. Am J Obstet Gynecol. 1992; 166:479.
- Ettinger C., Friedman E. Gynecologic consequences of long term unopposed estrogen replacement therapy. Maturitas, 1988; 10:271-282.
- Ettinger B., Genant HK., Cann CE. Postmenopausal bone loss is prevented by treatment with low-dosage estrogen with calcium. Ann Intern Med. 1987; 106:40.
- Ewertz M. Hormone therapy in the menopause and brest cancer risk – a review. Maturitas. 1996; 23:241.
- Felson DT., Zhang Y., Hannan MT., et al. The effect of postmenopausal estrogen therapy on bone density in elderly women. New Engl J Med. 1993; 329:1141.
- Field CS., Ory SJ., Wahner HW., et al. Preventive effects of transdermal 17b-estradiol on osteoporotic changes after surgical menopause: a two-year placebo-controlled trial. Am J Obstet Gynecol. 1993; 168:114.
- Gallager JC., Kable WT., Goldgar, D. Effect of progestin therapy on cortical and trabecular bone: comparison with estrogen. Am J Med. 1991; 90:171.
- Gambrell RD., Babgnell CA., Greenblatt RB. Role of estrogens and progesterone in the etiology and prevention of endometrial cancer: a review. Am J Obstet Gynecol. 1983; 146:696.
- Genant H.K., Baylink D.J., Gallagher J.C. Estrogens in the prevention of osteoporosis in postmenopausal women. Am J Obstet Gynecol. 1989; 161:1842-1846.
- Genazzani AR., Petraglia F., Fucchinetti F., et al. Increase of proopiomelanocortin-related peptides during subjective menopausal flushes. Am J Obstet Gynecol. 1984; 149:775.
- Gosden RG. Follicular status at menopause. Hum Reprod. 1987; 2:617.
- Grady D., Rubin SM., Petitti DB., et al. Hormone therapy to prevent disease and prolong life in postmenopausal women. Ann Intern Med, 1992; 117:1016.
- Grodstein F., Colditz GA., Stampfer MJ. Postmenopausal hormone use and cholecystectomy in a large prospective study. Obstet Gynecol. 1994; 83:5.
- Gruchow HW., Anderson AJ., Barboriak JJ., et al. Postmenopausal use of estrogen and occlusion of coronary arteries. Am Heart J. 1988; 115:954.
- Hacker J., George M. Compendio de Ginecología y Obstetricia. Ed. Interamericana, (4a) 1986: 483-493.
- Hargrove T., Osteen KG. An alternative method of hormone replacement therapy using the natural sex steroids. Infertil Reprod Clin North Am. 1995; 6:653.
- Hartwell D., Riis B.J., Christiansen C. Changes in vitamin D metabolism during natural and medical menopause. J Clin Endocrinol Metab, 1990;71:127-132.
- Hassager C., Christiansen C. Blood pressure during oestrogen/progestogen substitution therapy in healthy post – menopausal women. Maturitas, 1988; 9:315.
- Hazzard WR. Estrogen replacement and cardiovascular disease: serum lipids and blood pressure effects. Am J Obstet Gynecol, 1989;161:1847-1853.
- Henderson BE. The cancer question: an overview of recent epidemiologic and retrospective data. Am J Obstet Gynecol, 1989;161:1859-1864.
- Henderson BE., Paganini-Hill A., Ross RK. Estrogen replacement therapy and protection from acute myocardial infarction. Am J Obstet Gynecol. 1988; 159:312.
- Henderson BE., Paganini-Hill A., Ross RK. Decreased mortality in users of estrogen replacement therapy. Arch Intern Med. 1991; 151:75.
- Hill K. The demography of menopause. Maturitas. 1996; 23: 113.
- Hong MG., Romm PA., Reagan K., et al. Effects of estrogen replacement therapy on serum lipid values and angiographically defined coronary artery disease in postmenopausal women. Am J Cardiol. 1992; 69:176.
- Hulka BS., Meirik O. Reserch on the menopause. Maturitas. 1996; 23:109.
- Hutchinson KA. Treatment considerations for the “problem” menopause patient. Infertil Reprod Clin North Am. 1995; 6: 697.
- Hution W. Current perspectives in the management of the menopausal and postmenopausal patient: introduction. Gynecol Obstet, 1990;75:4:1-3.
- Jaffe RB. Menopausia y el período perimenopáusico. En Yen SSC., Jaffe RB. Endocrinología de la reproducción. Ed Panamericana (3a); 1993:414-433.
- Johnston CC. Osteoporosis. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 103-115.
- Johnston CC., Slemenda CW., Melton LJ. Clinical use of bone densitometry. New Engl J Med. 1991; 324:1105.
- Jones GS., Muasher SJ. Hormonal changes in the perimenopause. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 257-268.
- Jones JR., Jesionowska H. Estrogen therapy and cancer. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:329-344.
- >Judd HL., Meldrum D.R., Deftos L.J. Estrogen replacement therapy indications and complications. Annals Int Med, 1983; 98: 195-199.
- Judd HL., Shamonki MI., Frumar AM., et al. Origin of serum estradiol in postmenopausal women. Obstet Gynecol. 192; 59: 680.
- Kannel WB. Metabolic risk factors for coronary heart disease in women: perspective from the Framingham Study. Am Heart J. 1987; 114:413.
- Karafin L. Urologic problems. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 171-181.
- Kaufert PA. The social and cultural context of menopause. Maturitas. 1996; 23:169.
- Kaufert PA., Gilbert P., Tate R. The Manitoba Project: a re-examination of the link between menopause and depression. Maturitas. 1992; 14:143.
- Kelly TL., Slovik DM., Schoenfeld DA., et al. Quantitative digital radiography vs. Dual photon absorptiometry of the lumbar spine. J Clin Endocrinol Metab. 1988; 67:839.
- Kiel DP., Felson DT., Anderson JJ., et al. Hip fracture and the use of estrogen in postmenopausal women: the Framingham Study. New Engl J Med. 1987; 317:1169.
- Komm BS., Terpening CM., Benz DJ., et al. Estrogen binding receptor on RNA, and biologic response in osteoblast-like osteosarcoma cells. Science. 1988; 241:81.
- Kronnenberg F. Hot flashes : epidemiology and physiology. Ann NY Acad Sci. 1990; 592:52.
- Kronnenberg F., Barnard RM. Modulation of menopausal hot flushes by ambient temperature. J Therm Biol. 1992; 17: 43.
- Krouse TB. Menopausal pathology. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:27-70.
- Lalonde CJ., Daniell JF. Management of abnormal uterine bleeding in the perimenopausal woman: medical versus surgical therapies. Infertil Reprod Clin North Am. 1995; 6:793.
- >Lauritzen C. Clinical use of oestrogens and progestogens. Maturitas. 1990; 12:199.
- Leiblum SR., Bachmann GA. The sexuality of the climacteric woman. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:137-154.
- Liel Y., Kraus S., Levy J., et al. Evidence that estrogens modulate activity and increase the number of 1,25 – dihydroxyvitamin D receptors in osteoblast-like cells. Endocrinology. 1992; 130:2597.
- Lindheim SR., Legro RS., Bernstein L., et al. Behavioral stress responses in premenopausal and postmenopausal women and the effects of estrogen. Am J Obstet Gynecol. 1992; 167:1831.
- Lindsay R. The menopause and osteoporosis. Obstet Gynecol. 1996; 87 (suppl):16.
- Lindsay R. Prevention and treatment of osteoporosis. Lancet. 1993; 341:801.
- Lindsay R., Hart DM., Clark DM. The minimum effective dose of estrogen for postmenopausal bone loss. Obstet Gynecol. 1984; 63:759.
- Lindsay R., Hart DM, Forrest C. Prevention of spinal osteoporosis in oophorectomized women. Lancet 1980; 2: 1151 – 1154.
- Lobo RA. Cardiovascular implication of estrogen replacement therapy. Obstet Gynecol, 1990;75 (4 suppl):18-24.
- Longcope C., Jaffe W., Griffing G. Production rates of androgens and oestrogens in postmenopausal women. Maturitas. 1981; 3:215.
- Love RR., Mazess RB., Barden HS., et al. Effects of tamoxifen on bone mineral density in postmenopausal women with breast cancer. New Engl J Med. 1992; 326:852.
- MacNaughton J., Banah M., McCloud P., et al. Age related changes in follicle stimulating hormone, luteinizing hormone, oestradiol and immunoreactive inhibin in women of reproductive age. Clin Endocrinol. 1992; 36:339.
- Marslew U., Overgaard K., Riis BJ., et al. Two new combinations of estrogen and progestogen for prevention of postmenopausal bone loss: long-term effects on bone, calcium and lipid metabolism, climatceric symptoms and bleeding. Obstet Gynecol. Obstet Gynecol. 1992; 79:202.
- Marslew U., Riis B.J., Christiansen C. Bleeding patterns during continuous combined estrogen-progestagen therapy. Am J Obstet Gynecol, 1991;164 (5):1: 1163-1168.
- Matthews KA., Meilhan E., Kuller LH., et al. Menopause and risk factors for coronary heart disease. New Engl J Med. 1989; 321:641.
- McKinlay SM. The normal menopause transition: an overview. Maturitas. 1996; 23:137.
- McKinlay SM., Barmbilla DJ., Posner JG. The normal menopause transition. Maturitas. 1992; 14 :103.
- Meir J., Stampfer W. A prospective study of postmenopausal estrogen therapy and coronary heart disease. N Eng J Med, 1985;313:1044-1049.
- Midgette AS., Baron JA Cigarette smoking and the risk of natural menopause. Epidemiology. 1990; 1:474.
- Mitshell D.R. Estrogen replacement therapy: an overview. Am J Obstet Gynecol, 1989;161: 1825-1827.
- Nabulsi AA., Folsom AR., White A., et al. Association of hormone-replacement therapy with various cardiovascular risk factor in postmenopausal women. New Engl J Med. 1993; 328:1069.
- Nachtigall LE. Enhancing patient compliance with hormone replacement therapy at menopause. Obstet Gynecol, 1990; 75 (4 suppl):77-80.
- Nachtigall MJ., Smilen SW., Nachtigall RAD., et al. Incidence of breast cancer in a 22-year study of women receiving estrogen-progestin replacement therapy. Obstet Gynecol. 1992; 80:827.
- Naessén T., Persson I., Thor L., et al. Maintained bone density at advanced ages after long-term treatment with low-dose estradiol implants. Br J Obstet Gynecol. 1993; 100:454.
- Nilas L., Christiansen C. Bone mass and its relationship to age and the menopause. J Clin Endocrinol Metab. 1987; 65: 697.
- Nilsson K., Heimer G. Low-dose oestradiol in the treatment of urogenital oestrogen deficiency – a pharmacokinetic and pharmacodynamic study. Maturitas. 1992; 15:121.
- Nordin C., Morris H.A., Need A.G. Relationships between plasma calcium fractions, other bone-related variables, and serum folicle stimulating hormone levels in premenopausal, perimenopausal and postmenopausal women. Am J Obstet Gynecol, 1990;163:140-145.
- Notelovitz M. Estrogen replacement therapy: indications, contraindications and agent selection. Am J Obstet Gynecol, 1989; 161:1832-1841.
- Obel EB., Munk-Jensen N., Svenstrup B., et al. A two-year double-blind controlled study of the clinical effect of combined and sequential postmenopausal replacement therapy and steroid metabolism during treatment. Maturitas. 1993; 16:13.
- Oldenhave A., Jaszmann LJB., Haspels AA., et al. Impact of climateric on well-being. Am J Obstet Gynecol. 1993; 168: 772.
- Onatra W., Sánchez J., Acuña G., et al. Epidemiología de la menopausia en Colombia: estudio cooperativo. Rev Col Obstet Ginecol. 1994 ; 45 (supl):20.
- Paganini T., Ross M. Post-menopausal estrogens treatment and stroke: a prospective study. Br Med J, 1988; 297: 519 – 522.
- Palinkas LA., Barret-Connor E. Estrogen use and depressive symptoms in postmenopausal women. Obstet Gynecol. 1992; 80: 30.
- Pang SC., Greendale GA., Cedars MI., et al. Long-term effects of transdermal estradiol with and without medroxyprogesterone acetate. Fertil Steril. 1993; 59: 76.
- Parker CR., Porter JC. LHRH and TRH in the hypothalamus of women: effects of age and reproductive status. J Clin Endocrinol Metab. 1984; 58:488.
- Persson G., Bregkvist V. Risk of endometrial cancer after treatment with estrogens alone or in conjunction with progestogens: results of a prospective study. Br Med J, 1989; 298:147 – 151
- Persson I., Adami H-O., Bergkvist L., et al. Risk of endometrial cancer after treatment with oestrogens alone or in conjunction with progestogens: results of a prospective study. Br Med J. 1989; 298: 147.
- Pettiti DB, Perlman JA., Sidney S. Noncontraceptive estrogens and mortality: long-term follow-up of women in the Walnut Creek Study. Obstet Gynecol. 1987; 70: 289.
- Pines A., Fishman EZ., Levo Y., et al. The effects of hormone replacement therapy in nomrla postmenopausal women: measurements of Doppler-derived parameters of aortic flow. Am J Obstet Gynecol. 1991; 164: 806.
- Prince RL., Smith M., Dick MI., et al. Prevention of postmenopausal osteoporosis: a comparative study of exercise, calcium supplementation, and hormone-replacement therapy. New Engl J Med. 1991; 325: 1189.
- Quigley MET., Martin PL., Burnier AM., et al. Estrogen therapy arrests bone loss in elderly women. Am J Obstet Gynecol. 1987; 156: 1516.
- Ravnikar V. Physiology and treatment of hot flushes. Obstet Gynecol, 1990; 75 (4 suppl): 3-7.
- REvans MC., et al. Effect of calcium supplementation on bone loss in postmenopausal women. eid IR., Ames RW., New Engl J Med. 1993; 328: 460.
- Rof 17-a estradiol on ibot C., Tremolieres F., Pouielles JM. Preventive effects of transdermal administration postmenopausal bone loss: a two year prospective study. Obstet Gynecol, 1990; suppl): 42 – 45.75 (4 supp): 42-45.
- Richardson SJ., Senikas V., Nelson JF. Follicular depletion during the menopausal transition – evidence for accelerated loss and ultimate exhaustion. J Clin Endocrinol Metab. 1987; 65:1231.
- Riggs BL., Hodgson SF., O’Fallon WM., et al. Effect of fluoride treatment of the fracture rate in postmenopausal women with osteoporosis. New Engl J Med. 1990; 322:802.
- Rodríguez KA., Onatra W. La menopausia: un estado fisiológico complejo. Acta Med Col. 1993; 18:257.
- Sánchez F. Terapia de sustitución hormonal. Rev Col Obstet Ginecol. 1994 ; 45 (supl):10.
- Sarrel P.M. Sexuality and menopause. Obstet Gynecol, 1990; 75 (4 suppl):26-30.
- >Schinfeld JS. Sex steroid hormone metabolism in the climacteric woman. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994: 269 – 288.
- Seeman E., Hooper JL., Bach LA., et al. Reduced bone mass in daughters of women with osteoporosis. New Engl J Med. 1989; 320: 554.
- Semmens JP., Wagner G. Effects of estrogen therapy on vaginal physiology during menopause. Obstet Gynecol. 1985; 66: 15.
- Shaaban MM. The perimenopause and contraception. Maturitas. 1996; 23: 181.
- Shangold MM. Exercise in the menopausal woman. Obstet Gynecol, 1990; 75 (4 suppl): 53-57.
- Shapiro S., Kelly JP., Rosenberg L., et al. Risk of localized and widespread endometrial cancer in relation to recent and discontinued use of conjugated estrogens. New Engl J Med. 1985; 313: 969.
- Sharp SC. Hormone replacement in menopausal women with endocrine disease. Infertil Reprod Clin North Am. 1995; 6: 721.
- Sherwin BB. Hormones, mood, and cognitive functioning in postmenopausal women. Obstet Gynecol. 1996; 87 (suppl): 20.
- Sillero M., Delgado M., Rodigues R., et al. Menopausal hormone replacement therapy and risk of breast cancer : a meta-analysis. Obstet Gynecol. 1992; 79: 286.
- Stampfer MJ., Colditz GA., Willet WC., et al. Postmenopausal estrogen therapy and cardiovascular disease: ten-year follow-up from the Nurses’ Health Study. New Engl J Med. 1991; 325:756.
- Steinberg KK., Thacker SB., Smith SJ., et al. A meta-analysis of the effect of estrogen replacement therapy on the risk of breast cancer. JAMA. 1991; 265:1985.
- Stevenson JC. Pathogenesis, prevention and treatment of osteoporosis. Obstet Gynecol, 1990; 75 (4 suppl): 36-40.
- Sbone tevenson JC., Cust MP., Gangar KF., et al. Effects of transdermal versus oral hormone replacement therapy on density in spine and proximal femur in postmenopausal women. Lancet. 1990; 336:1327.
- Storm T., Thamsborg G., Steiniche T., et al. Effect of intermittent cyclical etidronate therapy on bone mass and fracture rate in women with postmenopausal osteoporosis. N Engl J Med. 1990; 322:1265.
- Speroff L. Postmenopausal hormone therapy and breast cancer. Obstet Gynecol. 1996; 87 (suppl):44.
- Speroff L., Glass RH., Kase NG. Menopause and postmenopausal hormone therapy. En Speroff L., Glass RH., Kase NG. Clinical Gynecologic Endocrinology and Infertility. Ed. Williams & Wilkins (5a), 1994; 583-649.
- SGambrell RD., Butzin CA., et al. The relationship between breast cancer survival and prior trickland DM., postmenopausal estrogen use. Obstet Gynecol. 1992; 80:400.
- Strumpf P.G. Pharmacocynetics of estrogen. Obstet Gynecol, 1990; 75 (4 suppl):9-23.
- Sullivan JM., Fowlkes LP. The clinical aspects of estrogen and the cardiovascular system. Obstet Gynecol. 1996; 87 (suppl): 36.
- Sullivan JM., Vander Zwaag R., Lemp GF., et al. Postmenopausal estrogen use and coronary atherosclerosis. Ann Intern Med. 1988; 108:358.
- Sutnick MR. Nutritional aspects of the menopause. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:155-169.
- Tataryn IV., Lomax P., Bajorek JG., et al. Postmenopausal hot flushes: a disorder of thermoregulation. Maturitas. 1980; 2: 101.
- Teran A-Z., Gambrell RD. Menopause, comprehensive management. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:307-327.
- Thorneycroft IH., Koulianos G. Hormonal treatment of menopause of women. En Carr BR., Blackwell RE. Textbook of reproductive medicine. Ed Appleton & Lange (1a); 1993:601-618
- Tiegs RD., Body JJ., Wahner HW., et al. Calcitonin secretion in postmenopausal osteoporosis. New Engl J Med. 1985; 312: 1097.
- Tikkanen MJ. The menopause and hormone replacement therapy: lipids, lipoproteins, coagulation and fibrinolytic factors. Maturitas. 1996; 23:209.
- Tobias J.H., Maxwell J.D., Chambers T.J. Hormone replacement for osteoporosis. Lancet, 1990; 335:1471-1476.
- Urban R.J., Pavlov S.N., Rivier J.E. Suppresive action of a gonadotropin releasing hormone antagonist on luteinizing hormone, foliculle stimulating hormone, and prolactin releasing in estrogen defficient postmenopausal women. Am J Obstet Gynecol, 1990;162: 1255-1260.
- Uthian W.H. Biosynthesis and physiologic effects of estrogen and pathophysiologic effects of estrogen defficiency: A review. Am J Obstet Gynecol, 1989;161: 1828-1831.
- Varma T.R., Patel R.H., Rosemberg D. Effect of hormone replacement therapy on antitrombin III activity in postmenopausal women. In Jour Gynecol Obstet, 1986; 24:1:69-73
- Voigt LF, Weiss NS., Chu JR., et al. Progestagen supplementation of exogenous oestrogens and risk of endometrial cancer. Lancet. 1991; 338:274.
- Voutilainen S., Hippelainen M., Hulklo S., et al. Left ventricular diastolic function by Doppler echocardiography in relation to hormone replacement therapy in healthy postmenopausal women. Am J Cardiol. 1993; 71:614.
- Walker RF. Neuroendocrine correlates of female reproductive senescence. En Eskin BA . The Menopause: Comprehensive Management. McGraw Hill Inc. (3a). 1994:229-255.
- Walsh BR., Schiff I. Physiology of the climaxteric. En Carr BR., Blackwell RE. Textbook of reproductive medicine. Ed Appleton & Lange (1a); 1993: 587-559.
- Walsh BW., Schiff I., Rosner B., et al. Effects of postmenopausal estrogen replacement on the concentrations and metabolism of plasma lipoproteins. New Engl J Med. 1991 ; 325 :1196.
- Wark JD. Osteoporotic fractures: background and prevention strategies. Maturitas. 1996; 23:193.
- Warner SL. Preventive healt care for the menopausal woman. Infertil Reprod Clin North Am. 1995; 6:675.
- Weinstein L. Hormonal therapy in the patient with surgical menopause. Obstet Gynecol, 1990; 75 (4 suppl):47-49.
- Weinstein L., Bewtra C., Gallagher JC. Evaluation of a continuous low dose regimen of estrogen-progestin for treatment of the menopausal patient. Am J Obstet Gynecol. 1990; 162: 1534.
- Weiss NS., Hill DA. Postmenopausal estrogens and the incidence of gynecologic cancer. Maturitas. 1996; 23:235.
- Whitcroft SI., Crook D., Marsh MS., et al. Long-term effects of oral and transdermal hormone replacement therapies on serum lipid and lipoprotein concentrations. Obstet Gynecol. 1994; 84: 222.
- Whitehead M.I., Hillard T.C., Crock D. The role and use of progestagens. Obstet Gynecol, 1990; 75 (4 suppl): 59-74.
- Wiklund I., Karlberg J., Mattson LA. Quality of life in postmenopausal women on a regimen of transdermal estradiol therapy: a double-blind placebo-controlled study. Am J Obstet Gynecol. 1993; 168: 824.
- Wild RA. Estrogen: effects on the cardiovascular tree. Obstet Gynecol. 1996; 87 (suppl):27.
- Wile AG., Opfell RW., Margileth DA. Hormone replacement therapy in previously treated breast cancer patients. Am J Surg. 1993; 165: 372.
- Wingo PA., Layde PM., Lee NC., et al. The risk of breast cancer in postmenopausal women who have used estrogen replacement therapy. JAMA. 1987; 257:209.
- Yang CP., Daling JR., Band PR., et al. Noncontraceptive hormone use and risk of breast cancer. Cancer Causes Control. 1992; 3: 475.